
Tok в ваkууме
Свободные электроны при обычной температуре не покидают металл. Работа, к-рую надо совершить для удаления эл-на из металла в вакуум, называют работой выхода. Её существование связано с необходимостью преодолеть притяжение определяемого отрывом электрона положительного ЭЗ внутри металла (заряда ионов в узлах кристаллич. решётки) и сопротивление «электронного облака», возникающего вблизи поверхности металла. Это облако по толщине равно неск-ким межатомным расстояниям (10-10… 10-9м) и вместе с наружным слоем положительных ионов решётки образует двойной электрич. слой. Разность потенциалов в этом слое, называемая поверхностным скачком потенциала, определяется работой выхода электрона из металла:
 Работа выхода
Работа выхода
 зависит от природы металла и от чистоты
его поверхности, колеблется в пределах
единиц eV
(eV
электрон-Вольт,
1
eV
=1.610-19Дж).
зависит от природы металла и от чистоты
его поверхности, колеблется в пределах
единиц eV
(eV
электрон-Вольт,
1
eV
=1.610-19Дж).
Термоэлектронная эмиссия (ТЭ) испускание электронов нагретыми металлами. ТЭ наблюдается обычно в вакуумном диоде (схема рис.1,а). В схеме цепи с диодом измеряют вольтамперную характеристику I(U) при измерениях следствий ТЭ снимается зависимость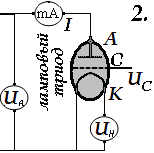
 Её ход для относит-но небольших UА
определяется законом
3/2
(Богуславского-Ленгмюра)
Её ход для относит-но небольших UА
определяется законом
3/2
(Богуславского-Ленгмюра)
 зависит от формы, размера и взаимного
положения электродов). С повышением
анодного напряжения UА
происходит насыщение
тока
(рис.1,б).
Катод в данной цепи м-но нагревать (в
этом
одно из условий наблюдения ТЭ),
изменение температуры T
регулируется напряжением
зависит от формы, размера и взаимного
положения электродов). С повышением
анодного напряжения UА
происходит насыщение
тока
(рис.1,б).
Катод в данной цепи м-но нагревать (в
этом
одно из условий наблюдения ТЭ),
изменение температуры T
регулируется напряжением
 С увеличением температуры нарастает
и величина тока насыщения, поск-ку всё
большее число электронов способно
преодолеть притяжение объёмного заряда
решётки и вырваться из металла катода.
Явление
ТЭ
и
устанавливается
в связи с возможностью тока эмитировавших
электронов через вакуум между электродами
диода с появлением разности потенциалов.
Насыщение силы тока означает, что
основная часть электронов, эмитировавших
с поверхности катода при данной его
темпepaтуре
T,
достигает анода; плотность тока насыщения
устанавливается формулой
РичардсонаДэшмана
С увеличением температуры нарастает
и величина тока насыщения, поск-ку всё
большее число электронов способно
преодолеть притяжение объёмного заряда
решётки и вырваться из металла катода.
Явление
ТЭ
и
устанавливается
в связи с возможностью тока эмитировавших
электронов через вакуум между электродами
диода с появлением разности потенциалов.
Насыщение силы тока означает, что
основная часть электронов, эмитировавших
с поверхности катода при данной его
темпepaтуре
T,
достигает анода; плотность тока насыщения
устанавливается формулой
РичардсонаДэшмана
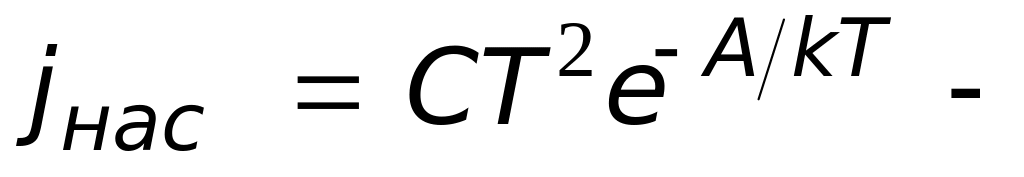 (А
работа выхода эл-нов из катода,
С
постоянная для всех
металлов, k
–
постоянная Больцмана).
(А
работа выхода эл-нов из катода,
С
постоянная для всех
металлов, k
–
постоянная Больцмана).
Явление ТЭ в подобной цепи используется для выпрямления переменного тока такое устройство как диод (электронная лампа) характеризуется односторонней проводимостью.
Размещение между анодом и катодом третьего электрода (сетки C) с регулируемым напряжением
 даёт возможность управлять силой тока
(модулировать ток) в цепи анодного
напряжения (рис.2).
Такие
электронные лампы носят название
триодов
и используются в радиотехнике в схемах
усиления и ранее - в устройствах
логических элементов ЭВМ.
даёт возможность управлять силой тока
(модулировать ток) в цепи анодного
напряжения (рис.2).
Такие
электронные лампы носят название
триодов
и используются в радиотехнике в схемах
усиления и ранее - в устройствах
логических элементов ЭВМ.
Ток в жидкостях
Вещества, в которых при прохождении тока происходят химические превращения, называют электролитами (подобные среды ещё именуют проводниками 2-го рода). К их числу относятся растворы солей или щелочей в воде и нек-рых других жидкостях, а также расплавы солей, являющиеся в твёрдом состоянии ионными кристаллами.
Электропроводимость у электролитов существует за счет ионов (заряженных атомов или частей молекул – т.н. радикалов), которые появляются в растворе благодаря распаду на части молекул растворенного вещества под действием молекул растворителя. В воде, например, обладающей большой диэлектрической проницаемостью, ослабляются электрические связи между атомами растворённых молекул. При распаде молекулы на два иона, каждый из них приобретает избыточный ЭЗ за счет захвата электрона одним из атомов (отрицательный ион) и потери его другим. Распад молекулы в растворе носит название диссоциации, диссоциирует только часть молекул, поэтому вводится коэффициент , определяющий эту часть по отношению к общему числу молекул. Заряды, приобретённые в рез-те диссоциации, меняют химические свойства ионов (по сравнению с атомами) и делают их химически неактивными относительно молекул воды.
Ионы в отсутствие электрического поля (ЭП) движутся хаотично, и ток при этом не возникает. Под действием ЭП ионы приходят в упорядоченное движение, которое накладывается на хаотическое. При этом происходит направленный перенос заряда ионов. Ионы оказываются окружёнными так называемыми сольватными оболочками из молекул растворителя. Их движение поэтому можно рассматривать как перемещение шариков в вязкой среде. При движении таких частиц сила сопротивления пропорциональна скорости
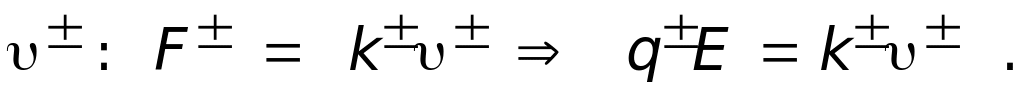 Здесь знаки
соответствуют знаку зарядов ионов;
соответственно различными будут и
направления скоростей в ЭП
с напряжённостью E,
Здесь знаки
соответствуют знаку зарядов ионов;
соответственно различными будут и
направления скоростей в ЭП
с напряжённостью E,
 коэффициент трения иона при движении.
Ион движутся с ускорением под действием
ЭП
E,
пока
кулоновская сила не станет уравновешенной
силой трения. Величина
коэффициент трения иона при движении.
Ион движутся с ускорением под действием
ЭП
E,
пока
кулоновская сила не станет уравновешенной
силой трения. Величина
 определяет скорость ионов при
напряжённости ЭП
в 1
В/м,
т.е.
определяет скорость ионов при
напряжённости ЭП
в 1
В/м,
т.е.
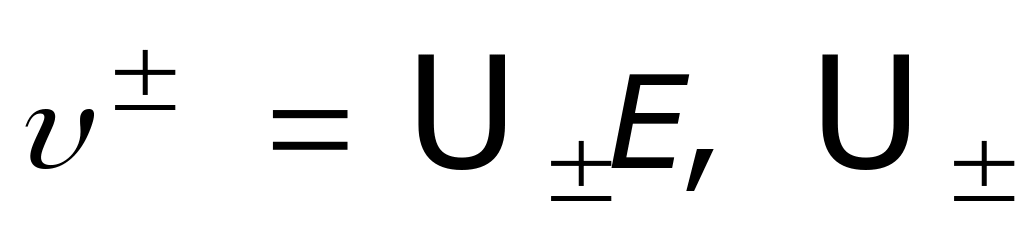 носят название коэффициентов
подвижности
(их величины м-т быть различными у ионов
противоположных знаков).
носят название коэффициентов
подвижности
(их величины м-т быть различными у ионов
противоположных знаков).
Плотность тока в растворе по определению
 ЭЗ
электрона,
ЭЗ
электрона,
 число
ионов /концентрация/ в ед-це объёма),
т.е., с учётом различия знаков заряда у
ионов и их валентности
число
ионов /концентрация/ в ед-це объёма),
т.е., с учётом различия знаков заряда у
ионов и их валентности
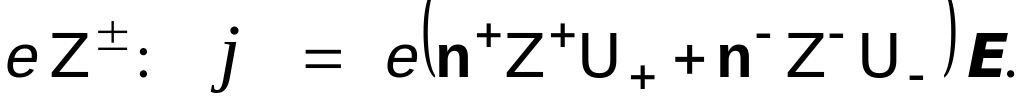 В случае одинаковой валентности закон
Ома для электролитов
формулируется так:
В случае одинаковой валентности закон
Ома для электролитов
формулируется так:

 (
- коэффициент
диссоциации).
С
повышением температуры значения
удельной проводимости электролитов
(
- коэффициент
диссоциации).
С
повышением температуры значения
удельной проводимости электролитов
 возрастают из-за увеличения
возрастают из-за увеличения
 и
и
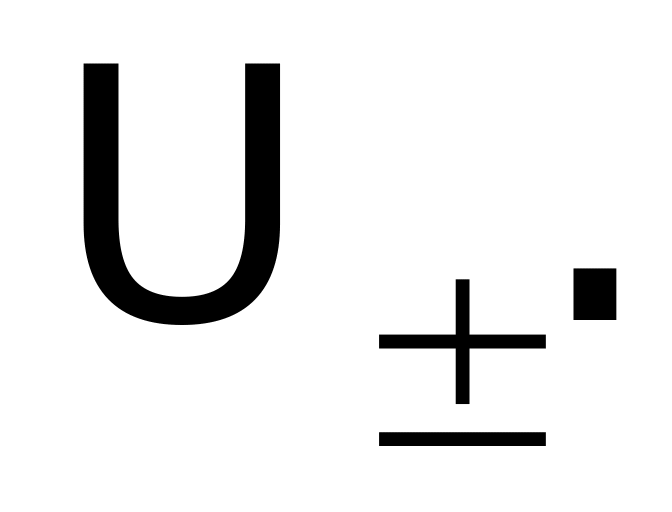
Итак, если в электролит ввести электроды, то катионы движутся к катоду, а отрицат. ионы (анионы) – к аноду. При утрате заряда на поверхности электродов ионы превращаются в нейтральные атомы или радикалы. Эти частицы не могут существовать в растворе без заряда и вступают в химические реакции с растворителем или веществом электродов. Вблизи электродов происходит выделение новых веществ, которые отсутствовали в растворе. Этот процесс выделения веществ на электродах при прохождении через электролит электрич. тока называется электролизом. Количественно электролиз характеризуется законом Фарадея: выделившаяся на электроде масса m = kq. Здесь k — электрохимич. эквивалент; переменный ЭЗ q(t) чаще выражается ч/з силу тока i: dq = i(t) dt. Тогда m = k
 масса вещества (металла), выделившегося
на катоде за время .
Величину k
выражают также
т.о.
масса вещества (металла), выделившегося
на катоде за время .
Величину k
выражают также
т.о.
 где
X
= A/Z
–
химичecкий
эквивалент,
А
—
атомная
масса,
Ζ
—
валентность;
F
—
число
Фарадея.
где
X
= A/Z
–
химичecкий
эквивалент,
А
—
атомная
масса,
Ζ
—
валентность;
F
—
число
Фарадея.
