
- •Химическая кинетика
- •Основные понятия и определения
- •Виды химических реакций
- •Простые реакции. Молекулярность
- •Сложные реакции
- •С труктура темы
- •Формальная кинетика
- •Определение скорости химической реакции
- •Основной закон химической кинетики – закон «действующих масс»
- •Кинетические параметры
- •Порядок реакции
- •Константа скорости
- •Кинетические уравнения
- •Кинетическое уравнение реакции нулевого порядка
- •Кинетическое уравнение реакции первого порядка
- •Кинетическое уравнение реакции второго порядка
- •Кинетическое уравнение реакции третьего порядка
- •Теория скоростей химических реакций
- •Распределение молекул по энергиям
- •Энергия активации
- •Зависимость скорости реакции от температуры
- •Правило Вант-Гоффа
- •Уравнение Аррениуса
- •Э Рис. 6.6. Определение энергии активации кспериментальное определение энергии активации и предэкспоненциального множителя
- •Физический смысл предэкспоненциального множителя
- •Основы теории активных соударений
- •Теория активированного комплекса
- •Кривая потенциальной энергии
- •Виды сложных реакций
- •Реакции с последовательными стадиями
- •Реакции с параллельными стадиями
- •Обратимые реакции
- •Каталитические реакции
- •Цепные реакции
- •Кинетическое равновесие
- •Условие равновесия
- •Кинетическое равновесие устанавливается при равенстве скоростей прямой и обратной реакции.
- •Константа равновесия
- •Смещение равновесия. Принцип Ле-Шателье
- •Влияние концентрации
- •Влияние давления
- •Влияние температуры.
- •Влияние катализатора.
- •Расчеты кинетических и термодинамических величин
- •Изотерма химической реакции
- •Зависимость константы равновесия от температуры. Изобара химической реакции
Распределение молекул по энергиям
В
Рис. 6.5 Распределение
молекул по энергии
 (6.7)
(6.7)
которое показывает количество молекул, обладающих энергией от Е – dE до Е + dE В графической форме это распределение показано на рис. 6.5. Уравнение 6.7. является дифференциальным. Более общий случай, для больших интервалов энергий, описывается распределением Больцмана в интегральном виде:
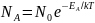 (6.7.1)
(6.7.1)
здесь NA – число молекул с энергией ЕA, N0 – общее число молекул, k=R/Na – константа Больцмана, равная отношению газовой постоянной и числа Авагадро.
На рисунке 6.5 приведены две кривые распределения, расчитанные для разных температур. Максимумы на каждой кривой соответствуют средней энергии (ось Х) и наибольшему числу молекул (ось Y). Эта средняя энергия при повышении температуры незначительно смещается в область высоких энергий, и в дальнейшем будем считать (для небольшого интервала температур) ее постоянной. Молекулы, обладающие средней энергией, при соударении не способны прореагировать друг с другом, для этого необходима более высокая энергия, которую обозначим Е*. Все частицы, имеющие энергию > Е* будут вступать в реакцию, для определения этого значения введем понятие энергии активации ЕA.
Энергия активации
Энергия активации ЕA это разность между значениями средней энергии частиц (молекул, радикалов, ионов и др.), вступающих в элементарный акт химической реакции, и средней энергии всех частиц, находящихся в реагирующей системе (рис. 6.5.). Энергия активации – важнейшая кинетическая характеристика, для любой реакции она имеет определенное значение и, будем считать, не зависит от температуры. Это позволяет расчитывать время протекания реакции для определенного интервала температур.
Определим энергию активации так:
минимальная избыточная энергия (относительно средней величины), которой должна обладать частица в момент столкновения, чтобы вступить в элементарный акт химического превращения.
Энергия активации необходима для разрыва связей в исходных молеулах, поэтому различные химические реакции имеют строго определенное значения этой энергии. Обычно, энергию активации выражают в кДж/моль, и она может изменяется в широких пределах от долей до сотен кДж/моль. Так, для реакций в растворах первого и второго порядков энергия активации принимает значения 50-150 кДж/моль, а для реакций третьего порядка близка к нулю.
Зависимость скорости реакции от температуры
Из рассмотренных закономерностей следует, что скорость реакций должна сильно зависеть от температуры. Это объясняется тем, что при высоких температурах резко возрастает число активных соударений. При энергии активации равной 10 кДж/моль повышение температуры с 300 до 310 К (100) приведет к увеличению числа активных соударений в соответствии с распределением Больцмана:
N2/N1 = exp(-Ea(T1-T2)/R T1T2 = exp(10000*10/8,31*300*310) ≈ 3,5
Поскольку скорость реакции пропорциональна числу активных соударений, то и она должна увеличится более чем в три раза. Следует отметить, что существует небольшое число реакций (в основном тримолекулярные) для которых повышение температуры может привести к замедлению процесса. Это связано, с тем что для таких реакций энергия активации мала, а общее число тройных соударений при этом может уменьшаться.
