
- •Санкт-Петербург
- •Общие сведения
- •Выполнение работы
- •Образование комплексных соединений
- •Опыт 3. Образование и реакции амминокомплекса меди.
- •Опыт 9. Образование труднорастворимого гексацианоферрата (III).
- •Реакции, сопровождающиеся разрушением комплексных ионов
- •Опыт 13. Разрушение комплекса при разбавлении раствора.
Опыт 3. Образование и реакции амминокомплекса меди.
Налить в две пробирки по 10 капель р-ра сульфата меди (II).В первую пробирку добавить 2 капли раствора соли бария. Во вторую пробирку внести кусочек гранулированного олова и наблюдать выделение на его поверхности красноватого налета меди.
Уравнения реакции:
а) CuSO4+BaCl2=BaSO4 + CuCl2
Cu2++SO42-+Ba2++2Cl- =BaSO4 +Cu2++2Cl-
Ba2++SO42-= BaSO4
б)СuSO4+Sn=SnSO4+Cu –выделяется красноватый налет
В первый момент выделяется осадок сульфата гидроксомеди (II), который затем растворяется вследствие образования амминокомплекса меди.
2CuSO4 +2
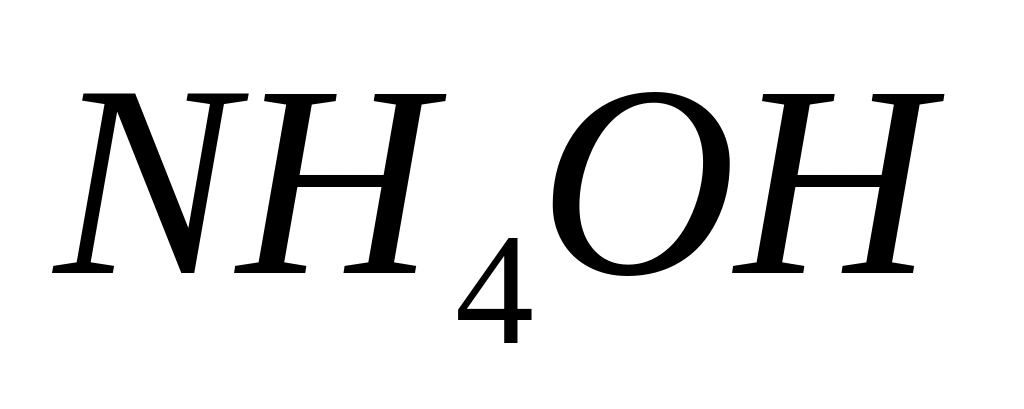 = (CuOH)2SO4
+(NH4)2SO4
= (CuOH)2SO4
+(NH4)2SO4
2Cu2+ + 2SO42- + 2NH41+ + 2OH1 = (CuOH)2SO4 + 2NH41+ + SO42-
2Cu2+ + SO42- + 2OH1- = (CuOH)2SO4
минуя промежуточную стадию образования сульфата гидроксомеди (II):
CuSO4 + 6NH4OH = [Cu(NH3)4](OH)2 + (NH4)2SO4 + 4H2O
Cu2+ + SO42- + 6NH41+ + 6OH1- = [Cu(NH3)4]2+ + 2OH1- + 2NH41+ + SO42- + 4H2O
Cu2+ + 4NH41+ +4OH1- = [Cu(NH3)4]2+ + 4H2O
Полученный раствор комплексной соли меди разделить в две пробирки и провестите же два опыта, которые были проделаны с раствором сульфата меди.
а) (CuOH)2SO4+BaCl2=BaSO4 +(CuOH)2Cl2 - выделяется осадок
2CuOH++SO42-+Ba2++2Cl- = BaSO4 +2CuOH++2Cl-
SO42-+Ba2+ = BaSO4
б) (CuOH)2SO4+ Sn=SnSO4+2CuOH - выделяется гидроксид меди (l)
В ходе первой реакции образовался осадок белого цвета: сульфат гидроксомеди (II) - (CuOH)2SO4, через некоторое время осадок растворяется, раствор меняет цвет на
тетраамминомеди (II).
Опыт 4.Получение комплексного основания кадмия. Получить в пробирке осадок гидроксида кадмия, добавляя к раствору его соли равный объем раствора гидроксида натрия. На полученный гидроксид подействовать концентрированным раствором аммиака до полного растворения осадка.
CdSO4+2NaOH = Cd(OH)2 + Na2SO4 студенистый, белый осадок
Cd+2+SO4-2+2Na++2OH- =Cd(OH)2 +2Na++SO4-2
Cd+2+2OH-=Cd(OH)2
б) Cd(OH)2 + 4NH3 = [Cd(NH3)4](OH)2 осадок растворился
Cd2++2OH- +4H++4NH2- =[Cd(NH3)4]+2 +2OH-
Cd2++4H++4NH2- =[Cd(NH3)4]+2
[Cd(NH3)4](OH)2 является более сильным электролитом, т к диссоциирует в воднос растворе, в отличае от Cd(OH)2.
Опыт 5. Получение тетрайодовисмутата калия. В пробирку к 3-4 каплям раствора нитрата висмута прибавлять по каплям раствор йодида калия до выпадения темно-бурого осадка йодида висмута. Растворить этот осадок в избытке раствора йодида калия.
Bi(NO3)3+3KI= BiI3 + 3KNO3 - выпал темно- бурый осадок
Bi3++ 3NO3-+3K++3I- = BiI3 +3K++3NO3-
Bi3++3I-= BiI3
б) BiI3+ KI= K[BiI4]
Bi3++3I-+K++I-= K++[BiI4]-
Bi3++3I-+ I-=[BiI4]-
-растворение выпавшего вначале осадка йодида висмута и образование светло-бурого раствора.
. Окраска раствора может быть обусловлена присутствием ионов Bi3+ и I-.
Так как лиганды, представляют собой связанные ковалентно анионы , то единственной возможной лигандой является I-. Комплексообразователем может быть ион Bi3+, так как в молекуле любого комплексного соединения один из ионов, обычно положительно заряженный является комплексообразователем и располагается в центральном месте молекулы. С лигандами I- комплексообразователь Bi3+, может образовывать сложный ион [BiI4]-.
Опыт 6. Получение комплексного йодида ртути. Налить в пробирку 3−4 капли раствора нитрата ртути (II) и добавить 1−2 капли раствора иодида калия. Отметить цвет образующегося осадка дийодида ртути. В пробирку по каплям добавить избыток раствора иодида калия до полного растворения полученного осадка, которое обусловлено образованием в растворе комплексных анионов тетрайодомеркурата.
Hg(NO3)2 + 2KI = HgI2 ↓+ 2KNO3, осадок оранжевого цвета
HgI2 + 2KI = K2[HgI4], светло желтый раствор;
Этот анион можно выделить в осадок ионами серебра: в пробирку добавить 1-2 капли раствора нитрата серебра.
K2[HgI4] + 2AgNO3 = Ag2[HgI4]↓ + 2KNO3, желтый порошкообразный осадок;
2K+
+ [HgI4]-
+ 2Ag-
+ 2NO3-
= Ag2[HgI4]↓
+ 2K+
+
![]()
2Ag- + [HgI4]- = Ag2[HgI4]↓;
В первой реакции выпадает оранжевый осадок йодида ртути - HgI2, при добавлении избытка йодида калия осадок растворяется, что обусловлено образованием [HgI4]-2 (анион тетрайодомеркурата (II)).
Опыт 7. Образование гидроксокомплекса цинка. В пробирку налить 3−4 капли раствора сульфата цинка и добавить по каплям раствор гидроксида натрия, находящийся в штативе с реактивами, до выпадения осадка гидроксида цинка. Затем в вытяжном шкафу добавить по каплям 6 н. раствор едкого натра до полного растворения осадка вследствие образования комплексного аниона тетрагидроксоцинка (2−).
ZnSO4 + 2NaOH = Na2SO4 + Zn(OH)2↓ - студенистый осадок
Zn2+ + SO42- + 2Na+ + 2OH- = 2Na+ + SO42- + Zn(OH)2↓
Zn2+ + 2OH- = Zn(OH)2↓
Zn(OH)2 + 2NaOH = Zn(OH)42- - растворение осадка
Zn(OH)2 + 2Na+ + 2OH- = Zn(OH)42- + 2Na+
Zn(OH)2 + 2OH- = Zn(OH)42-
-Реакции с участием комплексных соединений, не сопровождающийся разрушением комплексного иона.
Гидроксида цинка - Zn(OH)2, после добавления избытка гидроксида натрия осадок растворяется, тем самым образуется комплекс тетрагидроксоцинкат натрия - Na2[Zn(OH)4].
+
Опыт 8.Внутрикомплексные соединения. В три пробирки внести по 3 капли раствора хлорида железа. Одну оставить в качестве контрольной. В две другие добавить по 3 капли раствора щелочи. К образовавшемуся осадку в одну из них добавить 12-15 капель 2 н. щавелевой кислоты , в другую – столько же 2 н. лимонной кислоты. В обе пробирки и в контрольную внести 1-2 капли раствора роданида калия или аммония, который образует с ионами F3+ ярко окрашеный роданид железа.
а) FeCl3 +3NaOH = 3NaCl+Fe(OH)3
Fe3++3Cl¬- +3Na++3OH- =3Na++3Cl- + Fe(OH)3
Fe3++3OH- = Fe(OH)3
б) Fe(OH)3+3C2H2O4=[Fe(C2O4)3]+3H2O+3H
[Fe(C2O4)3]+3KSCN=Fe(SCN)3
в) Fe(OH)3+ С6Н8O7=[Fe(C2O3)3]+H2O+9H
г) FeCl3+3KSCN= Fe(SCN)3+3KCl
Во всех пробирках наблюдается окрашивание в красный цвет. Остаток щавелевой кислоты является полидентантным лигандом.
