
Учебник Органическая химия Щеголев 2016
.pdf
12.2.4.3. Реакции с электрофилами
Ввиду выраженных ацидофобных свойств индола его реакции с сильными электрофилами в кислой среде приводят к продуктам олигомеризации. С более мягкими электрофилами осуществляется замещение в-положение. Если оно занято, то реакция протекает в -положение. Объяснить такое направление электрофильного замещения можно сравнением устойчивости образующихся -комплексов:
|
+ |
E |
|
+ |
E+ |
H |
|
N |
N |
||
|
|||
H |
H |
|
H E |
H E |
+ |
|
|
+ |
N |
N |
H |
H |
(Здесь не приведены граничные структуры с участием -электронной плотности бензольного кольца по причине их значительно меньшего вклада, но таких структур было бы в каждом случае на три больше.)
Как видно из приведѐнных направлений взаимодействия индола с электрофильной частицей, делокализация положительного заряда в случае атаки по -атому (второе направление) полнее и такой -комплекс устойчивее.
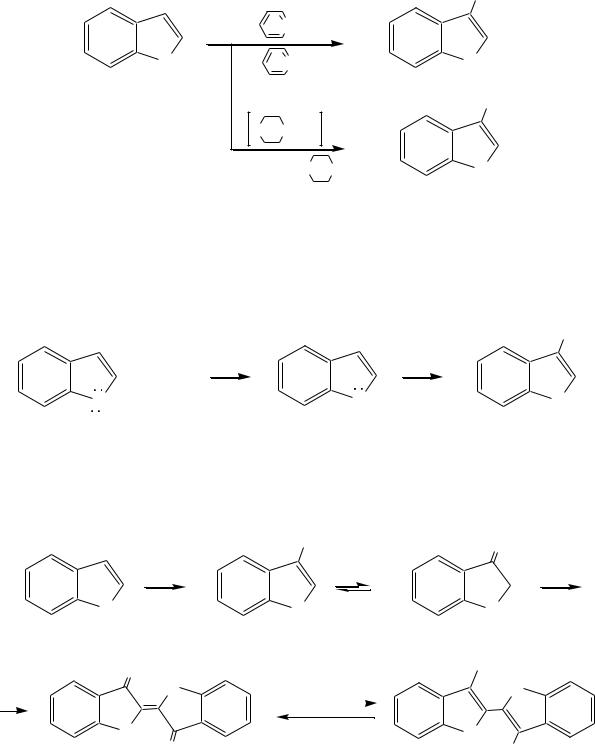
Нитрование индола осуществляется так же, как и пиррола, через образование солей, сульфирование — пиридинсульфотриоксидом, а для бромирования используется комплекс брома с диоксаном:
NO2
|
+ |
|
|
|
|||
|
|
|
|
||||
- |
+ H5C2O-NO2 |
|
-C2H5OK |
|
|
|
|
|
|
|
|
|
|
||
N K+ |
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
H |
631
|
|
|
|
SO3- |
|
|
N: SO3 |
|
|
N |
- |
+ |
|
N |
N:H |
|
|||
H |
|
|
|
H |
|
|
|
|
Br |
|
O |
O: Br+ Br- |
|
|
|
-HBr, |
- O |
O |
N |
|
|
|
|
H |
Алкилирование может осуществляться как по атому азота, так и по атому углерода. Направление реакции определяется главным образом температурой, а также природой металла и растворителем. Это можно изобразить схемой:
R
|
+ |
R-I |
|
|
T |
- |
-MI |
|
|
||
|
|
N |
|
||
N M+ |
|
|
|
N |
|
|
|
|
|
R |
H |
12.2.4.4. Реакции окисления
Мягкое окисление индола даѐт синий краситель индиго:
|
|
|
OH |
|
O |
|
2 |
[O] |
2 |
|
|
2 |
[O] |
|
|
|
|
|||
N |
|
|
N |
|
N |
|
H |
|
|
H |
|
H |
|
O |
H |
|
|
|
ONa H |
|
|
N |
|
Na2S2O4, NaOH |
N |
|
|
|
|
|
|
|
||
N |
|
|
O2 |
|
N |
|
H |
O |
|
|
|
H NaO |
|
индиго (синего цвета) |
|
соль белого индиго |
|
|||
Сильными окислителями (KMnO4) индиго окисляется до изатина:
632
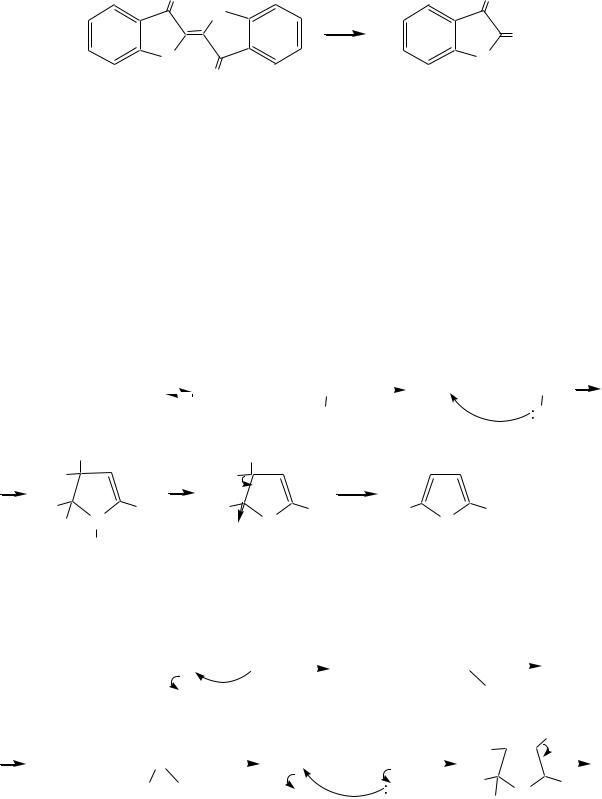
O |
H |
|
O |
|
N |
|
|
|
[O] |
2 |
O |
|
|
||
N |
|
|
N |
H |
O |
|
H |
изатин
12.2.5.СПОСОБЫ ПОЛУЧЕНИЯ ПИРРОЛА, ФУРАНА, ТИОФЕНА, ИНДОЛА
Внебольших количествах пиррол и тиофен содержатся в каменноугольной смоле. При этом тиофен выгоняется из неѐ вместе с бензолом.
К синтетическим способам получения можно отнести следующие.
4. Общим способом получения пиррола, фурана и тиофена и их производных является циклизация -дикарбонильных соединений. Механизм кислотно-катализируемого образования фуранов можно представить в следующем виде:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H+ |
+ |
|
|
R-C-CH2-CH2-C-R |
|
|
|
|
R-C-CH2-CH=C-R |
|
R-C-CH2-CH=C-R |
|||||||||||
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
O |
|
|
|
O |
OH |
|
OH |
OH |
|||||||||
|
H |
|
H |
|
|
|
|
|
|
H |
|
|
H |
|
|
|
|
|
|
R |
O |
R |
R + O |
R |
2 |
+ |
R |
O |
R |
|
+ |
|
|
|
-H O |
|
|
||
HO |
|
|
HOH |
|
-H |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
В синтезе пирролов необходима нуклеофильная атака аммиаком, а для получения тиофенов используются сульфиды фосфора. Например, механизм образования пирролов:
|
|
R-C-CH2-CH2-C-R |
|
|
+ :NH3 |
|
R-C-CH2-CH2-C-R |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
O |
|
|
|
|
|
|
|
|
|
|
O |
|
|
- |
|
+ |
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
O |
|
|
|
|
|
|
|
|
O |
NH3 |
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
H H |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R-C-CH2-CH2-C-R |
|
|
|
|
R-C-CH2-CH2-C-R |
|
|
|
|
H |
|
|
|
|
+ |
|
|
|
|||||||||||||||||
-H2O |
|
|
|
R- |
|
|
|
|
|
R |
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
O |
OH NH2 |
O |
|
|
NH |
|
|
O |
N |
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
||||
633

H
H |
|
|
|
|
|
|
R |
N |
R |
-H2O |
R |
N |
R |
|
||||||
HO |
|
|
|
|
||
H |
|
|
|
H |
|
5. Для получения фурана и его производных используют природные моносахариды. При нагревании в присутствии минеральных кислот может образоваться фурфурол:
HC=O |
|
|
|
|
|||||
H |
|
|
|
|
OH |
H+/ T |
|
O |
|
|
|
|
|
|
|||||
HO |
|
|
H |
|
|
|
C |
||
|
|
|
-3H2O |
|
|||||
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
||
H |
|
|
OH |
O |
H |
||||
|
|
|
|
||||||
|
|
|
|||||||
|
|
CH2OH |
|
|
|
|
|||
D-ксилоза |
|
|
|
фурфурол |
|
||||
или другие производные фурана в зависимости от природы исходного моно-
сахарида (гл. 7.1.2.3).
6. При нагревании гликаровых (гл. 7.1.2.1) кислот образуется пирослизевая кислота:
|
HOOC-CHOH-CHOH-CHOH-CHOH-COOH |
|
H+, t o |
||||||||||||
|
|
|
|
||||||||||||
|
-3H2O |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
t o |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
HOOC |
O |
COOH |
-CO2 |
O |
COOH |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
пирослизевая кислота
7. Пиррол образуется при нагревании аммониевых солей гликаровых кислот:
|
+ - |
|
|
|
|
- + |
NH t o |
|||||||
|
NH4 OOC-CHOH-CHOH-CHOH-CHOH-COO NH4 |
|
3 |
|
||||||||||
|
-4H2O |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
t o |
|
|
|
|
|
|
|
+NH4-OOC |
|
COO-NH4+ |
|
|
|
|
|
||||
|
|
|
N |
|
|
|
|
|
N |
|||||
|
|
|
|
-NH3,-CO2 |
|
|||||||||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
H |
|
|
|
|
|
|
|
H |
|
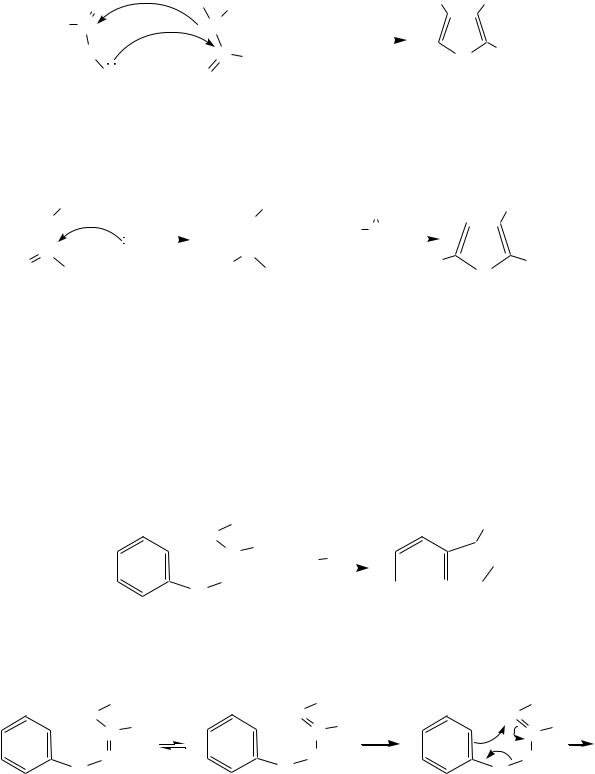
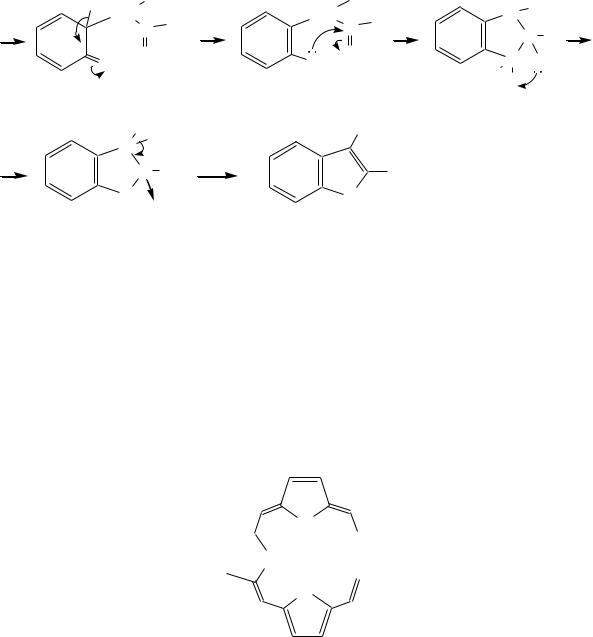
8. Универсальным и удобным в практическом выполнении методом получения производных пиррола является взаимодействие -амино-кетонов с кетонами, содержащими реакционноспособную метиленовую группу (син-
тез Кнорра*). Например:
634
H |
CH |
R |
|
|
R |
|
H |
R |
|
|
R' |
CH |
+ |
R' |
C |
||||
|
|
|
C |
|
C |
|
C R' |
||
|
|
|
|
|
|
|
|||
|
|
+NH |
|
+ |
|
+ |
|||
|
NH |
NH2 |
NH2 |
NH2 |
|||||
|
|
|
2 |
|
|
N |
|||
|
|
|
|
|
|
|
|
H H |
|
C |
RH |
|
R |
|
|
|
|
|
C R' |
-NH4+ |
R' |
N |
+ |
N |
|
H |
NH3 |
H |
|
12.2.6.ВАЖНЕЙШИЕ ПРЕДСТАВИТЕЛИ И МЕДИКО-БИОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ
Пиррол — бесцветная жидкость с запахом хлороформа с температурой кипения 130 С, малорастворим в воде.
Пирролидинкарбоновые кислоты (пролин и гидроксипролин) являются важными протеиногенными аминокислотами гл. 6.9.
Порфин — тѐмно-красное кристаллическое вещество. Его молекула содержит четыре пиррольных кольца:
N

 N: HH :N
N: HH :N


N
За счѐт двух водородных атомов (у атомов азота), которые могут быть замещены металлом, образуются устойчивые комплексы, в которых ион металла образует связи одновременно с четырьмя атомами азота.
Замещѐнные порфины называются порфиринами. Они лежат в основе очень важных природных соединений. Например, гем — небелковая часть красного вещества крови гемоглобина. По химическому составу гем является порфирином, содержащим катион Fe2+.
636
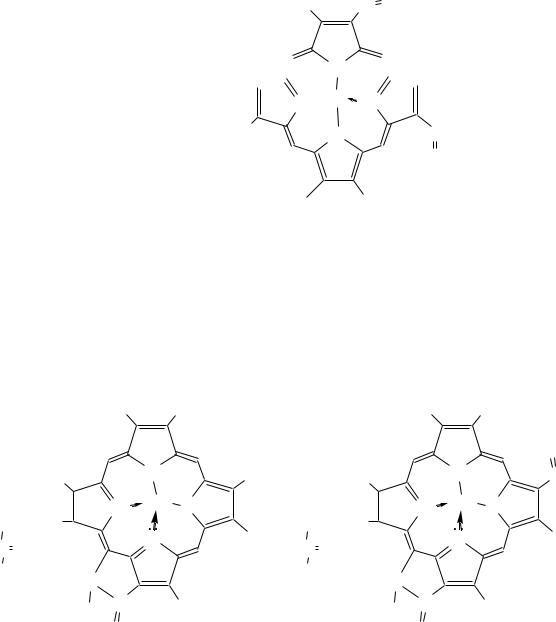
H3C HC CH2
H3C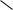
 N
N 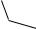
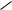 CH3
CH3
N: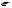 Fe :N
Fe :N
HOOC-CH2-CH2 |
N |
CH |
CH2
HOOC-CH2-CH2 CH3
гем
Другой пример — зелѐный пигмент растений хлорофилл, содержащий катион Mg2+. Из растений выделены хлорофилл а (сине-чѐрные кристаллы) и хлорофилл b (тѐмно-зелѐные кристаллы). Хлорофиллы были выделены Р.М. Вильштеттером*, им же была установлена формула хлорофилла а и структура его отдельных фрагментов. За эти работы Р.М. Вильштеттер был удостоен в 1915 году Нобелевской премии.
|
H3C |
CH=CH2 |
H3C |
CH=CH2 |
|||
|
|
|
|
|
|
|
O |
H3C |
|
N |
CH3 |
H3C |
|
N |
CH |
|
|
|
|
||||
CH2CH2 |
|
N: Mg N |
CH2CH2 |
N: |
Mg N |
|
|
|
N |
C2H5 |
|
N |
C2H5 |
||
C O |
|
C O |
|
||||
|
|
|
|
|
|
||
OC20H39 HC |
|
|
OC20H39 HC |
|
|
|
|
CH3OOC |
C |
CH3 |
CH3OOC |
C |
CH3 |
|
|
|
|
|
|||||
|
|
O |
|
|
O |
|
|
|
хлорофилл а |
|
|
хлорофилл b |
|
||
Витамин В12 (кобаламины: природные — оксикобаламин и метилко-
баламин, лекарственная форма — цианкобаламин) — тѐмно-красные кристаллические вещества, растворимые в воде. В основе молекул лежит фрагмент, структурно похожий на порфириновый, содержащий четыре пиррольных кольца и катион Co2+. Витамин В12 является активным средством против анемии, его применяют для лечения злокачественного малокровия, заболеваний нервной системы и печени.
Билирубиноиды — окрашенные вещества, которые содержат четыре бензольных кольца и встречаются в организмах позвоночных, а также некоторых беспозвоночных и даже в водорослях. Они образуются при биологическом окислении гемоглобина и родственных соединений. Важнейшим их
637
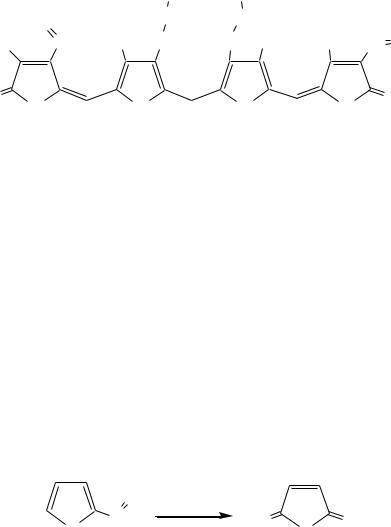
представителем является окрашенный в оранжевый цвет билирубин. Он встречается в желчи, а также в желчных камнях и выделяется с калом и мочой.
|
|
|
COOH |
COOH |
|
|
|
|
H2C |
|
CH2 |
|
CH |
|
|
|
|
|
|
2 |
|
|
|
H C |
CH |
H C |
CH |
H C |
CH3 |
H3C HC CH |
|
|
3 |
2 |
2 |
|
|
2 |
|
3 |
|
|
|
|
|
|
|
O |
N |
|
N |
|
N |
N |
O |
|
|
|
|
||||
|
H |
|
H |
|
H |
H |
|
|
|
|
билирубин |
|
|
||
Фуран — бесцветная жидкость с запахом хлороформа; температура кипения 31 С, малорастворим в воде.
Получают фуран из фурфурола (в промышленности) или пирослизевой кислоты (в лаборатории).
Фурфурол — бесцветная или слегка желтоватая жидкость с запахом корочки свежеиспечѐнного ржаного хлеба; температура кипения 162 С, умеренно растворим в воде (10 г на 100 г воды).
Фурфурол образуется при нагревании некоторых моносахаридов (в частности, ксилозы) с минеральными кислотами (гл. 7.1.2.3). Поэтому фурфурол получают из растительного сырья.
Фурфурол является очень важным исходным веществом для органического синтеза. Каталитическим окислением из него получают малеиновый ангидрид:
|
|
O |
[O] |
|
|
|
C |
|
|
O |
|
O |
|
O |
O |
||
H |
|
|
|
||
|
|
|
|
|
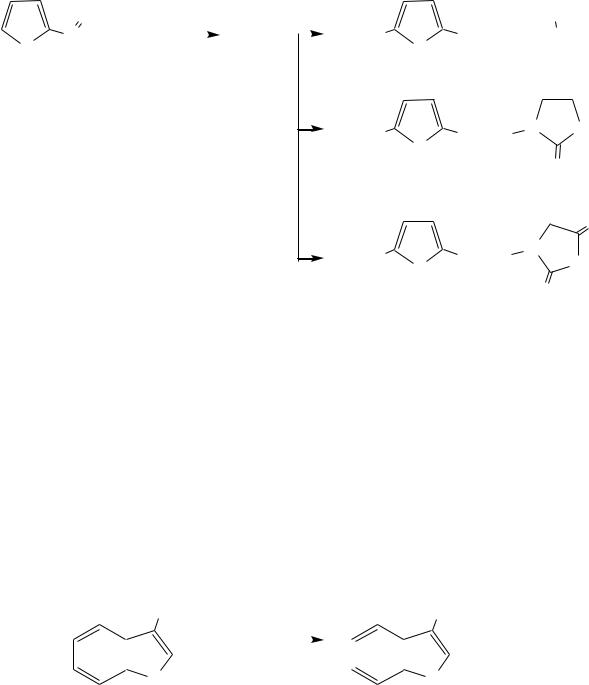
Нитрование фурфурола лежит в основе производства таких бактерицидных препаратов, как фурацилин, фуразолидон, фурадонин:
638
|
O |
CH3COONO2 |
|
|
|
O |
|||
|
|
|
|
|
|
|
|||
|
C |
|
O2N |
|
CH=N-NH-C-NH2 |
||||
O |
|
|
. . . |
|
O |
||||
H |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
фурацилин |
||
|
|
|
|
|
|
|
|
||
O2N |
|
CH=N |
N |
O |
O |
|
|
||
|
|
|
|
|
|
|
|
O |
|
|
|
фуразолидон |
|
|
|
|
|
|
O |
O2N |
|
CH=N |
N |
NH |
O |
|
|||
|
|
|
|
|
|
|
|
O |
|
|
|
фурадонин |
|
|
Тиофен — бесцветная жидкость с запахом, похожим на бензол; температура кипения 84 С, нерастворим в воде. Получают из каменноугольной смолы.
Индол — бесцветное кристаллическое вещество с неприятным запахом; температура плавления 52 С, температура кипения 253 С, нерастворим в воде. Используют в органическом синтезе и в парфюмерии.
Триптофан — одна из незаменимых протеиногенных -ами-нокислот
(гл. 6.9).
Триптамин — «биогенный амин», образующийся в организме человека и животных при декарбоксилировании аминокислоты триптофана под действием ферментов — декарбоксилаз.
|
|
CH2- |
CH-COOH |
|
|
|
|
CH2-CH2-NH2 |
|
|
|
|
|||||
|
|
NH2 |
|
|
|
|
|
|
|
|
- CO2 |
|
|
|
|||
|
|
|
|
|
|
|
||
|
|
N |
|
|
|
|
N |
|
|
|
H |
|
|
|
|
H |
|
триптофан |
|
|
триптамин |
|||||
Скатол (3-метилиндол) является конечным продуктом биологических превращений триптофана. Он обладает пронзительным запахом фекалий, однако в очень больших разбавлениях имеет цветочный запах и поэтому добавляется к цветочным композициям.
Серотонин (3-аминоэтил-5-гидроксииндол) является «биогенным амином». Он обладает высокой биологической активностью, содержится в сыворотке теплокровных, участвует в поддержании тонуса сосудов и процессе
639
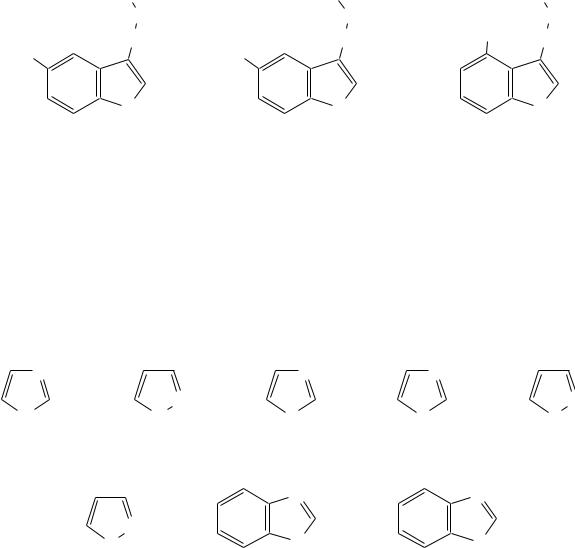
передачи нервных импульсов в центральной нервной системе. В организме образуется из триптофана.
Буфотенин был впервые выделен из кожи жаб. Кроме того, он содержится в некоторых растениях. Вызывает повышение кровяного давления и парализует дыхательные центры головного и спинного мозга.
Псилоцин является психоактивным веществом, выделенным из мексиканского священного гриба Teonanacatl. Он повышает психическую возбудимость и вызывает галлюцинации.
H2N |
(CH3)2N |
(CH3)2N |
||
CH2 |
CH2 |
OH |
CH2 |
|
CH2 |
CH2 |
CH2 |
||
|
||||
HO |
HO |
|
|
|
N |
N |
|
N |
|
H |
H |
|
H |
|
серотонин |
буфотенин |
псилоцин |
|
|
12.3. ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ С ДВУМЯ ГЕТЕРОАТОМАМИ
Среди этих гетероциклических соединений наиболее важны в практическом отношении имидазол, пиразол, оксазол, тиазол, изоксазол, изотиазол и конденсированные системы на их основе бензимидазол и бензотиазол.
N |
|
N |
N |
|
|
|
N |
|
N |
N |
N |
O |
S |
O |
H |
H |
|
|
|
имидазол |
пиразол |
оксазол |
тиазол |
изоксазол |
|
|
N |
N |
|
|
N |
N |
S |
|
|
S |
|
||
|
|
H |
|
|
|
изотиазол |
бензимидазол |
бензотиазол |
|
12.3.1. НОМЕНКЛАТУРА ИМИДАЗОЛА И ПИРАЗОЛА
Систематические названия имидазола и пиразола — 1,3-диазол и 1,2- диазол. Атомы цикла нумеруются начиная с гидрированного (или замещѐн-
640

 R'
R'
 N
N