
- •1. Химическая термодинамика
- •Домашнее задание
- •Подготовиться к проверке по теме 1 и выучить основные определения и формулы темы 2
- •2 Приложения первого начала термодинамики к химическим процессам
- •Следствия из закона Гесса. Методы расчета тепловых эффектов химических реакций
- •1. Расчет по стандартным теплотам образования
- •2. Расчет по стандартным теплотам сгорания
- •3. Метод термохимических уравнений
- •Домашнее задание
- •Найти теплоту образования сероуглерода используя следующие данные:
- •Теплоты сгорания веществ
- •3. Теплоемкость
- •Расчет тепловых эффектов химических реакций по уравнению Кирхгофа
- •Домашнее задание
Домашнее задание
Сколько теплоты выделится при сгорании 100 г этилового спирта. Значения стандартных теплот сгорания приведены в приложении.
В 100 г шоколада содержится: белка – 5,4 г, жира – 35,4 г, углеводов – 52,6 г. Рассчитайте ценность 550 г конфет в кДж и ккал.
Глицерин – один из продуктов метаболизма, который превращается окончательно в организме в СО2 (г) и Н2О (ж). Вычислите тепловой эффект реакции, пользуясь данными теплот образования веществ.
Вычислить количество теплоты, которое выделится при окислении 90 г глюкозы при с.у. Данные по теплотам образования веществ приведены в приложении.
Определите энергетическую ценность (в кДж и ккал) 250 г молока, содержащего 28% белка, 3,2% жира и 4,7% углеводов.
Рассчитайте тепловой эффект реакции окисления жидкого этанола до ацетальдегида по теплотам сгорания реагентов и продуктов.
Найти теплоту образования сероуглерода используя следующие данные:
Вычислить
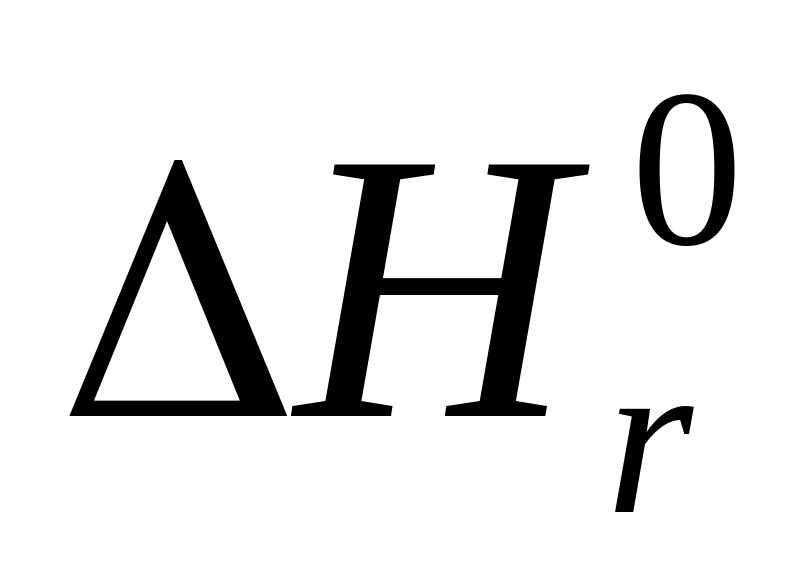 и Q
реакции:
и Q
реакции:
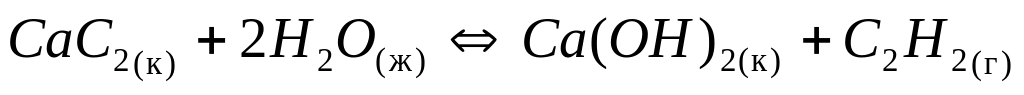 ,
если энтальпии образования
,
если энтальпии образования
 соответственно равны: –62,7; –285,84; –986,2;
226,75 кДж/моль.
соответственно равны: –62,7; –285,84; –986,2;
226,75 кДж/моль.Определить
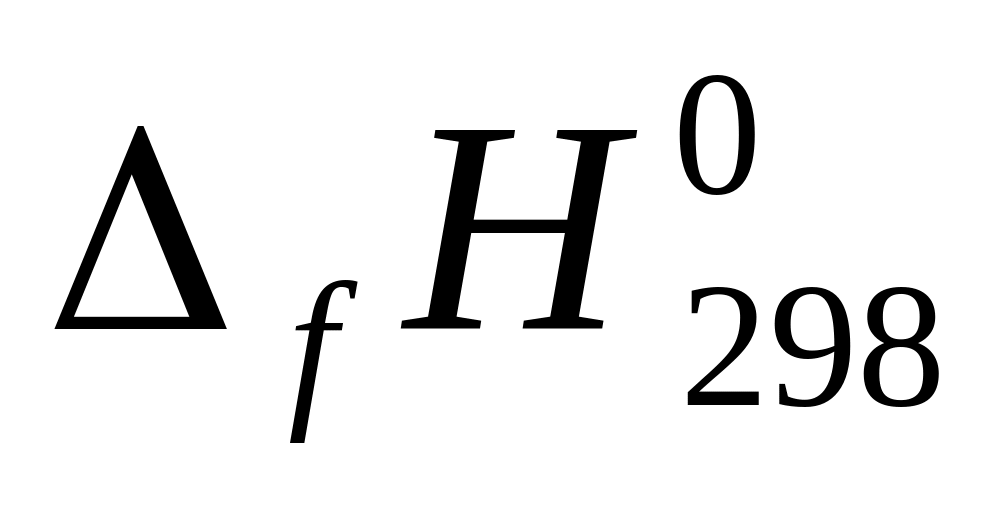 этилена,
используя следующие данные:
этилена,
используя следующие данные:
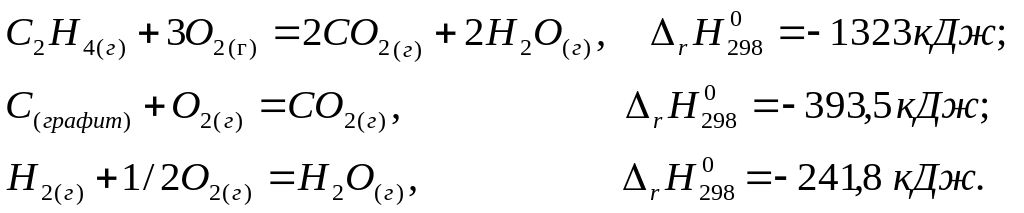
Сожжены с образованием H2O(г) равные объемы водорода и ацетилена, взятых при одинаковых условиях. В каком случае выделится больше теплоты? Во сколько раз?
Теплоты сгорания веществ
Вещество |
Состояние |
|
H2 |
Г |
|
С2Н5ОН |
Ж |
-1370,68 |
СН3СОН |
Г |
-1193,07 |
С6Н12О6 |
Кр. |
-2802,04 |
СН3(СН2)2СООН |
Ж |
-2270,9 |
СН3СН(ОН)СООН |
Ж |
-1777,04 |
C2H2 |
Г |
|
Термодинамические свойства веществ
Вещество |
Состояние |
|
|
|
C6H12O6 |
Кр. |
-1274,5 |
212,1 |
-910,6 |
C6H12O6 |
Водн. |
-1263,8 |
269,5 |
-917,0 |
C2H5OH |
Ж |
-276,98 |
160,67 |
-174,15 |
CO2 |
Г |
--393,51 |
213,66 |
-394,37 |
CH3(CH2)2COOH |
Ж |
-524,30 |
255,00 |
-376,69 |
СН3СН(ОН)СООН |
Ж |
-686 |
222 |
-539 |
H2 |
Г |
0 |
131 |
0 |
H2O |
Ж |
-285,8 |
70 |
-237 |
Глицерин |
Ж |
-668,60 |
204,47 |
-477,07 |
Глицилглицин |
Водн. |
-743,3 |
231,4 |
492,1 |
Глицин |
Водн. |
-523 |
158,6 |
-380 |
О2 |
Г |
0 |
205 |
0 |
CO(NH2)2 |
Кр. |
-333,17 |
104,60 |
-197,15 |
NH3 |
Водн. |
-80,8 |
110 |
-26,6 |
СН4 |
Г |
-85 |
186 |
-51 |
Cl2 |
Г |
0 |
223 |
0 |
CCl4 |
Г |
-107 |
309 |
-64 |
HCl |
Г |
-92,3 |
186,7 |
-95,3 |
СН3СОН |
Г |
-166 |
265 |
-134 |
C2H5OC2H5 |
Ж |
-279,49 |
253,13 |
-123,05 |
