
- •Химия радиоматериалов Лабораторный практикум
- •План лабораторных занятий по химии радиоматериалов
- •Техника безопасности при работе в лаборатории химии общие правила проведения работ
- •Правила техники безопасности
- •Правила противопожарной безопасности
- •Меры первой помощи при несчастных случаях
- •Лабораторная работа № 1
- •Лабораторная работа № 2
- •Часть 1. P-элементы III и IV групп (Алюминий. Углерод)
- •Часть 2. P-элементы V группы (Азот. Фосфор)
- •Часть 3. P-элементы VI группы (Сера)
- •Часть 4. Водород и р-элементы VII группы (Водород. Галогены)
- •Лабораторная работа № 3
- •Часть 1. D-элементы VI и VII групп (Хром. Марганец)
- •Часть 2. D-элементы VIII группы (Железо. Кобальт. Никель)
- •Лабораторная работа №4 определение качественного состава веществ
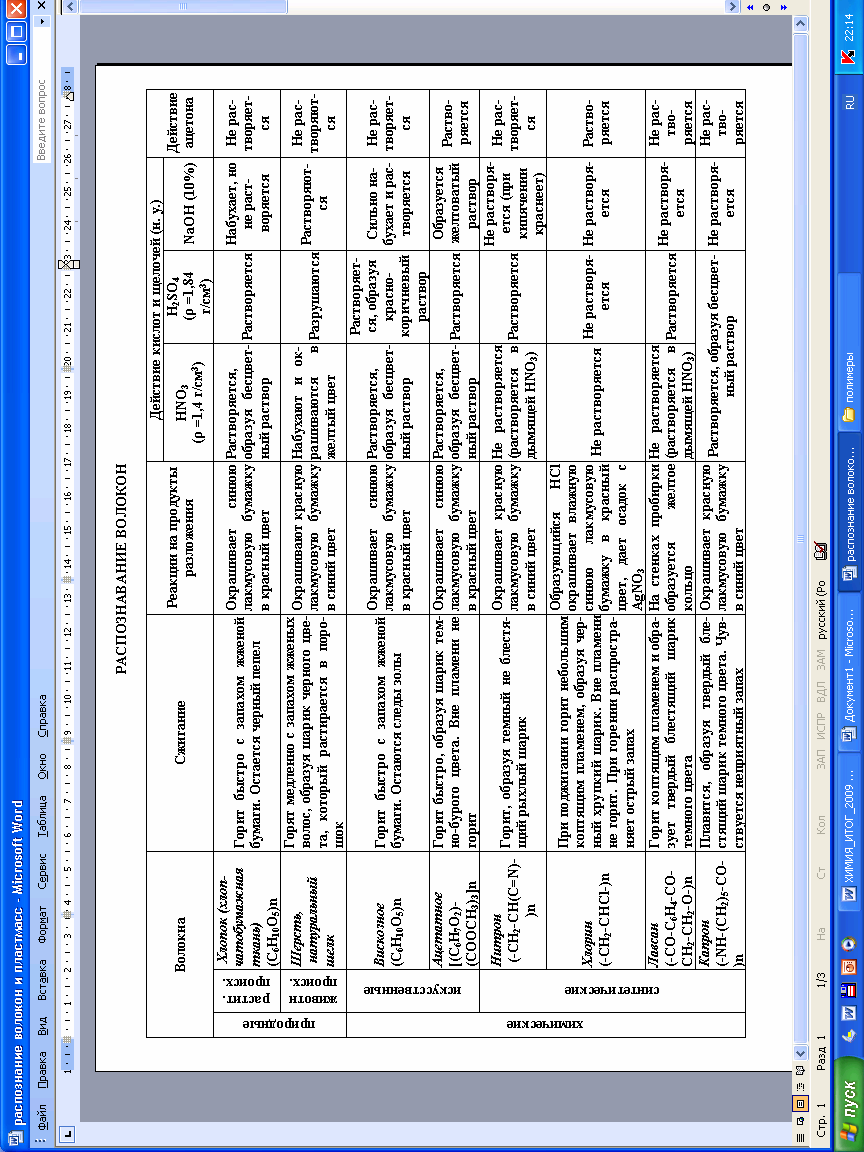
- •Лабораторная работа № 5 высокомолекулярные синтетические соединения (полимеры)
- •Приложения
- •1. Единицы измерения физических величин
- •2. Фундаментальные физические постоянные
- •3. Давление насыщенного водяного пара (р) в равновесии с водой
Приложения
1. Единицы измерения физических величин
Величина |
Единица измерения в СИ |
Связь с другими единицами |
Масса |
килограмм (кг) |
1 кг = 103 г = 106 мг |
Длина |
метр (м) |
1 м = 102 см = 109 нм = 1010Å |
Площадь |
метр2 (м2) |
1 м2 = 104 см2 |
Объем |
метр3 (м3) |
1 м3 = 103 л = 106 см3 |
Давление |
паскаль (Па) |
1 амт = 101325 Па = 760 Торр 1 бар = 105 Па = 0,987 атм = 750 Торр 1 Торр = 1 мм рт. ст. = 133,32 Па |
Энергия |
джоуль (Дж) |
1 Дж = 0,2392 кал = 6,25∙1018 эВ 1 кал = 4,184 Дж 1эВ = 1,60∙10–19 Дж |
2. Фундаментальные физические постоянные
Величина |
Символ |
Значение |
Размерность |
Постоянная Авогадро |
NA |
6,022137∙1023 |
моль–1 |
Постоянная Больцмана |
k |
1,380658∙10–23 |
Дж∙К–1 |
Постоянная Планка |
h |
6,626075∙10–34 |
Дж∙с |
Постоянная Фарадея |
F |
96485,31 |
Кл∙моль–1 |
Элементарный заряд |
e |
1,602177∙10–19 |
Кл |
Скорость света в вакууме |
с |
299792458 |
м∙с–1 |
Газовая постоянная |
R |
8,314510 1,987216 0,082058 |
Дж∙К–1∙моль–1 кал∙ К–1∙моль–1 л∙атм∙К–1∙моль–1 |
3. Давление насыщенного водяного пара (р) в равновесии с водой
t, °C |
p, кПа |
t, °C |
p, кПа |
t, °C |
p, кПа |
10 |
1,2270 |
22 |
2,642 |
32 |
4,753 |
12 |
1,4014 |
24 |
2,982 |
34 |
5,318 |
14 |
1,597 |
25 |
3,166 |
36 |
5,940 |
16 |
1,817 |
26 |
3,360 |
38 |
6,623 |
18 |
2,062 |
28 |
3,778 |
40 |
7,374 |
20 |
2,337 |
30 |
4,241 |
50 |
12,334 |
4. Произведение растворимости (ПР) малорастворимых веществ при 25°C
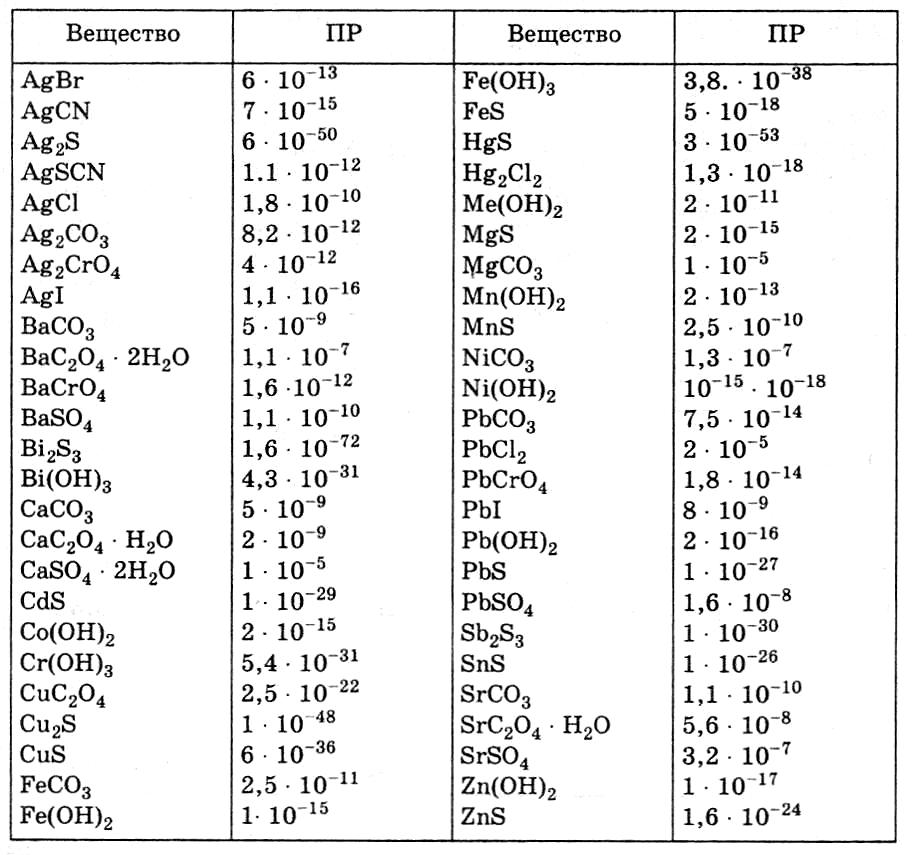
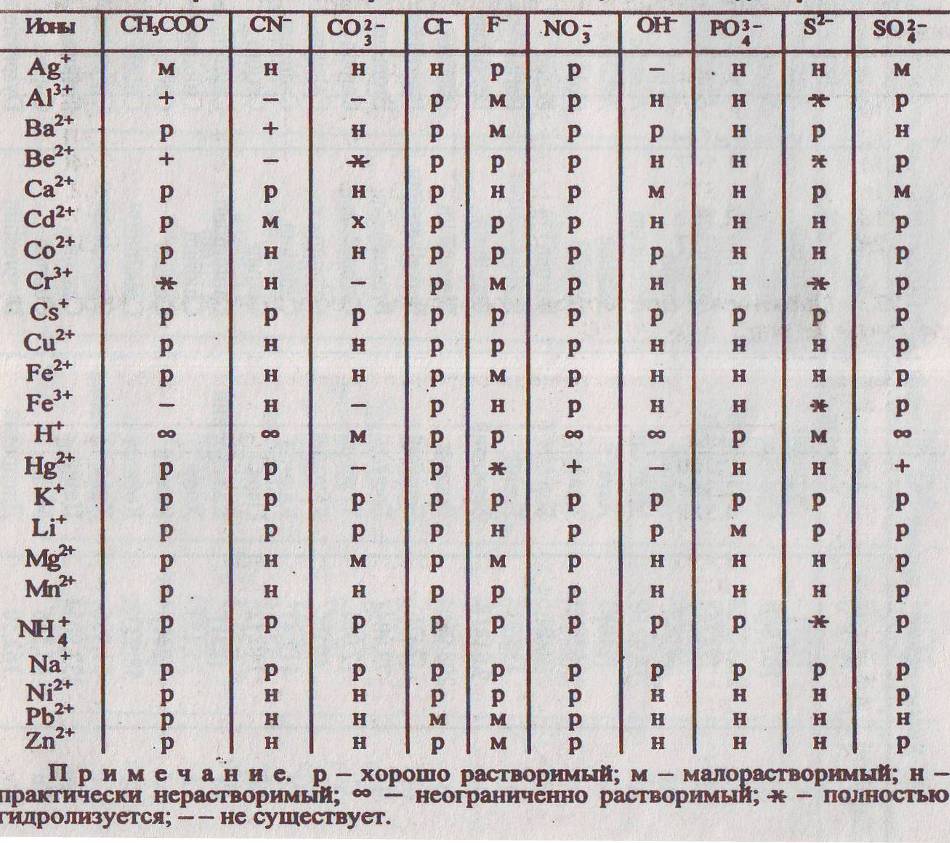
5. Растворимость неорганических веществ в воде при 25°C
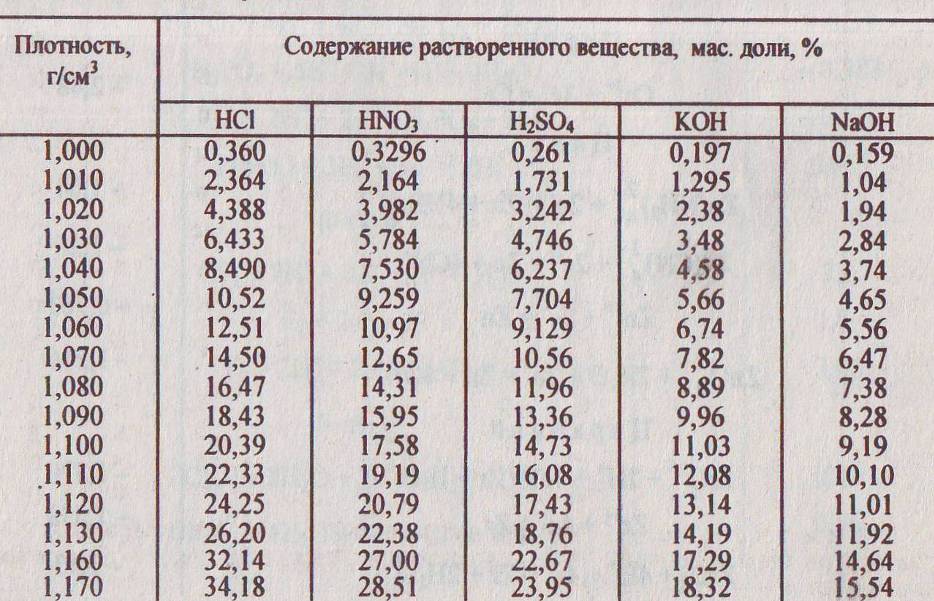
6. Плотность растворов некоторых неорганических кислот
и щелочей в воде при 20°C

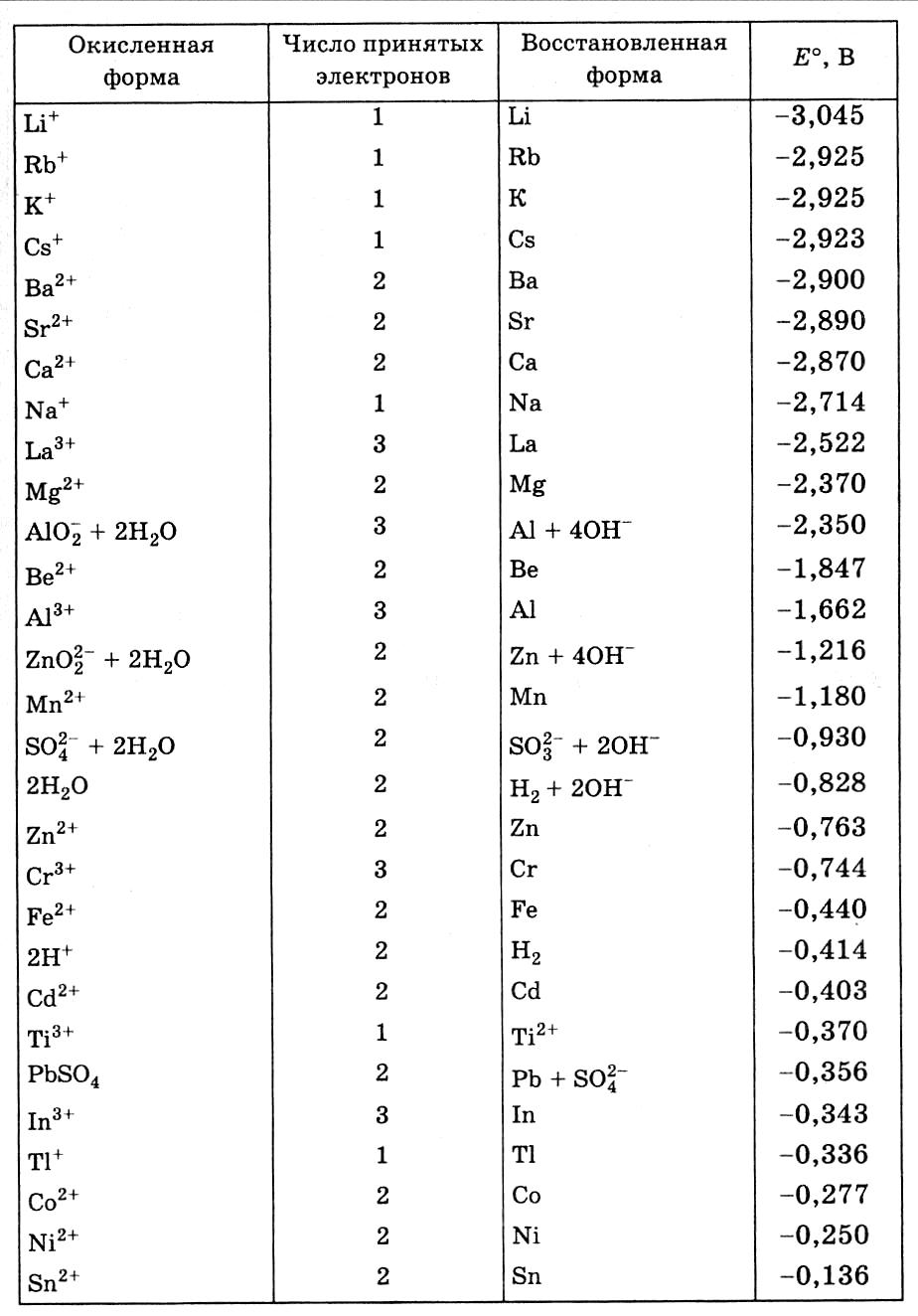
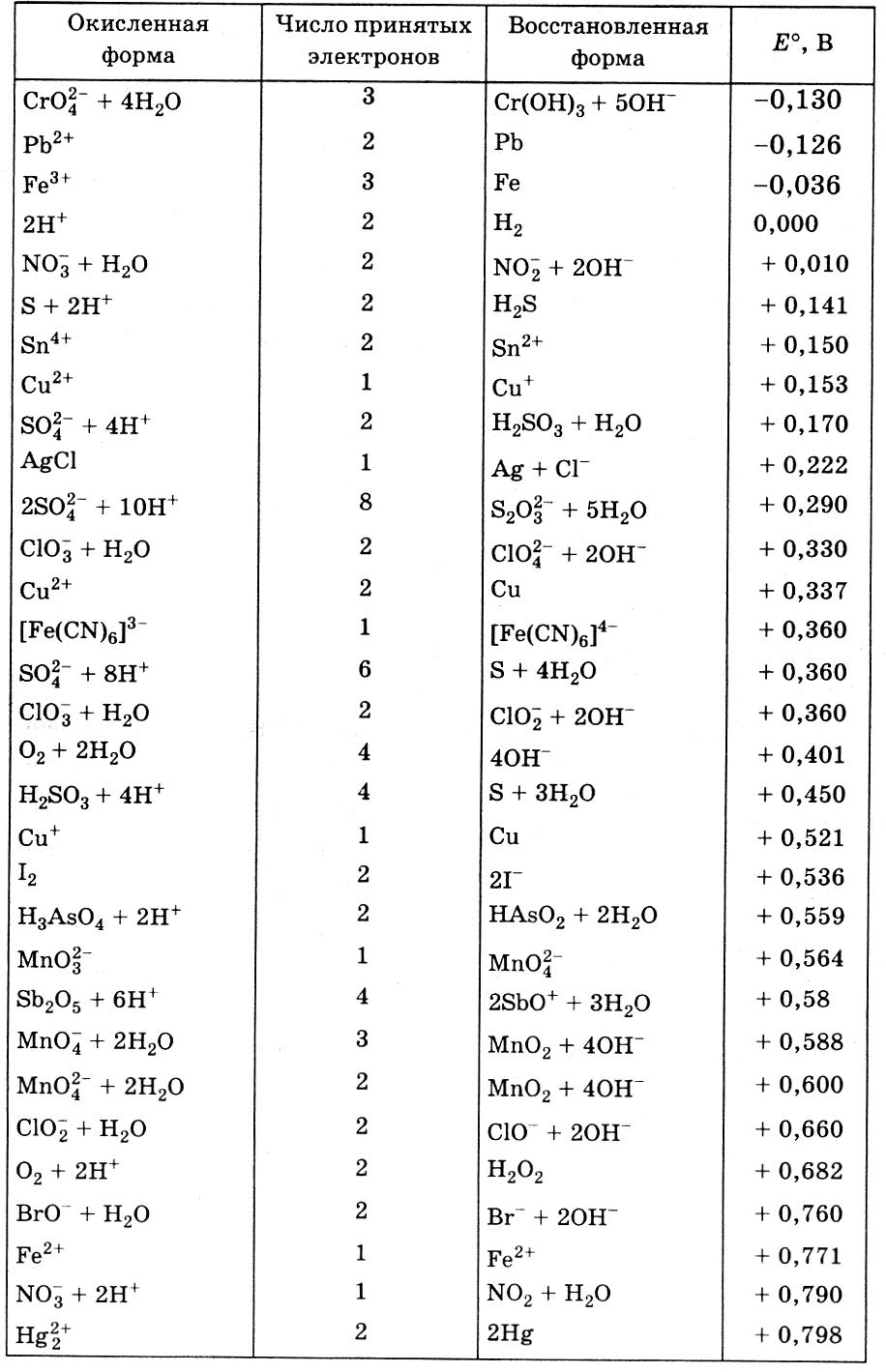
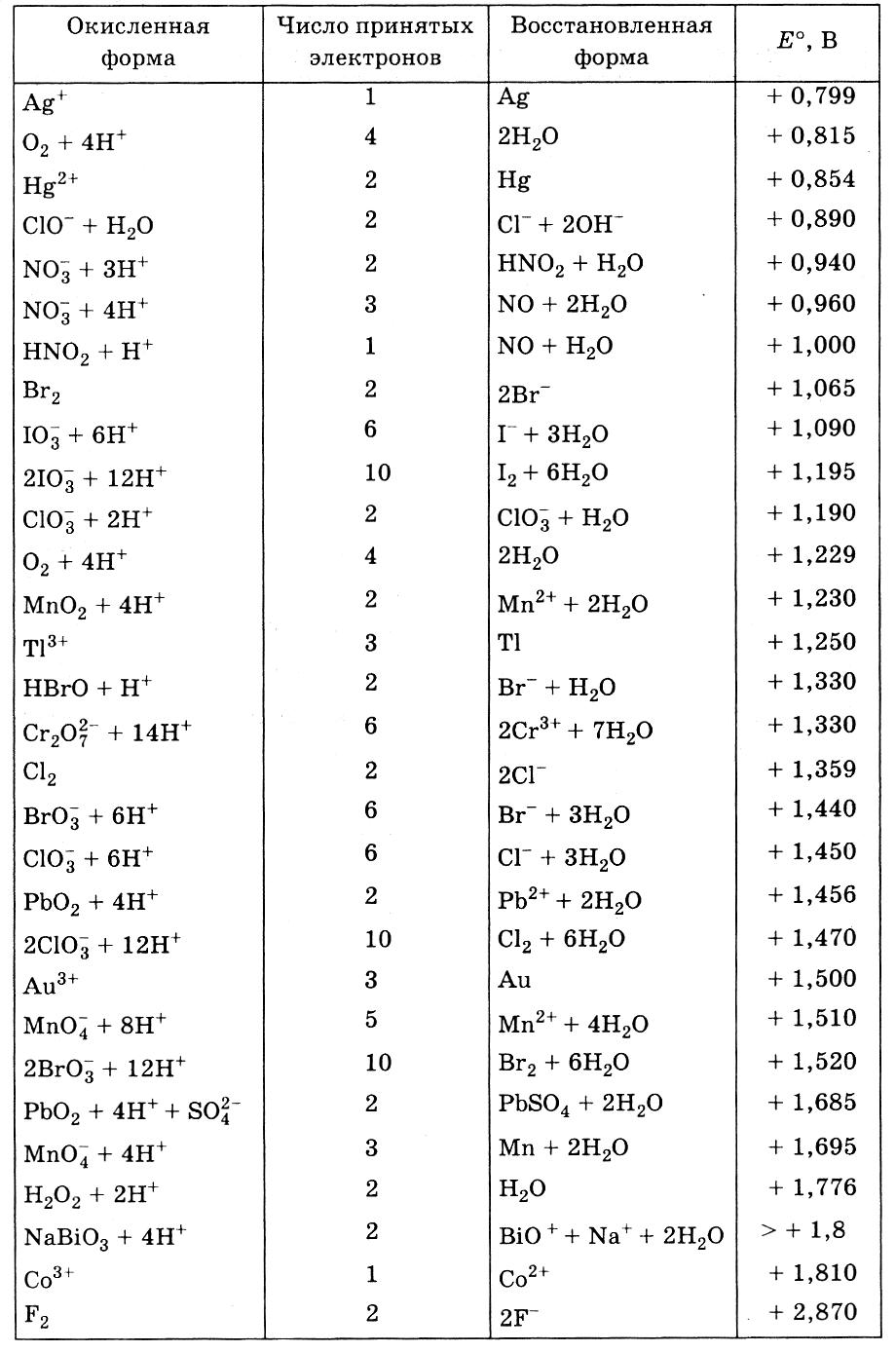
7. Стандартные электродные потенциалы некоторых систем
в водных растворах
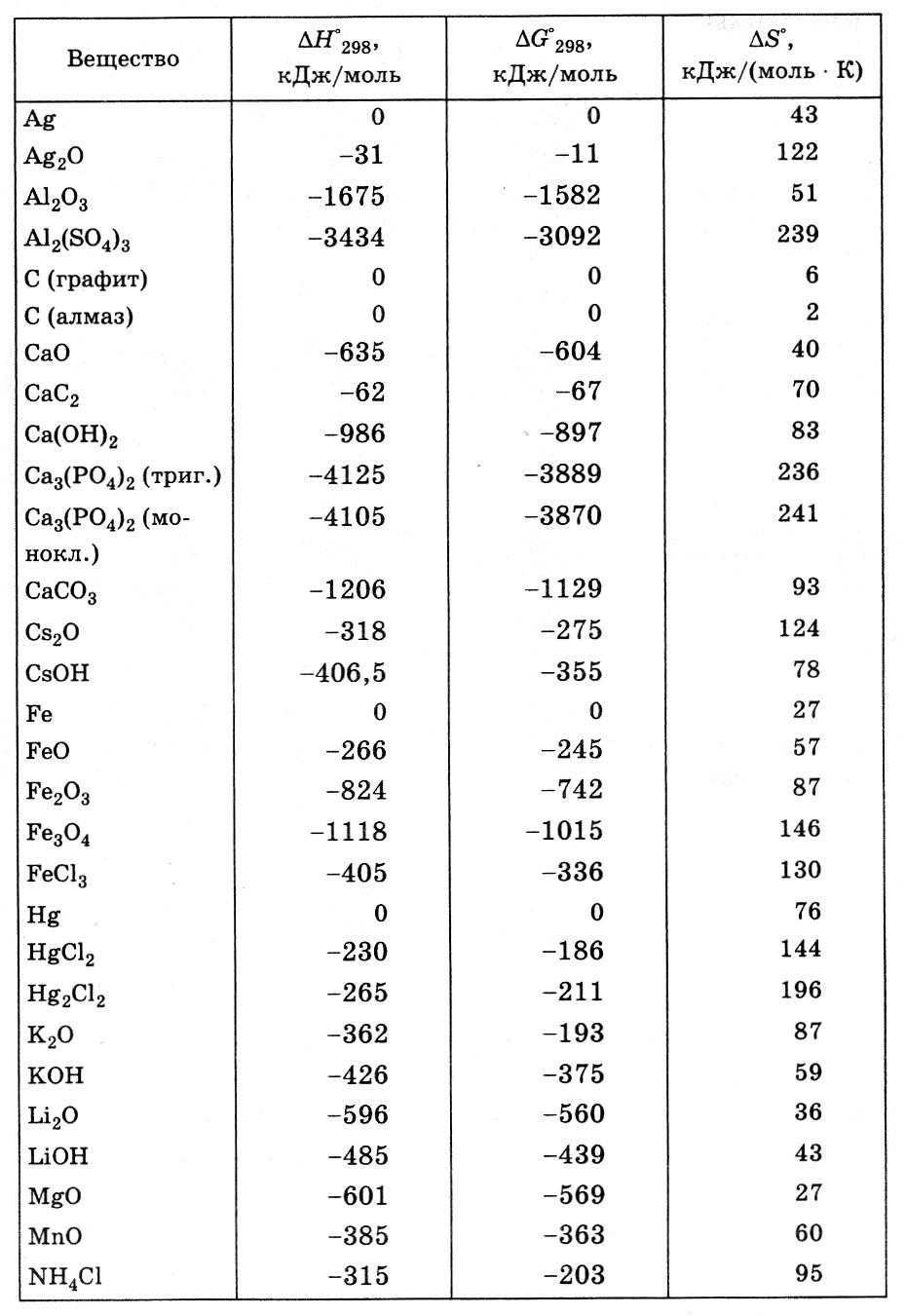
8. Термохимические константы некоторых кристаллических веществ
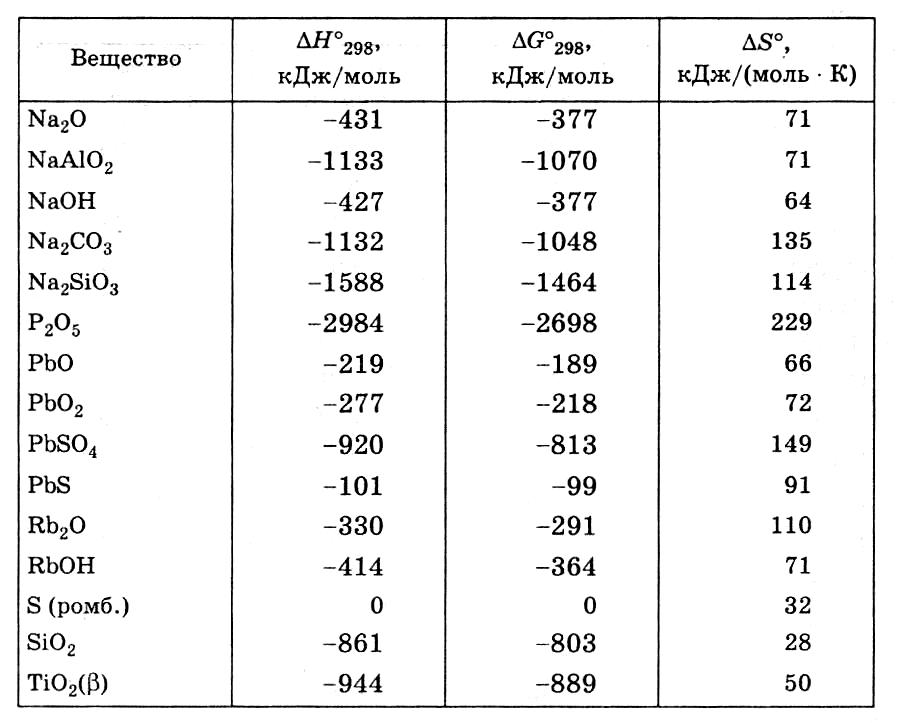
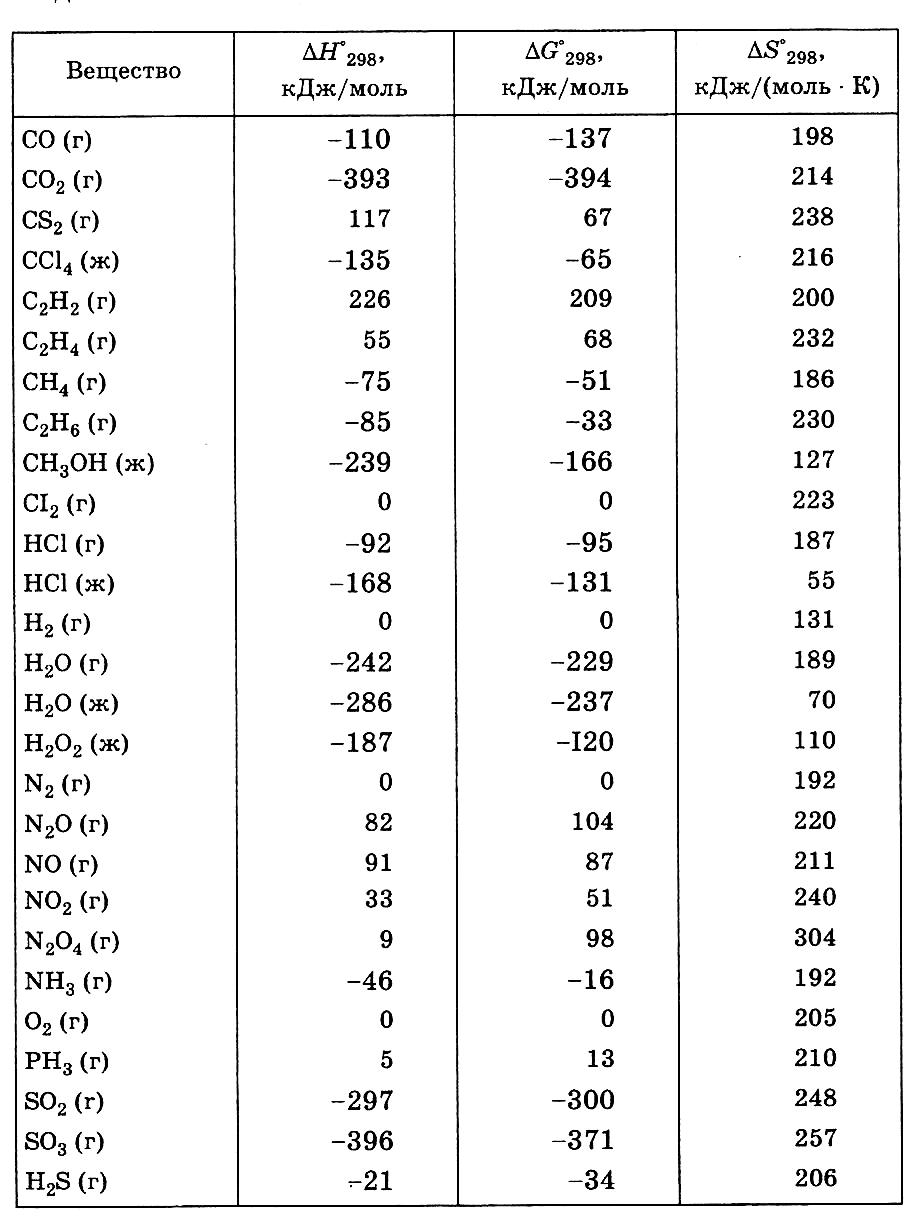
9. Термохимические константы некоторых газообразных и жидких веществ

1 Составьте уравнения реакций, назовите вещества и запишите наблюдения.
2 Составьте уравнения реакций, назовите вещества и запишите наблюдения.
3 Составьте уравнения реакций, назовите вещества и запишите наблюдения.
4 Составьте уравнения реакций, назовите вещества и запишите наблюдения.
5 Составьте уравнения реакций, назовите вещества и запишите наблюдения.
6 Составьте уравнения реакций, назовите вещества и запишите наблюдения.
7 Составьте уравнения реакций, назовите вещества и запишите наблюдения.
8Составьте уравнения реакций в молекулярной и сокращенной ионной форме (кроме опыта № 1), запишите наблюдения. Опыты с растворами выполняются полумикрометодом.
9 Составьте уравнения реакций, назовите вещества и запишите наблюдения.
