
- •Лабораторно-практическое занятие № 1 Фармацевтический анализ лекарственных средств группы карбоновых кислот и их производных
- •Калия ацетат (Kalii acetas)
- •Красно-бурый
- •Катион ацетония
- •Кальция лактат (Calcii lactas)
- •Натрия цитрат (Natrii citras)
- •Тринатриевая соль 2-гидроксипропан-1,2,3-трикарбоксилат
- •Кальция глюконат (Calcii gluconas)
- •Определение подлинности проводят по иону кальция и аниону глюконовой кислоты.
- •Спектр стандартного образца кальция глюконата.
- •Оценка чистоты. Для субстанции значение pH 2% водного раствора 6,0-7,2.
- •Количественное определение проводят методом комплексонометрического титрования. Натрия вальпроат (Natrii valproat)
- •Натриевая соль 2-пропилпентаноата
- •Аскорбиновая кислота (Acidum ascorbinicum )
- •1. Семинар - 90 мин
- •Контрольный тест – 15 мин
- •Лабораторная работа – 45 мин Фармацевтический анализ лекарственных средств группы карбоновых кислот и их производных
- •2.2. Подлинность
- •4. Защита лабораторной работы – 30 мин.
Лабораторно-практическое занятие № 1 Фармацевтический анализ лекарственных средств группы карбоновых кислот и их производных
Цель: Освоить методы контроля качества и стандартизации лекарственных средств группы карбоновых кислот и их производных по показателям «описание», «подлинность», «чистота», «содержание действующего вещества».
Структура занятия:
1. Семинар - 90 мин
2. Контрольный тест - 15 мин
3. Лабораторная работа – 45 мин
4. Защита лабораторной работы – 30 мин.
Карбоновые кислоты – это соединения, в которых функциональной группой является карбоксильная группа –СООН.
По физическим свойствам монокарбоновые кислоты алифатического ряда с числом атомов от 1 до 9 представляют собой бесцветные жидкости. Высшие алифатические, ароматические и практически все дикарбоновые кислоты – твердые вещества.
В карбоновых кислотах содержится ОН-кислотный центр, поэтому в растворах происходит их ионизация:

Карбоновые кислоты – слабые кислоты: например рКа(НСООН)=3,75, рКа(СН3СООН)=4,76. С увеличением алкильного радикала, обладающего электронодонорными свойствами, константа ионизации кислоты уменьшается.
Программа по дисциплине «Фармацевтическая химия» включает следующие лекарственные средства: калия ацетат, кальция лактат, натрия цитрат, кальция глюконат, натрия вальпроат, аскорбиновая кислота.
Калия ацетат (Kalii acetas)

C2H3KO2 Mr 98,1
Применяется как мочегонное средство, главным образом при отёках, связанных с нарушением кровообращения; как источник ионов калия при гипокалиемии.
Описание. Калия ацетат представляет собой белый кристаллический порошок без запаха или со слабым запахом уксусной кислоты. Гигроскопичен, на воздухе расплывается.
Очень легко растворяется в воде, легко – в спирте. Водные растворы имеют нейтральную или слабощелочную реакцию.
Определение подлинности проводят по ацетат-иону и по иону калия.
Реакции на ацетат-ион:
Образование сложного эфира – этилацетата (специфический фруктовый запах):
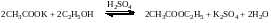
Реакция с FeCl3:
Fe3+ + CH3COO- ® Fe(CH3COO)3
Fe(CH3COO)3 + 2H2O ® Fe(OH)2(CH3COO)↓ + 2CH3COOH
Красно-бурый
При нагревании со щавелевой кислотой образуется уксусная кислота, обладающая характерным запахом:
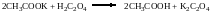
Реакции на ион калия:
С виннокаменной кислотой (при охлаждении) образуется осадок гидротартрата калия:
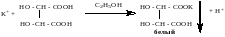
С натрия гексанитрокобальтатом(III) в уксуснокислой среде (рН 4-6) образуется кристаллический осадок:
2K+ + Na+ + [Co(NO2)6]3- ® K2Na[Co(NO2)6]¯
желтый
При внесении солей калия в пламя горелки, оно окрашивается в фиолетовый цвет.
Оценка чистоты. Раствор, полученный растворением 1 г субстанции в 20 мл воды, не содержащей CO2, имеет pH = 7,5-9. Допустимые примеси: хлориды, сульфаты, натрий, железо, тяжёлые металлы, восстанавливающие вещества, алюминий.
Количественное определение проводят методом кислотно-основного титрования в неводной среде. Титрантом является раствор HClO4 в ледяной уксусной кислоте. Индикатор – кристаллический фиолетовый: в точке эквивалентности наблюдают переход окраски из фиолетовой в зеленовато-желтую.
В титруемом растворе образуется ионная пара:
CH3COOK + CH3COOH CH3COOKH+∙CH3COO-
Титрант с растворителем также дают ионную пару:
СH3COOH + HClO4 CH3COOH2+ ∙ClO4-
