
- •1.Типы связующих, применяемых для получения армированных пластиков. Способы их совмещения с наполнителем.
- •2.Эпоксидные смолы
- •3. Полиамиды. Способы получения. Свойства и применение. Особенности переработки.
- •Производство и свойства полигексаметиленадипамида (анид, найлон 66, п-66).
- •Свойства и применение полиамидов
- •4.Полиэтилентерефталат Произв-во плёнок и волокон. Св-ва, переработка и применение.
- •Производство полиэтилентерефталата
- •6. Химические превращения пол-в: полимераналогичные превращения полимеров. Влияние различных факторов на реакционную способность макромолекул.
- •7. Радикальная полимеризация. Мономеры. Элементарные стадии процесса. Реакции передачи цепи.
- •8. Технология пластмасс. 8 вопрос
- •9 Анионная полимеризация. Типы инициирования. Полимеризация без обрыва цепи («живущие» полимеры).
- •10. Сополимеры. Состав и строение сополимеров. Технологические приемы получения блочных и привитых сополимеров.
- •11. Поликонденсация. Типы реакций. Мономеры. Элементарные стадии процесса. Равновесная поликонденсация. Технические приемы проведения.
- •Равновесная поликонденсация
- •12. Неравновесная поликонденсация. Технические приемы проведения. Неравновесная поликонденсация (нпк ) на границе раздела фаз «ж– ж»; «ж–г»; эмульсионное.
- •13 Растворы полимеров
- •Растворимость прежде всего зависит от химической природы полимерного в-ва. Полимер растворяется в веществе, близком по хим. Природе, и не растворяется в неподобном.
- •Наличие поперечных хим. Связей. Такие полимеры не растворяются, а только ограниченно набухают в подходящем раствор-ле.
- •Температура.
- •14. Поликондесация. Характеристика полимеров для поликонденсации. Типы реакций: равновесная, неравнов-я.
- •15. Получение ориентированных полимеров при синтезе и в условиях течения полимеров. Свойства ориентированных полимеров.
- •17. Номенклатура и классификация полимеров по происхождению, химическому составу, способу получения, полярности цепи, по поведению при переработке.
- •18. Получение полистирола блочным методом.
8. Технология пластмасс. 8 вопрос
Катионная полимеризация – процесс, в котором активная растущая частица несет положительный заряд. Обычно к катионной полимеризации относят все случаи образования полимера под действием катализаторов полимеризации , имеющих кислотный характер.
Мономеры. Под действием катализаторов катионного типа полимеризуется широкий круг органических веществ. Все эти вещества можно разделить на 2 класса:
1) ненасыщенные соединения, образующие полимеры за счет раскрытия двойных или тройных связей (этилен и его производные с алкильным и фенильным заместителем, полиены, алифатические альдегиды и кетоны).;
2) циклические соединения, образующие линейные полимеры за счет разрыва цикла (циклопропан, простые циклические эфиры, тиоэфиры, лактоны, лактамы).
При катионной полимеризации растущая цепь имеет положительный заряд. Катализаторами КП с точки зрения электрон. теории кислот и оснований являются кислоты Льюиса- т.е. акцепторы электронов. Наиболее распр. катализаторами явл.:
протонные кислоты НСlО4, Н2SO4, Н3РО4, НСl.
апротонные кислоты- кислоты Льюиса, катализаторы Фриделя-Крафта, относ. обычно к группе коардинацион. ненасыщен. солей и металлов МеХп, Х-галоген: ВF3, AlCl3, SnCl4, TiCl4, FeCl3.
Катализаторы 2-ой группы активны в присутствии сокатализаторов, к которым относятся галоген-алкилы, вода, спирты и др. соединения- доноры ионов водорода. Различные катализаторы проявляют различную активность, количественное сравнение их активности затруднено, т.к. механизм их действия в разных системах различен. В подавляющем большинстве случаев наиболее активны апротонные кислоты, которые обеспечивают высокую скорость процесса и приводят к образованию неразветвленных полимеров высокой молекулярной массы.
Реакция инициирования КП заключается во взаимодействии катиона с мономером. В некоторых случаях катионы образуются при диссоциации катализаторов НСlO4↔H++ClO4-, однако гораздо чаще катионы образ. в результате диссоциации комплекса катализатора и сокатализатора
ВF3 + H2O → ВF3 • H2O →[ ВF3OH]-H+
При взаимодействии с мономером катионы смещают на себя электрон. плотность Н-связи с последующим образованием σ-связи катиона с β-углеродным атомом мономера (по отношению к заместителю). +
[ ВF3OH]-H+ + СН2=СН → H – CH2 – CH [ВF3OH]-
R R
Рост цепи КП происходит путем присоединения мономера к макрокатионам или путем его внедрения по ионной паре, наход. на концах растущих цепей.
Н[CH2 – CHR]nCH2- C+HR[ВF3OH]-+СН2=СНR → H[CH2-CHR]n+1CH2-C+HR [ВF3OH]-
Скорость роста цепи при КП зависит от степени раздел. ионов в ионной паре – наиболее активные свободные ионы, поэтому увеличение полярности растворителя, как правило, увеличивает скорость КП, вследствие увеличения степени полимеризации ионной пары. Характерной особенностью КП является наличие отрицательных значений энергии активации, что также связано с диссоциацией ионной пары, поскольку эта реакция- экзотермическая.
Обрыв цепи.КП чаще всего является мономолекулярной реакцией дезактивации активного центра путем внутримолекулярной передачи катиона водороду.
~ СН2 – C+ HR[ВF3OH]- → ~ СН2 = СНR + ВF3 • H2O
Передача цепи на мономер играет исключительную роль в КП, поскольку она определ. предельное значение молекулярной массы полимера. Эта реакция протекает в результате межмолекулярной передачи катиона – водороду.
~ СН2 – C+HR[ВF3OH]- + СН2 = СНR → ~ СН = СНR + СН3 – C+HR[ВF3OH]-
Обычно энергия активации катионной передачи цепи положительна, поэтому для увеличения молекулярной массы образов. полимера КП проводят при низких температурах до -800С. Поскольку суммарная энергия активации КП отрицательная, понижение температуры приводит обычно к увеличению молекулярной массы и к увеличению скорости процесса.
КП имеет преимущества по сравнению с радикальной, не только в скорости процесса, но и в том, что полимер образует более регулярную структуру (присоединение голова к хвосту), поскольку в КП катализатор учавствует на всех стадиях процесса.
Кинетика КП. Может быть записана в виде след. реакций:
Uин= Кин [кат] [M]
Uр= Кр [кат М+] [M]
Uобр= Кобр [кат М+]
Степень полимеризации определ. по уравнению:
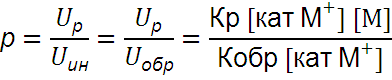
Uобщ= р • Uин
Особенности КП.
Очень высокие скорости процесса при низких температурах.
Молекулярная масса полимера ниже, чем при радикальной полимеризации, поскольку протекает в реакционной среде, содерж. воду, кислоты.
Макромолекулы, полученные при КП отличаются регулярностью построения цепи, т.к. присоединение происходит четко по типу голова к хвосту, что обуславливает лучшие свойства полимера, не смотря на его меньшую молекулярную массу.
