
- •Вступ. Значення легованих сталей у сучасній техніці і промисловості
- •1. Легуючі елементи і домішки
- •1.1.Легування, мікролегування і модифікування
- •1.2 Маркірування сталей
- •1.3 Класифікація легуючих елементів по впливу на α- і γ-області
- •1.3.1. Легуючі елементи, що розширюють γ-область
- •1.3.2. Легуючі елементи, що звужують γ-область
- •1.4. Вплив легуючих елементів на критичні крапки сталі
- •1.4.1 Вплив на температуру евтектоідного перетворення
- •1.4.2 Вплив на концентрацію вуглецю в крапках s і e
- •2. Фази в легованих сталях
- •2.1. Карбідна фаза в легованій сталі
- •2.1.1. Умови карбидоутворення
- •2.1.2. Кількісний склад карбідної фази
- •2.1.3 Розчинні і нерозчинні карбіди
- •2.1.4 Дисперсійне твердіння
- •2.1.5 Вплив надлишкових карбідів
- •2.2. Тверді розчини в легованих сталях
- •2.2.1. Взаємна розчинність компонентів у сталі
- •2.2.2. Тверді розчини заміщення
- •2.2.3. Тверді розчини впровадження
- •2.3. Структура і властивості легованого фериту
- •2.4. Структура і властивості легованого аустеніту
- •2.4.1 Легування стабільного аустеніту
- •2.4.2. Легування метастабільного аустеніту
- •2.5 Термодинамічна активність вуглецю в залізі
2.1.5 Вплив надлишкових карбідів
Надлишкові карбіди (нерозчинні при нагріванні до високих температур) значно, часто на кілька порядків крупніше, ніж розчинні, що особливо виділилися з мартенситу при відпустці.
Тому що вони не розчиняються при нагріванні під загартування, то їхні розміри, форма і розподіл по об’єму зберігаються після термообробки такими ж, якими вони були після кристалізації і пластичної деформації. Оскільки вони не змінюють склад твердого розчину, те їхня роль у сталі менша й інша, чим розчинних карбідів.
Впливати на ці карбіди термічною обробкою можна лише шляхом гомогенізації (для литих і мало деформованих сталей).
Нерозчинні карбіди перешкоджають росту зерна при нагріванні стали слабкіше, ніж розчинні. Вони можуть підвищувати зносостійкість і міцність стали, перешкоджаючи її пластичної течі.
Але в будь-якому випадку дисперсійне твердіння, зміцнення, стримування росту зерна в легованих сталях відбувається в основному за рахунок вторинних розчинних карбідів.
2.2. Тверді розчини в легованих сталях
2.2.1. Взаємна розчинність компонентів у сталі
У сталях можливі три випадки розчинності:
- компоненти практично не розчиняються друг у друзі; при цьому утворюється гетерогенна суміш компонентів зі своїми кристалічними гратами (наприклад, РЬ, S, Zr, Gf, Та, Ві у залізі);
- компоненти необмежено розчиняються друг у друзі; при цьому утворюються загальні кристалічні грати - безперервний твердий розчин (наприклад, Fe-Cr, Fe-V, Fe- Mn, Fe-Ni, Fe-Со); можливе утворення у твердому розчині проміжних інтерметалідних з'єднань;
- компоненти обмежено розчинні друг у друзі; утворюється обмежений твердий розчин із гратами розчинника; величина розчинності різна для кожної системи.
У більшості систем на основі заліза утворяться обмежені тверді розчини. У свою чергу вони поділяються на:
- розчини із широкою областю гомогеності (більше 2% розчинених легуючих елементів у залізі);
- розчини з вузькою областю гомогеності (0,2-2% розчинених елементів у залізі).
2.2.2. Тверді розчини заміщення
Утворення твердих розчинів підкоряється законові Юм-Розері.
Відповідно до цього закону, основними умовами утворення розчинів заміщення є:
ізоморфізм (однотипність грат компонентів);
співвідношення атомних розмірів компонентів (±8% - для необмежених розчинів і ±15% - для обмежених твердих розчинів);
близька електронна структура, тобто відносне розташування компонентів у періодичній системі Менделєєва.
Відповідно до першої умови Юм-Розери тверді розчини заміщення з залізом утворять:
Ni, Co, Мn - безперервні розчини на основі γ-Fе;
Cr, V - безперервні розчини на основі α-Fе.
У відповідності з другою умовою:
-Ni,
Co,
Mn
мають відношення
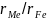 = 0,92-1,08 і утворюють необмежені тверді
розчини;
= 0,92-1,08 і утворюють необмежені тверді
розчини;
Мо, W мають відношення = 0,89-1,11 і утворюють обмежені тверді розчини;
Ті, Nb, Та мають радіуси на межі розмірного фактора й утворюють обмежені розчини з вузькою областю гомогеності або практично не розчинні в залізі.
Відповідно до третьої умови Юм-Розері найбільшу розчинність у залізі мають найбільш близькі до нього елементи V-VІІІ груп з малим розходженням у будівлі зовнішніх d- і s-електронних оболонок. Тому що електронна будівля атома визначає атомний радіус, то ця умова перегукується з другою умовою (розмірним фактором).
