
Молекулярная физика и термодинамика
ЗАДАНИЕ
N 9 сообщить
об ошибке
Тема:
Средняя энергия молекул
В
соответствии с законом равномерного
распределения энергии по степеням
свободы средняя кинетическая энергия
молекулы идеального газа при
температуре T равна:  .
Здесь
.
Здесь  ,
где
,
где  ,
,  и
и  –
число степеней свободы поступательного,
вращательного и колебательного движений
молекулы соответственно. Для гелия (
–
число степеней свободы поступательного,
вращательного и колебательного движений
молекулы соответственно. Для гелия ( )
число i равно …
)
число i равно …
|
|
|
3 |
|
|
|
5 |
|
|
|
7 |
|
|
|
6 |
Решение:
Для
статистической системы в состоянии
термодинамического равновесия на каждую
поступательную и вращательную степени
свободы приходится в среднем кинетическая
энергия, равная  ,
а на каждую колебательную степень –
,
а на каждую колебательную степень –  .
Средняя кинетическая энергия молекулы
равна:
.
Здесь
.
Средняя кинетическая энергия молекулы
равна:
.
Здесь  –
сумма числа поступательных, вращательных
и удвоенного числа колебательных
степеней свободы молекулы:
,
где
–
число степеней свободы поступательного
движения, равное 3;
–
число степеней свободы вращательного
движения, которое может быть равно 0, 2,
3;
–
число степеней свободы колебательного
движения, минимальное количество которых
равно 1.
Для гелия
(
) (одноатомной
молекулы)
–
сумма числа поступательных, вращательных
и удвоенного числа колебательных
степеней свободы молекулы:
,
где
–
число степеней свободы поступательного
движения, равное 3;
–
число степеней свободы вращательного
движения, которое может быть равно 0, 2,
3;
–
число степеней свободы колебательного
движения, минимальное количество которых
равно 1.
Для гелия
(
) (одноатомной
молекулы)  ,
,  и
и  .
Следовательно,
.
Следовательно,  .
.
ЗАДАНИЕ
N 10 сообщить
об ошибке
Тема:
Распределения Максвелла и Больцмана
На
рисунке представлены графики функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где  –
доля молекул, скорости которых заключены
в интервале скоростей от
–
доля молекул, скорости которых заключены
в интервале скоростей от  до
до  в
расчете на единицу этого интервала.
в
расчете на единицу этого интервала.
 Для
этих функций верными являются утверждения,
что …
Для
этих функций верными являются утверждения,
что …
|
|
|
распределение 1 соответствует газу, имеющему наибольшую массу молекул |
|
|
|
распределение 3 соответствует газу, имеющему наибольшую температуру |
|
|
|
распределение 1 соответствует газу, имеющему наименьшую массу молекул |
|
|
|
распределение 3 соответствует газу, имеющему наименьшую температуру |
Решение:
Функция
Максвелла имеет вид  .
Полная
вероятность равна:
.
Полная
вероятность равна: ,
то есть площадь, ограниченная кривой
распределения Максвелла, равна единице
и при изменении температуры не
изменяется. Из формулы наиболее вероятной
скорости
,
то есть площадь, ограниченная кривой
распределения Максвелла, равна единице
и при изменении температуры не
изменяется. Из формулы наиболее вероятной
скорости  ,
при которой функция
,
при которой функция  максимальна,
следует, что при повышении температуры
максимум функции сместится вправо,
следовательно, высота максимума
уменьшится. Если сравнивать распределения
Максвелла по скоростям различных газов
при одной и той же температуре, то при
увеличении массы молекулы газа максимум
функции сместится влево, следовательно,
высота максимума увеличится.
максимальна,
следует, что при повышении температуры
максимум функции сместится вправо,
следовательно, высота максимума
уменьшится. Если сравнивать распределения
Максвелла по скоростям различных газов
при одной и той же температуре, то при
увеличении массы молекулы газа максимум
функции сместится влево, следовательно,
высота максимума увеличится.
ЗАДАНИЕ N 11 сообщить об ошибке Тема: Второе начало термодинамики. Энтропия При поступлении в неизолированную термодинамическую систему тепла в ходе обратимого процесса для приращения энтропии верным будет соотношение …
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Решение:
Отношение  в
обратимом процессе есть полный
дифференциал функции состояния системы,
называемой энтропией
в
обратимом процессе есть полный
дифференциал функции состояния системы,
называемой энтропией  системы:
системы:  .
В изолированных системах энтропия не
может убывать при любых, происходящих
в ней процессах:
.
В изолированных системах энтропия не
может убывать при любых, происходящих
в ней процессах:  .
Знак равенства относится к обратимым
процессам, а знак «больше» – к необратимым
процессам. Если в неизолированную
систему поступает тепло и происходит
необратимый процесс, то энтропия
возрастает за счет не только полученного
тепла, но и необратимости процесса:
.
.
Знак равенства относится к обратимым
процессам, а знак «больше» – к необратимым
процессам. Если в неизолированную
систему поступает тепло и происходит
необратимый процесс, то энтропия
возрастает за счет не только полученного
тепла, но и необратимости процесса:
.
ЗАДАНИЕ
N 12 сообщить
об ошибке
Тема:
Первое начало термодинамики. Работа
при изопроцессах
На
рисунке представлена диаграмма
циклического процесса идеального
одноатомного газа:
 За
цикл газ получает количество теплоты
(в
За
цикл газ получает количество теплоты
(в  ),
равное …
),
равное …
|
33 | |
Решение:
Цикл
состоит из изохорного нагревания (4–1),
изобарного расширения (1–2), изохорного
охлаждения (2–3) и изобарного сжатия
(3–4). На первых двух этапах цикла газ
получает теплоту. Согласно первому
началу термодинамики, количество
теплоты, получаемое газом, равно  ,
где
,
где  –
изменение внутренней энергии,
–
изменение внутренней энергии,  –
работа газа. Тогда
–
работа газа. Тогда  .
.
 Таким
образом, количество теплоты, получаемое
газом за цикл, равно
Таким
образом, количество теплоты, получаемое
газом за цикл, равно 
ЗАДАНИЕ
N 21 сообщить
об ошибке
Тема:
Первое начало термодинамики. Работа
при изопроцессах
Диаграмма
циклического процесса идеального
одноатомного газа представлена на
рисунке. Работа газа за цикл (в кДж)
равна …
|
5 | |
Решение:
Работу
газа в циклическом процессе можно найти,
определив площадь, ограниченную кривой
цикла в координатах  Цикл
имеет форму трапеции. Тогда
Цикл
имеет форму трапеции. Тогда 
ЗАДАНИЕ
N 22 сообщить
об ошибке
Тема:
Средняя энергия молекул
Средняя
кинетическая энергия молекул газа при
температуре  зависит
от их конфигурации и структуры, что
связано с возможностью различных видов
движения атомов в молекуле и самой
молекулы. При условии, что имеет место
поступательное, вращательное движение
молекулы как целого и колебательное
движение атомов в молекуле, отношение
средней кинетической энергии колебательного
движения к полной кинетической энергии
молекулы азота (
зависит
от их конфигурации и структуры, что
связано с возможностью различных видов
движения атомов в молекуле и самой
молекулы. При условии, что имеет место
поступательное, вращательное движение
молекулы как целого и колебательное
движение атомов в молекуле, отношение
средней кинетической энергии колебательного
движения к полной кинетической энергии
молекулы азота ( )
равно …
)
равно …
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Решение:
Для
статистической системы в состоянии
термодинамического равновесия на каждую
поступательную и вращательную степени
свободы приходится в среднем кинетическая
энергия, равная
,
а на каждую колебательную степень
– 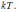 Средняя
кинетическая энергия молекулы равна:
.
Здесь
–
сумма числа поступательных, вращательных
и удвоенного числа колебательных
степеней свободы молекулы:
,
где
–
число степеней свободы поступательного
движения, равное 3;
–
число степеней свободы вращательного
движения, которое может быть равно 0, 2,
3;
–
число степеней свободы колебательного
движения, минимальное количество которых
равно 1.
Для молекулярного азота
(двухатомной молекулы)
,
Средняя
кинетическая энергия молекулы равна:
.
Здесь
–
сумма числа поступательных, вращательных
и удвоенного числа колебательных
степеней свободы молекулы:
,
где
–
число степеней свободы поступательного
движения, равное 3;
–
число степеней свободы вращательного
движения, которое может быть равно 0, 2,
3;
–
число степеней свободы колебательного
движения, минимальное количество которых
равно 1.
Для молекулярного азота
(двухатомной молекулы)
,  и
и  .
Следовательно,
.
Следовательно,  Полная
средняя кинетическая энергия
молекулы азота (
) равна:
Полная
средняя кинетическая энергия
молекулы азота (
) равна:  ,
энергия колебательного движения
,
энергия колебательного движения  ,
тогда отношение
,
тогда отношение  .
.
ЗАДАНИЕ
N 23 сообщить
об ошибке
Тема:
Распределения Максвелла и Больцмана
В
трех одинаковых сосудах находится
одинаковое количество газа, причем 
 На
рисунке представлены графики функций
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
–
доля молекул, скорости которых заключены
в интервале скоростей от
до
в
расчете на единицу этого интервала.
Для
этих функций верными являются утверждения,
что …
На
рисунке представлены графики функций
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
–
доля молекул, скорости которых заключены
в интервале скоростей от
до
в
расчете на единицу этого интервала.
Для
этих функций верными являются утверждения,
что …
|
|
|
кривая
1 соответствует распределению по
скоростям молекул газа при температуре |
|
|
|
кривая
3 соответствует распределению по
скоростям молекул газа при температуре |
|
|
|
кривая 2 соответствует распределению по скоростям молекул газа при температуре |
|
|
|
кривая 3 соответствует распределению по скоростям молекул газа при температуре |
Решение: Полная вероятность равна: , то есть площадь, ограниченная кривой распределения Максвелла, равна единице и при изменении температуры не изменяется. Из формулы наиболее вероятной скорости , при которой функция максимальна, следует, что при повышении температуры максимум функции сместится вправо, следовательно, высота максимума уменьшится.
ЗАДАНИЕ N 24 сообщить об ошибке Тема: Второе начало термодинамики. Энтропия В ходе необратимого процесса при поступлении в неизолированную термодинамическую систему тепла для приращения энтропии верным будет соотношение …
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Решение: Отношение в обратимом процессе есть полный дифференциал функции состояния системы, называемой энтропией системы: . В изолированных системах энтропия не может убывать при любых, происходящих в ней процессах: . Знак равенства относится к обратимым процессам, а знак «больше» – к необратимым процессам. Если в неизолированную систему поступает тепло и происходит необратимый процесс, то энтропия возрастает за счет не только полученного тепла, но и необратимости процесса: .
ЗАДАНИЕ
N 15 сообщить
об ошибке
Тема:
Распределения Максвелла и Больцмана
На
рисунке представлен график функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
–
доля молекул, скорости которых заключены
в интервале скоростей от
до
в
расчете на единицу этого интервала.
 Если,
не меняя температуры взять другой газ
с меньшей молярной массой и таким же
числом молекул, то …
Если,
не меняя температуры взять другой газ
с меньшей молярной массой и таким же
числом молекул, то …
|
|
|
максимум кривой сместится вправо в сторону больших скоростей |
|
|
|
площадь под кривой не изменится |
|
|
|
высота максимума увеличится |
|
|
|
площадь под кривой уменьшится |
Решение: Функция Максвелла имеет вид . Полная вероятность равна: , то есть площадь, ограниченная кривой распределения Максвелла, равна единице и при изменении температуры или массы молекул не изменяется. Из формулы наиболее вероятной скорости , при которой функция максимальна, следует, что при повышении температуры максимум функции сместится вправо, следовательно, высота максимума уменьшится. Если сравнивать распределения Максвелла по скоростям различных газов при одной и той же температуре, то при уменьшении массы молекул газа максимум функции сместится вправо, следовательно, высота максимума уменьшится.
ЗАДАНИЕ
N 16 сообщить
об ошибке
Тема:
Средняя энергия молекул
При
комнатной температуре отношение  молярных
теплоемкостей при постоянном давлении
и постоянном объеме равно
молярных
теплоемкостей при постоянном давлении
и постоянном объеме равно  для …
для …
|
|
|
кислорода |
|
|
|
водяного пара |
|
|
|
углекислого газа |
|
|
|
гелия |
Решение:
Из
отношения 
 найдем
найдем  ,
, 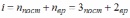 .
Так как 3 поступательные и 2 вращательные
степени свободы имеют двухатомные газы,
следовательно, это кислород.
.
Так как 3 поступательные и 2 вращательные
степени свободы имеют двухатомные газы,
следовательно, это кислород.
ЗАДАНИЕ
N 17 сообщить
об ошибке
Тема:
Второе начало термодинамики. Энтропия
На
рисунке изображен цикл Карно в координатах
(T,
S),
где S –
энтропия. Адиабатное сжатие происходит
на этапе …

|
|
|
4 – 1 |
|
|
|
2 – 3 |
|
|
|
1 – 2 |
|
|
|
3 – 4 |
Решение:
Адиабатные
процессы происходят без теплообмена с
окружающей средой, то есть система не
получает тепла и не отдает его,  Изменение
энтропии определяется как
Изменение
энтропии определяется как  ,
следовательно, при адиабатном процессе
энтропия остается постоянной. При
адиабатном сжатии над газом совершают
работу внешние силы, внутренняя энергия
увеличивается:
,
следовательно, при адиабатном процессе
энтропия остается постоянной. При
адиабатном сжатии над газом совершают
работу внешние силы, внутренняя энергия
увеличивается:  ,
температура газа увеличивается.
Адиабатное сжатие происходит на этапе
4 – 1.
,
температура газа увеличивается.
Адиабатное сжатие происходит на этапе
4 – 1.
ЗАДАНИЕ
N 18 сообщить
об ошибке
Тема:
Первое начало термодинамики. Работа
при изопроцессах
На
(P,V)-диаграмме
изображены 2 циклических процесса.
 Отношение
работ
Отношение
работ  ,
совершенных в этих циклах, равно …
,
совершенных в этих циклах, равно …
|
2 | |
Решение:
Работа
газа в координатных осях  за
цикл численно равна площади фигуры,
ограниченной диаграммой кругового
процесса. При осуществлении кругового
процесса в прямом направлении (по часовой
стрелке) работа газа за цикл положительна,
так как при расширении газ совершает
большую работу, чем затрачивается на
его сжатие. Если круговой процесс
осуществляется в обратном направлении
(против часовой стрелки), то работа газа
за цикл отрицательна. Работы газа в
первом и втором циклах численно равны
площадям прямоугольников:
за
цикл численно равна площади фигуры,
ограниченной диаграммой кругового
процесса. При осуществлении кругового
процесса в прямом направлении (по часовой
стрелке) работа газа за цикл положительна,
так как при расширении газ совершает
большую работу, чем затрачивается на
его сжатие. Если круговой процесс
осуществляется в обратном направлении
(против часовой стрелки), то работа газа
за цикл отрицательна. Работы газа в
первом и втором циклах численно равны
площадям прямоугольников:  и
и  Отношение
работ, совершенных в этих циклах:
Отношение
работ, совершенных в этих циклах: 
ЗАДАНИЕ
N 1 сообщить
об ошибке
Тема:
Первое начало термодинамики. Работа
при изопроцессах
Один
моль идеального одноатомного газа в
ходе некоторого процесса получил  теплоты.
При этом его температура понизилась
на
теплоты.
При этом его температура понизилась
на  .
Работа (
.
Работа ( ),
совершенная газом, равна …
),
совершенная газом, равна … 
|
5000
| |
Решение:
Согласно
первому началу термодинамики,  ,
где
,
где  –
количество теплоты, полученное газом,
–
приращение его внутренней энергии,
–
количество теплоты, полученное газом,
–
приращение его внутренней энергии,  –
работа, совершенная газом. Отсюда
–
работа, совершенная газом. Отсюда  .
Приращение внутренней энергии в данном
случае
.
Приращение внутренней энергии в данном
случае  ,
так как температура газа в ходе процесса
понизилась.
,
так как температура газа в ходе процесса
понизилась.  .
Тогда работа, совершенная газом, равна
.
Тогда работа, совершенная газом, равна 
ЗАДАНИЕ N 2 сообщить об ошибке Тема: Второе начало термодинамики. Энтропия Если КПД цикла Карно равен 60%, то температура нагревателя больше температуры холодильника в ______ раз(а).
|
|
|
2,5 |
|
|
|
3 |
|
|
|
2 |
|
|
|
1,7 |
Решение:
КПД
обратимого цикла Карно равен:  ,
или
,
или  ;
следовательно,
;
следовательно,  ;
отсюда
;
отсюда  и
и 
ЗАДАНИЕ
N 3 сообщить
об ошибке
Тема:
Распределения Максвелла и Больцмана
На
рисунке представлен график функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
–
доля молекул, скорости которых заключены
в интервале скоростей от
до
в
расчете на единицу этого интервала:
 Для
этой функции верными являются утверждения …
Для
этой функции верными являются утверждения …
|
|
|
положение максимума кривой зависит не только от температуры, но и от природы газа (его молярной массы) |
|
|
|
при увеличении числа молекул площадь под кривой не изменяется |
|
|
|
с ростом температуры газа значение максимума функции увеличивается |
|
|
|
для газа с бόльшей молярной массой (при той же температуре) максимум функции расположен в области бόльших скоростей |
Решение:
Из
определения функции распределения
Максвелла следует, что выражение  определяет
долю молекул, скорости которых заключены
в интервале скоростей от
до
(на
графике это – площадь заштрихованной
полоски). Тогда площадь под кривой
равна
и
не изменяется при изменении температуры
и числа молекул газа. Из формулы наиболее
вероятной скорости
определяет
долю молекул, скорости которых заключены
в интервале скоростей от
до
(на
графике это – площадь заштрихованной
полоски). Тогда площадь под кривой
равна
и
не изменяется при изменении температуры
и числа молекул газа. Из формулы наиболее
вероятной скорости  (при
которой функция
максимальна)
следует, что
(при
которой функция
максимальна)
следует, что  прямо
пропорциональна
прямо
пропорциональна 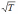 и
обратно пропорциональна
и
обратно пропорциональна  ,
где
и
,
где
и  –
температура и молярная масса газа
соответственно.
–
температура и молярная масса газа
соответственно.
ЗАДАНИЕ N 4 сообщить об ошибке Тема: Средняя энергия молекул Если не учитывать колебательные движения в молекуле углекислого газа, то средняя кинетическая энергия молекулы равна …
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Решение:
Средняя
кинетическая энергия молекулы равна:  ,
где
,
где  –
постоянная Больцмана,
–
термодинамическая температура;
–
сумма числа поступательных, вращательных
и удвоенного числа колебательных
степеней свободы молекулы:
.
Для молекулы углекислого газа
–
постоянная Больцмана,
–
термодинамическая температура;
–
сумма числа поступательных, вращательных
и удвоенного числа колебательных
степеней свободы молекулы:
.
Для молекулы углекислого газа  число
степеней свободы поступательного
движения
,
вращательного –
число
степеней свободы поступательного
движения
,
вращательного –  ,
колебательного –
,
колебательного –  ,
поэтому
,
поэтому  Следовательно,
средняя кинетическая энергия
молекулы
Следовательно,
средняя кинетическая энергия
молекулы  равна:
равна: 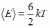 .
.
ЗАДАНИЕ
N 25 сообщить
об ошибке
Тема:
Первое начало термодинамики. Работа
при изопроцессах
Двум
молям водорода сообщили  теплоты
при постоянном давлении. При этом его
температура повысилась на ______ К.
(Считать
связь атомов в молекуле жесткой.
теплоты
при постоянном давлении. При этом его
температура повысилась на ______ К.
(Считать
связь атомов в молекуле жесткой.  )
Ответ
округлите до целого числа.
)
Ответ
округлите до целого числа.
|
10
| |
Решение:
Согласно
первому началу термодинамики, количество
теплоты, получаемое газом, равно
,
где
–
изменение внутренней энергии,
–
работа газа. Количество теплоты,
сообщаемое газу при постоянном давлении
можно представить в виде  Здесь
–
число степеней свободы молекул
двухатомного газа с жесткой связью
атомов в молекуле. Отсюда
Здесь
–
число степеней свободы молекул
двухатомного газа с жесткой связью
атомов в молекуле. Отсюда 
ЗАДАНИЕ N 26 сообщить об ошибке Тема: Второе начало термодинамики. Энтропия Максимальное значение КПД, которое может иметь тепловой двигатель с температурой нагревателя 327°С и температурой холодильника 27°С, составляет ____ %.
|
|
|
50 |
|
|
|
92 |
|
|
|
8 |
|
|
|
46 |
Решение:
КПД
реального теплового двигателя всегда
меньше КПД идеального (обратимого)
теплового двигателя, работающего в тех
же условиях, то есть при одних и тех же
температурах нагревателя и холодильника.
Коэффициент полезного действия идеального
теплового двигателя определяется только
температурами нагревателя и холодильника: .
Таким образом, максимальное значение
КПД, которое может иметь рассматриваемый
тепловой двигатель, равно
.
Таким образом, максимальное значение
КПД, которое может иметь рассматриваемый
тепловой двигатель, равно  .
.
ЗАДАНИЕ N 27 сообщить об ошибке Тема: Распределения Максвелла и Больцмана На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где – доля молекул, скорости которых заключены в интервале скоростей от до в расчете на единицу этого интервала: Для этой функции верными являются утверждения …
|
|
|
положение максимума кривой зависит не только от температуры, но и от природы газа (его молярной массы) |
|
|
|
при увеличении числа молекул площадь под кривой не изменяется |
|
|
|
с ростом температуры газа значение максимума функции увеличивается |
|
|
|
для газа с бόльшей молярной массой (при той же температуре) максимум функции расположен в области бόльших скоростей |
Решение: Из определения функции распределения Максвелла следует, что выражение определяет долю молекул, скорости которых заключены в интервале скоростей от до (на графике это – площадь заштрихованной полоски). Тогда площадь под кривой равна и не изменяется при изменении температуры и числа молекул газа. Из формулы наиболее вероятной скорости (при которой функция максимальна) следует, что прямо пропорциональна и обратно пропорциональна , где и – температура и молярная масса газа соответственно.
ЗАДАНИЕ N 28 сообщить об ошибке Тема: Средняя энергия молекул Если не учитывать колебательные движения в молекуле водорода при температуре 200 К, то кинетическая энергия в (Дж)всех молекул в 4 г водорода равна …
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Решение:
Средняя
кинетическая энергия одной молекулы
равна:
,
где
–
постоянная Больцмана,
–
термодинамическая температура;
–
сумма числа поступательных, числа
вращательных и удвоенного числа
колебательных степеней свободы
молекулы
.
Молекула водорода  имеет
3 поступательные и 2 вращательные степени
свободы, следовательно,
имеет
3 поступательные и 2 вращательные степени
свободы, следовательно, 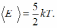 В
4 г водорода содержится
В
4 г водорода содержится  молекул,
где
молекул,
где  масса
газа,
масса
газа,  молярная
масса водорода,
молярная
масса водорода,  число
Авогадро. Кинетическая энергия всех
молекул будет равна:
число
Авогадро. Кинетическая энергия всех
молекул будет равна: 
ЗАДАНИЕ N 17 сообщить об ошибке Тема: Второе начало термодинамики. Энтропия В ходе необратимого процесса при поступлении в неизолированную термодинамическую систему тепла для приращения энтропии верным будет соотношение …
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Решение: Отношение в обратимом процессе есть полный дифференциал функции состояния системы, называемой энтропией системы: . В изолированных системах энтропия не может убывать при любых, происходящих в ней процессах: . Знак равенства относится к обратимым процессам, а знак «больше» – к необратимым процессам. Если в неизолированную систему поступает тепло и происходит необратимый процесс, то энтропия возрастает за счет не только полученного тепла, но и необратимости процесса: .
ЗАДАНИЕ N 18 сообщить об ошибке Тема: Первое начало термодинамики. Работа при изопроцессах Один моль идеального одноатомного газа в ходе некоторого процесса получил теплоты. При этом его температура понизилась на . Работа ( ), совершенная газом, равна …
|
5000
| |
Решение: Согласно первому началу термодинамики, , где – количество теплоты, полученное газом, – приращение его внутренней энергии, – работа, совершенная газом. Отсюда . Приращение внутренней энергии в данном случае , так как температура газа в ходе процесса понизилась. . Тогда работа, совершенная газом, равна
ЗАДАНИЕ
N 19 сообщить
об ошибке
Тема:
Средняя энергия молекул
Отношение
средней кинетической энергии вращательного
движения к средней энергии молекулы с
жесткой связью  .
Это имеет место для …
.
Это имеет место для …
|
|
|
водорода |
|
|
|
водяного пара |
|
|
|
гелия |
|
|
|
метана
( |
Решение:
Средняя
кинетическая энергия молекулы равна:
,
где
–
постоянная Больцмана,
–
термодинамическая температура,
–
сумма числа поступательных, вращательных
и удвоенного числа колебательных
степеней свободы молекулы:
.
Средняя энергия вращательного движения  .
Таким образом, с учетом того что связь
атомов в молекуле по условию является
жесткой (в этом случае
),
отношение
.
Таким образом, с учетом того что связь
атомов в молекуле по условию является
жесткой (в этом случае
),
отношение  .
Отсюда
,
что имеет место для газов с двухатомными
и многоатомными линейными молекулами.
Следовательно, это – водород.
.
Отсюда
,
что имеет место для газов с двухатомными
и многоатомными линейными молекулами.
Следовательно, это – водород.
ЗАДАНИЕ
N 20 сообщить
об ошибке
Тема:
Распределения Максвелла и Больцмана
На
рисунке представлены графики функций
распределения молекул идеального
газа  во
внешнем однородном поле силы тяжести
от высоты
во
внешнем однородном поле силы тяжести
от высоты  для
двух разных газов, где
для
двух разных газов, где  массы
молекул газа (распределение
Больцмана).
массы
молекул газа (распределение
Больцмана).
 Для
этих функций верными являются утверждения,
что …
Для
этих функций верными являются утверждения,
что …
|
|
|
масса |
|
|
|
концентрация
молекул газа с меньшей массой на
«нулевом уровне» |
|
|
|
масса меньше массы |
|
|
|
концентрация молекул газа с меньшей массой на «нулевом уровне» больше |
Решение:
Зависимость
концентрации молекул идеального газа
от высоты
для
некоторой температуры
определяется
распределением Больцмана:  ,
где
,
где  концентрация
молекул на высоте
концентрация
молекул на высоте  ,
,  масса
молекулы,
масса
молекулы, 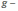 ускорение
свободного падения,
ускорение
свободного падения,  постоянная
Больцмана. Из формулы следует, что при
постоянной температуре концентрация
газа больше там, где меньше потенциальная
энергия его молекул
постоянная
Больцмана. Из формулы следует, что при
постоянной температуре концентрация
газа больше там, где меньше потенциальная
энергия его молекул  ,
и уменьшается с высотой по экспоненциальному
закону. При одной и той же температуре
молекулы, имеющие меньшую массу, более
равномерно распределяются по высоте,
и поэтому концентрация молекул газа на
«нулевом уровне»
уменьшается,
а на высоте
увеличивается.
,
и уменьшается с высотой по экспоненциальному
закону. При одной и той же температуре
молекулы, имеющие меньшую массу, более
равномерно распределяются по высоте,
и поэтому концентрация молекул газа на
«нулевом уровне»
уменьшается,
а на высоте
увеличивается.
ЗАДАНИЕ N 1 сообщить об ошибке Тема: Второе начало термодинамики. Энтропия При плавлении вещества энтропия неизолированной термодинамической системы …
|
|
|
увеличивается |
|
|
|
остается постоянной |
|
|
|
убывает |
|
|
|
может как убывать, так и оставаться постоянной |
Решение: Отношение в обратимом процессе есть полный дифференциал функции состояния системы, называемой энтропией системы: . В изолированных системах энтропия не может убывать при любых, происходящих в ней процессах: . Знак равенства относится к обратимым процессам, а знак «больше» – к необратимым процессам. Разрушение кристаллической решетки при плавлении вещества приводит к возрастанию энтропии, так как если в неизолированную систему поступает тепло и происходит необратимый процесс, то энтропия возрастает за счет не только полученного тепла, но и необратимости процесса: .
ЗАДАНИЕ
N 2 сообщить
об ошибке
Тема:
Распределения Максвелла и Больцмана
На
рисунке представлен график функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
–
доля молекул, скорости которых заключены
в интервале скоростей от
до
в
расчете на единицу этого интервала.
 Для
этой функции неверными являются
утверждения, что …
Для
этой функции неверными являются
утверждения, что …
|
|
|
при понижении температуры величина максимума функции уменьшается |
|
|
|
при понижении температуры площадь под кривой уменьшается |
|
|
|
с ростом температуры наиболее вероятная скорость молекул увеличивается |
|
|
|
положение максимума кривой зависит не только от температуры, но и от природы газа |
Решение: Полная вероятность равна: , то есть площадь, ограниченная кривой распределения Максвелла, равна единице и при изменении температуры не изменяется. Из формулы наиболее вероятной скорости , при которой функция максимальна, следует, что при повышении температуры максимум функции сместится вправо, следовательно, высота максимума уменьшится.
ЗАДАНИЕ N 3 сообщить об ошибке Тема: Средняя энергия молекул Если не учитывать колебательные движения в молекуле водорода при температуре 200 К, то кинетическая энергия в (Дж)всех молекул в 4 г водорода равна …
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ЗАДАНИЕ N 4 сообщить об ошибке Тема: Первое начало термодинамики. Работа при изопроцессах При адиабатическом расширении 2 молей одноатомного газа его температура понизилась с 300 К до 200 К, при этом газ совершил работу (в Дж), равную …
|
2493
| |
Решение:
При
адиабатическом расширении работа газа
находится по формуле: 
ЗАДАНИЕ N 11 сообщить об ошибке Тема: Второе начало термодинамики. Энтропия При поступлении в неизолированную термодинамическую систему тепла в ходе обратимого процесса для приращения энтропии верным будет соотношение …
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ЗАДАНИЕ N 12 сообщить об ошибке Тема: Распределения Максвелла и Больцмана В трех одинаковых сосудах находится одинаковое количество газа, причем На рисунке представлены графики функций распределения молекул идеального газа по скоростям (распределение Максвелла), где – доля молекул, скорости которых заключены в интервале скоростей от до в расчете на единицу этого интервала. Для этих функций верными являются утверждения, что …
|
|
|
кривая 1 соответствует распределению по скоростям молекул газа при температуре |
|
|
|
кривая 3 соответствует распределению по скоростям молекул газа при температуре |
|
|
|
кривая 2 соответствует распределению по скоростям молекул газа при температуре |
|
|
|
кривая 3 соответствует распределению по скоростям молекул газа при температуре |
ЗАДАНИЕ
N 13 сообщить
об ошибке
Тема:
Первое начало термодинамики. Работа
при изопроцессах
Диаграмма
циклического процесса идеального
одноатомного газа представлена на
рисунке. Отношение работы при нагревании
газа к работе при охлаждении по модулю
равно …

|
2
| |
Решение:
Работа
при нагревании газа численно равна
площади под графиком процесса 1 –
2:  Работа
при охлаждении численно равна площади
под графиком процесса 3 – 4:
Работа
при охлаждении численно равна площади
под графиком процесса 3 – 4:  Отношение
работ, совершенных в этих процессах,
равно:
Отношение
работ, совершенных в этих процессах,
равно:  Модуль
отношения:
Модуль
отношения: 
ЗАДАНИЕ
N 14 сообщить
об ошибке
Тема:
Средняя энергия молекул
Молярная
теплоемкость идеального газа при
постоянном давлении равна 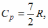 где
где  –
универсальная газовая постоянная. Число
вращательных степеней свободы молекулы
равно …
–
универсальная газовая постоянная. Число
вращательных степеней свободы молекулы
равно …
|
|
|
2 |
|
|
|
3 |
|
|
|
1 |
|
|
|
0 |
ЗАДАНИЕ N 25 сообщить об ошибке Тема: Первое начало термодинамики. Работа при изопроцессах Один моль идеального одноатомного газа в ходе некоторого процесса получил теплоты. При этом его температура понизилась на . Работа ( ), совершенная газом, равна …
|
5000 | |
Решение: Согласно первому началу термодинамики, , где – количество теплоты, полученное газом, – приращение его внутренней энергии, – работа, совершенная газом. Отсюда . Приращение внутренней энергии в данном случае , так как температура газа в ходе процесса понизилась. . Тогда работа, совершенная газом, равна
ЗАДАНИЕ
N 26 сообщить
об ошибке
Тема:
Второе начало термодинамики. Энтропия
На
рисунке изображен цикл Карно в
координатах  ,
где S –
энтропия. Адиабатное расширение
происходит на этапе …
,
где S –
энтропия. Адиабатное расширение
происходит на этапе …
|
|
|
2–3 |
|
|
|
4–1 |
|
|
|
1–2 |
|
|
|
3–4 |
Решение:
Адиабатным
называется процесс, протекающий без
теплообмена с окружающей средой.
Следовательно, для такого процесса
Изменение
энтропии определяется как
,
следовательно, в адиабатном процессе
энтропия остается постоянной. Согласно
первому началу термодинамики, для
адиабатного процесса  .
При адиабатном расширении газ совершает
работу над внешними телами (
.
При адиабатном расширении газ совершает
работу над внешними телами ( ),
следовательно, внутренняя энергия
уменьшается (
),
следовательно, внутренняя энергия
уменьшается ( ).
Это означает, что температура газа
понижается.
Таким образом, адиабатное
расширение происходит на этапе 2–3.
).
Это означает, что температура газа
понижается.
Таким образом, адиабатное
расширение происходит на этапе 2–3.
ЗАДАНИЕ
N 27 сообщить
об ошибке
Тема:
Средняя энергия молекул
При
комнатной температуре отношение
молярных
теплоемкостей при постоянном давлении
и постоянном объеме равно  для …
для …
|
|
|
гелия |
|
|
|
водяного пара |
|
|
|
воздуха |
|
|
|
кислорода |
ЗАДАНИЕ
N 28 сообщить
об ошибке
Тема:
Распределения Максвелла и
Больцмана
Формула  описывает
распределение одинаковых молекул
массой
описывает
распределение одинаковых молекул
массой  по
высоте в изотермической атмосфере;
здесь
по
высоте в изотермической атмосфере;
здесь  –
концентрация молекул при
,
–
их концентрация на высоте
.
Для этой зависимости справедливы
следующие утверждения …
–
концентрация молекул при
,
–
их концентрация на высоте
.
Для этой зависимости справедливы
следующие утверждения …
|
|
|
приведенные
на рисунке кривые соответствуют
распределениям для одного и того же
газа при разных температурах, причем |
|
|
|
приведенные
на рисунке кривые соответствуют
распределениям для двух разных газов
при одинаковой температуре, причем
массы молекул удовлетворяют
соотношению |
|
|
|
приведенные
на рисунке кривые соответствуют
распределениям для одного и того же
газа при разных температурах, причем |
|
|
|
приведенные
на рисунке кривые соответствуют
распределениям для двух разных газов
при одинаковой температуре, причем
массы молекул удовлетворяют
соотношению |
Решение: Зависимость концентрации молекул идеального газа от высоты для некоторой температуры определяется распределением Больцмана: , где концентрация молекул на высоте , масса молекулы, ускорение свободного падения, постоянная Больцмана. Из формулы следует, что концентрация газа уменьшается с высотой по экспоненциальному закону. При одной и той же температуре молекулы, имеющие меньшую массу, вследствие теплового движения более равномерно распределяются по высоте, и поэтому концентрация молекул газа на «нулевом уровне» меньше, чем для более тяжелых молекул (при одинаковом общем количестве молекул). Для молекул, имеющих бόльшую массу, скорость изменения концентрации выше. С другой стороны для одного и того же газа чем выше температура, тем выше интенсивность хаотического теплового движения, и концентрация молекул газа на «нулевом уровне» меньше концентрации тех же молекул при более низкой температуре. При этом скорость уменьшения концентрации при увеличении высоты при боле высокой температуре ниже, то есть экспоненциальный спад более пологий.






















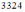


 )
) больше
массы
больше
массы 
 меньше
меньше

 :
:

 :
:

 :
:

