
Вопрос 1.
Электронное
строение атома.



Заряд
n=
элементарному заряду
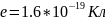
Ядро атома состоит из протонов (Z) и нейтронов(N).Сумма Z и N в ядре ат. - называется массовым числом А. Число е в нейтральном атоме равно числу протонов в яд
Постулаты Бора ре атомов
1) в каждом атоме существует несколько стационарных состояний (говоря языком планетарной модели, несколько стационарных орбит) электронов, двигаясь по которым электрон может существовать, не излучая; 2) при переходе электрона из одного стационарного состояния в другое атом излучает или поглощает порцию энергии. .
Вопрос 2.
Открытие Периодического закона относится к 1869 г. Закон был сформулирован следующим образом: свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов. В настоящее время Периодический закон Д. И. Менделеева формулируется следующим образом: свойства элементов и образуемых ими простых и сложных веществ находятся в периодической зависимости от заряда ядра атомов элементов. В свете учения о строении атома находит объяснение периодическое изменение свойств элементов с ростом заряда ядра, связанных с электронной конфигурацией их атомов.
Вопрос 3.
Двойственность свойств электрона проявляется в том, что он, с одной стороны, обладает свойствами частицы (имеет определенную массу покоя), а с другой - его движение напоминает волну и может быть описано определенной амплитудой, длиной волны, частотой колебаний и др. Поэтому нельзя говорить о какой-либо определенной траектории движения электрона - можно лишь судить о той или иной степени вероятности его нахождения в данной точке пространства.
3 основных идеи квантовой механики.
а)дискретность или квантование
б)корпускулярно волновой дуализм
в)вероятности х-р микромира.
Вопрос 4.
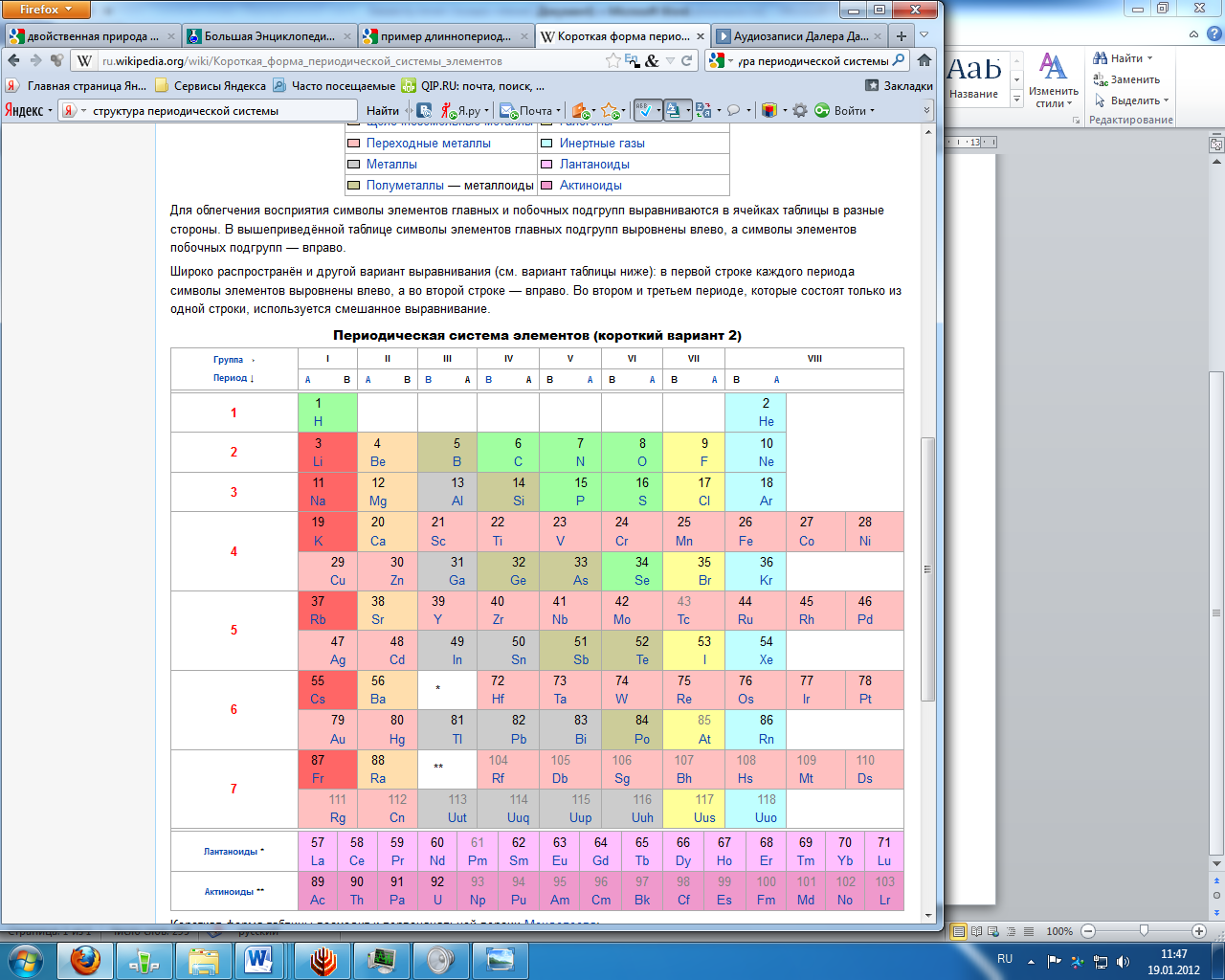
Структура периодической системы элементов
Главный принцип построения Периодической системы - выделение в ней периодов (горизонтальных рядов) и групп (вертикальных столбцов) элементов. Современная Периодическая система состоит из 7 периодов (седьмой период должен закончиться 118-м элементом). Короткопериодный вариант Периодической системы содержит 8 групп элементов, каждая из которых условно подразделяется на группу А (главную) и группу Б (побочную). В длиннопериодном варианте Периодической системы - 18 групп, имеющих те же обозначения, что и в короткопериодном. Элементы одной группы имеют одинаковое строение внешних электронных оболочек атомов и проявляют определенное химическое сходство.
Номер группы в Периодической системе определяет число валентных электронов а атомах элементов. При этом в группах, обозначенных буквой А, содержатся элементы, в которых идет заселение s- и р-подуровней - s-элементы (IA- и IIA-группы) и р-элементы (IIIA-VIIIA-группы), а в группах, обозначенной буквой Б, находятся элементы, в которых заселяются d-подуровни - d-элементы. Поскольку в каждом большом периоде должно находиться по 10 d-элементов (у которых заполняются пять d-орбиталей), то Периодическая система должна содержать 10 соответствующих групп. Однако традиционно используется нумерация групп лишь до восьми, поэтому число групп d-элементов расширяется за счет введения дополнительных цифр - это IБ-VIIБ, VIIIБ0, VIIIБ1 и VIIIБ2-группы. Для f-элементов номеров групп не предусмотрено. Обычно их условно помещают в ячейки Периодической системы, отвечающие лантану (лантаноиды) и актинию (актиноиды). Символы лантаноидов и актиноидов выносятся за пределы Периодической системы в виде отдельных рядов.
Номер периода в Периодической системе соответствует числу энергетических уровней атома данного элемента, заполненных электронами.
Номер периода = Число энергетических уровней, заполненных электронами = Обозначение последнего энергетического уровня
Порядок формирования периодов связан с постепенным заселением энергетических подуровней электронами. Последовательность заселения определяется принципом минимума энергии, принципом Паули и правилом Гунда.
Периодическое изменение свойств элементов в периоде объясняется последовательностью заполнения электронами уровней и подуровней в атомах при увеличении порядкового номера элемента и заряда ядра атома.

Каждому элементу (кроме f-элементов) в Периодической системе соответствуют вполне определенные координаты: номер периода и номер группы. По этим координатам можно не только найти элемент в таблице Д.И. Менделеева, но и построить его электронную конфигурацию, учитывая физический смысл значения чисел, соответствующих номерам периода и группы, а также наличие буквы в номере группы, определяющей принадлежность элемента к секциям s- и p-элементов или d-элементов.
Длиннопериодная
Короткопериодная
Вопроc 5
 (принцип
Гейзенберга)
(принцип
Гейзенберга) -неопределенность,
т.е. ошибка в определении импульса
микрообъекта по координате х.
-неопределенность,
т.е. ошибка в определении импульса
микрообъекта по координате х.

x - неопределённость координаты.
Два следствия из принципа:
а) Движение электрона это движение без траектории отказ в квантовой механике от понятия траектории движения любого микрообъекта связан с наличием у них волновых свойств. Вместо понятия орбита движ. появилось понятие пребывания электрона в определенной части объема атома.
б) электрон в атоме не может упасть на ядро. Падение электрона на ядро существенно бы уменьшило неопределенность его координаты 10000 или 1000 раз, при этом резко должна возрастать неопределенность энергии.
