
- •Вопрос №1
- •Вопрос №2
- •Вопрос №3
- •Вопрос №4
- •Вопрос№5
- •Вопрос№6
- •Вопрос№7
- •Вопрос№8
- •Вопрос№9
- •Вопрос№10
- •Вопрос№11
- •Вопрос№12
- •Вопрос№13
- •Вопрос№14
- •Вопрос№15
- •Вопрос№16
- •Вопрос№17
- •Вопрос№18
- •Вопрос№19
- •Вопрос№20
- •Вопрос№21
- •Вопрос№22
- •Вопрос№23
- •Вопрос№24
- •Вопрос№25
- •Вопрос№26
- •Вопрос№27
- •Вопрос№28
- •Вопрос№29
- •Вопрос№30
- •Вопрос№31
- •Вопрос№32
- •Вопрос№33
- •Вопрос№34
- •Вопрос№35
- •Вопрос№36
Вопрос№34
Обратимые и необратимые процессы, пути изменения состояния термодинамической системы. Процесс называют обратимым, если он допускает возвращение рассматриваемой системы из конечного состояния в исходное через ту же последовательность промежуточных состояний, что и в прямом процессе, но проходимую в обратном порядке. При этом в исходное состояние возвращается не только система, но и среда. Обратимый процесс возможен, если и в системе, и в окружающей среде он протекает равновесно. При этом предполагается, что равновесие существует между отдельными частями рассматриваемой системы и на границе с окружающей средой. Обратимый процесс - идеализированный случай, достижимый лишь при бесконечно медленном изменении термодинамических параметров. Скорость установления равновесия должна быть больше, чем скорость рассматриваемого процесса. Если невозможно найти способ вернуть и систему, и тела в окружающей среде в исходное состояние, процесс изменения состояния системы называют необратимым. Второй закон термодинамики, являясь важнейшим законом природы, определяет направление, по которому протекают термодинамические процессы, устанавливает возможные пределы превращения теплоты в работу при круговых процессах, позволяет дать строгое определение таких понятий, как энтропия, температура и т.д. В этой связи второй закон термодинамики существенно дополняет первый. Энтропией называется термодинамическая величина, изменение которой в системе пропорционально ее тепловой энергии, деленной на абсолютную температуру. Для любого процесса можно найти бесконечно малое изменение энтропии, т. е. ее дифференциал dS=δQ/T, где δQ- элементарная теплота В интегральной форме для любого процесса изменение энтропии равно

Вопрос№35
Т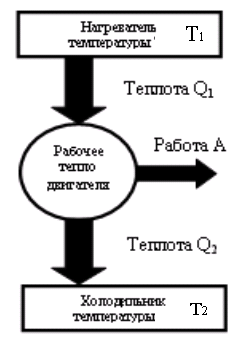 епловые
машины могут иметь разную конструкцию.
Это может быть паровой двигатель,
двигатель внутреннего сгорания,
реактивный двигатель. Любой тепловой
двигатель работает по замкнутому циклу
и имеет нагреватель, рабочее тело
двигателя и холодильник. В процессе
работы теплового двигателя рабочее
тело двигателя получает от нагревателя
количество теплоты Q1,
совершает работу A и передает
холодильнику количество теплоты Q2<Q1.
Для замкнутого цикла изменение внутренней
энергии равно нулю (∆U=0).
Следовательно, согласно I началу
термодинамики, работа, совершаемая
двигателем, равна A=Q1-Q2
Коэффициентом
полезного действия (КПД) теплового
двигателя называется отношение работы,
совершаемой двигателем, к количеству
теплоты, полученному от нагревателя
η=Q1-Q2/Q1
КПД тепловой машины всегда меньше
единицы η=1-Q2/Q1
Следовательно, невозможно всю теплоту
превратить в работу. Ученые всегда
стремились повысить КПД. В первой
половине XIX в. французский ученый Сади
Карно показал, что максимально возможное
значение КПД тепловой машины равно
ηmax=T1-T2/T1=1-T2/T1,
где T1 - температура нагревателя,
T2 - температура холодильника.
Из сравнения уравнений (4.18) и (4.19) следует,
что ηmax ≥ η
или 1-T2/T1≥1Q2/Q1.
Отсюда Q2/T2≥Q1/T1
На основании этого неравенства можно
прийти к понятию энтропия и второму
началу термодинамики. Повышение КПД
тепловых двигателей и приближение его
к максимально возможному значению -
важнейшая техническая задача. Однако,
все тепловые двигатели выделяют большое
количество теплоты, что называется
тепловым загрязнением, и выбрасывают
в атмосферу вредные для растений и
животных химические соединения. Первая
теорема Карно. КПД обратимого цикла
Карно, осуществляемого между двумя
источниками теплоты, не зависит от
свойств рабочего вещества, с помощью
которого этот цикл осуществляется.
Вторая теорема Карно. КПД необратимого
цикла Карно всегда меньше обратимого
цикла Карно, осуществляемого между
одними и теми же источниками теплоты,
имеющими постоянные, но разные температуры.
епловые
машины могут иметь разную конструкцию.
Это может быть паровой двигатель,
двигатель внутреннего сгорания,
реактивный двигатель. Любой тепловой
двигатель работает по замкнутому циклу
и имеет нагреватель, рабочее тело
двигателя и холодильник. В процессе
работы теплового двигателя рабочее
тело двигателя получает от нагревателя
количество теплоты Q1,
совершает работу A и передает
холодильнику количество теплоты Q2<Q1.
Для замкнутого цикла изменение внутренней
энергии равно нулю (∆U=0).
Следовательно, согласно I началу
термодинамики, работа, совершаемая
двигателем, равна A=Q1-Q2
Коэффициентом
полезного действия (КПД) теплового
двигателя называется отношение работы,
совершаемой двигателем, к количеству
теплоты, полученному от нагревателя
η=Q1-Q2/Q1
КПД тепловой машины всегда меньше
единицы η=1-Q2/Q1
Следовательно, невозможно всю теплоту
превратить в работу. Ученые всегда
стремились повысить КПД. В первой
половине XIX в. французский ученый Сади
Карно показал, что максимально возможное
значение КПД тепловой машины равно
ηmax=T1-T2/T1=1-T2/T1,
где T1 - температура нагревателя,
T2 - температура холодильника.
Из сравнения уравнений (4.18) и (4.19) следует,
что ηmax ≥ η
или 1-T2/T1≥1Q2/Q1.
Отсюда Q2/T2≥Q1/T1
На основании этого неравенства можно
прийти к понятию энтропия и второму
началу термодинамики. Повышение КПД
тепловых двигателей и приближение его
к максимально возможному значению -
важнейшая техническая задача. Однако,
все тепловые двигатели выделяют большое
количество теплоты, что называется
тепловым загрязнением, и выбрасывают
в атмосферу вредные для растений и
животных химические соединения. Первая
теорема Карно. КПД обратимого цикла
Карно, осуществляемого между двумя
источниками теплоты, не зависит от
свойств рабочего вещества, с помощью
которого этот цикл осуществляется.
Вторая теорема Карно. КПД необратимого
цикла Карно всегда меньше обратимого
цикла Карно, осуществляемого между
одними и теми же источниками теплоты,
имеющими постоянные, но разные температуры.
