
- •Лекція №14. Поверхневі явища. Адсорбція на межі поділу рухомих фаз
- •За здатністю молекул пар до іонізації їх поділяють на класи:
- •Іоногенні колоїдні пар:
- •Лекція №15. Адсорбція на твердому адсорбенті
- •Теорія мономолекулярної адсорбції (Ленгмюр, 1915):
- •Адсорбція на межі тверде тіло ‑ розчин
- •Лекція №16. Застосування адсорбції
- •Застосування адсорбції
- •Лекція №16. Дисперсні системи. Колоїдні розчини. Методи добування та очищення
- •Грубодисперсні системи
- •Загальна характеристика
- •Очищення колоїдних розчинів
- •Лекція №17. Будова колоїдних частинок. Стійкість колоїдних розчинів. Коагуляція
- •Механізми утворення пеш
- •Стійкість колоїдних розчинів
- •Між колоїдними частинками діють дві взаємно протилежні сили:
- •Стійкість дисперсної системи
- •У цукровій промисловості при очищенні соку цукрового буряка (дифузійний сік)
- •Лекція №18. Властивості колоїдних розчинів
- •Рівняння Релея (теорія світлорозсіювання для сферичних непоглинаючих світло частинок, 1871р.)
- •Визначення концентрації спирту в розчині
- •Конденсаційні методи.
- •Диспергаційні методи.
- •Тип емульсії визначають:
- •Методи одержання емульсій
- •Емульгування ‑ одержання емульсій шляхом диспергування однієї рідини в іншій струшуванням, інтенсивним перемішуванням. Емульгуванню сприяють:
- •Високомолекулярні сполуки класифікують:
- •І За походженням
- •Іі. За формою макромолекул
- •Склоподібний стан
- •Кристалічний стан
- •В’язко-текучий стан
- •Залежність властивостей некристалічних полімерів від температури
- •Властивості полімерів:
- •Властивості розчинів вмс:
- •Властивості розчинів вмс:
- •Властивості розчинів вмс
- •Кількісні характеристики процесу набухання
- •Тиск набухання
- •Ступінь набухання (α)
- •Форми існування води у полімерах
- •Лекція №21. Високомолекулярні сполуки – важлива складова частина продуктів харчування
- •Зміна колагену при тепловій обробці
- •Основні зміни, що відбуваються з білками при їх нагріванні
- •Зміни вуглеводів у технологічних процесах
- •Способи уповільнення реакції меланоїдиноутворення:
- •Зміни кольору та формування смако-ароматичного комплексу при тепловій обробці продуктів
- •Роль білків і крохмалю у хлібопекарському виробництві
- •Речовини, які змінюють структуру і фізико-хімічні властивості харчових продуктів
Зміна колагену при тепловій обробці
І етап |
температура 60 ‑ 650С |
с |
зварювання |
|
|
|
|
ІІ етап (тривале нагрівання з водою) |
температура 65 ‑ 1000С |
д |
утворення глютину (розчинна речовина), тканина розм’якшується |
Фактори, що впливають на швидкість переходу колагену в глютин:
температура (підвищення температури);
тривалість теплової обробки;
кисле середовище (денатурація, прискорює розм’якшення);
структура сполучної тканини.
Основні зміни, що відбуваються з білками при їх нагріванні
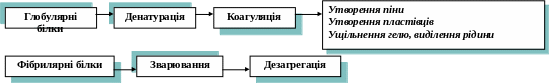
Кістки містять фібрилярний білок – осеїн, подібний за будовою до колагену. При варінні кісткових бульйонів частина осеїну переходить у глютин. Розчини, що містять більше 1% глютину, при охолодженні утворюють драглі. На цій властивості базується приготування заливних холодних страв з желатином і варіння драглів. При варінні м’яса ущільнюється білковий гель ‑ міофібрил, що спричиняє зменшення маси і об’єму продукту.
Освітлення бульйонів основане на денатурації білків при нагріванні. Введений у каламутний бульйон яєчний білок коагулює і утворює порувату масу, яка має значну питому поверхню (твердий адсорбент). На цій поверхні відбувається адсорбція емульгованих часточок жиру і завислих часточок денатурованого білка та насичених жирних кислот, утворених в результаті гідролізу жиру.
При зберіганні риби відбуваються такі процеси:
Механічне руйнування структури тканин кристалами льоду, утвореними при замерзанні води внаслідок глибокого охолодження (фізичний процес).
Пошкодження структури риби стимулює окислювальні та гідролітичні реакції і впливає на ферментативні процеси в рибі: окислення і гідроліз ліпідів
Зниження ферментативної активності тканин, розщеплення глікогену, денатурація і протеоліз білків.
Основний процес, що відбувається при зберіганні риби, ‑ денатурація білків. При тепловій обробці риби відбуваються такі ж самі процеси, як і при обробці м’яса. Проте із-за меншого вмісту сполучної тканини (1 ‑ 4%) риба потребує менш тривалої теплової обробки, ніж м'ясо. Зварювання колагену риб розпочинається вже при 40 С. Внаслідок високої здатності поглинати воду вироби з риби втрачають менше маси, ніж м’ясні вироби.
При дозріванні соленої риби: відбувається денатурація білків і протеоліз, окислювальний розпад ліпідів ‑ сіль прискорює ці процеси проте гальмує гідроліз ліпідів (при збільшенні концентрації солі відбувається гальмування протеолітичних ферментів і уповільнюється утворення вільних жирних кислот). Продукти окислення ліпідів (карбонільні сполуки) взаємодіють з продуктами гідролітичного розщеплення білків, утворюючи нові ароматичні та смакові компоненти, що покращують органолептичні властивості риби. Отже, на відміну від зберігання замороженої риби продукти окислення ліпідів при зберіганні соленої риби мають позитивне значення.
Білки овочів і фруктів містяться всередині тканинних клітин, заповнених рідиною. Рідина клітин (протоплазма і клітинний сік) – білкові золі. Поверхня протоплазми виявляє властивості напівпроникної мембрани. При тепловій обробці білки протоплазми згортаються: білки, що знаходяться в стані малоконцентрованого золю коагулюють з утворенням піни, пластівців (з прогрітих овочів у воду переходить більше поживних речовин).
Білки зернових і зернобобових культур знаходяться у вигляді сухих гелів, алейронових зерен. Варіння зернових продуктів і випікання тіста спричиняє денатурацію білків. В результаті ущільнюються обводнені білкові гелі за рахунок виділення значної кількості вологи. Волога залишається в продукті і поглинається клейстеризований крохмалем. Білки зерно борошняних продуктів згортаються при 50 – 70 С.
Білки яйця – концентровані колоїдні розчини (золі), в результаті денатурації утворюють гель, здатний утримувати воду.
Денатурація білків яйця: білкової частини – t = 50 ‑ 550С (поступове помутніння), t = 650С (загусання), t = 750С (непрозора біла драглеподібна маса); жовткової частини ‑ t = 70-750С.
Білки молока входять у склад молока у таких кількостях: казеїн – 82%, альбумін 12% і глобулін – 6%. Виділений з молока казеїн (білкова сирниста маса) не розчиняється у воді. У молоці міститься у вигляді казеїнату кальцію, що розчиняється у воді, набухаючи утворює колоїдні розчини. При нагріванні у кислому середовищі казеїнат кальцію згортається (при нагріванні молока з підвищеною кислотністю).
Казеїн – складний білок, фосфопротеїд, що входить до складу молока і молочних продуктів у колоїдному стані. Денатурація казеїну – поява плівки на поверхні молока (t = 40-450С).
При збільшенні кислотності молока, при дії сичужних ферментів: |
Молочна кислота зв’язує кальцій, казеїн випадає в осад (рН = 4,6) |
+ |
Виділяється рідина, утворюється коагель (використовується при виробництві сирів) |
При кип’ятінні молока на поверхні утворюється пінка внаслідок адсорбції у поверхневому шарі білків, що при нагріванні коагулюють.

 корочування
волокон у довжину
корочування
волокон у довжину еструкція
еструкція температура
температура