- •Лекція №14. Поверхневі явища. Адсорбція на межі поділу рухомих фаз
- •За здатністю молекул пар до іонізації їх поділяють на класи:
- •Іоногенні колоїдні пар:
- •Лекція №15. Адсорбція на твердому адсорбенті
- •Теорія мономолекулярної адсорбції (Ленгмюр, 1915):
- •Адсорбція на межі тверде тіло ‑ розчин
- •Лекція №16. Застосування адсорбції
- •Застосування адсорбції
- •Лекція №16. Дисперсні системи. Колоїдні розчини. Методи добування та очищення
- •Грубодисперсні системи
- •Загальна характеристика
- •Очищення колоїдних розчинів
- •Лекція №17. Будова колоїдних частинок. Стійкість колоїдних розчинів. Коагуляція
- •Механізми утворення пеш
- •Стійкість колоїдних розчинів
- •Між колоїдними частинками діють дві взаємно протилежні сили:
- •Стійкість дисперсної системи
- •У цукровій промисловості при очищенні соку цукрового буряка (дифузійний сік)
- •Лекція №18. Властивості колоїдних розчинів
- •Рівняння Релея (теорія світлорозсіювання для сферичних непоглинаючих світло частинок, 1871р.)
- •Визначення концентрації спирту в розчині
- •Конденсаційні методи.
- •Диспергаційні методи.
- •Тип емульсії визначають:
- •Методи одержання емульсій
- •Емульгування ‑ одержання емульсій шляхом диспергування однієї рідини в іншій струшуванням, інтенсивним перемішуванням. Емульгуванню сприяють:
- •Високомолекулярні сполуки класифікують:
- •І За походженням
- •Іі. За формою макромолекул
- •Склоподібний стан
- •Кристалічний стан
- •В’язко-текучий стан
- •Залежність властивостей некристалічних полімерів від температури
- •Властивості полімерів:
- •Властивості розчинів вмс:
- •Властивості розчинів вмс:
- •Властивості розчинів вмс
- •Кількісні характеристики процесу набухання
- •Тиск набухання
- •Ступінь набухання (α)
- •Форми існування води у полімерах
- •Лекція №21. Високомолекулярні сполуки – важлива складова частина продуктів харчування
- •Зміна колагену при тепловій обробці
- •Основні зміни, що відбуваються з білками при їх нагріванні
- •Зміни вуглеводів у технологічних процесах
- •Способи уповільнення реакції меланоїдиноутворення:
- •Зміни кольору та формування смако-ароматичного комплексу при тепловій обробці продуктів
- •Роль білків і крохмалю у хлібопекарському виробництві
- •Речовини, які змінюють структуру і фізико-хімічні властивості харчових продуктів
Лекція №21. Високомолекулярні сполуки – важлива складова частина продуктів харчування
Основні питання:
Теплова дія на білки харчових продуктів. Процеси, що відбуваються при зберіганні та тепловій обробці м’яса, риби, молока, яєць, зернобобових культур.
Зміни вуглеводів у технологічних процесах. Меланоїдиноутворення. Карамелізація сахаридів.
Зміни кольору та формування смако-ароматичного комплексу при тепловій обробці продуктів.
Роль білків і крохмалю у хлібопекарному виробництві.
Речовини, що змінюють структуру і фізико-хімічні властивості харчових продуктів.
У підприємствах харчування найбільш поширеним процесом є теплова обробка продуктів.
Залежно від характеру і мети технологічного процесу теплова обробка повинна забезпечити:
підтримання температури продукту на певному рівні;
нагрівання холодного або охолодження гарячого продукту;
заморожування продукту.
Всі ці процеси пов’язані з передачею теплоти продукту, що підлягає тепловій обробці, або з відніманням від продукту теплоти (теплообмін).
Теплова обробка харчових продуктів тваринного або рослинного походження спричиняє глибокі фізико-хімічні зміни білків, які входять до складу продукту. Фізичні зміни їжі полягають у її подрібненні, перемішуванні, утворенні драглів, суспензій, емульсій і частковому розчиненні. Хімічні зміни пов’язані з рядом послідовних стадій розщеплення білків, вуглеводів на більш прості сполуки.
Процеси, що відбуваються при зберіганні м’яса (дозрівання):
На початку зберігання «жорсткість» м’яса збільшується, потім вона відновлюється і м'ясо стає м’яким.
Гліколіз – перетворення глікогену на молочну кислоту – ферментативний процес.
Денатурація і протеоліз – часткове розщеплення в основному білків саркоплазми до пептидів і амінокислот. Ці процеси носять ферментативний характер (білки сполучної тканини не підлягають протеолізу), розпочинаються при 0 С, при підвищенні температури зростають, що спричиняє розм’якшення тканин і покращення органолептичних показників м’яса.
При тривалому зберігання м’яса відбувається окислення ліпідів, зростає пероксидне число жиру.
При взаємодії вуглеводів з утвореними амінокислотами може відбуватися карбоміламінна реакція (реакція Майяра) з утворенням меланоїдинів – сполук коричневого кольору з гіркуватим присмаком і не здатних засвоюватися організмом.
При дозріванні м’яса зменшується водоутримуюча здатність і виділяється незначна кількість соку.

М’ясні продукти перед вживанням обов’язково піддають тепловій обробці, оскільки при цьому відбувається розм’якшення продукту. Сполучні тканини частково желатинуються, що спричиняє краще засвоєння продукту. В процесі теплової обробки м’ясних продуктів при 60 – 70 С відбувається денатурація білків: 90% всіх розчинних білків денатурує і втрачає розчинність.
Денатурація білків ‑ зміна нативної структури білкової молекули під впливом зовнішніх факторів. Спочатку відбувається руйнування третинної структури міофібрилярних і саркоплазмових білків з виділенням вільної води. За деяких умов вивільнена вода може поглинатися вторинною структурою білків сполучної тканини (колаген і еластин) з утворенням желатинованих сполук. Відбувається частковий гідроліз м’язових білків з утворенням розчинних у воді азотовмісних продуктів (пептидів і амінокислот). Загальна кількість таких продуктів – 10% від вихідної кількості білка. При варінні азотовмісні речовини переходять у бульйон у вигляді піни, при смаженні залишаються на пательні.
Деструкція ‑ нагрів денатурованого білка вище 1000С, проходить руйнування макромолекули (відбувається за допомогою протеолітичних ферментів, що сприяє розм’якшенню м’яса, послабленню клейковини тіста, отриманню білкових гідролізатів).
Денатурація відбувається при дії:
фізичних факторів: високий тиск, температура, ультразвук, іонізуюче випромінювання, збивання, струшування;
хімічних факторів: зміна рН середовища, додавання органічних і неорганічних кислот, лугів, солей важких металів.
|
Ознаки денатурації (зміни властивостей білків):
|
Результат денатурації ‑ коагуляція або зсідання білків.
На температуру денатурації впливають: сіль – зниження температури; цукор – підвищення температури.
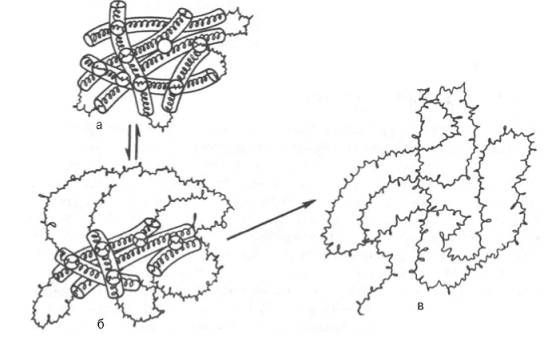
Глобулярні білки в результаті денатурації згортаються (коагулюють). Руйнуються водневі зв’язки вторинної структури білка, поліпептидні ланцюги розгортаються, а потім знову згортаються, але розташування їх у просторі набуває нової форми.
Фібрилярні білки при денатурації зварюються, волокна стають склоподібними.
В результаті набухання послаблюються та частково розриваються водневі зв’язки, які утримують поліпептидні ланцюги (волокна білка розриваються на окремі поліпептидні ланцюги) ‑ дезагрегація.
Волокна скорочуються у довжину в 3-4 рази та значно збільшуються в об’ємі (за рахунок розриву внутрішніх зв’язків) ‑ зварювання.
Волокна колагену стають менш щільними, більш еластичними. Частина колагену переходить у розчинний білок глютин, розчини якого при охолодженні утворюють драглі.