
- •Глава 1. Основные понятия химии
- •1.1. Составление химических формул веществ. Понятие о валентности и степени окисления
- •Задание для самостоятельной работы
- •1.2. Химические уравнения
- •1.3. Классификация химических реакций
- •Глава 2. Основные классы неорганических соединений
- •2.1. Оксиды
- •2.1.1. Получение оксидов
- •2.1.2. Классификация и свойства оксидов
- •I. Оксиды металлов.
- •1. Оснóвные оксиды.
- •2. Кислотные оксиды.
- •3. Амфотерные оксиды.
- •II. Оксиды неметаллов.
- •2.2. Гидроксиды
- •I. Гидроксиды металлов.
- •2.2.1. Получение гидроксидов металлов
- •1. Оснóвные гидроксиды.
- •2. Кислотные гидроксиды.
- •3. Амфотерные гидроксиды.
- •II. Гидроксиды неметаллов.
- •2.2.2. Получение кислот
- •2.3. Соли
- •2.3.1. Классификация солей
- •1. Средние (нормальные) соли.
- •2. Кислые соли.
- •3. Оснóвные соли.
- •4. Комплексные соли.
- •5. Двойные соли.
- •6. Смешанные соли.
- •7. Гидратные соли (кристаллогидраты).
- •2.3.2. Физические свойства солей
- •2.3.3. Химические свойства солей
- •Задание для самостоятельной работы
- •Глава 3. Основные законы химии
- •3.1. Международная система единиц (система си)
- •3.2. Атомные и молекулярные массы
- •1. Атомная (или молекулярная) масса m0.
- •2. Относительная атомная (или молекулярная) масса Ar (Mr).
- •3. Молярная масса вещества m.
- •1. Закон сохранения массы веществ.
- •2. Закон постоянства состава.
- •3. Закон стехиометрических соотношений.
- •3.4. Газовые законы
- •Решение.
- •Глава 4. Строение Атома
- •Решение.
- •4.1. Строение электронных оболочек атомов
- •4.2. Электронные конфигурации атомов
- •1. Принцип Паули.
- •2. Правило Хунда.
- •3. Принцип наименьшей энергии.
- •Решение.
- •Решение.
- •Задание для самостоятельной работы
- •4.3. Периодический закон д.И.Менделеева
- •Задание для самостоятельной работы
- •Глава 5. Химическая связь
- •5.1. Ковалентная связь
- •1. Обменный механизм.
- •2. Донорно-акцепторный механизм.
- •5.2. Ионная связь
- •5.3. Металлическая связь
- •5.4. Водородная связь
- •Решение.
- •Задание для самостоятельной работы
- •Глава 6. Физико-химические основы протекания химических реакций
- •6.1. Основы химической термодинамики
- •6.1.1. Термохимические уравнения и расчеты
- •I следствие:
- •Решение.
- •II следствие:
- •Решение.
- •Решение.
- •Решение.
- •Решение.
- •Задание для самостоятельной работы
- •6.2. Скорость химических реакций
- •6.2.1. Основы химической кинетики
- •Решение.
- •1. Зависимость скорости реакции от концентраций реагентов.
- •Решение.
- •Решение.
- •Решение.
- •2. Зависимость скорости реакции от температуры.
- •Решение.
- •Решение.
- •Задание для самостоятельной работы
- •6.3. Химическое равновесие
- •6.3.1. Смещение химического равновесия. Принцип Ле Шателье
- •1. Влияние изменения концентрации.
- •2. Влияние температуры.
- •2. Влияние давления.
- •Решение.
- •Задача №3
- •Задача №4
- •Задание для самостоятельной работы
- •Глава 7. Растворы
- •7.1. Основные способы выражения концентрации растворов
- •Решение.
- •Решение.
- •Решение.
- •Решение.
- •Решение.
- •Решение.
- •Решение.
- •Решение.
- •Решение.
- •Решение.
- •Задание для самостоятельной работы
- •7.2. Теория электролитической диссоциации
- •7.2.1. Факторы, влияющие на степень диссоциации электролитов
- •Решение.
- •7.2.2. Реакции в растворах электролитов
- •Решение.
- •7.3. Ионное произведение воды. Водородный показатель
- •Решение.
- •Решение.
- •Шкала значений pH
- •Решение.
- •Решение.
- •Решение.
- •Решение.
- •Решение.
- •Решение.
- •Решение.
- •7.4.1. Усиление и подавление гидролиза
- •Решение.
- •Задание для самостоятельной работы
- •Глава 8. Окислительно-восстановительные реакции
- •8.1. Окислители и восстановители
- •8.2. Классификация окислительно-восстановительных реакций
- •8.3.2. Метод электронно-ионного баланса
- •Решение.
- •Задание для самостоятельной работы
3. Амфотерные гидроксиды.
Амфотерными называются гидроксиды, которые могут обратимо диссоциировать как с образование ионов OH, так и ионов H+:
Zn2+ + 2OH ⇄ Zn(OH)2 + 2H2O ⇄ 2H+ + [Zn(OH)4]2
Амфотерные гидроксиды образуют те же металлы, которые образуют амфотерные оксиды. Например: Be(OH)2, Zn(OH)2, Al(OH)3 и др.
Все амфотерные гидроксиды малорастворимы в воде.
Амфотерные гидроксиды могут проявлять свойства основных и кислотных гидроксидов. Двойственность амфотерных гидроксидов проявляется в том, что они реагируют как с кислотами:
Al(OH)3 + 3HCl = AlCl3 + 3H2O,
так и со щелочами:
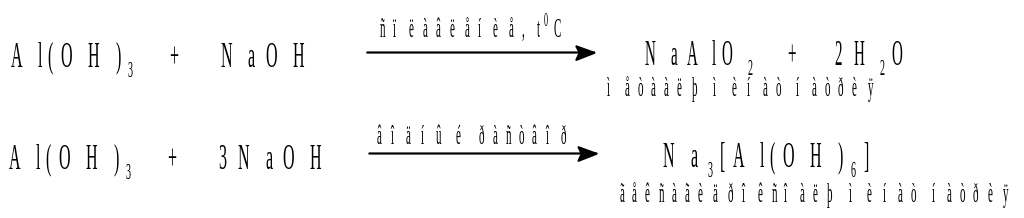
II. Гидроксиды неметаллов.
Гидроксиды неметаллов бывают только кислотными. Их называют кислотами. Они полностью или обратимо диссоциируют в растворах с образованием катионов H+ и аниона Ann:
H2SO4 2H+ + SO42
H2CO3 2H+ + CO32
Кислоты бывают также бескислородными: HCN, HCl, H2S и др.
Названия некоторых кислот и их анионов приведены в таблице 1. В скобках приведены некоторые тривиальные (исторически сложившиеся) названия.
Таблица 1. Названия некоторых кислот и их анионов.
Кислота |
Анион |
||
Бескислородные кислоты |
|||
Формула |
Название |
Формула |
Название |
HF |
Фтороводородная (Плавиковая) |
F |
Фторид |
HCl |
Хлороводородная (Соляная) |
Сl |
Хлорид |
HBr |
Бромоводородная |
Br |
Бромид |
HI |
Иодоводородная |
I |
Иодид |
H2S |
Сероводородная |
S2 |
Сульфид |
HCN |
Циановодородная (Синильная) |
CN |
Цианид |
HSCN |
Тиоциановодородная (Родановодородная) |
SCN |
Тиоцианат (Роданид) |
Кислородсодержащие кислоты |
|||
HClO |
Хлорноватистая |
СlO |
Гипохлорит |
HClO2 |
Хлористая |
ClO2 |
Хлорит |
HClO3 |
Хлорноватая |
ClO3 |
Хлорат |
HClO4 |
Хлорная |
ClO4 |
Перхлорат |
H2SO4 |
Серная |
SO42 |
Сульфат |
H2SO3 |
Сернистая |
SO32 |
Сульфит |
HNO3 |
Азотная |
NO3 |
Нитрат |
HNO2 |
Азотистая |
NO2 |
Нитрит |
HPO3 |
Метафосфорная |
PO3 |
Метафосфат |
H3PO4 |
Ортофосфорная |
PO43 |
Ортофосфат |
H4P2O7 |
Пирофосфорная |
P2O74 |
Пирофосфат |
H3PO3 |
Фосфоновая (Фосфористая) |
HPO32 |
Фосфонат (Фосфит) |
H3PO2 |
Фосфиновая (Фосфорноватистая) |
H2PO2 |
Фосфинат (Гипофосфит) |
H2CO3 |
Угольная |
CO32 |
Карбонат |
H2SiO3 |
Кремниевая |
SiO32 |
Силикат |
H3BO3 |
Борная |
BO2 B4O72 |
Метаборат Тетраборат |
HMnO4 |
Марганцовая |
MnO4 |
Перманганат |
H2CrO4 |
Хромовая |
CrO42 |
Хромат |
H2Cr2O7 |
Дихромовая |
Cr2O72 |
Дихромат |
Органические кислоты |
|||
HCOOH |
Муравьиная |
HCOO |
Формиат |
CH3COOH |
Уксусная |
CH3COO |
Ацетат |
