
- •Характеристика сточных вод. Основные загр. В-ва в ст.Водах разных пр-в
- •Показатели качества сточных вод (ч.1)
- •Показатели качества сточных вод (ч.2)
- •Оценка качества сточных вод
- •Определение систем водообеспеч. И водоотв. Прямоточное и оборотное вс.
- •Системы канализации пп. Условия выпуска ст.Вод пп в гор.Канализацию.
- •Первичные отстойники, осветлители, нефтеловушки.
- •Открытые и напорные гидроциклоны
- •Типы фильтров.
- •Химические методы очистки. Нейтрализация и различные типы нейтрализаторов.
- •Химические методы очистки. Окисление и различные методы окисления.
- •Химические методы очистки. Восстановление. Реагентные методы выделения загр. В-в в виде малорастворимых и нерастворимых соединений. Схема реаг. Оч-ки.
- •Физико-химические методы очистки сточных вод. Коагуляция, флокуляция. Технология и оборудование.
- •1.Понятие о коагуляции и применяемых коагулянтах
- •2. Флокуляция
- •3.Технология коагуляционной и флокуляционной очистки сточных вод и используемое оборудование
- •Сорбция. Технология и оборудование.
- •Флотация. Технология и оборудование.
- •1.Флотация с выделением воздуха из раствора
- •2.Напорная флотация
- •3.Флотация с механическим диспергированием воздуха
- •4.Флотация с подачей воздуха через пористые материалы
- •5.Очистка методом пенного фракционирования (пенной сепарацией)
- •6.Понятие о химической, биологической и ионной флотации
- •Экстракция. Технология и оборудование.??????
- •Ионный обмен, регенерация ионитов. Технология и оборудование.
- •Электрохимическая очистка сточных вод, методы. Электрокоагуляция.
- •Электрофлотация, электродиализ, гальванокоагуляция.
- •Электрофлотация
- •2.Электродиализ
- •3.Гальванокоагуляционная очистка сточных вод
- •Применение методов обратного осмоса и ультрафильтрации для очистки сточных вод.
- •Методы термической обработки сточных вод. Концентрирование сточных вод.
- •1.Очистка сточных вод с выделением растворенных веществ (концентрирование сточных вод)
- •Выделение растворенных веществ из конц. Растворов. Термоокислительный метод
- •1.Выделение растворенных веществ из концентрированных растворов
- •2.Термоокислительные методы обезвреживания сточных вод
- •Биологическая очистка сточных вод. Технология, естественные и искусственные методы биологической очистки.
- •Биофильтры, аэротенки, окситенки.
- •Выделение тяжёлых металлов и глубокая очистка ст.Вод.
- •Обработка осадков сточных вод. Состав и свойства осадков. Основные процессы
- •Методы уплотнения осадков.
- •1. Гравитационное уплотнение осадков
- •2 .Флотационное уплотнение осадков
- •3 .Центробежное уплотнение осадков
- •Анаэробное сбраживание осадков. Технология и оборудование.
- •Аэробная стабилизация. Кондиционирование осадков.
- •Обезвоживание осадка.
- •1. Сушка осадков на иловых площадках
- •2. Фильтрование
- •3. Центрифугирование и сепарирование
- •Методы очистки воды от радиоактивных загрязнений.
Химические методы очистки. Восстановление. Реагентные методы выделения загр. В-в в виде малорастворимых и нерастворимых соединений. Схема реаг. Оч-ки.
При содержании в сточных водах легко восстанавливаемых соединений меди, хрома, мышьяка, ртути применяют методы восстановительной очистки.
Катионы меди, содержащиеся в кислых сточных водах, могут быть выделены цементацией на железном скрапе или никелевом песке.
Медь выделяется на железе или никеле в виде металла, и вместо нее в раствор переходят катионы железа или никеля. Метод цементации применяют для грубой, предварительной очистки достаточно концентрированных по меди сточных вод. Очищенная цементацией вода затем нейтрализуется до рН = 8 – 9 при одновременной доочистке ее от оставшихся катионов меди и перешедших в раствор катионов железа или никеля.
Высокотоксичные соединения шестивалентного хрома содержатся в промывных сточных водах и отработанных технологических растворах, образовавшихся в процессе хромирования, при химической обработке поверхностей стальных изделий (травление, пассирование), при анодировании изделий из алюминия и при проведении других технологических процессов. Обработка сточных вод осуществляется в две ступени:
1) перевод (восстановление) шестивалентного хрома в трехвалентную форму;
2) осаждение трехвалентного хрома в виде гидроксида.
В качестве реагентов-восстановителей наибольшее распространение получили натриевые соли сернистой кислоты – сульфит (Na2SO3), бисульфит (NaHSO3) и гидросульфит (Na2SO5). Кроме того, используют следующие восстановители: сульфит железа (FeSO4), диоксид серы (SO2), гидразин (N2Н4) и др.
Скорость и полнота восстановления Сг6+ до Сг3+ указанными солями в значительной степени зависит от величины рН, причем наибольшая скорость наблюдается при рН = 2 – 2,5, что требует дополнительного подкисления сточных вод. Для этих целей обычно используют 10 –15 %-ные растворы серной кислоты.
Для очистки сточных вод от шестивалентного хрома используют установки непрерывного или периодического действия.
После восстановления в кислой среде шестивалентного хрома до трехвалентного состояния сточные воды подвергают нейтрализации, которой осаждается в виде гидроксида. В качестве реагентов-нейтрализаторов используют Са(ОН)2, Nа2СО3, NаОН.
Метод восстановления также применяют для очистки сточных вод от соединений ртути. Их восстанавливают до металлического состояния, а образовавшуюся ртуть отделяют от воды (отстаиванием, фильтрованием или флотацией). В качестве реагента-восстановителя используют алюминиевую пудру, железный порошок, гидросульфид натрия, гидразин, сульфид железа и др.
При выделении мышьяка из концентрированных растворов (до 110 г/л) используют диоксид серы, который восстанавливает мышьяковую кислоту до мышьяковистой. Последняя имеет малую растворимость в кислой и нейтральной среде и осаждается в виде триоксида мышьяка.
Реагентные методы выделения загрязняющих веществ в виде малорастворимых и нерастворимых соединений.
Известно, что вещества условно можно разделить на растворимые, малорастворимые и практически нерастворимые. Растворимость первых составляет примерно 1 г вещества в 100 мл растворителя (воды) или приблизительно 0,1 М по катиону, а последних – менее 0,1 г вещества в 100 мл растворителя или примерно 0,01 М по катиону. Вещества, занимающие промежуточное положение между ними, называют малорастворимыми. (В химической и экологической литературе нередко используют термин «труднорастворимые соединения», включая в него как практически нерастворимые, так и малорастворимые вещества.)
Основные классы нерастворимых веществ. К ним в первую очередь относятся все гидрооксиды, за исключением гидрооксидов щелочных металлов, аммония и бария, причем Ca(OH)2 и SR(OH)2 – малорастворимы. Все средние карбонаты и фосфаты нерастворимы, за исключением соответствующих соединений щелочных металлов и аммония. Все сульфиды, за исключением сульфидов щелочных и щелочноземельных металлов, нерастворимы.
Для очистки производственных сточных вод от соединений тяжелых цветных металлов и в первую очередь от соединений Cu, Ni, Со, Рb, Сd, Hg их осаждают в виде соответствующих гидрооксидов, сульфатов либо карбонатов. Растворимость вышеуказанных соединений может быть охарактеризована также произведением растворимости.
Для выделения из кислых сточных вод тяжелых цветных металлов и железа используются те же реагенты, что и при нейтрализации
В многокомпонентных сточных водах значения рН, соответствующие началу и окончанию осаждения гидроксидов, существенно сдвинуты в сторону больших величин.
Следует указать, что ионы тяжелых цветных металлов могут осаждаться не только в виде гидроксидов, но и гидроксид-карбонатов (в случае использования для осаждения реагентов, содержащих в своем карбонатные ионы). Гидроксиды цинка, свинца, меди, алюминия и некоторых других металлов растворяются в избытке едкой щелочи с образованием комплексных анионов.
Цинк, алюминий и некоторые другие металлы, обладающие амфотерными свойствами, могут содержаться в виде анионов в щелочных сточных водах. Для их удаления используют растворы кислот. При этом образуются осадки гидроксидов этих металлов.
Необходимо указать, что эффективнее совместное осаждение ионов двух или нескольких металлов при одной и той же величине рН, чем при осаждении каждого металла в отдельности.
Это связано с образованием смешанных кристаллов и адсорбционными процессами на их поверхности.
При обработке щелочными реагентами сточных вод, содержащих ионы тяжелых цветных металлов, Достигается снижение их концентраций до величин, позволяющих осуществлять сброс очищенной воды в городскую канализацию или водоемы санитарно-бытового пользования.
В том случае, когда требуется более глубокая степень очистки, тяжелые металлы рекомендуется выделять в виде сульфидов. Обычно в виде сульфидов выделяют Cu, Co, Ni, Fe, Sn, Mo, As, Sb, Hg, Ag, Zn, Cd, Pb.
В качестве осадителя обычно используют Na2S.
В отечественной практике для выделения из сточных вод сурьмы и мышьяка в виде малорастворимых сульфидов в качестве реагента-осадителя используют сульфат железа.
Sb3+ в зависимости от величины рН содержится в сточных водах в виде анионов тиосолей (SbS2–), либо в виде кислородсодержащих анионов, что практически встречается редко.
Существуют методы осаждения катионов тяжелых цветных металлов в виде труднорастворимых соединений, в основе которых лежат окислительно-восстановительные реакции. Примером этого является способ выделения из растворов и промышленных сточных вод двухвалентного кобальта с использованием органического реагента – этилксантогената калия KSCSOC2H5. Двухвалентный кобальт в процессе осаждения окисляют до трехвалентного состояния двухвалентной медью.
Содержание меди и кобальта в очищенных указанном способе водах не превышает ПДК. В осадок переходят смешанные ксантогенаты меди и кобальта.
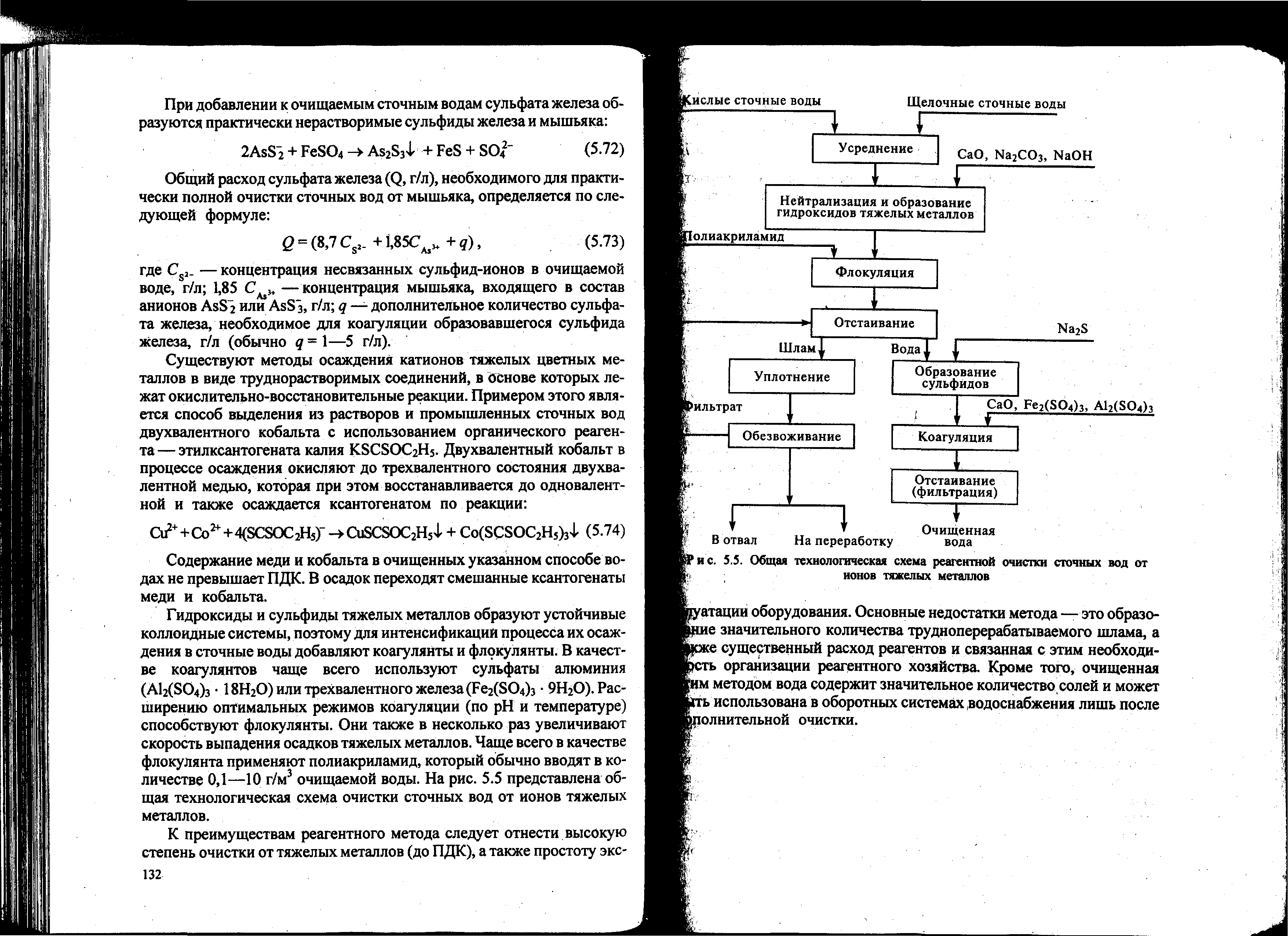
Гидроксиды и сульфиды тяжелых металлов образуют устойчивые коллоидные системы, поэтому для интенсификации процесса их осаждения в сточные воды добавляют коагулянты и флокулянты. В качестве коагулянтов чаще всего используют сульфаты алюминия (А12(SO4)3∙18Н2О) или трехвалентного железа (Fе2(SО4)3∙9Н2О). Расширению оптимальных режимов коагуляции (по рН и температуре) способствуют флокулянты. Они также в несколько раз увеличивают скорость выпадения осадков тяжелых металлов. Чаще всего в качестве флокулянта применяют полиакриламид, который обычно вводят в количестве 0,1 – 10 г/м3 очищаемой воды. На рис. 4.5 представлена общая технологическая схема очистки сточных вод от ионов тяжелых металлов.
К преимуществам реагентного метода следует отнести высокую степень очистки от тяжелых металлов (до ПДК), а также простоту эксплуатации оборудования.
О сновные
недостатки метода – это образование
значительного количества
трудноперерабатываемого шлама, а также
существенный расход реагентов и связанная
с этим необходимость организации
реагентного хозяйства. Кроме того,
очищенная этим методом вода содержит
значительное количество солей и может
быть использована в оборотных системах
водоснабжения лишь после дополнительной
очистки.
сновные
недостатки метода – это образование
значительного количества
трудноперерабатываемого шлама, а также
существенный расход реагентов и связанная
с этим необходимость организации
реагентного хозяйства. Кроме того,
очищенная этим методом вода содержит
значительное количество солей и может
быть использована в оборотных системах
водоснабжения лишь после дополнительной
очистки.
