
- •6.Хлорофиллы (химические и оптические свойства, структура и функции)
- •7. Каротиноиды (химические и оптические свойства, структура и функции)
- •17. Фотосинтез и урожай. Пути повышения продуктивности фотосинтеза посевов с.Х культур.
- •23. Хемиосмотическая теория фотофосфорилирования
- •6)Классификация ферментов дыхания (оксидоредуктазы).
- •10. Окислительное декарбоксилирование пирувата (локализация, мультиферментный комплекс, энергетика).
- •11.Общая характеристика цикла ди- и трикарбоновых кислот.
- •12).Окислительное фосфорилирование.
- •17).Интенсивность дыхания в зависим. От вида и возраста древ.Раст.
- •23. Ионные каналы, насосы, переносчики ионов элементов минерального питания.
- •24. Движущие силы ионного транспорта в растительной клетке.
- •2) Биогеохимические провинции
- •23. Ионные каналы, насосы, переносчики ионов элементов минерального питания.
- •24. Движущие силы ионного транспорта в растительной клетке.
- •25.Принципы оносительной и абсол избират поглащ ионов элементов питания.
- •11. Грмональная система цветкогого раст
- •28. Причины деформации надземных органов древесных растений.
- •21. Характеристика возрастных изменений древесных растений.
- •22. Общий возраст раст и возраст отдельных органов.
- •Тема 8
- •4 Вопрос
- •Вопрос 5
- •11.Вопрос Границы приспособления и устойчивости
- •13. Устойчивость растений к тяжелым металлам.
- •15. Физиологические механизмы устойчивости растений к засухе.
Физиология раст
Тема:1
1-предмет задачи и методы физиологии ратении
Физиология растений — наука, которая изучает процессы жизнедеятельности и функции растительного организма. Слово «физиология» греческого происхождения; оно состоит из двух слов: physis — природа и logos — понятие, учение. Физиология растений является наиболее развитой отраслью экспериментальной ботаники, которая в XIX в. выделилась в самостоятельную науку. Она тесно связана с химией, физикой, биохимией, биофизикой, микробиологией, молекулярной биологией.
Перед научными работниками, физиологами растений поставлены такие задачи: изучить обмен веществ и энергии в растительном организме, фотосинтез, хемосинтез, биологическую фиксацию азота из атмосферы и корневое питание растений; разработать методы повышения использования растми солнечной энергии и питательных веществ почвы, обогащения почвы азотом; создать новые, более эффективные формы удобрений и разработать методы их применения; исследовать действие биологически активных веществ с целью использования их в растениеводстве; разработать методы более продуктивного использования воды растением. Без решения этих вопросов невозможно решение и ряда других проблем земледелия и растениеводства, направленных на повышение урожайности.
Интенсивное применение минеральных удобрений, гербицидов, физиологически активных веществ, химических препаратов для защиты растений от болезней и вредителей требует глубокого и всестороннего изучения их влияния на рост и обмен веществ растительных организмов с целью значительного повышения продуктивности сельскохозяйственных растений.
Решение поставленных задач имеет большое значение для разработки проблем ускорения научно-технического прогресса в растениеводстве и дальнейшего развития сельского хозяйства нашей страны.
Основной метод познания процессов, явлений в физиологии — эксперимент, опыт. Следовательно, физиология растений — наука экспериментальная.
Для изучений физико-химической сути функций, процессов в физиологии растений широко применяют методы: лабораторно-аналитический, вегетационный, полевой, меченых атомов, электронной микроскопии, электрофореза, хроматографического анализа, ультрафиолетовой и люминесцентной микроскопии, спектрофотометрии и др. Кроме того, используют фитотроны и лаборатории искусственного климата, в которых выращивают раст и проводят опыты в условиях определенного состава воздуха, нужной температуры и освещения. Применяя эти методы, физиологи исследуют раст на молекулярном, субклеточном, клеточном и организменном (интактное растение) уровнях.
3-История возникновения Фиология раст
Физиология растений — одна из молодых отраслей биологии. Возникновение ее можно отнести к концу XVIII — началу XIX в. Ф. р. развивалась первоначально как составная часть ботаники, занимающаяся преимущественно проблемой почвенного питания растений. Голландский естествоиспытатель Ян ван Гельмонт (1629) экспериментально решал вопрос о том, за счёт чего строят свои ткани раст и пришёл к ошибочному с современной точки зрения заключению, что основной источник питания раст не почва, а вода. Его опыты имели большое значение для изучения растений, т.к. он впервые применилколичественный метод – взвешивание.
В конце 17 в. было установлено наличие у растений пола.
В 1727 англичанин С. Гейлс обнаружил передвижение веществ и воды по тканям раст. Впервые идею о воздушном питании растений высказал в 1753 М. В. Ломоносов, который отметил, что деревья, растущие на бедном питательном веществами песке, не могут получить через корни необходимого количества питательных веществ, и сделал вывод, что раст получают питание через листья из воздуха.
Важнейшую роль в последующем развитии Ф. р. и всего естествознания в целом сыграло открытие англ. химика ДжозефаПристли, который установил, что зелёные раст в ходе своей жизнедеятельности изменяют состав воздуха, возвращают ему способность поддерживать горение и сохранять жизнь животных (1771). Это явление получило в дальнейшем названиефотосинтеза.
В это время начали складываться представления о фотосинтезе как процессе усвоения солнечной энергии зеленым растением, нашедшие более или менее законченное выражение в труде швейцских учёных Ж. Сенебье и Н. Т. Соссюра (конца 18 – начала 19 вв.), голландского естествоиспытателя Я. Ингенхауза (1779). Пятитомная «Физиология растений» Сенебье, появившаяся в 90-х годах XVIII в., была попыткой охватить, весь известный тогда материал наблюдений и опытов как содержание единой научной дисциплины. Позднее немецкий учёный Ю. Р. Майер, французский агрохимик Ж. Б. Буссенго (1868) и др. расшифровали отдельные стороны фотосинтеза, как процесса усвоения углекислого газа и воды, происходящего с выделением кислорода при обязательном участии света, показали зависимость фотосинтеза от света и установили связь между поглощением углекислоты и выделением кислорода у растений в процессе дыхания.
Тема:2
физиология и биохимия растительной клетки
1-Структурно-функциональная организация эукариот.клетки Мембранная система. Эта система представлена клеточной плазматической (цитоплазматической) мембраной, цитоплазматической (эндоплазматической) сетью (рети-кулом) и пластинчатым комплексом Гольджи. Плазматическая (цитоплаз-матическая) мембрана имеет толщину 8-12 нм и состоит из трех слоев, два из которых являются белковыми слоями толщиной по 3 нм каждый, а третий (внутренний) — двойным фосфолипидным слоем толщиной 6 нм (рис. 47). Плазматическая мембрана является полупроницаемой структурой. Через нее в клетку входят питательные вещества и выходят все «отходы» (продукты секреции). Она создает барьер проницаемости. Цитоплазматическая (эндоплазматическая) сеть (рети-кулум) представлена пронизывающими однослойными мембранными полостями (трубочками, цистернами, вакуолями) разных размеров, заполненными белковыми гранулами В составе цитоплазмы обнаруживают ферменты, полисахариды, АТФ, тРНК, ионы Са, Na, К и других химических элементов. Основная функция цитоплазматиче-ского матрикса заключается в том, что он является внутренней средой клетки, поддерживающей мембранные системы, орга-неллы и включения. В нем осуществляются гликолиз, активация аминокислот и другие реакцииКлеточные органеллы. Эти структуры представлены ядром, хромосомами, ядрышком, центриолями, митохондриями, рибо-сомами, лизосомами. Они характерны за некоторыми исключениями как для клеток животных, так и для клеток растений. Ядро в клетке имеет форму и размеры, зависящие от формы, размеров и функций клетки. В клетках эукариотических организмов содержится, как правило, по одному ядру, реже по два и более
Хромосомы. Хромосомы располагаются в ядре. Их название введено в литературу В. Вальдейлом в 1883 г. Они имеют форму палочек, нитей, петель. Для каждой хромосомы характерны индивидуальные особенности, касающиеся длины и положения перетяжки (центромеры) по длине хромосомы. Каждая из митотичес-ких индивидуальных хромосом состоит из двух сестринских хроматид, удерживаемых центромерой. В зависимости от локализации центромер различают метацентрические, субметацентричес-кие, акроцентрические и телоцентрические хромосомы (рис. 51). Количество хромосом постоянно в ядрах соматических клеток, где они находятся в парах. Диплоидный набор хромосом называют кариотипом (от греч. caryon — ядро, type — форма, тип). Для разных организмов характерны разные по количеству диплоидные наборы хромосом. В зависимости от строения хромосомы человека классифицируют на группы. Ядрышко — это очень мелкая структура диаметром 1—5 мкм, которая локализуется в ядре. Количество ядрышек бывает разным — от одного до нескольких. Центральная часть в ядрышке представлена фибриллярной частью (цепи, ДНК- ядрышковые организаторы и рибонуклеопротеиды) и гранулярной (формирующиеся субъединицы рибосом). Ядрышко является местом синтеза рРНК. Матрицей для синтеза рРНК является ДНК ядрышкового организатора Центриоли представляют собой гранулярные цилиндры диаметром около 0,15 мкм и длиной 0,5 мкм, локализующиеся парами в клетке около ядра. Эти пары называют диплосомами (центросома-ми). Митохондрии присутствуют во всех клетках организмов, которые используют для дыхания кислород. В одной клетке может находиться 50-5000 митохондрий. Они имеют форму палочек, нитей или гранул (рис. 54), а их размеры достигают 7 мкм.
2-основные постулаты современной клеточной теории
Клеточная теория Клеточная структура является главной, но не единственной формой существования жизни. Неклеточными формами жизни можно считать вирусы. Правда, признаки живого (обмен веществ, способность к размножению и т.п.) они проявляют только внутри клеток, вне клеток вирус является сложным химическим веществом. По мнению большинства учёных, в своём происхождении вирусы связаны с клеткой, являются частью её генетического материала, "одичавшими" генами. Выяснилось, что существует два типа клеток - прокариотические (клетки бактерий и архебактерий), не имеющие отграниченного мембранами ядра, и эукариотические (клетки растений, животных, грибов и протистов), имеющие ядро, окружённое двойной мембраной с ядерными порами. Между клетками прокариот и эукариот существует и множество иных различий. У большинства прокариот нет внутренних мембранных органоидов, а у большинства эукариот есть митохондрии и хлоропласты. В соответствии с теорией симбиогенеза, эти полуавтономные органоиды - потомки бактериальных клеток. Таким образом, эукариотическая клетка - система более высокого уровня организации, она не может считаться целиком гомологичной клетке бактерии (клетка бактерии гомологична одной митохондрии клетки человека).
Клеточная теория рассматривала организм как сумму клеток, а жизнепроявления организма растворяла в сумме жизнепроявлений составляющих его клеток. Считая клетку всеобщим структурным элементом, клеточная теория рассматривала как вполне гомологичные структуры тканевые клетки и гаметы, протистов и бластомеры. Применимость понятия клетки к протистам является дискуссионным вопросом клеточного учения в том смысле, что многие сложно устроенные многоядерные клетки протистов могут рассматриваться как надклеточные структуры. В тканевых клетках, половых клетках, протистах проявляется общая клеточная организация, выражающаяся в морфологическом выделении кариоплазмы в виде ядра, однако эти структуры нельзя считать качественно равноценными, вынося за пределы понятия «клетка» все их специфические особенности. В частности, гаметы животных или растений - это не просто клетки многоклеточного организма, а особое гаплоидное поколение их жизненного цикла, обладающее генетическими, морфологическими, а иногда и экологическими особенностями и подверженное независимому действию естественного отбора. В то же время практически все эукариотические клетки, несомненно, имеют общее происхождение и набор гомологичных структур - элементы цитоскелета, рибосомы эукариотического типа и др.
Догматическая клеточная теория игнорировала специфичность неклеточных структур в организме или даже признавала их, как это делал Вирхов, неживыми. В действительности, в организме кроме клеток есть многоядерные надклеточные структуры (синцитии, симпласты) и безъядерное межклеточное вещество, обладающее способностью к метаболизму и потому живое. Установить специфичность их жизнепроявлений и значение для организма является задачей современной цитологии. В то же время и многоядерные структуры, и внеклеточное вещество появляются только из клеток. Синцитии и симпласты многоклеточных - продукт слияния исходных клеток, а внеклеточное вещество - продукт их секреции, т.е. образуется оно в результате метаболизма клеток. Проблема части и целого разрешалась ортодоксальной клеточной теорией метафизически: всё внимание переносилось на части организма — клетки или «элементарные организмы».
3-Структура и функции протопласта Протопласт- содержимое растительной клетки; состоит из клеточной мембраны, цитоплазмы и ядра, но не включает клеточную оболочку П. получают искусственно для клонирования и регенерации из них целых р-ний, применения в клеточной инженерии В состав протопласта входит цитоплазма (Ц) и одно или несколько ядер. По химическому составу П содержит белки, жиры, углеводы и минеральные вещества. П на 75-90% состоит из воды. Белки могут быть связаны с другими органическими соединениями и образовывать сложные соединения – протеиды
4- Структура и общая характеристика мембран клетки. Плазматическая (цитоплазматическая) мембрана — обязательный компонент любой клетки. Она отграничивает клетку и обеспечивает сохранение существующих различий между клеточным содержимым и окружающей средой. Мембрана служит высокоизбирательным «входным» селективным фильтром и отвечает за активный транспорт веществ в клетку и из нее. Цитоплазматическую мембрану растительной клетки обычно называют плазмалеммой. Как и любая биологическая мембрана, она представляет собой липидный бислой с большим количеством белков. Основу липидного бислоя составляют фосфолипиды. Помимо них в состав липидного слоя входят гликолипиды и стерины. Липиды достаточно активно перемещаются в пределах своего монослоя, но возможны и их переходы из одного монослоя в другой. Такой переход, называемый «флип-флоп» (от англ. flip-flop), осуществляется ферментом флипазой. Кроме липидов и белков в плазмалемме присутствуют углеводы. Соотношение липидов, белков и углеводов в плазматической мембране растительной клетки составляет приблизительно 40:40: 20. Мембранные белки связаны с липидным бислоем различными способами. Первоначально белки мембран разделяли на два основных типа: периферийные и интегральные. Периферийные белки ассоциированы с мембраной за счет присоединения к интегральным белкам или липидному бислою слабыми связями: водородными, электростатическими, солевыми мостиками. Они в основном растворимы в воде и легко отделяются от мембраны без ее разрушения. Некоторые периферийные белки обеспечивают связь между мембранами и цитоскелетом. Интегральные белки мембран нерастворимы в воде.
Мембраны, виды, состав и функции. Мембраны- клеточные структуры липопротеиновой природы, отделяют клеточное содержимое от внешней среды, регулируют обмен м/у клеткой и средой, делят протопласт на отсеки, или компартменты, предназначенные для тех или иных специализированных метаболических путей. Некоторые хим. реакции, в частности световые реакции фотосинтеза в хлоропластах или окислительное фосфорилирование при дыхании в митохондриях, протекают на самих мембранах. На мембранах располагаются+ и рецепторные участки для распознания внешних стимулов (гормонов или других хим. в-в), поступающих из окр. среды или из другой части самого организма. Различают наружные ограничивающие мембраны, в том числе мембрану протоплазмы (плазмалемму), вакуоли (тоноплат), ядра, митохондрий, пластид, лизосом и субъединиц диктиосом, а также внутренние мембраны цитоплазмы (ЭДС), митохондрий и пластид. Мембраны обладают след. св-ми: подвижностью, текучестью, способностью замыкаться, полупроницаемостью в зависимости от тургорного давления. Общие функции мембран: барьерная, избирательная проницаемость для ионов и метаболитов, место локализации интегральных белков. Специфические функции: ближний транспорт по симпласту, фотосинтетическое фосфорилирование, окислительное фосфорилирование, место локализации редокс-системы, рецепторная. Хим. состав: белки, липиды, вода, полисахариды, кальций.
Свойства мембран. Мембраны — структуры очень динамичные. Они быстро восстанавливаются после повреждения, а также растягиваются и сжимаются при клеточных движениях. Важнейшим свойством мембраны является также избирательная проницаемость. Это значит, что молекулы и ионы проходят через нее с различной скоростью, и чем больше размер молекул, тем меньше скорость прохождения их через мембрану. Это свойство определяет плазматическую мембрану как осмотический барьер. Максимальной проникающей способностью обладает вода и растворенные в ней газы; значительно медленнее проходят сквозь мембрану ионы. Функции биологических мембран следующие: Отграничивают содержимое клетки от внешней среды и содержимое органелл от цитоплазмы. Обеспечивают транспорт веществ в клетку и из нее, из цитоплазмы в органеллы и наоборот. Выполняют роль рецепторов (получение и преобразование сит-налов из окружающей среды, узнавание веществ клеток и т. д.). Являются катализаторами (обеспечение примембранных химических процессов). Участвуют в преобразовании энергии.
5-структура и функции эндоплазматической сети. Эндоплазматическая сеть, Эндоплазматический ретикулум (ЭПР) — сложная система каналов, окруженных мембранами (6—7 нм), пронизывающая всю толщу цитоплазмы. Каналы имеют расширения — цистерны, которые могут обособляться в крупные пузырьки и сливаться в вакуоли. Каналы и цистерны ЭПР заполнены электронно-прозрачной жидкостью, содержащей растворимые белки и другие соединения. К мембране ЭПР могут быть прикреплены рибосомы. Благодаря этому поверхность мембран становится шероховатой. Такие мембраны носят название гранулярных, в отличие от гладких — агранулярных. Мембраны ЭПР связаны с мембраной ядра. Имеются данные, что эндоплазматический ретикулум возникает благодаря выростам, образующимся на наружной ядерной мембране. С другой стороны ядерная оболочка воссоздается из пузырьков ЭПР на стадии телофазы. Физиологическое значение эндоплазматического ретикулума многообразно. Мембраны ЭПР разделяют клетку на отдельные отсеки (компартменты) и тем клетке по всей цитоплазме. Аппарат Гольджи имеет два конца, два полюса: на одном полюсе, формирующем, образуются новые цистерны, на втором полюсе, секретирующем, происходит образование пузырьков. И тот, и другой процесс происходят непрерывно: по мере того как одна цистерна образует пузырьки и, таким образом, расформировывается, ее место занимает другая цистерна. Расстояние между отдельными цистернами постоянно (20—25 нм). Одна из основных функций аппарата Гольджи — это накопление и секреция веществ и, прежде всего углеводов, что проявляется в его участии в формировании клеточной оболочки и плазмалеммы. Одновременно цистерны аппарата Гольджи, по-видимому, могут служить для удаления некоторых веществ, выработанных клеткой.
6 - Вакуоли — крупные мембранные пузырьки или полости в цитоплазме, заполненные клеточным соком. Вакуоли образуются в клетках растений и грибов из пузыревидных расширений эндоплазматического ретикулума или из пузырьков комплекса Гольджи. В меристематических клетках растений вначале возникает много мелких вакуолей. Увеличиваясь, они сливаются в центральную вакуоль, которая занимает до 70—90% объема клетки и может быть пронизана тяжами цитоплазмы (рис. 1.12).
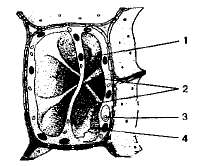
Рис. 1.12. Вакуоль в растительной клетке: 1 — вакуоль; 2 — цитопяаз-матические тяжи; 3 — ядро; 4 — хлоропласты.
Содержимое вакуолей —клеточный сок. Он представляет собой водный раствор различных неорганических и органических веществ. Большинство из них являются продуктами метаболизма протопласта, которые могут появляться и исчезать в различные периоды жизни клетки. Химический состав и концентрация клеточного сока очень изменчивы и зависят от вида растений, органа, ткани и состояния клетки. В клеточном соке содержатся соли, сахара (прежде всего сахароза, глюкоза, фруктоза), органические кислоты (яблочная, лимонная, щавелевая, уксусная и др.), аминокислоты, белки. Эти вещества являются промежуточными продуктами метаболизма, временно выведенными из обмена веществ клетки в вакуоль. Они являются запасными веществами клетки.
Помимо запасных веществ, которые могут вторично использоваться в метаболизме, клеточный сок содержит фенолы, танины (дубильные вещества), алкалоиды, антоцианы, которые выводятся из обмена в вакуоль и таким путем изолируются от цитоплазмы.
Танины особенно часто встречаются в клеточном соке (а также в цитоплазме и оболочках) клеток листьев, коры, древесины, незрелых плодов и семенных оболочек. Алкалоиды присутствуют, например, в семенах кофе (кофеин), плодах мака (морфин) и белены (атропин), стеблях и листьях люпина (люпинин) и др. Считается, что танины с их вяжущим вкусом, алкалоиды и токсичные полифенолы выполняют защитную функцию: их ядовитый (чаще горький) вкус и неприятный запах отталкивают растительноядных животных, что предотвращает поедание этих растений.
В вакуолях также часто накапливаются конечные продукты жизнедеятельности клеток (отходы). Таким веществом для клеток растений является щавелевокислый кальций, который откладывается в вакуолях в виде кристаллов различной формы.
В клеточном соке многих растений содержатся пигменты, придающие клеточному соку разнообразную окраску. Пигменты и определяют окраску венчиков цветков, плодов, почек и листьев, а также корнеплодов некоторых растений (например, свеклы).
Клеточный сок некоторых растений содержит физиологически активные вещества — фитогормоны (регуляторы роста), фитонциды, ферменты. В последнем случае вакуоли действуют как лизосомы. После гибели клетки мембрана вакуоли теряет избирательную проницаемость, и ферменты, высвобождаясь из нее, вызывают автолиз клетки.
Функции вакуолей следующие:
Вакуоли играют главную роль в поглощении воды растительными клетками. Вода путем осмоса через ее мембрану поступает в вакуоль, клеточный сок которой является более концентрированным, чем цитоплазма, и оказывает давление на цитоплазму, а следовательно, и на оболочку клетки. В результате в клетке развивается тургорное давление, определяющее относительную жесткость растительных клеток и обусловливающее растяжение клеток во время их роста.
В запасающих тканях растений вместо одной центральной часто бывает несколько вакуолей, в которых скапливаются запасные питательные вещества (жиры, белки). Сократительные (пульсирующие) вакуоли служат для осмотической регуляции, прежде всего, у пресноводных простейших, так как в их клетки путем осмоса непрерывно поступает вода из окружающего гипотонического раствора (концентрация веществ в речной или озерной воде значительно ниже, чем концентрация веществ в клетках простейших). Сократительные вакуоли поглощают избыток воды и затем выводят ее наружу путем сокращений.
8- Химический состав кл.стенки Клеточная стенка растительных клеток состоит, главным образом, из полисахаридов. Все компоненты, входящие в состав клеточной стенки, можно разделить на 4 группы: Структурные компоненты, представленные целлюлозой у большинства автотрофных растений. Компоненты матрикса, т. е. основного вещества, наполнителя оболочки - гемицеллюлозы, белки, липиды. Компоненты, инкрустирующие клеточную стенку, (т.е. откладывающиеся и выстилающие ее изнутри) - лигнин и суберин.
Компоненты, адкрустирующие стенку, т.е. откладывающиеся на ее поверхности, - кутин, воск. Основной структурный компонент оболочки - целлюлоза представлена неразветвленными полимерными молекулами, состоящими из 1000-11000 остатков - D глюкозы, соединенных между собой гликозидными связями. Наличие гликозидных связей создает возможность образования поперечных стивок. Благодаря этому, длинные и тонкие молекулы целлюлозы объединяются в элементарные фибриллы или мицеллы. Каждая мицелла состоит из 60-100 параллельно расположенных цепей целлюлозы. Мицеллы сотнями группируются в мицеллярные ряды и составляют микрофибриллы диаметром 10-15 нм. Целлюлоза обладает кристаллическими свойствами благодаря упорядоченному расположению мицелл в микрофибриллах. Микрофибриллы, в свою очередь перевиваются между собой как пряди в канате и объединяются в макрофибриллы. Макрофибриллы имеют толщину около 0,5 мкм. и могут достигать в длину 4мкм. Целлюлоза не обладает ни кислыми, ни щелочными свойствами. Структура клеточной стенки Клеточная стенка (оболочка) является неотъемлемым компонентом клеток растений и грибов и представляет собой продукт их жизнедеятельности. Она придает клеткам механическую прочность, защищает их содержимое от повреждений и избыточной потери воды, поддерживает форму клеток и их размер, а также препятствует разрыву клеток в гипотонической среде. Клеточная стенка участвует в поглощении и обмене различных ионов, т. е. является ионообменником. Через клеточную оболочку осуществляется транспорт веществ.В состав клеточной стенки входят структурные компоненты (целлюлоза у растений и хитин у грибов), компоненты матрикса (гемицеллюлоза, пектин, белки), инкрустирующие компоненты (лигнин, суберин) и вещества, откладывающиеся на поверхности оболочки (кутин и воск).
Функции клеточной стенки Клеточные стенки обеспечивают отдельным клеткам и растению в целом механическую прочность и опору. В некоторых тканях прочность усиливается благодаря интенсивной лигнификации (небольшое количество лигнина присутствует во всех клеточных стенках). Особо важную роль играет лигнификация клеточных стенок у древесных и кустарниковых пород. . Относительная жесткость клеточных стенок и сопротивление растяжению обусловливают тургесцентность клеток, когда в них осмотическим путем поступает вода. Это усиливает опорную функцию во всех растх и служит единственным источником опоры для травянистых растений и для таких органов, как листья, т. е. там, где отсутствует вторичный рост. Клеточные стенки также предохраняют клетки от разрыва в гипотонической среде.
Ориентация целлюлозных микрофибрилл ограничивает и в известной мере регулирует как рост, так и форму клеток, поскольку от расположения этих микрофибрилл зависит способность клеток к растяжению. Если, например, микрофибриллы располагаются поперек клетки, опоясывая ее как бы обручами, то клетка, в которую путем осмоса поступает вода, будет растягиваться в продольном направлении. Стенки клеток эндодермы корня пропитаны суберином и поэтому служат барьером на пути движения воды. У некоторых клеток их видоизмененные стенки хранят запасы питательных веществ; таким способом, например, запасаются гемицеллюлозы в некоторых семенах.
9-Общая характеристика класса растительных белков. Белки́ (протеи́ны, полипепти́ды) — высокомолекулярные органические вещества, состоящие из соединённых в цепочку пептидной связью альфа-аминокислот. В живых организмах аминокислотный состав белков определяется генетическим кодом, при синтезе в большинстве случаев используется 20 стандартных аминокислот. Множество их комбинаций дают большое разнообразие свойств молекул белков. Кроме того, аминокислоты в составе белка часто подвергаются посттрансляционным модификациям, которые могут возникать и до того, как белок начинает выполнять свою функцию, и во время его «работы» в клетке. Часто в живых организмах несколько молекул белков образуют сложные комплексы, например, фотосинтетический комплекс. Функции белков в клетках живых организмов более разнообразны, чем функции других биополимеров — полисахаридов и ДНК. Так, белки-ферменты катализируют протекание биохимических реакций и играют важную роль в обмене веществ. Некоторые белки выполняют структурную или механическую функцию, образуя цитоскелет, поддерживающий форму клеток. Также белки играют важную роль в сигнальных системах клеток, при иммунном ответе и в клеточном цикле. Белки — важная часть питания животных и человека, поскольку в их организме не могут синтезироваться все необходимые аминокислоты и часть из них поступает с белковой пищей. В процессе пищеварения ферменты разрушают потреблённые белки до аминокислот, которые используются при биосинтезе белков организма или подвергаются дальнейшему распаду для получения энергии. Определение аминокислотной последовательности первого белка — инсулина — методом секвенирования белков принесло Фредерику Сенгеру Нобелевскую премию по химии в 1958 году. Первые трёхмерные структуры белков гемоглобина и миоглобина были получены методом дифракции рентгеновских лучей, соответственно, Максом Перуцем и Джоном Кендрю в 1958 году, за что в 1962 году они получили Нобелевскую премию по химии.
Функции белков:
Так же как и другие биологические макромолекулы (полисахариды, липиды) и нуклеиновые кислоты, белки — необходимые компоненты всех живых организмов, они участвуют в большинстве жизненных процессов клетки. Белки осуществляют обмен веществ и энергетические превращения. Белки входят в состав клеточных структур — органелл, секретируются во внеклеточное пространство для обмена сигналами между клетками, гидролиза пищи и образования межклеточного вещества. Многие функции белки выполняют благодаря своей ферментативной активности. Так, ферментами являются двигательный белок миозин, регуляторные белки протеинкиназы, транспортный белок натрий-калиевая аденозинтрифосфатаза и др. Каталитическая функция Наиболее хорошо известная роль белков в организме — катализ различных химических реакций. Ферменты — группа белков, обладающая специфическими каталитическими свойствами, то есть каждый фермент катализирует одну или несколько сходных реакций. Ферменты катализируют реакции расщепления сложных молекул (катаболизм) и их синтеза (анаболизм), а также репликации и репарации ДНК и матричного синтеза РНК. Известно несколько тысяч ферментов; среди них такие, как, например, пепсин, расщепляют белки в процессе пищеварения. В процесс посттрансляционной модификации некоторые ферменты добавляют или удаляют химические группы на других белках. Известно около 4000 реакций, катализируемых белками. Ускорение реакции в результате ферментативного катализа иногда огромно: например, реакция, катализируемая ферментом оротат-карбоксилазой, протекает в 1017 быстрее некатализируемой (78 миллионов лет без фермента, 18 миллисекунд с участием фермента). Молекулы, которые присоединяются к ферменту и изменяются в результате реакции, называются субстратами. Хотя ферменты обычно состоят из сотен аминокислот, только небольшая часть из них взаимодействует с субстратом, и ещё меньшее количество — в среднем 3—4 аминокислоты, часто расположенные далеко друг от друга в первичной аминокислотной последовательности — напрямую участвуют в катализе. Часть фермента, которая присоединяет субстрат и содержит каталитические аминокислоты, называется активным центром фермента.
Структурная функцияСтруктурные белки цитоскелета, как своего рода арматура, придают форму клеткам и многим органоидам и участвуют в изменении формы клеток. Большинство структурных белков являются филаментозными белками: например, мономеры актина и тубулина — это глобулярные, растворимые белки, но после полимеризации они формируют длинные нити, из которых состоит цитоскелет, позволяющий клетке поддерживать форму. Коллаген и эластин — основные компоненты межклеточного вещества соединительной ткани (например, хряща), а из другого структурного белка кератина состоят волосы, ногти, перья птиц и некоторые раковины.
Защитная функция Существуют несколько видов защитных функций белков:
Физическая защита. В ней принимает участие коллаген — белок, образующий основу межклеточного вещества соединительных тканей (в том числе костей, хряща, сухожилий и глубоких слоев кожи)дермы); кератин, составляющий основу роговых щитков, волос, перьев, рогов и др. производных эпидермиса. Обычно такие белки рассматривают как белки со структурной функцией. Примерами этой группы белков служат фибриногены и тромбины, участвующие в свёртывании крови.
Химическая защита. Связывание токсинов белковыми молекулами может обеспечивать их детоксикацию. Иммунная защита. Белки, входящие в состав крови и других биологических жидкостей, участвуют в защитном ответе организма как на повреждение, так и на атаку патогенов. Белки системы комплемента и антитела (иммуноглобулины) относятся к белкам второй группы; они нейтрализуют бактерии, вирусы или чужеродные белки. Антитела, входящие в состав адаптативной иммунной системы, присоединяются к чужеродным для данного организма веществам, антигенам, и тем самым нейтрализуют их, направляя к местам уничтожения. Антитела могут секретироваться в межклеточное пространство или закрепляться в мембранах специализированных В-лимфоцитов, которые называются плазмоцитами. В то время как ферменты имеют ограниченное сродство к субстрату, поскольку слишком сильное присоединение к субстрату может мешать протеканию катализируемой реакции, стойкость присоединения антител к антигену ничем не ограничена.
Регуляторная функция Многие процессы внутри клеток регулируются белковыми молекулами, которые не служат ни источником энергии, ни строительным материалом для клетки. Эти белки регулируют транскрипцию, трансляцию, сплайсинг, а также активность других белков и др. Регуляторную функцию белки осуществляют либо за счёт ферментативной активности (например, протеинкиназы), либо за счёт специфического связывания с другими молекулами, как правило, влияющего на взаимодействие с этими молекулами ферментов. Так, транскрипция генов определяется присоединением факторов транскрипции — белков-активаторов и белков-репрессоров к регуляторным последовательностям генов. На уровне трансляции считывание многих мРНК также регулируется присоединением белковых факторов, а деградация РНК и белков также проводится специализированными белковыми комплексами. Важнейшую роль в регуляции внутриклеточных процессов играют протеинкиназы — ферменты, которые активируют или подавляют активность других белков путём присоединения к ним фосфатных групп.
Сигнальная функция Сигнальная функция белков — способность белков служить сигнальными веществами, передавая сигналы между клетками, тканями, о́рганами и разными организмами. Часто сигнальную функцию объединяют с регуляторной, так как многие внутриклеточные регуляторные белки тоже осуществляют передачу сигналов. Сигнальную функцию выполняют белки-гормоны, цитокины, факторы роста и др. Клетки взаимодействуют друг с другом с помощью сигнальных белков, передаваемых через межклеточное вещество. К таким белкам относятся, например, цитокины и факторы роста. Цитокины — небольшие пептидные информационные молекулы. Они регулируют взаимодействия между клетками, определяют их выживаемость, стимулируют или подавляют рост, дифференцировку, функциональную активность и апоптоз, обеспечивают согласованность действий иммунной, эндокринной и нервной систем. Примером цитокинов может служить фактор некроза опухоли, который передаёт сигналы воспаления между клетками организма.
Транспортная функция Растворимые белки, участвующие в транспорте малых молекул, должны иметь высокое сродство (аффинность) к субстрату, когда он присутствует в высокой концентрации, и легко его высвобождать в местах низкой концентрации субстрата. Примером транспортных белков можно назвать гемоглобин, который переносит кислород из лёгких к остальным тканям и углекислый газ от тканей к лёгким, а также гомологичные ему белки, найденные во всех царствах живых организмов. Некоторые мембранные белки участвуют в транспорте малых молекул через мембрану клетки, изменяя её проницаемость. Липидный компонент мембраны водонепроницаем (гидрофобен), что предотвращает диффузию полярных или заряженных (ионы) молекул. Мембранные транспортные белки принято подразделять на белки-каналы и белки-переносчики. Белки-каналы содержат внутренние, заполненные водой поры, которые позволяют ионам (через ионные каналы) или молекулам воды (через белки-аквапорины) перемещаться через мембрану. Многие ионные каналы специализируются на транспорте только одного иона; так, калиевые и натриевые каналы часто различают эти сходные ионы и пропускают только один из них. Белки-переносчики связывают, подобно ферментам, каждую переносимую молекулу или ион и, в отличие от каналов, могут осуществлять активный транспорт с использованием энергии АТФ. «Электростанция клетки» — АТФ-синтаза, которая осуществляет синтез АТФ за счёт протонного градиента, также может быть отнесена к мембранным транспортным белкам.Запасная (резервная) функция белков К таким белкам относятся так называемые резервные белки, которые запасаются в качестве источника энергии и вещества в семенах растений и яйцеклетках животных; белки третичных оболочек яйца (овальбумины) и основной белок молока (казеин) также выполняют, главным образом, питательную функцию. Ряд других белков используется в организме в качестве источника аминокислот, которые в свою очередь являются предшественниками биологически активных веществ, регулирующих процессы метаболизма.Рецепторная функция Белковые рецепторы могут как находиться в цитоплазме, так и встраиваться в клеточную мембрану. Одна часть молекулы рецептора воспринимает сигнал, которым чаще всего служит химическое вещество, а в некоторых случаях — свет, механическое воздействие (например, растяжение) и другие стимулы. При воздействии сигнала на определённый участок молекулы белок-рецептор происходят её конформационные изменения. В результате меняется конформация другой части молекулы, осуществляющей передачу сигнала на другие клеточные компоненты. Существует несколько механизмов передачи сигнала. Некоторые рецепторы катализируют определённую химическую реакцию; другие служат ионными каналами, которые при действии сигнала открываются или закрываются; третьи специфически связывают внутриклеточные молекулы-посредники. У мембранных рецепторов часть молекулы, связывающаяся с сигнальной молекулой, находится на поверхности клетки, а домен, передающий сигнал, внутри.Моторная (двигательная) функция Целый класс моторных белков обеспечивает движения организма (например, сокращение мышц, в том числе локомоцию (миозин), перемещение клеток внутри организма (например, амебоидное движение лейкоцитов), движение ресничек и жгутиков, а также активный и направленный внутриклеточный транспорт (кинезин, динеин). Динеины и кинезины проводят транспортировку молекул вдоль микротрубочек с использованием гидролиза АТФ в качестве источника энергии. Динеины переносят молекулы и органоиды из периферических частей клетки по направлению к центросоме, кинезины в противоположном направлении. Динеины также отвечают за движение ресничек и жгутиков эукариот. Цитоплазматические варианты миозина могут принимать участие в транспорте молекул и органоидов по микрофиламентам.
. Стуктуры белковой молекулы.Молекулы белков представляют собой линейные полимеры, состоящие из α-L-аминокислот (которые являются мономерами) и, в некоторых случаях, из модифицированных основных аминокислот (правда, модификации происходят уже после синтеза белка на рибосоме). Для обозначения аминокислот в научной литературе используются одно- или трёхбуквенные сокращения. Хотя на первый взгляд может показаться, что использование в большинстве белков «всего» 20 видов аминокислот ограничивает разнообразие белковых структур, на самом деле количество вариантов трудно переоценить: для цепочки всего из 5 аминокислот оно составляет уже более 3 миллионов, а цепочка из 100 аминокислот (небольшой белок) может быть представлена более чем в 10130 вариантах. Белки длиной от 2 до нескольких десятков аминокислотных остатков часто называют пептидами, при большей степени полимеризации — белками, хотя это деление весьма условно. При образовании белка в результате взаимодействия α-аминогруппы (-NH2) одной аминокислоты с α-карбоксильной группой (-COOH) другой аминокислоты образуются пептидные связи. Концы белка называют C- и N-концом (в зависимости от того, какая из групп концевой аминокислоты свободна: -COOH или -NH2, соответственно). При синтезе белка на рибосоме новые аминокислоты присоединяются к C-концу, поэтому название пептида или белка даётся путём перечисления аминокислотных остатков начиная с N-конца. Последовательность аминокислот в белке соответствует информации, содержащейся в гене данного белка. Эта информация представлена в виде последовательности нуклеотидов, причём одной аминокислоте соответствует в ДНК последовательность из трёх нуклеотидов — так называемый триплет или кодон. То, какая аминокислота соответствует данному кодону в мРНК, определяется генетическим кодом, который может несколько отличаться у разных организмов. Синтез белков на рибосомах происходит, как правило, из 20 аминокислот, называемых стандартными. Триплетов, которыми закодированы аминокислоты в ДНК, у разных организмов от 61 до 63 (то есть от числа возможных триплетов (4³ = 64), вычтено число стоп-кодонов (1—3)). Поэтому появляется возможность, что большинство аминокислот может быть закодировано разными триплетами. То есть, генетический код может является избыточным или, иначе, вырожденным. Это было окончательно доказано в эксперименте при анализе мутаций. Генетический код, кодирующий различные аминокислоты имеет разную степень вырожденности (кодируются от 1 до 6 кодонами), это зависит от частоты встречаемости данной аминокислоты в белках, за исключением аргинина. Часто основание в третьем положении оказывается несущественным для специфичности, то есть одна аминокислота может быть представлена четырьмя кодонами, различающимися только третьим основанием. Иногда различие состоит в предпочтении пурина пиримидину. Это называют вырожденностью третьего основания.
9-Классификация и характеристика углеводов В химическом плане углеводы можно определить как альдегидные или кетонные производные полиатомных спиртов или как соединения, при гидролизе которых образуются эти производные. Моносахариды – углеводы, которые не могут быть гидролизованы до более простых форм. Их можно подразделить на триозы, тетрозы, петнозы, гексозы, гептозы и октозы в зависимости от числа содержащихся в их молекуле атома углерода; их можно также разделить на альдозы и кетозы в зависимости от присутствия альдегидной или кетоновой группы. Из гексоз наиболее важное значение имеют глюкоза, галактоза, фруктоза и манноза.Гликозиды – соединения, образующиеся путем конденсации моносахарида с гидроксильной группой другого соединения, которым может быть другой моносахарид или вещество неуглеводной природы. Гликозиды найдены в составе многих лекарств и пряностей, они являются также компонентами животных тканей. Сердечные гликозиды обнаружены во многих растх и влияют на работу сердечной мышцы. Дисахариды при гидролизе дают две молекулы моносахарида (одинаковых или различных). Примером служит сахароза, лактоза или мальтоза. Олигосахариды при гидролизе дают 3-6 моносахаридов. Физиологически важными дисахаридами являются мальтоза, сахароза, лактоза и трегалоза. Полисахариды дают при гидролизе более 6 молекул моносахаридов. Они могут быть линейными или разветвленными. Примерами служат крахмал и декстрины.
10-Общая характеристика класса липидов растении. Липиды- разнообразные по структуре соединения, характеризующиеся почти полным отсутствием полярных групп в строении молекулы. В связи с этим липиды растворимы в неполярных жидкостях (эфир, хлороформ). В агрономии все в-ва, растворимые в этих растворителях, получили название «сырого жира». Характерной особенностью липидов явл. высокое содержание в молекулах гидрофобных радикалов и групп, что делает их нерастворимыми в воде. Все липиды могут быть разделены на две группы: жиры и жироподобные в-ва, или липоиды. К жироподобным в-вам относят фосфолипиды, сфинголипиды, гликолипиды, стероиды (играют опред. роль в структуре клеточных мембран, являются витаминами группы D), воски(защищают), кутин и суберин, растворимые в жирах пигменты (хлорофиллы, каротиноиды, фикобилины). Обладают гидрофобными сво-ми. Растворимы в бензине, бензоле, хлороформе, эфирах, ацетоне. Участвуют в адсорбции, откладываются в запас, защитные функции (предохраняют от обезвоживания).
11-Общая характеристика класса нуклеиновых кислот. Их состав, структура и функции. НК- это высокомолекулярные биополимеры, сост. из соединенных м/у собой фосфодиэфирными связями нуклеотидов. Нуклеотид- хим. соединение остатков трех в-в: азотистого основания, моносахарида, фосф. кислоты. В зависимости от набора азотистых оснований, сахара и структуры молекулы НК подразд. на дезоксирибонуклеиновую(ДНК) и рибонуклеиновою (РНК) кислоты. в РНК входят (аденин, гуанин, цитозин, урацил, сахар- рибоза. в ДНК входят (аденин, гуанин, цитозин, тимин, сахар- дезоксирибоза). НК играют роль в хранении и передаче данных. НК имеют структуру в основе кт. лежит принцип комплементарности, она проявл. в том, что азотистые основания взаимодействуют др. с др. посредством образования водородных связей строго попарно- А с Т или У, Г с Ц. В интерфазе клеточного деления ДНК входит в состав ядерного в-ва- хроматина. Основой структуры хроматина явл. нуклеосомы. Структура молекул РНК достаточно разнообразна. Так, матричная (информационная) РНК предст. собой одинарную спираль, для транспортной РНК характерно сочетание одинарных и спаренных участков, рибосомальная РНК имеет более сложную структуру. Все функции НК обеспечиваются принципами комплементарности и матричного воспроизводства. Роль ДНК сост. в хранении, передаче и реализации наследственной информации. Функции НК: 1. реплекация ( репликация НК осуществляется благодаря образованию водородных связей м/у комплементарными основаниями исходной и дочерней цепей) 2. транскрипция (в рез-те транскрипции ДНК образуются клеточные РНК (мРНК, рРНК и тРНК). 3. трансляция (генетическая информация, закодированная в нуклеотидной последовательности ДНК, переводится не только на язык нукл
12- КЛАССИФИКАЦИЯ ФЕРМЕНТОВ
По первой в истории изучения ферментов классификации их делили на две группы: гидролазы, ускоряющие гидролитические реакции, и десмолазы, ускоряющие реакции негидролитического распада. Затем была сделана попытка разбить ферменты на классы по числу субстратов, участвующих в реакции. В соответствии с этим ферменты классифицировали на три группы. 1. Катализирующие превращения двух субстратов одновременно в обоих направлениях: А+В) С+D. 2. Ускоряющие превращения двух субстратов в прямой реакции и одного в обратной: А+В) С. 3. Обеспечивающие каталитическое видоизменение одного субстрата как в прямой, так и в обратной реакции: А) В.Одновременно развивалось направление, где в основу классификации ферментов был положен тип реакции, подвергающейся каталитическому воздейсвию. Наряду с ферментами, ускоряющими реакции гидролиза (гидролазы), были изучены ферменты, участвующие в реакциях переноса атомов и атомных групп (феразы), в изомеризации (изомеразы), расщеплении (лиазы), различных синтезах (синтетазы) и т. д. Это направление в классификации ферментов оказалось наибо-лее плодотворным, так как объединяло ферменты в группы не по надуманным, формальным признакам, а по типу важнейших биохимических процессов, лежащих в основе жизнедеятельности любого организма. По этому принципу все ферменты делят на 6 классов.1. Оксидоредуктазы — ускоряют реакции окисления — восстановления.2. Трансферазы — ускоряют реакции переноса функциональных групп и молекулярных остатков. 3. Гидролазы — ускоряют реакции гидролитического распада. 4. Лиазы — ускоряют негидролитическое отщепление от субстратов определенных групп атомов с образованием двойной связи (или присоединяют группы атомов по двойной связи). 5. Изомеразы — ускоряют пространственные или структурные перестройки в пределах одной молекулы. 6. Лигазы — ускоряют реакции синтеза, сопряженные с распадом богатых энергией связей.Эти классы и положены в основу новой научной классификации ферментов.К классу оксидоредуктаз относят ферменты, катализирующие реакции окисления — восстановления. Окисление протекает как процесс отнятия атомов Н (электронов) от субстрата, а восстановление — как присоединение атомов Н (электронов) к акцептору.В класс трансфераз входят ферменты, ускоряющие реакции переноса функциональных групп и молекулярных остатков от одного соединения к другому. Это один из наиболее обширных классов: он насчитывает около 500 индивидуальных ферментов. В зависимости от характера переносимых группировок различают фосфотрансферазы, аминотрансферазы, гликозилтрансферазы, ацилтрансферазы, трансферазы, переносящие одноуглеродные остатки (метилтрансферазы, формил-трансферазы), и др. Например, амидазы ускоряют гидролиз амидов кислот. Из них важную роль в биохимических процессах в организме играют уреаза, аспарагиназа и глутаминаза.
13-Общие свойства ферментов
Будучи белками, ферменты обладают всеми их свойствами. Вместе с тем биокатализаторы характеризуются рядом специфических качеств, тоже вытекающих из их белковой природы. Эти качества отличают ферменты от катализаторов обычного типа. Сюда относятся термолабильность ферментов, зависимость их действия от значения рН среды, специфичность и, наконец, подверженность влиянию активаторов и ингибиторов. Термолабильность ферментов объясняется тем, что температура, с одной стороны, воздействует на белковую часть фермента, приводя при слишком высоких значениях к денатурации белка и снижению каталитической функции, а с другой стороны, оказывает влияние на скорость реакции образования фермент-субстратного комплекса и на все последующие этапы преобразования субстрата, что ведет к усилению катализа. Зависимость каталитической активности фермента от температуры выражается типичной кривой. До некоторого значения температуры (в среднем до 50 °С) каталитическая активность растет, причем на каждые 10 °С примерно в 2 раза повышается скорость преобразования субстрата. В то же время постепенно возрастает количество инактивированного фермента за счет денатурации его белковой части. При температуре выше 50 °С денатурация ферментного белка резко усиливается и, хотя скорость реакций преобразования субстрата продолжает расти, активность фермента, выражающаяся количеством превращенного субстрата, падает. Детальные исследования роста активности ферментов с повышением температуры, проведенные в последнее время, показали более сложный характер этой зависимости, чем указано выше: во многих случаях она не отвечает правилу удвоения активности на каждые 10°С в основном из-за постепенно нарастающих конформационных изменений в молекуле фермента. Температура, при которой каталитическая активность фермента максимальна, называется его температурным оптимумом.Температурный оптимум для различных ферментов неодинаков. В общем для ферментов животного происхождения он лежит между 40 и 50°С, а растительного — между 50 и 60°С. Однако есть ферменты с более высоким температурным оптимумом, например, у папаина (фермент растительного происхождения, ускоряющий гидролиз белка) оптимум находится при 80°С. В то же время у каталазы (фермент, ускоряющий распад Н2O2 до Н2О и O2) оптимальная температура действия находится между 0 и -10°С, а при более высоких температурах происходит энергичное окисление фермента и его инактивация. Зависимость активности фермента от значения рН среды была установлена свыше 50 лет назад. Для каждого фермента существует оптимальное значение рН среды, при котором он проявляет максимальную активность. Большинство ферментов имеет максимальную активность в зоне рН поблизости от нейтральной точки. В резко кислой или резко щелочной среде хорошо работают лишь некоторые ферменты.Переход к большей или меньшей (по сравнению с оптимальной) концентрации водородных ионов сопровождается более или менее равномерным падением активности фермента.Влияние концентрации водородных ионов на каталитическую активность ферментов состоит в воздействии ее на активный центр. При разных значениях рН в реакционной среде активный центр может быть слабее или сильнее ионизирован, больше или меньше экранирован соседними с ним фрагментами полипептидной цепи белковой части фермента и т.п. Кроме того, рН среды влияет на степень ионизации субстрата, фермент-субстратного комплекса и продуктов реакции, оказывает большое влияние на состояние фермента, определяя соотношение в нем катионных и анионных центров, что сказывается на третичной структуре белковой молекулы. Последнее обстоятельство заслуживает особого внимания, так как определенная третичная структура белка-фермента необходима для образования фермент-субстратного комплекса.Специфичность — одно из наиболее выдающихся качеств ферментов. Эго свойство их было открыто еще в прошлом столетии, когда было сделано наблюдение, что очень близкие по структуре вещества — пространственные изомеры (a — и b-метилглюкозиды) расщепляются по эфирной связи двумя совершенно разными ферментами.
еотидной.
14-Кинетика ферментативных реакций
Кинетика ферментативных реакций определяется образованием фермент-
K1 K2
E +S → ES → E + P V= __V max [s_]_ A+B=AB+P=AP+D
Vm + [s]
субстратного комплекса: Где Е - фермент, S - субстрат, ES - фермент-убстратный комплекс, реакция образования которого обратима и характеризуется константами К1 и К-1 соответственно. Распад фермент-субстратного комплекса протекает по уравнению первого порядка, он практически необратим и характеризуется константой скорости К2. Эта стадия
процесса является более медленной, т.е. лимитирующей. Начальная скорость (Vo). При обычных условиях, когда [S] >> [E], начальная скорость прямо пропорциональна концентрации фермента. Максимальная скорость (Vmax). При фиксированной концентрации фермента, скорость реакции стремится к конечному максимальному значению, в то время как концентрация субстрата растет. Насыщение фермента субстратом наступает, когда весь фермент включен в фермент-субстратный комплекс. Константа Михаэлиса (Km). В случае, когда все активные центры заняты, и свободные молекулы фермента отсутствуют, Vo=Vmax. При таком условии говорят о 100% насыщении. При 50% насыщении, когда Vo=1/2 Vmax из уравнения Михаэлиса - Ментен следует: Vmax / 2 = Vmax [S] / Km + [S], или в преобразованном виде: Km + [S] = 2 [S]; Km = [S]. Следовательно, Km имеет размерность концентрации. Таким образом, Кm – это такая концентрация субстрата, которая необходима для связывания половины имеющегося фермента и достижения половины максимальной скорости. Из этого определения следует, что Km можно использовать для оценки сродства фермента по отношению к данному субстрату. Оценить субстратную специфичность можно по такому правилу: чем ниже значение Km, тем лучше (предпочтительнее) субстрат для данного фермента. Km и Vmax - кинетические параметры, отражающие механизмы действия фермента. Кинетика ферментативных реакций Vmax отражает эффективность действия фермента. Для сравнения каталитической активности различных ферментов необходимо выразить Vmax через количество каждого фермента. Такое преобразование приводит к величине, которую называют молярной активностью (или числом оборотов фермента). Она выражается числом моль субстрата, реагирующего с одним моль фермента за единицу времени. Активность фермента можно выразить также в единицах (ед. или Е) активности. Одна единица катализирует превращение субстрата со скоростью1 мкмоль /мин. Удельная активность - это активность в единицах, отнесённая к 1 мг белка.
Ингибиторы ферментов
Действие ферментов можно полностью или частично подавить (ингибировать) определенными химическими веществами (ингибиторами). По характеру действия ингибиторы могут быть обратимыми и необратимыми. В основе этого деления лежит прочность соединения ингибитора с ферментом. Другой способ деления ингибиторов основывается на характере места их связывания. Одни из них связываются с ферментом в активном центре, а другие - в удаленном от активного центра месте. Они могут связывать и блокировать функциональную группу молекулы фермента, необходимую для проявления его активности. При этом они необратимо, часто ковалентно, связываются с ферментом или фермент - субстратным комплексом и необратимо изменяют нативную конформацию. Это, в частности, объясняет действие Hg2+, Pb2+, соединений мышьяка. Ингибиторы такого рода могут быть полезны при изучении природы ферментативного катализа. Например, диизопропилфторфосфат ингибирует ферменты, имеющие серин в активном центре. Таким ферментом является ацетилхолинэстераза, катализирующая
следующую реакцию:
Реакция происходит каждый раз после проведения нервного импульса, прежде чем второй импульс будет передан через синапс. Диизопропилфторфосфат - одно из отравляющих веществ нервно-паралитического действия, так как приводит к утрате способности нейронов проводить нервные импульсы. Действие диизопропилфторфосфата на фермент Терапевтическое действие аспирина как жаропонижающего и фермента.
15- витамины и их роль в жизнь растение
Витамины – Уникальные функции витаминов определяются тем , что они как правило является коферментами основных каталитических белков или непосредственно участвуют в важнейших биохимических реакциях.Так витамин С (аскорбиновая кислота) необходим для осуществления окислительно-восстановительных процессов.Роль этого витамина многокрано возрастает при заболеваниях раст , животного ,животного, человека. Витамины не менее необходимы растм, чем животным и человеку. При недостатке витаминов у растений нарушается обмен веществ, замедляется рост. Исследователи продолжают выяснять физиологическую роль витаминов. Уже установлено, что витамины принимают непосредственное участие, например, в фотосинтезе, питании и размножении.
16-Механизмы выделения и поглощение веществ растительной клеткой
Из внешней среды в клетку раст непрерывно поступают питательные вещества. Это естественный процесс, без которого жизнедеятельность клетки была бы невозможна. Причем клетка осуществляет поглощение, несмотря на ограниченную проницаемость плазмалеммы. Живая клетка обладает способностью к избирательному накоплению питательных веществ. Клетка накапливает калий в концентрации, превышающей его содержание в морской воде в десятки раз. Вместе с тем морская вода содержит значительно большее количество натрия по сравнению с клеткой. Таким образом, клетка, несмотря на наличие полупроницаемой мембраны, обладает способностью к избирательному накоплению растворенных веществ. На протяжении истории физиологии растений учеными были созданы многочисленные теории относительно механизмов проникновения растворенных веществ в клетку. Многие из этих теорий оказались несостоятельными, в частности из-за того, что под проникновением веществ в клетку понималось только их поступление в клеточный сок.
Поглощение питательных веществ клеткой может быть пассивным и активным. Пассивное поглощение — это поглощение, не требующее затраты энергии. Оно связано с процессом диффузии и идет по градиенту концентрации данного вещества. С термодинамической точки зрения направление диффузии определяется химическим потенциалом вещества. Чем выше концентрация вещества, тем выше его химический потенциал. Передвижение идет в сторону меньшего химического потенциала. Необходимо отметить, что направление движения ионов определяется не только химическим, но также электрическим потенциалом. Следовательно, пассивное передвижение ионов может идти по градиенту химического и электрического потенциала. Таким образом, движущей силой пассивного транспорта ионов через мембраны является электрохимический потенциал.
Электрический потенциал на мембране — трансмембранный потенциал может возникать в силу разных причин:
1.Если поступление ионов идет по градиенту концентрации (градиенту-химического потенциала), однако благодаря разной проницаемости мембраны с большей скоростью поступает либо катион, либо анион. В силу этого на мембране возникает разность электрических потенциалов, что, в свою очередь, приводит к диффузии противоположно заряженного иона.
2. При наличии на внутренней стороне мембраны белков, фиксирующих определенные ионы, т. е. иммобилизирующих их. За счет фиксированных зарядов создается дополнительная возможность поступления ионов противоположного заряда (доннановское равновесие) .
3. В результате активного (связанного с затратой энергии) транспорта либо катиона, либо аниона. В этом случае противоположно заряженный ион может передвигаться пассивно по градиенту электрического потенциала. Явление, когда потенциал генерируется активным поступлением через мембрану ионов одного заряда, носит название электрогенного насоса. Термин «насос» показывает, что поступление идет с потреблением свободной энергии.
Активный транспорт — это транспорт, идущий против электрохимического потенциала с затратой энергии, выделяющейся в процессе метаболизма (рис.11).
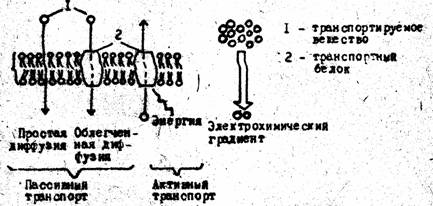
Рис.11. Пассивный и активный транспорт
Имеется ряд доказательств существования активного транспорта ионов. В частности, это опыты по влиянию внешних условий. Так, оказалось, что поступление ионов зависит от температуры. В определенных пределах с повышением температуры скорость поглощения веществ клеткой возрастает. В отсутствие кислорода, в атмосфере азота, поступление ионов резко тормозится и может даже наблюдаться выход солей из клеток корня наружу. Под влиянием дыхательных ядов, таких, как KCN, СО, поступление ионов также затормаживается. С другой стороны, увеличение содержания АТФ усиливает процесс поглощения. Все это указывает на то, что между поглощением солей и дыханием существует тесная связь.
Многие исследователи приходят к выводу о тесной взаимосвязи между поглощением солей и синтезом белка. Так, хлорамфеникол — специфический ингибитор синтеза белка — подавляет и поглощение солей. Активное поступление ионов осуществляется с помощью особых транспортных механизмов — насосов. Насосы подразделяются на две группы:
1.Электрогенные (упомянутые ранее), которые осуществляют активный транспорт иона какого-либо одного заряда только в одном направлении. Этот процесс ведет к накоплению заряда одного типа на одной стороне мембраны.
2. Электронейтральные, при которых перенос иона в одном направлении сопровождается перемещением иона такого же знака в противоположном либо перенос двух ионов с одинаковыми по величине, но разными по знаку зарядами в одинаковом направлении.
Способность клетки к избирательному накоплению питательных солей, зависимость поступления от интенсивности обмена служат доказательством того, что наряду с пассивным имеет место и активное поступление ионов. Оба процесса часто идут одновременно и бывают настолько тесно связаны, что разграничить их трудно.
18- Диффузия — это процесс, ведущий к равномерному распределению молекул растворенного вещества и растворителя. Как всякое движение, диффузия требует энергии. Диффузия всегда направлена от большей концентрации данного вещества к меньшей, от системы, обладающей большей свободной энергией, ксистеме с меньшей свободной энергией. Свободной энергией называется часть внутренней энергии системы, которая может быть превращена в работу. Свободная энергия, отнесенная к 1 молю вещества, носит название химического потенциала. Таким образом, химический потенциал — это мера энергии, которую данное вещество использует на реакции или движение. Химический потенциал — функция концентрации. Скорость диффузии зависит от температуры, природы вещества и разности концентраций. Чем выше концентрация данного вещества, тем выше его активность и его химический потенциал. Диффузионное передвижение вещества всегда идет от большего к меньшему химическому потенциалу. Наибольший химический потенциал у чистой воды. Добавление к воде молекул растворенного вещества приводит к возникновению связи между молекулами воды и растворенного вещества, что уменьшает ее активность, еесвободную энергию, ее химический потенциал. В том случае, если диффундирующие вещества встречают на своем пути мембрану, движение замедляется, а в некоторых случаях прекращается.
Диффузия воды по направлению от своего большего к меньшему химическому потенциалу через мембрану носит название осмоса.
Иначе говоря, осмос — это диффузия воды или другого растворителя через полупроницаемую перепонку, вызванная разностью концентраций или разностью химических потенциалов. Осмос — результат неравенства химических потенциалов воды по разные стороны мембраны.
Идеальная полупроницаемая мембрана пропускает молекулы воды и не пропускает молекулы растворенного вещества. В 1877 г. немецкий физиологПфеффер приготовил искусственную полупроницаемую мембрану. Для этого в пористый фарфоровый сосуд наливали раствор медного купороса и помещали в другой сосуд, в свою очередь заполненный раствором ферроцианида калия. В порах первого фарфорового сосуда растворы соприкасались и реагировали друг с другом. В результате в порах образовалась пленка из ферроцианида меди [Сu2Fe(СN)6], которая обладала полупроницаемостью. Таким образом, была создана как бы модель клетки: полупроницаемая пленка имитировала цитоплазму, а стенки сосуда —пектоцеллюлозную оболочку. Сосуд, в порах которого образовалась полупроницаемая мембрана, заполненный раствором сахарозы, помещали в воду. Такой прибор получил название осмометра (рис.9).
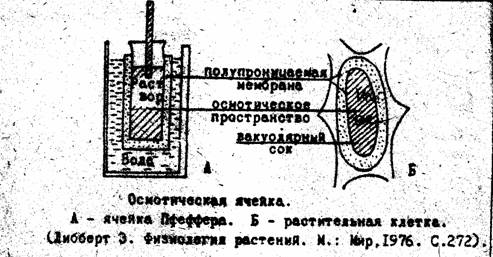
Рис.9. Осмометр Пфеффера
Химический потенциал воды во внутреннем сосуде будет тем меньше, чем выше концентрация сахарозы. Таким образом, поступление воды в раствор через полупроницаемую перегородку обусловливается разностью между свободной энергией чистой воды и раствора и происходит самопроизвольно по градиенту свободной энергии воды. В осмометре при наличии полупроницаемой мембраны вода будет поступать в раствор, который при этом будет становиться все более разбавленным и движение воды будет замедляться. Однако равновесия не наступит, поскольку возникнет гидростатическое давление. Если к осмометру присоединить трубку, вода будет подниматься по ней. Наконец давление столба воды уравновесит силу, с которой молекулы воды поступают в осмометр. Такимобразом, энергия молекул воды, которая уменьшилась благодаря введению растворенного вещества, восполнится давлением столба воды либо грузом, т. е. давлением, которое мы приложим извне. Это давление повышает химический потенциал раствора (Iр), делая его равным химическому потенциалу чистой воды (IВ).
Согласно закону термодинамики самопроизвольно идут только процессы, сопровождающиеся выделением энергии. В большинстве случаев измерить свободную энергию в абсолютном выражении не представляется возможным. Однако можно измерить разность между конечным (g2) и начальным энергетическим состоянием (g1). Поскольку g1 больше g2, то изменение Δg будет иметь отрицательное значение. В нашем случае g1— это химический потенциал чистой воды, a g2—это химический потенциал воды после добавления растворенного вещества. Δg будет равно, но противоположно по знаку тому давлению, которое надо приложить к системе, чтобы предотвратить поступление в него воды через полупроницаемую мембрану. Δg и будет осмотический потенциал (Ψосм) раствора.
Таким образом, осмотический потенциал равен разности между химическим потенциалом раствора и химическим потенциалом чистой воды и всегда отрицателен. Осмотический потенциал показывает недостаток энергии в растворе по сравнению с чистой водой, вызванный взаимодействием вода — растворенное вещество. Иначе говоря, осмотический потенциал показывает, насколько прибавление растворенного вещества снижает активность воды.
Осмотический потенциал относится к так называемым коллигативным свойствам раствора, таким, как понижение точки замерзания или повышение точки кипения. Все эти показатели зависят от молярной концентрации. 1 моль раствора любого недиссоциированного вещества имеет осмотический потенциал 22,7 бара. Поскольку уменьшение химического потенциала, или активности воды, пропорционально числу частиц, то при растворении диссоциированных веществ абсолютное значение осмотического потенциала будет больше, для чего вводится соответствующий (изотонический) коэффициент. Надо учесть, что осмотический потенциал любого раствора проявляется только в условиях системы раствор — полупроницаемая мембрана — растворитель.
Сказанное дает возможность измерить осмотический потенциал раствора (Ψосм). Присоединив манометр, можно измерить давление, которое надо приложить к системе, чтобы предотвратить поступление воды в раствор. Оно будет по абсолютной величине равно, но противоположно по знаку осмотическому потенциалу раствора. Этапы поступления ионов
Поглощение ионов клеткой начинается с их взаимодействия с клеточной оболочкой. Еще работами Д. А. Сабинина и И. И. Колосова было показано, что клеточная оболочка способна к быстрой адсорбции ионов. Причем эта адсорбция в ряде случаев носит обменный характер. В дальнейшем в опытах с выделенными клеточными оболочками было показано, что их можно рассматривать как ионообменник. На поверхности клеточной оболочки оказываются адсорбированными ионы Н+ и NСОз-, которые в эквивалентных количествах меняются на ионы, находящиеся во внешней среде. Ионы могут частично локализоваться вмежмицеллярных и межмолекулярных промежутках клеточной стенки, частично связываться и фиксироваться в клеточной стенке электрическими зарядами. Первый этап поступления характеризуется большой скоростью и обратимостью. Поступившие ионы легко вымываются. Это диффузионный пассивный процесс, идущий по градиенту электрохимического потенциала.
Объем клетки, доступный для свободной диффузии ионов, получил название свободного пространства (СП). В СП включаются клеточные стенки и промежутки, которые могут возникать между клеточной стенкой и плазмалеммой. Поскольку в клеточную оболочку входят амфотерные соединения (белки), заряд которых меняется при разных рН, то в зависимости от рН скорость адсорбции катионов и анионов также может меняться. Для того чтобы поступить в цитоплазму и включиться в метаболизм клетки, ионы должны пройти через мембрану — плазмалемму (второй этап поступления). Спорным является вопрос о том, существуют ли в мембранах поры или каналы. Вероятно наличие каналов, образованных белками, пронизывающими мембрану. Перенос ионов через мембрану может идти пассивным и активным путем. Наиболее распространено мнение, что ионы проникают через мембрану с помощью переносчиков. Опыты, проведенные на искусственных липидных мембранах, показа ли, что перенос ионов (например, К+) может проходить под влиянием некоторых антибиотиков, вырабатываемых бактериями и грибами,— ионофоров. В одних случаях катион входит во внутреннюю полость молекулы ионофора (рис. 12). Образованный комплексдиффундирует через мембраны во много раз быстрее по сравнению со свободным ионом. Ионофоры другого типа взаимодействуют с мембранами и, таким образом, формируют поры.
ФОТОСИНТЕЗ
1.фотосинтез – основа биоэнергетики растений. Значение для обеспечения автотрофности. Космическая роль фотосинтеза.
Фотосинтез – это процесс трансформации поглощенной энергии света в химическую энергию органических соединений. Причем в процессе восстанавливаются не только СО2, но и нитраты или сульфаты, а энергия может быть направлена на различные эндергонические процессы, в том числе на транспорт веществ.
Все формы жизни во Вселенной нуждаются в энергии для роста и поддержания жизни. Водоросли, высшие раст и некоторые типы бактерий улавливают непосредственно энергию солнечного излучения и используют ее для синтеза основных пищевых веществ. Животные не умеют использовать солнечный свет непосредственно в качестве источника энергии, они получают энергию, поедая раст или других животных, питающихся растми. Итак, в конечном счете источником энергии для всех метаболических процессов на нашей планете, служит Солнце, а процесс фотосинтеза необходим для поддержания всех форм жизни на Земле.
Мы пользуемся ископаемым топливом — углем, природным газом, нефтью и т. д. Все эти виды топлива — не что иное, как продукты разложения наземных и морских растений или животных, и запасенная в них энергия была миллионы лет назад получена из солнечного света. Ветер и дождь тоже обязаны своим возникновением солнечной энергии, а следовательно, энергия ветряных мельниц и гидроэлектростанций в конечном счете также обусловлена солнечным излучением.
Важнейший путь химических реакций при фотосинтезе — это превращение углекислоты и воды в углероды и кислород. Суммарную реакцию можно описать уравнением СO2+H2O [СH2O]+O2
Углеводы, образующиеся в этой реакции, содержат больше энергии, чем исходные вещества, т. е. СO2 и H2O. Таким образом, за счет энергии Солнца энергетические вещества (СO2 и H20) превращаются в богатые энергией продукты — углеводы и кислород. Энергетические уровни различных реакций, описанных суммарным уравнением, можно охарактеризовать величинами окислительно-восстановительных потенциалов, измеряемых в вольтах. Значения потенциалов показывают, сколько энергии запасается или растрачивается в каждой реакции. Итак, фотосинтез можно рассматривать как процесс образования лучистой энергии Солнца в химическую энергию растительных тканей.
Содержание СO2 в атмосфере остается почти полным, несмотря на то, что углекислый газ расходуется в процессе фотосинтеза. Дело в том, что все раст и животные дышат. В процессе дыхания в митохондриях кислород, поглощаемый из атмосферы живыми тканями, используется для окисления углеводов и других компонентов тканей с образованием в конечном счете двуокиси углерода и воды и с сопутствующим выделением энергии. Высвобождающаяся энергия запасается в высокоэнергетические соединения — аденозинтрифосфат (АТФ), который и используется организмом для выполнения всех жизненных функций. Таким образом дыхание приводит к расходованию органических веществ и кислорода и увеличивает содержание СO2 на н планете. На процессы дыхания во всех живых организмах и на сжигание всех видов топлива, содержащих углерод, в совокупности расходуется в масштабах Земли в среднем около 10000 тонн O2 в секунду. При такой скорости.потребления весь кислород в атмосфере должен бы иссякнуть примерно, через 3000 лет. К счастью для нас, расход органических веществ и атомного кислорода уравновешивается созданием углеводов и кислорода в результате фотосинтеза. В идеальных условиях скорость фотосинтеза в зеленых тканях растений примерно в 30 раз превышает скорость дыхания в тех же тканях, таким образом, фотосинтез служит важным фактором, регулирующим содержание O2 на Земле.
2. Общее и парциальные уравнения фотосинтеза.
Общее уравнение фотосинтеза:6CO2 + 6 H2O ––– (свет, хлоропласты)–––> C6H12O6 + 6 O2 . В ходе этого процесса из веществ, бедных энергией – углекислого газа и воды – образуется углевод глюкоза (C6H12O6) – богатое энергией вещество, кроме того образуется также молекулярный кислород. Очень образно описал это явление русский ученый, физиолог растений – К.А. Тимирязев.
Уравнению фотосинтеза соответствуют две парциальные реакции:
1)световая
реакция или превращение энергии -процесс
локализации в тилакойдах хлоропласта.
 ]
]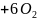
2)темновая
реакция или превращение веществ -процесс
локализации в строме хлоропласта.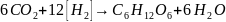
3. Лист как орган фотосинтеза. Лист-орган фотосинтеза, который поглощает и запасает солнечную энергию и осуществляет газообмен с атмосферой. В среднем лист поглощает 80-85% фотосинтетически активной радиации (ФАР) и 25%энергии инфракрасных лучей. На фотосинтез расходуется 1.5-2% поглощенной ФАР, остальная энергия расходуется на испарение воды- транспирацию. Лист отличается плоской структурой и небольшой толщиной. Большое значение для эффективного улавливания света имеет архитектоника растений - пространственное расположение органов, те листья располагаются на растении не заслоняя друг друга. Особенности обеспечивающие эффективность фотосинтеза:1)наличие покровной ткани-эпидермиса, защищающего лист от излишней потери воды. Клетки нижнего и верхнего эпидермиса лишены хлоропластов и имеют крупные вакуоли. как линзы фокусируют свет на расположенную глубже хлорофильную ткань. Нижний и верхний эпидермис имеют устьица, через которые происходит диффузия СО2 внутрь листа.2)наличие специализированной фотосинтетической ткани-хлоренхимы. Основная хлорофилоносная ткань - палисадная паренхима, которая расположена на освещаемой части листа. В каждой клетке палисадной паренхимы находится 30-40 хлоропластов.3)наличие сильно развитой системы жилок проводящих путей, что обеспечивает быстрый отток ассимилятов и снабжение фотосинтезирующих клеток водой и необходимыми минеральными веществами. В зависимости от внешних условий при кот происходит формирование и функционирование листьев анатомическое строение их может меняться.
4. Структура и функции хлоропластов.Хлоропласты — пластиды высших растений, в которых идет процесс фотосинтеза, т. е. использование энергии световых лучей для образования из неорганических веществ (углекислого газа и воды) органических веществ с одновременным выделением в атмосферу кислорода. Хлоропласты имеют форму двояковыпуклой линзы, размер их около 4-6 мкм. Находятся они в паренхимных клетках листьев и других зеленых частей высших растений. Число их в клетке варьирует в пределах 25-50.
Снаружи хлоропласт покрыт оболочкой, состоящей из двух липопротеиновых мембран, внешней и внутренней. Обе мембраны имеют толщину около 7нм, они отделены друг от друга межмембранным пространством около 20-30нм. Внутренняя мембрана хлоропластов, как и других пластид образует складчатые впячивания внутрь матрикса или стромы. В зрелом хлоропласте высших растений видны два типа внутренних мембран. Это- мембраны, образующие плоские, протяженные ламеллы стромы, и мембраны тилакоидов, плоских дисковидных вакуолей или мешков.
Основная функция хлоропластов, состоит в улавливании и преобразовании световой энергии.
В состав мембран, образующих граны, входит зеленый пигмент — хлорофилл. Именно здесь происходят световые реакции фотосинтеза — поглощение хлорофиллом световых лучей и превращение энергии света в энергию возбужденных электронов. Электроны, возбужденные светом, т. е. обладающие избыточной энергией, отдают свою энергию на разложение воды и синтез АТФ. При разложении воды образуются кислород и водород. Кислород выделяется в атмосферу, а водород связывается белком ферредоксином.
Хлоропласты обладают известной автономией в системе клетки. В них имеются собственные рибосомы и набор веществ, определяющих синтез ряда собственных белков хлоропласта. Имеются также ферменты, работа которых приводит к образованию липидов, входящих в состав ламелл, и хлорофилла. Благодаря всему этому хлоропласты способны самостоятельно строить собственные структуры. Еще одной очень важной функцией является, усвоение углекислоты в хлоропласте или, как принято говорить, фиксация углекислоты, то есть включение ее углерода в состав органических соединений
5. Пигменты фотосинтетического аппарата (общ.характеристика)Способность растений осуществлять фотосинтез связана с наличием у них пигментов. Главнейшим из них является магнийсодержащий порфириновый пигмент — хлорофилл.
В природе встречается пять разных типов хлорофилла, которые незначительно различаются по своей молекулярной структуре. Хлорофилл а присутствует у всех водорослей и высших растений; хлорофилл b — у зеленых, харовых и эвглеповых и у высших растений; хлорофилл с — у бурых водорослей, золотистых, диатомей и динофлагеллат; хлорофилл d — у красных водорослей; хлорофилл е обнаружен лишь однажды, по-видимому, это хлорофилл с; наконец, различные виды бактериохлорофилла — у фотосинтезирующих бактерий. Для синезеленых и красных водорослей характерно наличие билипротеинов: фикоцианина и фикоэритрина. Наиболее хорошо изучен хлорофилл а. Молекула его состоит из четырех пиррольных колец, с азотом которых связан атом магния, а к одному из колец присоединен одноатомный ненасыщенный спирт фитол.
Молекула хлорофилла встроена в мембрану — погружена гидрофобной фитольной цепью в ее липидную часть. Чистый раствор хлорофилла а имеет максимум поглощения при 663 нм. В интактной, неповрежденной, нормально функционирующей клетке хлорофилл характеризуется еще максимумами поглощения при 672 и 683 нм. Высокая эффективность поглощения света хлорофиллами обусловлена наличием в их молекуле большого числа сопряженных двойных связей.
6.Хлорофиллы (химические и оптические свойства, структура и функции)
По химическому составу хлорофилл представляет сложный эфир дикарбоновой кислоты хлорофиллина. Хлорофиллин представляет собой азотосодержащееметаллоорганическое соединение, относящееся к магний-порфиринам. В центре молекуле хлорофилла расположен атом магния, который соединён с четырьмя азотами пиррольных группировок. В пиррольных группировках хлорофилла имеется система чередующихся двойных и простых связей. Это и есть хромофорная группа хлорофилла, обуславливающая его окраску.
Наличие магния обнаруживается легко. Стоит только подействовать на спиртовую вытяжку хлорофилла слабым раствором соляной или какой-нибудь другой кислоты, чтобы определить магний. При этом произойдёт изменение окраски – вытяжка приобретает жёлто-бурый оттенок.
Хлорофилл поглощает солнечную энергию и направляет её на химические реакции, которые не могут протекать без энергии, получаемой извне. Раствор хлорофилла в проходящем свете имеет зелёный цвет, но при увеличении толщины слоя или концентрации хлорофилла он приобретает красный цвет.
Хлорофилл поглощает свет не сплошь, а избирательно. При пропускании из семи видимых цветов, которые постепенно переходят друг в друга. При пропускании белого света через призму и раствор хлорофилла на полученном спектре наиболее интенсивное поглощение будет в красных и сине-фиолетовых лучах. Зелёные лучи поглощаются мало, поэтому в тонком слое хлорофилл имеет в проходящем свете зелёный цвет. Однако с увеличением концентрации хлорофилла полосы поглощения расширяются (значительная часть зелёных лучей также поглощается) и без поглощения проходит только часть крайних красных.
Спектры поглощения хлорофилла а и b очень близки.
В отражённом свете хлорофилл, кажется вишнёво-красным, так как он излучает поглощённый свет с изменением длины его волны. Это свойство хлорофилла называется флюоресценцией.
Хлорофиллы выполняют важную функцию в процессе фотосинтеза, их относят к основным фотосинтетическим пигментам. Они поглощают необходимую для фотосинтеза световую энергию в видимой области спектра (сине-фиолетовой и красной), работают в реакционных центрах фотосистем (хлорофилл «а») и светособирающих комплексах (хлорофилл «а» и «в»), участвуют в миграции энергии в ходе фотосинтеза. Кроме этого, хлорофиллы участвуют в фотоокислении воды, являются компонентами электрон-транспортной цепи фотосинтеза.
7. Каротиноиды (химические и оптические свойства, структура и функции)
Каротиноиды (от лат. carota – морковь и греч. eidos – вид) – желто-оранжевые пигменты, которые синтезируются высшими растми, а также грибами, бактериями, водорослями. Каротиноиды обеспечивают красную, желтую и пурпурную окраску плодов и цветов. Каротиноиды являются полиненасыщенными соединениями терпенового ряда, которые содержат в молекуле 40 углеродных атомов. В состав молекулы входят циклогексановые кольца и остатки изопрена.Разделяют на углеводные каротиноиды, С40-ксантофилы, гемо-, апо- и нор-каротиноиды. Каротиноиды выделяют из растений органическими растворителями с последующим разделением методом хроматографии.
Химические и оптические свойства каротиноидов. Среди каротиноидов самое важное значение имеют альфа-, бета-, гамма-каротины. Данные изомеры отличаются строением циклогексановых колец и биологической активностью. Все каротины не растворимы в воде и растворяются в органических растворителях – бензоле, хлороформе, эфире, жирах и маслах. Легко окисляются кислородом воздуха, нестойкие при нагревании в присутствии кислот и щелочей, разрушаются под действием света. Каротины синтезируются в растх. Характерной является также особенность каротиноидов избирательно абсорбироваться на минеральных и некоторых органических абсорбентах, что позволяет разделять их при помощи методов хроматографирования.
Уже тот факт, что каротиноиды всегда присутствуют в хлоропластах, позволяет считать, что они принимают участие в процессе фотосинтеза. В настоящее время установлено, что каротиноиды, поглощая определенные участки солнечного спектра, передают энергию этих лучей на молекулы хлорофилла. Тем самым они способствуют использованию лучей, которые хлорофиллом не поглощаются. Физиологическая роль каротиноидов не ограничивается их участием в передаче энергии на молекулы хлорофилла. По данным русского исследователя Д.И. Сапожникова, на свету происходит взаимопревращение ксантофиллов (виолаксантин превращается в зеаксантин), что сопровождается выделением кислорода. Спектр действия этой реакции совпадает со спектром поглощения хлорофилла, что позволило высказать предположение об ее участии в процессе разложения воды и выделения кислорода при фотосинтезе. Имеются данные, что каротиноиды выполняют защитную функцию, предохраняя различные органические вещества, в первую очередь молекулы хлорофилла, от разрушения на свету в процессе фотоокисления. Ряд исследователей указывают, что каротиноиды играют определенную роль в половом процессе у растений. Известно, что в период цветения высших растений содержание каротиноидов в листьях уменьшается. Одновременно оно заметно растет в пыльниках, а также в лепестках цветков.
8 Понятие о светособирающем комплексе и фотосинтетической единице.Хлорофилл выполняет две функции: поглощения и передачу энергии. Более 90 % всего хлорофилла хлоропластов входит в состав светособирающих комплексов (ССК), выполняющих роль антенны, передающей энергию к реакционному центру фотосистем I или II. Помимо хлорофилла в ССК имеются каротиноиды, а у некоторых водорослей и цианобактерий — фикобилины, роль которых заключается в поглощении света тех длин волн, которые хлорофилл поглощает сравнительно слабо.Передача энергии идёт резонансным путём (механизм Фёрстера) и занимает для одной пары молекул 10-10-10-12 сек., расстояние на которое осуществляется перенос составляет около 1 нм. Передача сопровождается некоторыми потерями энергии (10 % от хлорофилла a к хлорофиллу b, 60 % от каратиноидов к хлорофиллу), из-за чего возможна только от пигмента с максимумом поглощения при меньшей длине волны к пигменту с большей. Именно в таком порядке взаимно локализуются пигменты ССК, причём наиболее длинноволновые хлорофиллы находятся в реакционных центрах. Обратный переход энергии невозможен.
ССК растений расположен в мембранах тилакоидов, у цианобактерий основная его часть вынесена за пределы мембран в прикреплённые к нимфикобилисомы — палочковидные полипептидно-пигментные комплексы, в которых находятся различные фикобилины: на периферии фикоэритрины (с максимумом поглощения при 495—565 нм), за ними фикоцианины (550—615 нм) и аллофикоцианины (610—670 нм), последовательно передающие энергию на хлорофилл a (680—700 нм) реакционного центра.
ФОТОСИНТЕТИЧЕСКАЯ ЕДИНИЦА — объединение молекул хлорофилла, которые поглощают кванты света, с ферментативным центром, где происходит превращение энергии электронного возбуждения в ее химическую форму во время фотосинтеза. Находится в хлорофиллсодержащих фотосинтетических мембранах — тилакоидах. Ганс Гаффрон предположил, что свет поглощается сотнями молекул хлорофилла, которые затем переносят свою энергию возбуждения к тому месту, где протекают химические реакции. Это место называется реакционным центром. Таким образом, функция большинства молекул хлорофилла в фотосинтетической единице состоит в поглощении света
9.Общая характеристика световой фазы фотосинтеза.Световая фаза фотосинтеза осуществляется в хлоропластах, где на мембранах расположены молекулы хлорофилла. Хлорофилл поглощает энергию солнечного света. Эта энергия используется на синтез молекул АТФ из АДФ и фосфорной кислоты и способствуют расщеплению молекул воды: 2H20=4H++4+O2. Образующийся при этом кислород выделяется в окружающую среду. Для того чтобы понять, куда идут протоны и электроны, познакомимся более детально с процессами световой фазы фотосинтеза.
Под влиянием энергии солнечного света молекула хлорофилла возбуждается, и один из ее электронов переходит на более высокий энергетический урввень. Богатый энергией электрон участвует в окислительно-восстановительных реакциях и отдает избыточную энергию, проходя по цепи переносчиков электронов. Эта цепь образована различными белками, встроенными во внутреннюю мембрану хлоропласта. Отдаваемая электроном энергия используется на синтез молекул АТФ. Таким образом, энергия солнечного света необходима для перемещения электронов по цепи переносчиков электронов. При этом световая энергия преобразуется в химическую и запасается в молекулах АТФ.
Молекулы хлорофилла, потерявшие электроны, присоединяют электроны, образующиеся при расщеплении молекулы воды. Процесс расщепления молекул воды под влиянием солнечной энергии называют фотолизом (от греч. fotos – свет и lisis – растворение). В результате фотолиза образуются:
Электроны, заполняющие «дырки» в молекулах хлорофилла.
Протоны H+, которые соединяются с веществом НАДФ+ – переносчиком ионов водорода и электронов и восстанавливают его до НАДФ•Н.
Молекулярный кислород, который выделяется в окружающую среду.
Таким образом, в результате световой фазы фотосинтеза восстанавливается НАДФ+ и образуется НАДФ•Н, синтезируется АТФ из АДФ и фосфорной кислоты, выделяется молекулярный кислород. АТФ и НАДФ•H используются в реакциях темновой фазы фотосинтеза.
10. . Фотосинтетическое фосфорилирование
Фотосинтетическое фосфорилирование - присоединение неорганического фосфата к АДФ с использованием лучистой энергии. Различают циклическое и нециклическое фотосинтетическое фосфорилирование.
Нециклическое фотосинтетическое фосфорилирование - фотосинтетическое фосфорилирование, которое происходит за счет восстановления хлорофилла электронами гидроксильных ионов воды, которая предварительно подверглась фотолизу. Энергия электрона используется для зарядки АТФ, а протоны воды, соединяясь с НАДФ, образуют его восстановительную форму.
Циклическое фотосинтетическое фосфорилирование - фотосинтетическое фосфорилирование, которое происходит с восстановлением молекул хлорофилла за счет возвращения их собственных электронов, ранее сорванных с орбиты квантом света. При этом АТФ образуется за счет энергии электронов активированного светом хлорофилла.
11. Основные этапы С3-фиксации СО2. Фотосинтез, образование живыми растительными клетками органических веществ, таких, как сахара и крахмал, из неорганических – из СО2 и воды – с помощью энергии света, поглощаемого пигментами растений. Это процесс производства пищи, от которого зависят все живые существа – раст, животные и человек. У всех наземных растений и у большей части водных в ходе фотосинтеза выделяется кислород. Некоторым организмам, однако, свойственны другие виды фотосинтеза, проходящие без выделения кислорода.
Главную реакцию фотосинтеза, идущего с выделением кислорода, можно записать в следующем виде:

К органическим веществам относятся все соединения углерода за исключением его оксидов и нитридов. В наибольшем количестве образуются при фотосинтезе такие органические вещества, как углеводы (в первую очередь сахара и крахмал), аминокислоты (из которых строятся белки) и, наконец, жирные кислоты(которые в сочетании с глицерофосфатом служат материалом для синтеза жиров). Из неорганических веществ для синтеза всех этих соединений требуются вода (Н2О) и диоксид углерода (СО2). Для аминокислот требуются, кроме того, азот и сера. Раст могут поглощать эти элементы в форме их оксидов, нитрата (NO3–) и сульфата (SO42–) или в других, более восстановленных формах, таких, как аммиак (NH3) или сероводород (сульфид водорода H2S). В состав органических соединений может включаться при фотосинтезе также фосфор (раст поглощают его в виде фосфата) и ионы металлов – железа и магния. Марганец и некоторые другие элементы тоже необходимы для фотосинтеза, но лишь в следовых количествах. У наземных растений все эти неорганические соединения, за исключением СО2, поступают через корни. СО2 раст получают из атмосферного воздуха, в котором средняя его концентрация составляет 0,03%. СО2 поступает в листья, а О2 выделяется из них через небольшие отверстия в эпидермисе, называемые устьицами. Открывание и закрывание устьиц регулируют особые клетки – их называют замыкающими – тоже зеленые и способные осуществлять фотосинтез. Когда на замыкающие клетки падает свет, в них начинается фотосинтез. Накопление его продуктов вынуждает эти клетки растягиваться. При этом устьичное отверстие открывается шире, и СО2 проникает к нижележащим слоям листа, клетки которых могут теперь продолжать фотосинтез. Устьица регулируют и испарение воды листьями, т.н. транспирацию, поскольку большая часть водяных паров проходит именно через эти отверстия.
Водные раст добывают все необходимые им питательные вещества из воды, в которой живут. СО2 и ион бикарбоната (HCO3–) тоже содержатся и в морской, и в пресной воде. Водоросли и другие водные раст получают их непосредственно из воды.
Свет в фотосинтезе играет роль не только катализатора, но и одного из реагентов. Значительная часть световой энергии, используемой растми при фотосинтезе, запасается в виде химической потенциальной энергии в продуктах фотосинтеза. Для фотосинтеза, идущего с выделением кислорода, в той или иной мере пригоден любой видимый свет от фиолетового (длина волны 400 нм) до среднего красного (700 нм). При некоторых видах бактериального фотосинтеза, не сопровождающегося выделением O2, может эффективно использоваться свет с большей длиной волны, вплоть до дальнего красного (900 нм)
12. Общая характеристика С4-фиксации СО2. С4 фиксирование углерода один из 3 биохимических механизмов, вместе с C3 и Фотосинтез КУЛАЧКА, действующ в земле заводы «зафиксировать» двуокись углерода (связывающ газообразные молекулы к растворенным смесям внутри завода) для сахар продукция до конца фотосинтез. Вместе с фотосинтезом КУЛАЧКА, c4 фиксирование учтено выдвижением над более просто и более стародедовским c3 механизм фиксирования углерода работая в большинств заводах. Оба механизма отжимают тенденцию RuBisCO (первый энзим в Цикл Кельвин) к photorespire, или неныжная энергия путем использование кислорода break down смеси углерода к CO2. Как бы c4 фиксирование требует больше поступления энергии чем c3in the form of ATP. C4 заводы отделяют rubisco от атмосферического кислорода, углерода отладки в mesophyll клетки и использование oxaloacetate и малат к ferry фикчированный углерод к rubisco и остальноям энзимов цикла Кельвин изолированных в клетках пачк-оболочки. Промежуточное звено смешивает оба содержит 4 атома углерода, следовательно имя c4.
13. Фиксация СО2 у суккулентов (САМ-метаболизм) Суккуленты знакомы всем, даже тем, кто об этом не подозревает. Эти причудливой формы раст с сочными (от лат. succus- сок) тканями зеленых стеблей и (или) листьев, растущие в крайне засушливых и жарких странах, главным образом в тропиках, давно (со времени великих географических открытий) привлекают к себе внимание как специалистов-ботаников, так и любителей комнатных растений. Уже сравнительно давно ботаники обнаружили, что типичные суккуленты (кактусы, толстянки и др.) отличаются от других "несуккулентных" ксерофитов особым типом метаболизма, позволяющим им тратить примерно в 30 раз меньше воды, чем "обычным" растм. CAM-метаболизм (CAM - Crassulacean Acid Metabolism) заключается в том, что благодаря усложнению внутренней структуры органов ассимиляции процесс фотосинтеза протекает в две стадии. На первой стадии фотосинтезирующие клетки суккулентов фиксируют CO2 в темноте (при обычных типах фотосинтеза поглощается в дневные часы) с помощью фосфоенолпируваткарбоксилазы с образованием органических кислот, которые запасаются в вакуолях тех же клеток. Затем, в течение дня, когда устьица закрыты, CO2 высвобождается и включается в цикл Кальвина - далее фотосинтез протекает по традиционной схеме.Итак, понятие суккулентности, на наш взгляд, включает наличие водозапасающих тканей в зеленых органах ассимиляции (листьях и стеблях) и особого, САМ-типа, метаболизма, позволяющего экономно тратить запасенную влагу. Такое определение наряду с наличием водозапасающих тканей должно отражать особый тип фотосинтеза. Это ограничивает круг суккулентов и отличает их от четырех других групп растений, распространенных в сухих биотопах: эфемеров, эфемероидов, склерофитов и пойкилогидрических (высыхающих) растений. Последние, представленные в основном мхами, лишайниками и водорослями, ведут себя подобно микроорганизмам: в отсутствие влаги высыхают, но не полностью.
14. Общая характеристика фотодыхания. Раст, использующие только путь Кальвина — Бенсона,. принято называть С3-растми, поскольку первый стабильный продукт фотосинтеза представлен у них трехуглеродным соединением ФГК. У С3-растений значительная часть фиксированного при фотосинтезе углерода тут же теряется вследствие распада продуктов фиксации и выделения СО2 в реакциях, идущих с потреблением кислорода. Процесс этот происходит только на свету, и потому он был назван фотодыханием. Фотодыхание открыто сравнительно недавно. Объясняется это позднее его открытие тем, что выделение С02 при дыхании на свету маскируется поглощением С02 в процессе фотосинтеза. Первоначально предполагалось, что и в количественном отношении, и в смысле используемого пути световое дыхание идентично дыханию в темноте, однако затем выяснилось, что на свету выделяется больше СО2. Это удалось установить в результате тщательных измерений газообмена непосредственно вслед за включением или выключением света. Наблюдающееся на свету дополнительное выделение СО2 объясняется, как выяснилось, не усилением нормального процесса дыхания, а добавлением в этих условиях совершенно иного пути — фотодыхания.
Фотодыхание обусловлено тем, что в присутствии кислорода действующий в цикле Кальвина фермент RuBP-карбоксилаза может присоединять к RuBP не только СО2, но и О2, выполняя таким образом роль RuBP-оксигеназы. Присоединение кислорода к молекуле RuBP приводит к такому ее расщеплению, при котором вместо двух молекул ФГК, содержащих по три атома углерода, образуется одна молекула фосфогликолевой кислоты (содержащей два атома углерода) и одна молекула ФГК. Таким образом, в оксигеназной реакции не происходит никакой •фиксации СОг. Фосфогликолат позднее дефосфорилируется и превращается в гликолат, который поступает из хлоропласта в другую органеллу, также окруженную мембраной, в пероксисому. В пероксисоме гликолат вступает в реакцию с кислородом, в результате чего образуются глиоксилат и перекись водорода. Перекись тут же распадается на воду и кислород, а глиоксилат превращается в аминокислоту глицин. Затем уже вне перокеисомы, а именно в митохондриях, из глицина образуется аминокислота серии (которая может использоваться непосредственно в белковом синтезе или претерпевать дальнейшие превращения, ведущие к образованию глюкозы). При этой реакции из двух молекул глицина образуется одна молекула серила и одновременно выделяется СО2. Таким образом, какая-то часть углерода, фиксированного в цикле Кальвина — Бенсона, теряется без того, чтобы растение могло хоть как-то этот углерод использовать. Смысл фотодыхания нам пока не ясен, но, может быть, его полезная функция (если таковая существует) связана с тем, что оно играет необходимую роль в метаболизме азотистых соединений или в их переносе из одной органеллы в другую, обеспечивая превращение гликолата в глицин. Возможно также, что фотодыхание возникло на ранних этапах существования Земли с развитием фотосинтеза. В то время в земной атмосфере, очевидно, не было кислорода, поэтому фосфогликолат не мог образовываться под действием RuBP-карбоксилазы. Однако, когда кислород, выделявшийся в процессе фотосинтеза, начал накапливаться в атмосфере, в растх, возможно, началось накопление фосфоглнколата, и, может быть, фотодыхание возникло в процессе эволюции как средство, позволявшее ограничить это накопление.
15. влияние на фотосинтез внутренних и внешних факторов.Свет- непосредственно в ходе процесса фотосинтеза используется лишь 1-3% поглощенной солнечной энергии (ФАР)измеряемый (в мкмоль фотонов/м2*с). Ответная реакция фотосинтеза на поток фотонов может быть изображена световой кривой по типу параболы, состоящей из двух фаз. Первая фаза представляет собой линейную зависимость интенсивности фотосинтеза от потока квантов со световым компенсационным пунктом (СКП) в точке пересечения линии указанной зависимости с осью х. Вторая фаза – постепенное уменьшение наклона кривой по мере возрастания потока квантов и ее выход на плато, когда ИФ максимальна при ее насыщении светом. В линейной фазы световой кривой ИФ ограничивается активностью РДФ-карбоксилазы, а на плато фотосинтеза – скоростью регенерации РДФ.
Концентрация СО2 и О2 . зависимость ИФ от концентрации СО2 в воздухе выражается углекислотной кривой фотосинтеза, имеющий вид прямоугольной гиперболы для С4 – растений и непрямоугольный для – С3 растений. Углекислотное насыщение фотосинтеза у С4-растений, имеющих механизм концентрированияСО2 происходит при содержании диоксида углерода, близком к естественному. Его дальнейшее повышение как правило, не увеличивает ИФ в отличие от С3 видов, у которых ИФ значительно возрастает. В результате С3-виды, уступая С4 – видам по ИФ в нормальных условиях, превосходят их при высокой, например, при 0,1%-ной концентрации СО2. с увеличением концентрации О2 выше атмосферной ИФ подавляется в результате активации фотодыхания, а при снижении содержания кислорода, наоборот, ИФ возрастает. Измерение скоростей видимого яотосинтеза при нормальном содержании СО2 и О2 и при 3% О2 часто используют для оценки скорости фотодыхания. Наиболее однозначной реакцией растений на длительное выращивание при повышенной концентрации СО2 является увеличение площади листьев, уменьшение листовой обеспеченности биомассы, возрастание чистой продуктивности фотосинтеза. Это сопровождается существенной структурной и функциональной перестройкой фотосинтетического аппарата: увеличением толщины листовых пластинок за счет возрастания размеров клеток столбчатой и губчатой паренхимы, снижением содержания хлорофилла, а также отношения хлорофилла а к хлорофиллу б.
Температура. влияние температуры на фотосинтез бывает обратимым и необратимым. В первом случае указанное влияние не выходит за пределы устойчивости отдельных звеньев фотосинтеза. Для большинства растений обратимое влияние на фотосинтез наблюдается в диапазоне температур от 5 до 35 градусов Цельсия.
Водный режим. несмотря на то что при фотосинтезе используется лишь около 1 % поглощенной воды, дефицит последней сильно влияет на фотосинтез. Закрывание устьиц в результате дефицита вызывает снижение транспирации и поглощения СО2 листьями. Последнее обьясняется наряду с повышением устьичного сопротивления и снижением содержания хлорофилла тем, что водный дефицит может непосредственно изменять эффективность отдельных звеньев фотосинтеза.
Минеральное питание. Прямое действие на фотосинтез связано с тем, что минеральные вещества входят в состав ферментов и пигментов или непосредственно участвуют в процессе фотосинтеза в качестве активаторов.
Болезни растений. Грибные патогенны, такие, как ржавчина мучнистая роса, не приводят к быстрой гибели хозяина, так как их развитие возможно только на живой ткани. ИФ больных растений зерновых кулдьтур значительно ниже по сравнению со здоровыми. Это обьясняется скорее нарушением структуры фотосинтетического аппарата, чем реакцией устьиц.
16.взаимодействие факторов при фотосинтезе.
В естественных условиях факторы внешней среды действубт совместно. Поэтому газообмен раст отражает взаимодействие всех внутренних и внешних факторов. С повышением освещенности оптимальная и максимальная температуры видимого фотосинтеза повышаются на несколько градусов. Для растений это выгодно, так как сильное освещение всегда связано с нагревом листа. Если оно в конце концов приводит к перегреву, то свет уже перестает быть фактором, определяющим фотоситез, и ИФ снижается. Аналогично взаимодействуют свет и СО2. пр и повышении концентрация последнего радиация при которой КДП фотосинтеза достигает максимума, также должна увеличиться, что следует иметь виду при обогащения воздуха СО2 в теплицах зимний период.
