
- •7.6.1.1. Нитрование
- •1.6.1.2. Галогенирование
- •7.6.1.3. Сульфирование
- •7.6.1.3. Алкилирование по Фриделю-Крафтсу
- •7.6.1.4. Ацилирование
- •7.6.1.5. Хлорметилирование
- •4.4.3.2. Реакционная способность галогенов в реакции АdЕ
- •4.4.4. Присоединение галогеноводородов
- •4.4.4.1. Механизм реакции
- •4.4.4.2. Направление электрофильного присоединения
- •4.4.4.4. Перегруппировка
7.6.1.4. Ацилирование
Ацилирование - это реакция введения ацила RCO- или ароила ArCO-. При ацилировании ароматического кольца в качестве ацилирующего агента обычно используют хлорангидриды и ангидриды карбоновых кислот:
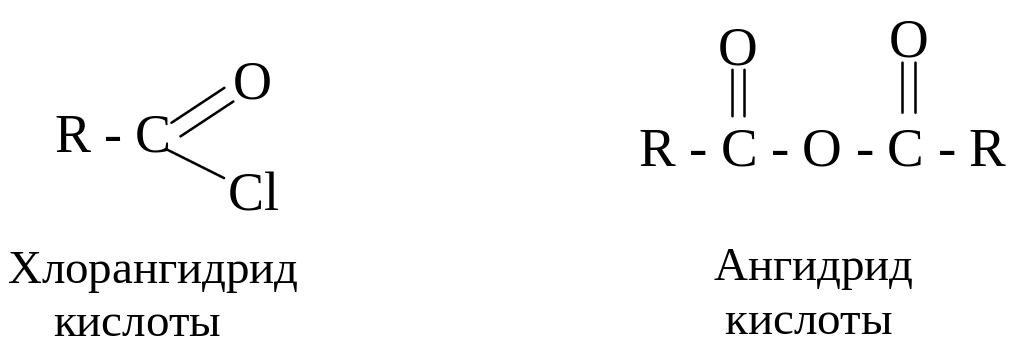
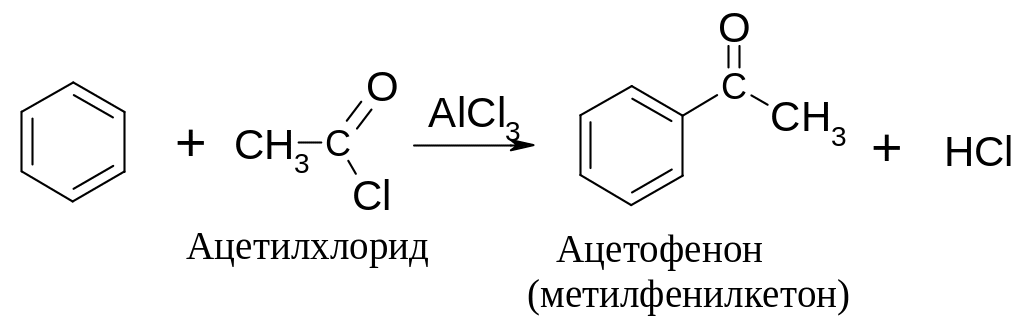
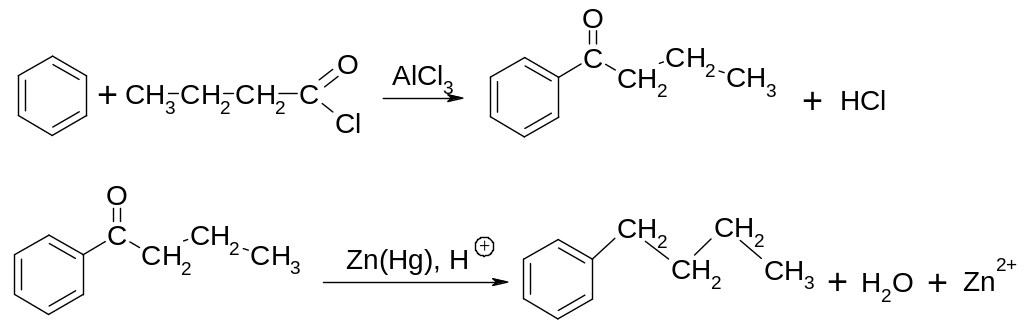
Пример: ацилирование бензола хлорангидридом уксусной кислоты.
Механизм реакции
Активная частица – электрофил - образуется в реакции между ацетилхлоридом и хлоридом алюминия.
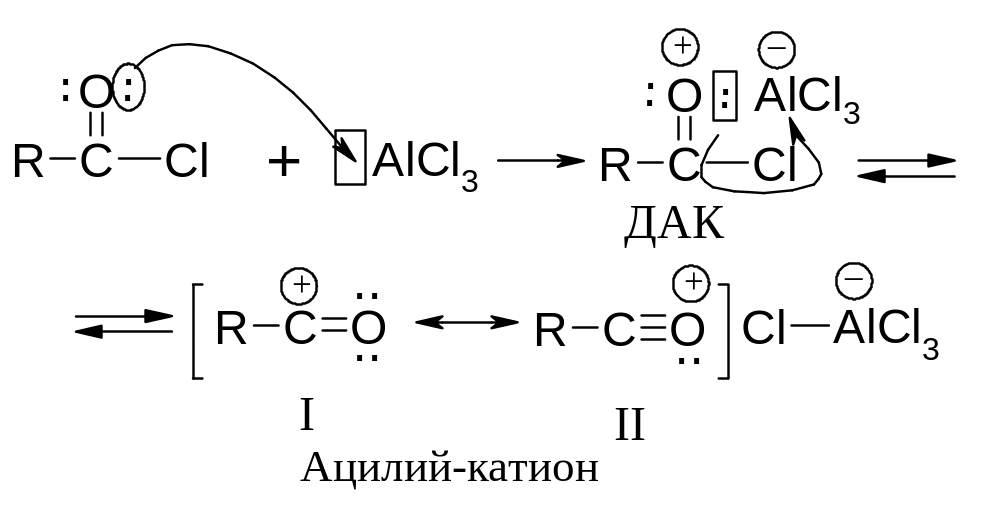
Ацилий-катион достаточно устойчив:
Атака ароматического ядра ацилий-катионом приводит к образованию -комплекса (карбокатиона), в следующей стадии отрыв протона даёт конечный продукт - кетон.
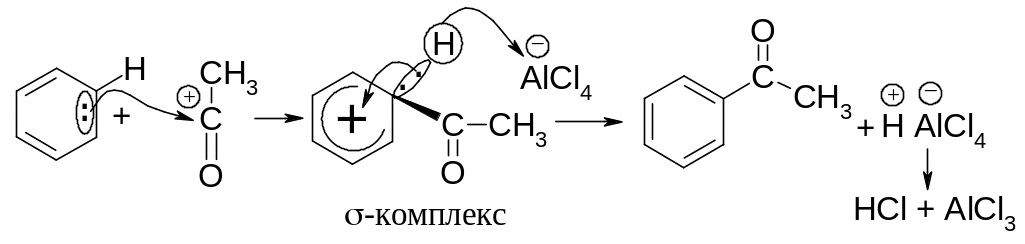
Образующийся кетон является основанием, он даёт устойчивый продукт с хлоридом алюминия.
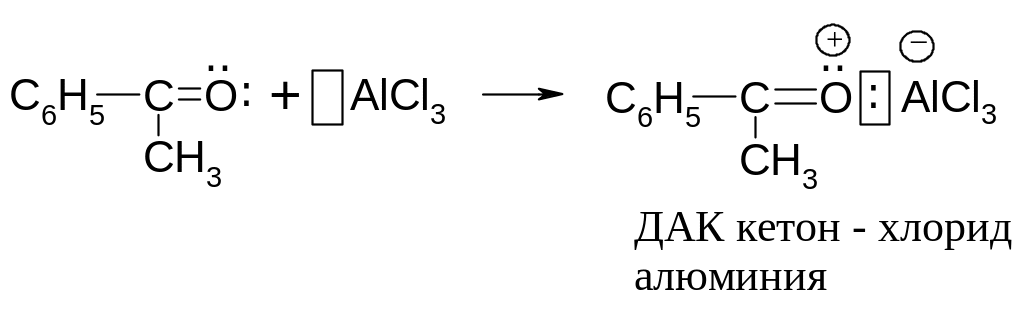
Так хлористый алюминий выводится из реакционной среды. Поэтому возникает необходимость вводить в реакцию ацилирования эквимолекулярное количество катализатора.
По окончании реакции кетон выделяют из комплекса действием воды.
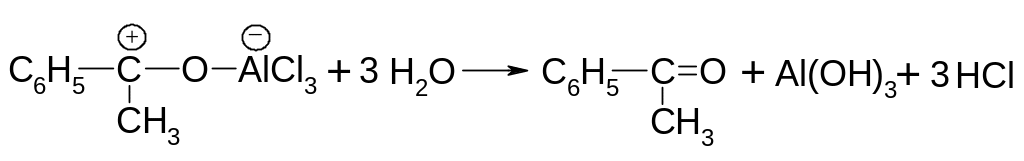
Ацильную группу можно ввести в бензольное кольцо и с помощью ангидридов карбоновых кислот.
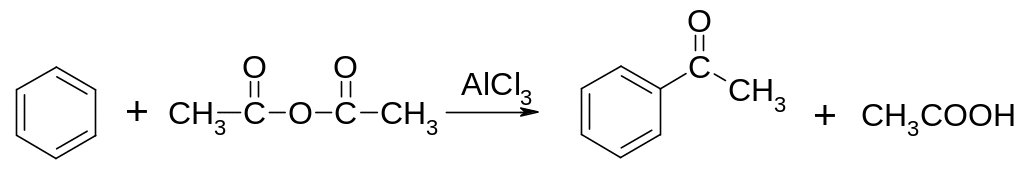
Образование ацилий-катиона происходит в соответствии со следующей схемой:
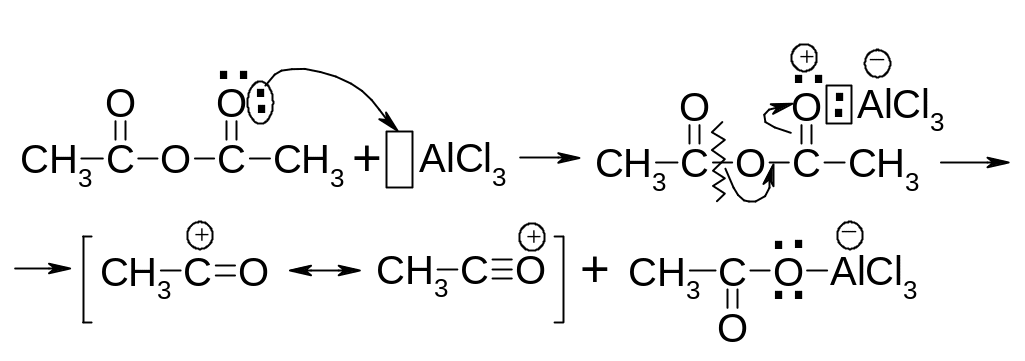
7.6.1.5. Хлорметилирование
Хлорметильную группу можно ввести непосредственно в кольцо по способу, сходному с реакцией Фриделя - Крафтса, - взаимодействием бензола с формальдегидом и хлороводородом в присутствии хлористого алюминия или хлористого цинка.
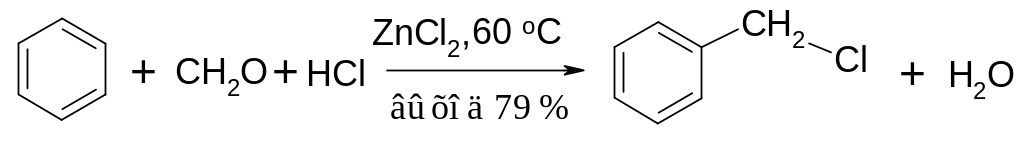
Правила ориентации электрофильного замещения в бензольном кольце
Все заместители делятся на два типа: первого рода (о- и п-ориентанты) и второго рода (м-ориентанты).
Заместители первого рода, кроме Alk-группы, более электроотрицательны, чем углерод, поэтому они уменьшают электронную плотность кольца по механизму отрицательного индуктивного эффекта (-I-эффект). Однако в большинстве заместителей первого рода атом, связанный с бензольным кольцо, имеет неподеленную пару электронов, способную вступать в р,п-сопряжение (+М-эффект). Относительная сила -I и +М-эффектов и определяет реакционную способность соединения.
Заместители второго рода более электроотрицательны, чем углерод (-I-эффект) и, кроме NR -группы, имеют п-связи, способные вступать в сопряжение с бензольным кольцом.
|
|
|
Орто-, пара-ориентанты |
Мета-ориентанты |
|
Активирующие: -O-NH, -NHR, -NR -OH, -OR -NHCOR -SH, -SR -Alk, -Aч Дезактивирующие: -F, -Cl, -Bч, -I |
Дезактивирующие -NR, -NO -SOH, -COR, -CHO -COOH, -COOR -CN, -CCl-CF -CHNO и др. |
|
Билет 19 вопрос 1
. Присоединение галогенов
Алкены реагируют с бромом и хлором в инертном растворителе (например, в четыреххлористом углероде), образуя вицинальные дигалогениды (vicinalis - соседний).
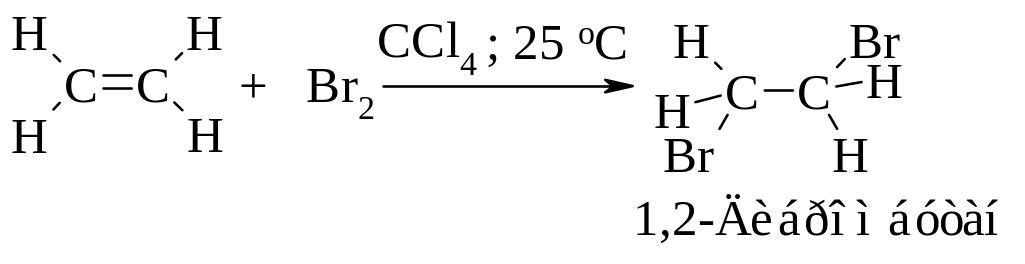
Этот процесс протекает как электрофильное присоединение.
Первая стадия. Неполярная молекула галогена поляризуется под действием богатой электронами двойной углерод-углеродной связи. Изменение распределения электронной плотности в одной молекуле под влиянием внешних условий (растворитель, другие молекулы, ионы) называется поляризацией. Поляризованная таким образом молекула галогена взаимодействует с -cистемой, образуя -комплекс:
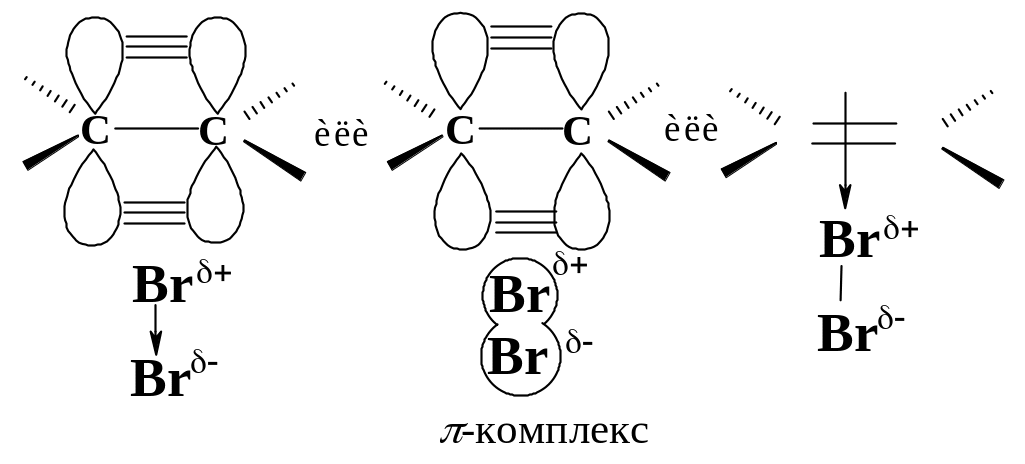
Вторая стадия. -Комплекс разрушается, ион брома Вr- электрофил - присоединяется к атому углерода и образуется -комплекс - карбокатион. Вторая стадия - медленная, определяет скорость всего процесса.
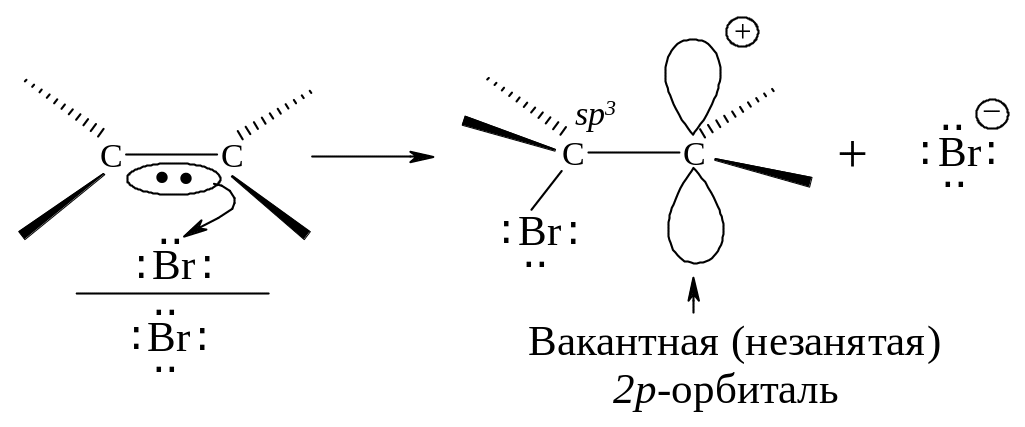
Положительно заряженный атом углерода находится в sр2-гибридизованном состоянии (его 2р-орбиталь не занята). Свободная 2р-орбиталь перекрывается с неподеленной парой электронов атома брома, образуя циклический ион бромония.
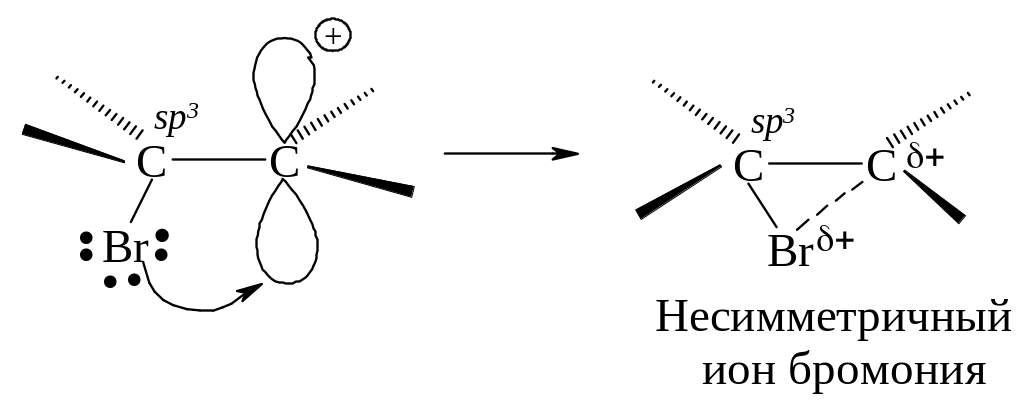
Третья стадия. Оставшийся анион брома (нуклеофил - ядро любящий) атакует образовавшийся циклический ион бромония по второму атому углерода.
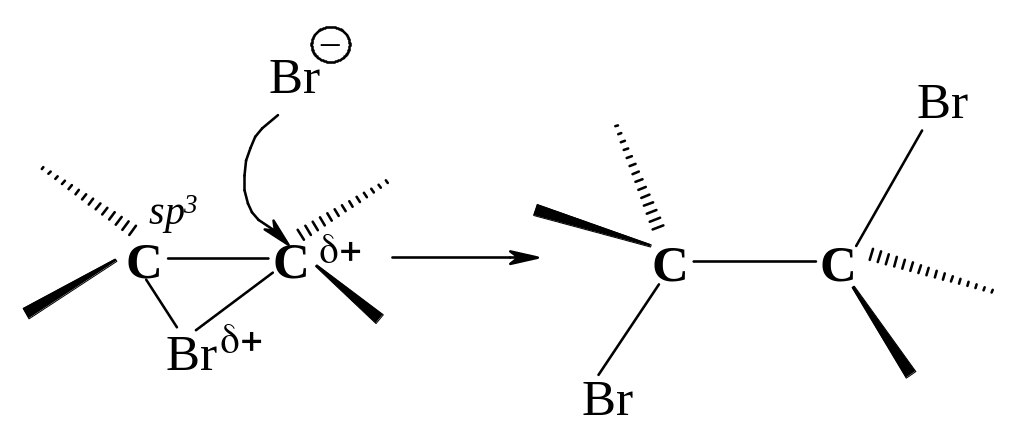
Стадия 2 – медленная, с высокой энергией активации
Доказательствами справедливости этого механизма служат следующие факты:
1). При проведении бромирования в растворе, содержащем помимо аниона брома другой нуклеофил (например, анион хлора), в продуктах реакции появляется наряду с дибромидом соединение, содержащее хлор.
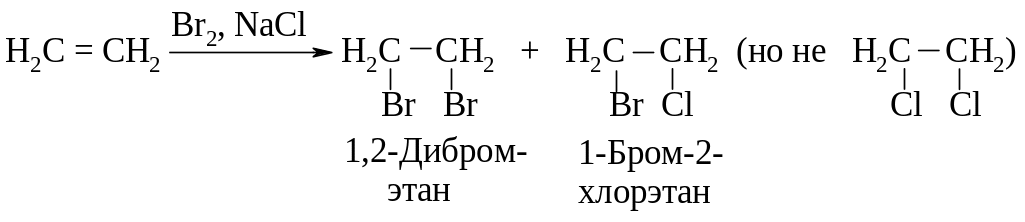
2). В соответствии со стадией 3 (рис. 4.8) электрофил - катион брома и нуклеофил - анион брома должны присоединяться к aлкeнy с противоположных сторон, т.е. в транс-положение.
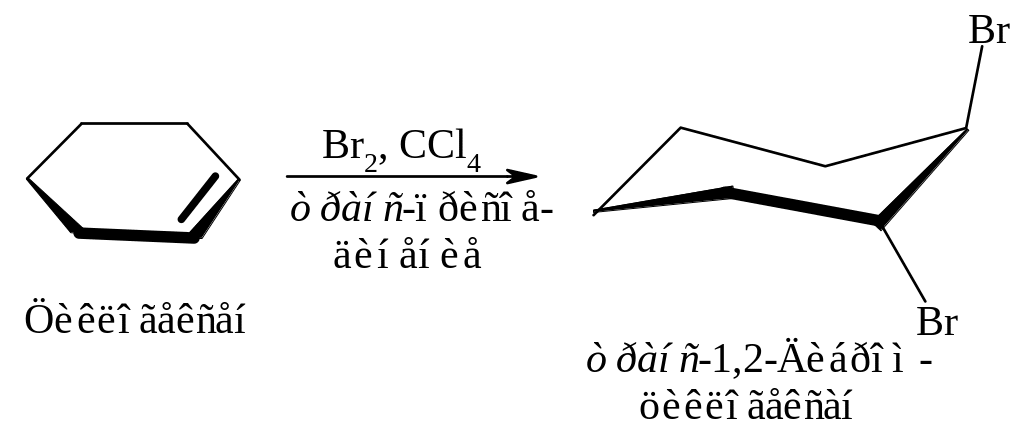
Присоединение брома к циклогексену действительно происходит в транс-положение.
