
- •Глава1. Статистические распределения.
- •§1.1. Введение. Термодинамический и статистический подходы.
- •§1.4. Биномиальное распределение молекул в объеме.
- •§1.5. Статистическое распределение. Квазизамкнутость.
- •§1.6. Фазовое пространство. Функция распределения.
- •§1.7. Функция распределения по энергиям.
- •§1.8.Энтропия.
- •Глава 2. Распределение Гиббса.
- •§2.1. Канонический ансамбль. Распределение Гиббса.
- •§2.2. Распределение Максвелла и его свойства.
- •§2.3. Распределение Больцмана и его свойства.
- •Глава 3. Квантовые статистические распределения.
- •§3.1. Статистическая сумма. Большой канонический ансамбль.
- •§3.2. Идеальный газ Бозе - Эйнштейна.
- •§3.3. Идеальный газ Ферми - Дирака.
- •§3.4. Статистический оператор (матрица плотности) и корреляционные функции.
§1.4. Биномиальное распределение молекул в объеме.
Пусть
N
молекул находятся в объеме V.
Выделим объем V1
в
объеме V.
Будем интересоваться макросостоянием,
когда в объеме V1
находится n
частиц, а в оставшемся объеме (V
-
V1)
находится (N
- n)
молекул. Вероятность того, что одна
молекула находится в V1,
равна V1/V.
Вероятность, что две частицы находятся
в объеме V1,
равна
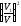 .
Вероятность того, что n
частиц в V1:
-
.
Вероятность того, что n
частиц в V1:
-
 .
Остальные (N
- n)
молекул должны быть в оставшемся объеме
(V
-
V1),
т.е. нужно учесть вероятность того, что
они попали в этот объем, которая равна
.
Остальные (N
- n)
молекул должны быть в оставшемся объеме
(V
-
V1),
т.е. нужно учесть вероятность того, что
они попали в этот объем, которая равна
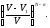 Итак,
полная вероятность такого “микросостояния”
Итак,
полная вероятность такого “микросостояния”
 (1.19)
(1.19)
Введем понятие статистического веса (), т.е. числа способов, которым реализуется данное макросостояние из различных микросостояний. Так как макросостояние газа не зависит от перестановок частиц, то
 (1.20)
(1.20)
Итак, полная вероятность данного макросостояния равна
 (1.21)
(1.21)
Введем обозначения
 ,
,
 .
(1.22)
.
(1.22)
Полученное распределение вероятностей
 (1.23)
(1.23)
называется биномиальным распределением. Название произошло от сходства с алгебраическим биномом Ньютона:

Свойства биномиального распределения:
1) По определению, p + q = 1,

2)
Ясно, что вероятность состояния с очень
малыми n
или (N
- n)
при фиксированных V1
и V
очень мала, так как при этом или
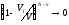 , или
, или
 .
.
В
общем случае нас интересуют достаточно
большие N
и n,
когда
переход от вероятности
 к вероятности
к вероятности
 осуществляется непрерывным образом.
Иначе говоря, мы полагаем, что dn
=
1 мала по сравнению с N.
Возьмем теперь разность вероятностей
двух соседних состояний и приравняем
ее нулю, чтобы найти максимум вероятности:
осуществляется непрерывным образом.
Иначе говоря, мы полагаем, что dn
=
1 мала по сравнению с N.
Возьмем теперь разность вероятностей
двух соседних состояний и приравняем
ее нулю, чтобы найти максимум вероятности:
 (1.24)
(1.24)
Из
равенства нулю выражения в скобках
имеем:
 ,
,
 .
.
Так как N >> 1 и n >> 1, получаем
 .
(1.25)
.
(1.25)
Поскольку
 - концентрация молекул в объеме, то
наиболее вероятное состояние осуществляется
тогда, когда число молекул в объеме V1
равно
- концентрация молекул в объеме, то
наиболее вероятное состояние осуществляется
тогда, когда число молекул в объеме V1
равно
n = n0V1, т.е. когда осуществляется равномерное распределение молекул по всему объему. Такое состояние называется стационарным или равновесным.
Определение: равновесным состоянием системы является ее наиболее вероятное состояние.
Схематически картина распределения вероятности при достаточно больших значениях числах частиц N и n выглядит как показано на рисунке (дискретные точки соединены сплошной линией) в виде острого максимума в окрестности nвер c очень маленькой шириной n. Условие нормировки может быть записано

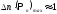
Если
за газом наблюдать достаточно большое
время, то окажется, что более вероятные
распределения молекул возникают чаще,
чем менее вероятные. Поэтому с течением
времени газ именно и переходит в наиболее
вероятные состояния, причем, достигнув
наиболее вероятного состояния, газ в
нем практически и остается. Существенно,
что равновесное состояние газа не
зависит от предыстории (или начального
состояния), т.е. от “пути”, которым газ
шел к равновесию. Независимость от
предыстории и постоянство во времени
свойств газа в равновесии имеют своим
следствием то, что равновесный газ можно
описать небольшим числом макроскопических
величин, характеризующих газ в целом
(для идеального газа - P,
V, T).
Итак, вероятность того, что число частиц в объеме V1 отклонится даже незначительно от nmax, ничтожна и быстро убывает с величиной отклонения. Но, тем не менее, число молекул в V1 не всегда строго равно nmax , а колеблется (флуктуирует) около этой величины.
Флуктуации числа молекул в объеме.
Ранее
мы ввели дисперсию
 и относительную квадратичную флуктуацию
и относительную квадратичную флуктуацию
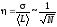 ,
где N
- число испытаний (число молекул).
Рассмотрим флуктуации для биномиального
распределения.
,
где N
- число испытаний (число молекул).
Рассмотрим флуктуации для биномиального
распределения.
Среднее
значение числа молекул
 в объеме V1
равно
в объеме V1
равно
 (1.26)
(1.26)
Чтобы сосчитать данную сумму, воспользуемся красивым формальным приемом. Запишем среднее значение через производную:
 (1.27)
(1.27)
На самом деле p + q = 1, но такое значение подставлять сразу нельзя. Этим можно воспользоваться только после вычисления производной.
 (1.28)
(1.28)
Интересно
отметить, что среднее значение совпадает
с наиболее вероятным значением n,
т.е. соответствует равномерному заполнению
всего сосуда. Когда V1
= V/2,
получаем
 .
.
Относительная квадратичная флуктуация.
Чтобы
сосчитать квадратичную флуктуацию
(дисперсию) необходимо знать
 .
Вычислим
.
Вычислим
 аналогично
тому, как это делалось в предыдущем
пункте:
аналогично
тому, как это делалось в предыдущем
пункте:

Здесь мы воспользовались тем, что p + q = 1. Итак,
 .
(1.29)
.
(1.29)
Сосчитаем теперь относительную квадратичную флуктуацию. Сначала запишем дисперсию, которая равна
 ,
(1.30)
,
(1.30)
и тогда для относительной квадратичной флуктуации получаем
 .
(1.31)
.
(1.31)
Важно,
что относительная
квадратичная флуктуация
убывает с ростом числа частиц в системе
 .
Физическое содержание полученного
выражения очень важно. Исследуем его.
Подставим в относительную квадратичную
флуктуацию выражения для p
и q
из (1.22):
.
Физическое содержание полученного
выражения очень важно. Исследуем его.
Подставим в относительную квадратичную
флуктуацию выражения для p
и q
из (1.22):
 (1.32)
(1.32)
Рассмотрим большой объем V1 V, тогда относительная флуктуация стремится к нулю ( 0), т.к. число частиц в объеме V фиксировано.
При
уменьшении объема V1
(V1
0) относительная флуктуация возрастает,
т.е. при V1
<< V
имеем

Для
 частиц в рассматриваемом объеме V1
= V/2
относительная флуктуация равна
частиц в рассматриваемом объеме V1
= V/2
относительная флуктуация равна
 .
.
Для
газа, находящегося в нормальных условиях,
 частиц/мм3.
При
V1
<< V
получаем очень малую величину относительной
квадратичной флуктуации
частиц/мм3.
При
V1
<< V
получаем очень малую величину относительной
квадратичной флуктуации

Итак, в макроскопических системах статистические флуктуации незначительны. С большой точностью все величины равны своим средним значениям. Иначе говоря, подавляющую часть времени газ находится в состояниях, в которых отклонения числа молекул от среднего не превышают относительную флуктуацию.
