
ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ ФАРМАЦИЯ
.pdf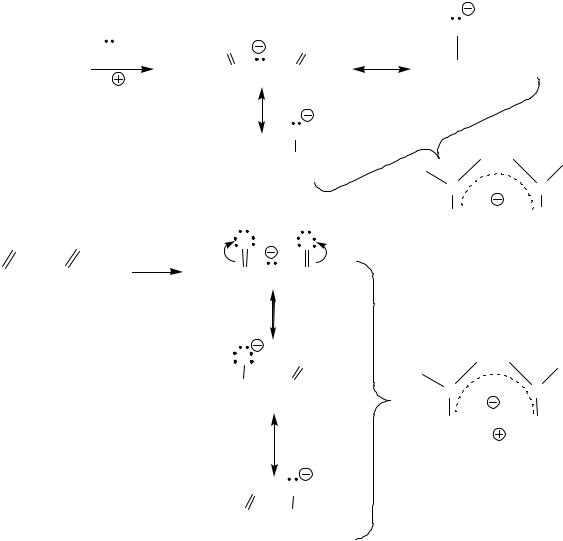
присутствия двух акцепторных групп. Образующиеся после действия оснований (третичных аминов – для кислоты; Na, C2H5ONa – для эфира) карбанионы, стабилизированы за счет делокализации электронной плотности.
H |
|
O |
O |
|
↓ |
NR3 |
|||
HO-C CH C-OH |
||||
HOOC←C→COOH |
|
|||
↑ |
-HNR3 |
|
|
|
H |
|
|
||
 O
O
HOOC-CH=C-OH
O |
O |
Na |
O |
O |
|
C2H5O-C←CH→C-OC2H5 |
H O-C←CH→C-OC H |
|
|||
C |
5 |
||||
|
↑ |
2 |
5 |
2 |
|
|
-H2 |
|
|
|
|
|
H |
|
|
|
|
|
|
|
O |
O |
|
|
|
C2H5O-C=CH−C-OC2H5 |
|
||
O  O
O
C2H5O-C−CH=C-OC2H5
 O
O
HO-C=CH-COOH
HO |
CH |
OH |
|
||
|
|
|
C |
|
C |
O |
|
O |
CH |
|
OC2 |
|
C2H5O |
|
H5 |
|
C |
C |
||
|
|||
O |
O |
|
|
Na |
|
|
натрмалоновый эфир
Синтезы на основе малоновой кислоты, её диэфира и динитрила
I. Реакции конденсации
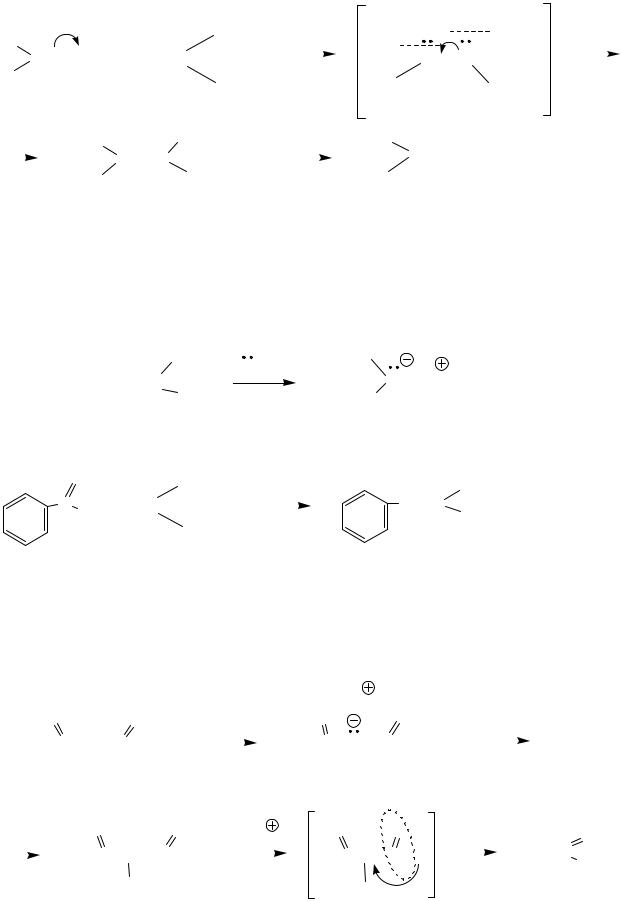
Малоновая кислота и её производные играют роль метиленовых компонент в синтезе производных непредельных кислот (реакции конденсации по типу кротоновой).
Примеры реакций
1.
158
CH3 +δ |
+δ |
-δ |
COOH |
N(C2H5)3 |
|
|
|
OH |
|
H |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
C |
|
O-δ + |
H→CH |
|
|
|
CH3 |
|
C |
|
|
C |
|
COOH |
|
|
|||||||
|
|
|
|
|
|
|
|
||||||||||||||||||
CH3 |
|
|
COOH |
|
|
|
CH3 |
|
|
|
|
|
|
|
|
COOH |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
CH3 |
|
|
COOH |
t0C |
CH3 |
C |
|
|
|
CH-COOH |
|||||||||||
|
|
|
|
C |
|
C |
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
COOH |
-CO2 |
CH3 |
||||||||||||||||||
|
|
|
|
CH |
|
|
3-метил-2-бутеновая кислота |
||||||||||||||||||
3 |
|
|
|
|
|
|
|
|
|
||||||||||||||||
Механизм реакции аналогичен механизму альдольной (кротоновой) конденсации (см. тему “Альдегиды, кетоны”).
Нуклеофилом в этих превращениях является малонил анион, который образуется в результате депротонирования СН2-группы основанием.
COOH |
N(C2H5)3 |
HOOC |
|
H→CH |
CH HN(C2H5)3 |
||
|
|||
COOH |
|
HOOC |
Nu
2.
O |
C≡N |
N(C2H5)3 |
|
C≡N |
||
C H |
CH=C |
|||||
+ CH2 |
|
|
C≡N |
|||
-H2O |
||||||
|
C≡N |
|
|
|||
бензальдегид |
динитрил малоновой |
бензилиденмалононитрил |
||||
|
кислоты, малононитрил |
|
|
|||
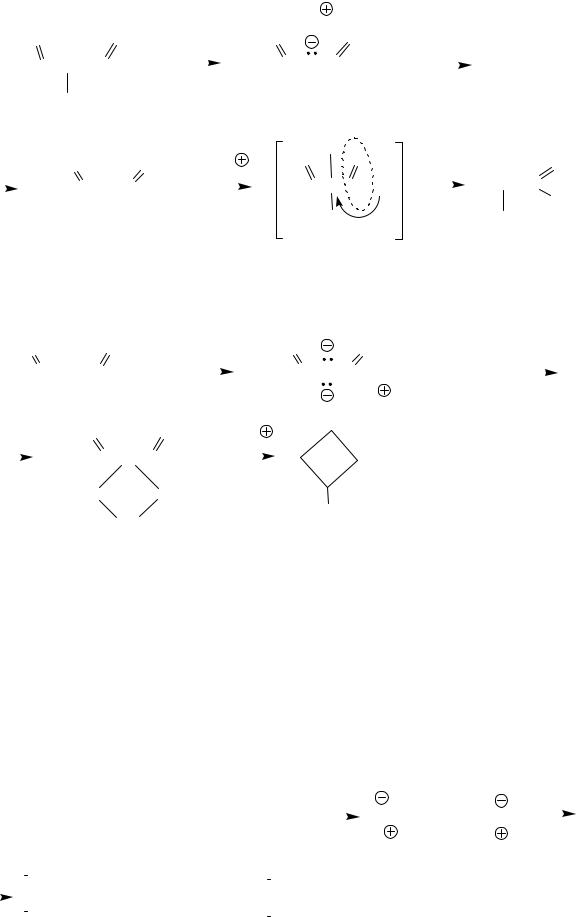
II. Получение карбоновых кислот из натрмалонового эфира
|
|
|
|
|
|
|
|
|
Na |
|
|
|
|
|
|
|
|
|
|
O |
O |
C2H5ONa |
O |
O |
|
|
R-Br |
|
|||||||
1. C2H5O-C CH2−C-OC2H5 |
|
|
C2H5O-C CH C-OC2H5 |
|
|
|
|
|
|
|
|||||||
|
|
|
-NaBr |
|
|||||||||||||
|
|
|
|
||||||||||||||
|
|
|
|
-C2H5OH |
|
(Nu) |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
SN2 |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
O |
O |
|
H3O |
|
O |
O |
|
|
|
|
|
|
O |
||
|
|
C2H5O-C CH C-OC2H5 |
HO-C-CH-C-OH |
|
|
|
|
R-CH2-C |
|||||||||
|
|
t0C |
|
|
|
|
OH |
||||||||||
|
|
|
|
||||||||||||||
|
|
|
R |
|
|
|
|
-CO2 |
|||||||||
|
|
|
-2C2H5OH |
|
R |
|
|
|
|
|
|
|
|||||
|
|
R - первичный алкил |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
159
|
|
O |
|
|
O |
|
|
|
|
|
Na |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
Na |
|
|
O |
|
|
R/ |
-Br |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
2. C H O-C CH C-OC H |
|
|
|
C2H5O-C C C-OC2H5 |
|
|
п |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||
2 5 |
|
|
2 5 |
-1/2 H2 |
|
|
|
-NaBr |
|
|
||||||||||
|
|
R |
|
|
|
R |
(Nu) |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
SN2 |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
R |
/ |
|
|
|
|
|
O |
R/ |
|
|
|
|
|
|
|
||
|
|
O |
O |
|
|
|
H3O |
O |
|
|
|
|
|
|
O |
|||||
|
|
|
|
|
|
|
HO-C-C−C-OH |
|
|
|
|
|
R-CH-C |
|||||||
|
|
C2H5O-C C C-OC2H5 |
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
-CO2 |
|
||||||||||||
|
|
|
t0C |
|
|
OH |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
R/ |
||||||
|
|
|
R |
|
|
-2C2H5OH |
|
|
|
|
|
|
|
|
||||||
R' – первичный алкил
С помощью этих синтезов можно получать различные карбоновые кислоты, в том числе с разветвленной цепью.
|
|
O |
O |
|
|
|
|
|
O |
O |
-δ +δ |
+δ -δ |
||
|
|
|
2 Na |
|
Br←CH2-CH2-CH2→Br |
|||||||||
3. C2H5O-C CH2−C-OC2H5 |
|
C2H5O-C C C-OC2H5 |
||||||||||||
|
- H2 |
|
|
-2 NaBr |
|
|||||||||
|
|
|
|
|
|
|
2 Na |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
O |
|
|
H3O |
|
|
|
|
|
||
|
|
|
C2H5O-C C C-OC2H5 |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
t0C |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
H2C |
CH2 |
-2C2H5OH |
циклобутанкарбоновая кислота |
||||||||
|
|
|
CH2 |
|
|
|
|
-CO2 |
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Аналогично можно получить циклоалканкарбоновые кислоты.
Использование адипиновой кислоты
Адипиновую кислоту и гексаметилендиамин используют в синтезе полиамидного волокна (найлона – 6,6). Реакция относится к реакциям
поликонденсации.
|
|
|
|
|
|
|
|
|
|
|
O |
O |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
t0C |
|
n HOOC-(CH2)4-COOH + n NH2 (CH2 )4 NH2 |
|
|
O-C-(CH2)4-C-O |
|||||||||||||||
|
|
-n H2O |
||||||||||||||||
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
n |
NH3 (CH2 )4 NH3 |
|||||||
|
|
O |
O |
|
|
|
||||||||||||
|
|
|
|
|
соль АГ |
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C-(CH2)4-C-NH (CH2)6-NH |
n |
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
найлон - 6,6 (полиамидное волокно) |
|
|
|
|
|
|
|
|
|
|
|||||||
160

При конденсации адипиновой кислоты с этиленгликолем образуются полиэфиры, из которых получают полиэфирные волокна (полиэстер).
НЕПРЕДЕЛЬНЫЕ ДВУХОСНОВНЫЕ КИСЛОТЫ
(на примере малеиновой и фумаровой кислот)
HOOC-CH=CH-COOH (Z,E) бутендиовая кислота
H |
COOH |
|
H |
|
|
|
COOH |
|||||
|
|
C |
|
|
|
|
|
|
|
C |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
C |
||
H |
COOH |
HOOC |
|
|
|
H |
||||||
Z - бутендиовая кислота |
E - бутендиовая кислота |
|||||||||||
ма |
леинова |
я |
|
фумаровая |
||||||||
т.пл. 1300С |
|
|
|
|
|
|
||||||
т.пл. 2870С |
||||||||||||
рКа 2,4 |
|
|
|
|
|
рКа 3,1 |
||||||
растворимость 1:2 |
|
|
|
|
|
1:150 |
||||||
в воде |
|
|
|
|
|
|
|
|
|
|||
нет в природе |
встречается в природе |
|||||||||||
ядовита |
|
(содержится в растениях, грибах) |
||||||||||
|
|
|
|
|
|
|
|
|
неядовита |
|||
На примере малеиновой и фумаровой кислот можно увидеть, как физические и биологические свойства соединений зависят от конфигурации молекулы.
Методы получения
|
H |
COOH |
|
|
|
|
H |
|
COOH |
|||
1. |
|
C |
|
t0C |
HOOC-CH2-CH-COOH |
t0C |
|
C |
||||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
медленная |
быстрая |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|||
|
|
C |
|
перегонка |
|
|
перегонка |
|
C |
|||
|
|
|
OH |
|
||||||||
|
HOOC |
H |
-H2O |
-H2O |
H |
|
COOH |
|||||
|
2-оксибутандиовая, |
|
||||||||||
|
|
|
|
|
|
|||||||
|
фумаровая кислота |
оксиянтарная кислота, |
|
|
малеиновая кислота |
|||||||
|
|
|
|
|
|
яблочная |
|
|
|
|
|
|
161

H |
|
|
|
|
|
|
O |
|
H |
|
COOH |
|
|
|
|
H |
C |
|
|
||||||
|
|
O2 / V2O5 |
H2O |
|
C |
|||||||
|
|
C |
|
|
|
|||||||
2. |
|
O |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
||
|
4500C |
|
|
|
|
|
|
|
||||
|
|
|
|
|
C |
|||||||
|
|
-CO2 |
C |
|
|
|
|
|||||
H |
|
C |
|
H |
|
COOH |
||||||
бензол |
H |
O |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
малеиновый ангидрид |
|
малеиновая кислота |
|||||||
Промышленный синтез.
Реакционная способность
Для двухосновных непредельных кислот характерны реакции по карбоксильным группам и двойной связи, аналогичные описанным ранее. Фумаровая кислота, в отличие от малеиновой, вследствие своего пространственного строения не дает ангидрида. Кислоты способны к взаимным превращениям под действием света через бирадикал, в котором вращение относительно σ - связи не затруднено.
|
H C COOH |
|
|
|
|
|
H C COOH |
|
|
|
C COOH |
|
|
|
|
|
O |
||||||||
ангидрид |
|
|
hν |
|
|
H |
t0C |
H C |
C |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
O |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
не образует |
|
|
|
|
или |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|||||||||
HOOC C H |
(I2, HNO2) |
HOOC |
C |
|
|
H |
C |
COOH |
- H2O |
C |
|||||||||||||||
|
H |
|
|
|
|
|
|
H |
O |
||||||||||||||||
фумаровая кислота |
|
|
A |
малеиновая кислота |
малеиновый |
||||||||||||||||||||
ангидрид
УГОЛЬНАЯ КИСЛОТА И ЕЕ ПРОИЗВОДНЫЕ
Номенклатура
|
|
HO-C |
-OH |
|
|
|
|
Cl-C-OH |
|
|
|
|
NH2-C |
-OH |
|
|
RO-C |
-OH |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
O |
|
|
||||
|
|
|
|
|
|
|
хлоругольная кислота |
карбаминовая кислота |
алкилкарбонат |
|||||||||||||||
|
|
|
|
|
|
(хлорангидрид угольной кислоты) |
(амид угольной кислоты) |
(сложный эфир) |
||||||||||||||||
|
|
Cl-C-Cl |
|
|
|
|
|
|
NH2-C-NH2 |
|
|
|
|
|
Cl-C-OR |
|||||||||
|
|
|
|
O |
|
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|
|
||
дихлорангидрид угольной |
|
карбамид, |
|
|
|
|
|
алкиловый эфир |
||||||||||||||||
кислоты, фосген |
|
|
|
|
|
|
мочевина |
|
|
|
|
|
хлоругольной кислоты |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(сложный эфир) |
|||||
RO-C-OR
O
диалкилкарбонат (сложный эфир)
NH2-C-OR
O
алкилкарбамат уретаны(общее название сложных эфиров карбаминовой кислоты)
N≡C-NH2
цианамид
(соединения, приведенные в квадратных скобках - нестабильны)
162

Синтез некоторых производных угольной кислоты и их свойства
Производные угольной кислоты, содержащие гидроксильную группу неустойчивы и разлагаются с выделением углекислого газа.
HO-C-OH |
|
|
|
|
|
|
CO2 |
+ |
H2O |
NH -C-OH |
|
|
|
CO |
+ |
NH |
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
2 |
2 |
|
3 |
|||
O |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
Cl-C-OH |
|
|
|
|
|
|
CO2 |
+ |
HCl |
C2H5O-C-OH |
|
|
|
CO2 |
+ |
C2H5OH |
|
|
|
|
|
|
|
|
|
||||||||||
O |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
Фосген (дихлорангидрид угольной кислоты) |
|
|
|
|
|
|
|||||||||||
CO + Cl2 |
|
|
|
УФ |
|
Cl-C-Cl |
|
|
|
|
|
|
|
||||
|
|
|
или |
|
|
|
|
|
|
|
|||||||
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
||||
|
акт. С / 2000C |
|
|
|
|
|
|
|
|
|
|||||||
Фосген – газ, относящийся к удушливым отравляющим веществам. Вступает в обычные реакции хлорангидридов.
|
|
|
|
изб. NH |
|
|
|
|
|
H2O |
|
|
|
|||||
NH Cl |
+ |
NH -C-NH |
2 |
|
|
3 |
Cl-C-Cl |
|
|
|
Cl-C-OH |
|
CO2 |
+ HCl |
||||
|
|
|
|
|
||||||||||||||
4 |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
||
|
|
карбамид |
|
|
C2H5OH |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
C2H5OH |
|
|
|
||||||
|
|
|
|
|
|
|
C2H5O-C-Cl |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
C2H5O-C-OC2H5 |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
NH3 |
|
|
O |
|
|
|
|
O |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
диэтилкарбонат |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
C2H5O-C-NH2
O
этилкарбамат
Уретаны - хорошо кристаллизующиеся устойчивые соединения, применяются в качестве успокаивающих, снотворных и жаропонижающих средств (здесь и далее названия лекарственных препаратов будут подчеркиваться)
|
|
|
|
|
CH3 |
|
|
|
NH2-C-OC2H5 |
NH2-C O C-CH2CH3 |
C6H5NH-C-OC2H5 |
||
|
|
|
O |
O |
CH3 |
O |
уретан, этилкарбамат |
апонал, |
|
эйфорин , |
|||
|
|
|
|
трет-пентилкарбамат |
|
|
|
успокаивающее |
N-фенилэтилкарбамат |
||||
|
и снотворное действие |
успокаивающее |
||||
|
жаропонижающее действие |
|||||
|
|
|
|
и снотворное действие |
||
|
|
|
|
|
||
Мочевина (диамид угольной кислоты, карбамид)
163
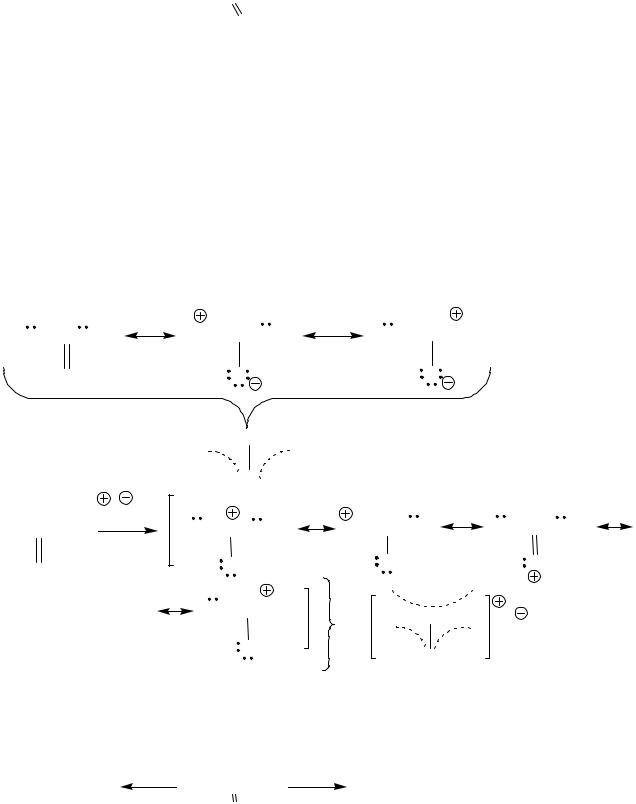
1500C
CO2 + 2 NH3  NH2-C-NH2 + H2O 450атм. O
NH2-C-NH2 + H2O 450атм. O
карбамид
Мочевина – белое кристаллическое вещество (т.пл. 1330С), растворима в воде. Мочевина – это диамид, обладающий слабыми основными и нуклеофильными свойствами.
1. Осно́вныесвойства
Мочевина обладает слабыми осно́внымисвойствами, в отличие от амидов карбоновых кислот. Причиной является наличие двух аминогрупп и образование при действии кислот карбкатиона, стабилизированного делокализацией электронной плотности. Ниже приведено описание строения мочевины и ее соли методом резонанса.
|
NH -C-NH |
2 |
|
NH2=C NH2 |
|
NH2 C=NH2 |
|
|||||
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
|
|
|
O |
|
|
|
|
|
|
NH2 C NH2 |
|
|
|
||||
|
|
|
|
|
|
|
O |
|
|
|
|
|
NH -C-NH |
H NO3 |
NH |
-C NH |
|
|
NH2=C NH2 |
NH2-C NH2 |
|||||
|
|
2 |
|
|||||||||
|
2 |
2 |
|
|
2 |
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
OH |
|
|
|
OH |
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2-C=NH2 |
|
NH2 C NH2 |
NO3 |
||||
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2. Свойства мочевины как диамида угольной кислоты |
|
|||||||||||
а) Гидролиз |
|
H2O |
|
|
|
|
|
H2O |
|
|
||
NH |
3 |
+ Na CO |
3 |
NH |
|
-C-NH |
2 |
|
NH4Cl + CO2 |
|
||
|
|
|
|
|
||||||||
|
2 |
NaOH |
2 |
O |
|
HCl |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
б) Реакции с HNO2 |
и |
|
Br2/NaOH (перегруппировка Гофмана, см. тему |
|||||||||
“Амиды карбоновых кислот”)
164

N2 + Na2CO3 |
+ NaBr |
Br |
2 |
|
NH2-C-NH2 |
HNO2 |
HO-C-OH |
|
H2O + CO2 |
||||||||
|
|
|
|
|
|
||||||||||||
NaOH |
-N2 |
|
|||||||||||||||
|
|
|
|
|
|
O |
|
|
|
|
|
||||||
|
|
|
|
|
|
O |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
в) Конденсация с NH3 ( из (NH4)2CO3 ), образование гуанидина |
|
||||||||||||||||
NH2-C-NH2 |
|
(NH4)2CO3 |
NH2-C-NH2 + H2O |
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
гуанидин |
|
|
|
|
|
|
|
|
Гуанидин – однокислотное основание, сравнимое по силе с NaOH (KOH).
NH2-C |
-NH2 |
H |
|
|
|
|
|
|||
|
NH2-C-NH2 |
|
NH2=C-NH2 |
|
и т.д. |
|||||
|
||||||||||
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
NH |
|
NH2 |
|
NH2 |
|
|
||||
Нитраты и перхлораты гуанидина являются взрывчатыми веществами и входят в состав ракетного топлива.
3. Нуклеофильные свойства
а) Ацилирование, образование уреидов
|
|
|
|
O |
|
|
|
|
|
|
O |
NH2-C-NH2 |
|
|
|
|
|
|
|
CH3-C-NH-C-NH2 + HCl |
|||
+ |
CH3-C |
|
|
|
|
|
|
||||
|
|
|
|||||||||
|
|
|
|
Cl |
|
|
|
|
|
|
O |
O |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
ацетилкарбамид, ацетилмочевина (уреид) |
|||
|
|
Br |
|
|
|
|
|
|
|
|
|
CH3-CH-CH-C-NH-C-NH2 |
бромурал, успокаювающее и снотворное средство, |
||||||||||
CH3 |
O |
O |
|
|
входит |
|
в |
состав валокардина |
|||
|
|
|
|
|
|
|
|||||
б) Ацилирование малоновым эфиром
|
NH-H |
O |
|
|
|
H |
O |
|
C2H5O-C |
|
|
|
N |
||
O=C |
+ |
|
|
|
|
C |
|
CH2 |
|
|
|
O C |
|
||
|
-2 C2H5OH |
|
|||||
|
NH-H |
C2H5O-C |
N |
C |
|||
|
|
|
|
|
|||
|
|
O |
|
|
|
H |
O |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
малонилмочевина барбитуровая кислота
Барбитуровая кислота является СН-кислотой, рКа 10, титруется как одноосновная кислота.
Для барбитуровой кислоты характерна кето-енольная и лактим-лактамная таутомерия.
165
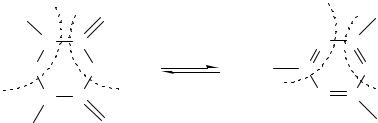
H O
лактам N C кетон
O  C CH2 N C
C CH2 N C
H O
166
|
|
|
OH |
лактим |
N |
C |
енол |
HO |
C |
|
CH |
|
N |
C |
|
|
|
|
OH |

Барбитураты – производные барбитуровой кислоты, являются снотворными препаратами.
|
NH2 |
C2H5O-C |
O |
|
|
|
|
|
H |
|
O |
|
|
|
|
|
|
|
|
|
N |
C |
|||
|
R |
|
t0 |
|
|
|
R |
|||||
O=C |
+ |
|
|
|
|
|
||||||
|
C |
|
|
|
O |
|
|
C |
C |
|
||
|
|
-2 C2H5OH |
|
|
|
|||||||
|
|
|
|
|
||||||||
|
NH2 |
C2H5O-C |
R/ |
|
|
|
N |
C |
R/ |
|||
|
|
O |
|
|
|
|
|
|
O |
|||
|
|
|
|
|
|
|
|
H |
|
|||
|
|
|
|
|
|
|
|
|
|
|
||
(Получение диалкилпроизводных малонового |
эфира |
|
изложено |
в теме |
||||||||
“Малоновая кислота”.) |
|
|
|
|
|
|
|
|
|
|
||
а) Снотворные длительного действия:
R=R’= -C2H5 барбитал (веронал)
R= -C2H5 , R’= -C6H5 фенобарбитал (люминал)
б) Снотворные средней продолжительности действия:
R= -C2H5 |
R/= -CH2-CH2- |
CH-CH3 |
барбамил |
|
|
|
|
CH3 |
|
R= -C2H5 |
R/= - |
CH-CH2-CH2-CH3 |
этанаминал |
|
|
||||
|
|
|
|
|
|
CH3 |
|
||
в) Снотворные кратковременного действия:
R= -CH3 R/= гексенал
При передозировке барбитуратов наступает угнетение дыхания с летальным исходом.
4. Поведение при нагревании
t0C
NH2-C-NH2 + NH2-C-NH2  NH2-C-NH-C-NH2
NH2-C-NH-C-NH2
O |
O |
-NH3 |
O O |
биурет
Биурет дает фиолетовое окрашивание с Cu(OH)2 , это реакция является качественной на содержание в соединении амидной группировки –NH-C(O).
166
