
ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ ФАРМАЦИЯ
.pdf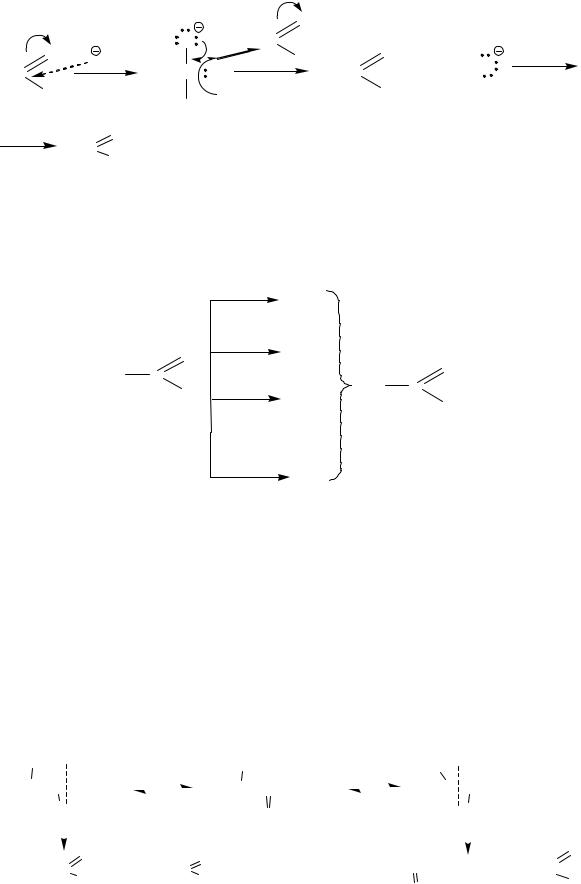
|
|
|
|
+δ O−δ |
|
|
|
|
+δ |
O−δ |
|
O |
H-C |
O |
|
|
NaOH |
|
|
H |
+ |
CH3-O |
||||
H-C |
OH |
H C H |
H-C |
H2O |
||||
H |
|
гидридный |
|
|
||||
|
|
OH |
OH |
метилат анион |
||||
|
|
|
перенос |
|
|
|
|
|
|
H-C |
O |
+ CH3OH |
|
|
|
|
|
|
ONa |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
V. Реакции окисления
1. Альдегиды окисляются в мягких условиях до карбоновых кислот, проявляя
свойства восстановителей.
O2 (воздух)
|
200C |
|
|
O |
KMnO4 |
|
|
200C |
O |
||
R C |
|||
Ag(NH3)2OH |
R C |
||
H |
|||
|
реактив Толленса |
OH |
|
|
-Ag |
|
Cu+2/ раствор
реактив Фелинга
-Cu2O
Реакции с реактивами Толленса (реакция серебряного зеркала) и Фелинга относятся к качественным.
2. Кетоны окисляются деструктивно в жестких условиях под действием KMnO4 и K2Cr2O7 в присутствии концентрированной серной кислоты после образования енолов ( правило Попова).
Пример реакции
реагент: KMnO4/ H2SO4, t0C
CH3 |
|
|
|
|
|
|
CH3 |
|
|
|
|
CH3 |
|
|
|
||
CH3-CH-C=CH-CH3 |
|
|
|
|
CH3-CH-C-CH2-CH3 |
|
|
|
CH3-C=C-CH2-CH3 |
||||||||
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|||||||||||
|
OH |
|
|
|
|
|
|
α O |
α/ |
|
|
|
|
OH |
|
||
|
|
|
O |
|
|
|
|
|
2-метилпентанон-3 |
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
O |
|
|
CH3-C-CH3 |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
CH3- |
CH-C |
|
+ |
|
|
CH3-C |
|
|
+ |
CH3-CH2C |
|||||||
|
|
|
OH |
|
|
|
|
|
OH |
|
|
|
|
O |
|
|
OH |
CH3 |
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
уксусная кислота |
|
|
|
|
|
|
пропионовая кислота |
||||||||
2-метилпропановая |
|
|
|
ацетон |
|
|
|||||||||||
кислота, изомасляная
128

Таким образом, при окислении этилизопропилкетона образуются три различные карбоновые кислоты и пропанон (ацетон). Анализ образующихся смесей позволяет установить строение исходного кетона.
Реакционная способность α,β - непредельных альдегидов на примере
акролеина
|
-δ |
|
+δ |
O |
-M, -I для карбонила |
CH2=CH-C |
H |
π,π − сопряжение |
|
Характерны реакции по карбонильной группе и двойной связи.
|
|
|
O |
|
|
|
|
|
|
-δ |
|
OH |
|
||
AdNu |
|
|
NH3 |
|
+δ |
|
|
O |
KCN 4 3 2 |
|
1 |
|
|||
|
|
|
|
|
|
|
|
||||||||
|
CH2-CH2-C |
|
|
|
|
CH =CH-C |
|
|
CH2=CH-CH-C≡N |
AdNu |
|||||
|
|
|
|
|
|
||||||||||
|
|
|
H |
|
|
|
|
2 |
|
H |
H2Oнитрил 2-окси-3-бутеновой кислоты |
||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
NH2 |
|
|
+δ |
-δ |
|
|
|
NaHSO3 |
|
||||
|
|
|
|
|
|
|
|||||||||
3-аминопропаналь |
|
|
|
|
|
|
|||||||||
|
|
|
|
H→Br |
|
C2H5OH |
|
OH |
|
||||||
|
|
|
|
|
|
|
|
|
|
AdNu |
|||||
|
|
CH2-CH2-C |
O |
|
|
|
|
|
H |
O |
|
CH2=CH-CH-SO3Na |
|||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
H |
|
|
|
|
CH2-CH2-C |
H |
|
гидросульфитное производное |
|||||
AdE |
|
Br |
|
|
|
|
|
||||||||
|
|
|
|
|
|
OC2H5 |
|
|
|
|
|
||||
3-бромпропаналь |
|
|
|
|
|
Ad |
E |
|
|||||||
|
|
|
|
3-этоксипропаналь (полуацетальное производное не |
|
||||||||||
образуется - менее устойчиво, чем полученный продукт)
Механизм присоединения этанола, AdE
O H |
CH2=CH-CH-OH |
C2H5OH |
||
CH2=CH-C |
CH2-CH=CH-OH |
|||
H |
|
|
Nu |
|
CH2-CH=CH-OH |
CH2-CH2-C |
O |
||
H |
||||
H O-C2H5 |
-H |
|
||
OC H |
5 |
|
||
|
2 |
|
||
Механизм присоединения аммиака, AdNu
|
-δ |
|
|
|
|
|
|
|
|
+δ |
O |
NH3 |
|
O |
O |
H |
|
|
O |
CH2=CH-C |
|
CH -CH-C |
|
CH2-CH=C |
CH |
-CH -C |
|||
|
H |
|
2 |
H |
H |
|
2 |
2 |
H |
|
|
|
|
|
|
||||
|
|
|
NH |
|
NH3 |
|
NH |
|
|
|
|
|
3 |
|
|
|
2 |
|
|
129

КАРБОНОВЫЕ КИСЛОТЫ
O
Функциональная группа C |
- карбоксил |
OH
Номенклатура
Суффикс – овая
H-C |
O |
метановая кислота, муравьиная |
|
OH |
|||
|
|||
|
|
||
CH -C |
O |
этановая кислота, уксусная |
|
3 |
OH |
||
|
|
O
CH3-CH2-C пропановая кислота, пропионовая
OH
CH3-CH2-CH2-C |
O |
бутановая кислота, масляная |
|
OH |
|||
|
|
O
CH3-CH-C 2-метилпропановая кислота, изомасляная
CH3 OH
Карбоновые кислоты имеют высокие температуры кипения, причиной является образование ассоциатов за счет водородных связей.
-δ |
+δ |
-δ |
|
+δ O .... H O |
+δ |
||
R-C |
|
|
C-R |
O H ...... O |
|||
-δ |
+δ |
-δ |
|
Методы получения
1. Карбонилирование щелочей и алкоголятов
|
|
t0 , p |
|
O |
HCl |
O |
|
||||||
а) CO + NaOH |
|
|
|
|
|
H-C |
|
|
|
|
H-C |
OH + NaCl |
|
|
|
|
|
|
ONa |
|
|||||||
|
|
|
метаноат натрия, |
|
|
||||||||
|
|
|
формиат |
|
|
|
|
|
|||||
б) R-ONa + CO |
t0 |
, p |
R-C |
O |
HCl |
O |
+ NaCl |
||||||
|
|
|
|
|
ONa |
|
|
R-C |
OH |
||||
|
|
|
|
|
|
|
|||||||
R-алкил |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
карбоновые кислоты |
||||
130
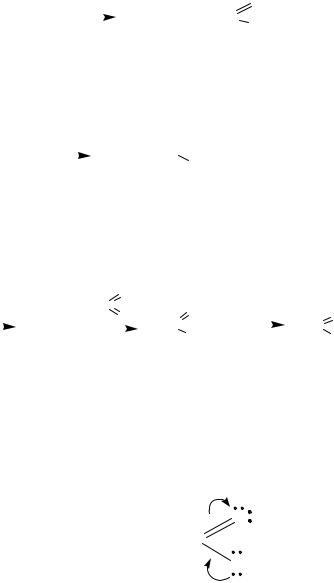
2. Металлокарбонильный синтез
R-CH=CH2 + CO + H2O |
Ni(CO)4 |
R-CH2-CH2-C |
O |
|||
|
|
|
OH |
|||
t0 |
, p |
|||||
R-алкил |
|
|||||
|
|
|
карбоновые кислоты |
|||
3. Окисление алканов
CH3-CH2-CH2-CH3 O2 (воздух) 2 CH3-C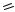 O
O
катализатор OH
4.Окисление спиртов, альдегидов (см. соответствующие темы).
5.Синтез из реактива Гриньяра
|
|
|
C |
O |
|
O |
|
|
|
|
|
|
|
R-Br + Mg |
|
R-MgBr |
O |
R-C |
HCl |
R-C |
O |
+ MgOHBr |
|||||
|
|
|
|
|
|
|
|
|
|||||
|
|
OMgBr |
H2O |
OH |
|||||||||
|
|
|
|
||||||||||
R-алкил |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
6. Гидролиз нитрилов (см. тему “Производные карбоновых кислот”).
Реакционная способность карбоновых кислот
H |
|
-δ |
|
+δ |
O |
||
α ↓ |
|||
|
|||
R C→C |
-δ +δ |
||
↑ |
|
O←H |
|
H |
|
|
|
Поляризация связей в молекулах карбоновых кислот
За счет р,π-сопряжения НПЭ атома кислорода гидроксильной группы и р-электронов π-связи карбонила дефицит элекронной плотности на атоме углерода карбонила (+δ) снижен. По этой причине карбоновые кислоты не склонны вступать в реакции присоединения по карбонильной группе, в отличие от альдегидов (кетонов). Кроме проявления ОН-кислотности, для карбоновых кислот характерны реакции замещения гидроксильной группы и атома водорода в α-положении.
I.ОН-кислотность карбоновых кислот
Карбоновые кислоты относятся к слабым кислотам, рКа 4-5.
131

R-COOH + H2O |
|
R-COO + H3O |
|
||
|
карбоксилат-анион |
|
0 |
O |
R-C |
O |
|
R-C |
|
|||
1,23 Α |
O |
|||
O |
|
|||
O |
|
|
||
|
|
|
||
R-C |
|
O |
|
|
O-H |
|
|
||
|
R-C |
|
||
0 |
|
|
||
|
O |
|
||
1,36 Α |
|
|
||
длины связей С-О |
|
0,127 нм |
|
|
в карбоновых кислотах |
|
|
|
Связи С-О в карбоксилат-анионе одинаковы по длине, электронная плотность распределена равномерна.
Влияние заместителей на величину рКа карбоновых кислот:
1. Донорные группы увеличивают прочность связи кислород-водород, это приводит к увеличению рКа кислот, т.е. уменьшению их силы.
|
H C |
O |
CH3→C |
O |
CH3-CH2→C O |
|
|
OH |
|
OH |
OH |
рКа |
3,75 |
|
4,76 |
|
4,86 |
2. Акцепторные группы уменьшают электронную плотность связи кислородводород, это приводит к уменьшению рКа кислот, т.е. увеличению их силы.
|
Cl |
|
Cl |
O |
|
O |
|
O |
|
↑ |
O |
↑ |
> CH2←C |
> CH →C |
|||
|
Cl← C←C |
> |
CH←C |
|
|
|
||
|
OH |
↓ |
OH |
↓ |
OH |
3 |
OH |
|
|
↓ |
|
||||||
|
|
|
||||||
|
Cl |
|
Cl |
|
Cl |
|
|
|
рКа |
0,66 |
|
1,25 |
|
2,87 |
|
4,76 |
|
Карбоновые кислоты реагируют с металлами, оксидами металлов, гидроксидами, аммиаком, солями более слабых кислот (OH, NH, CH - кислот). При этом образуются соли.
CH3−C |
O |
Zn |
Zn |
CH3 |
−C |
O |
Na |
CH3 |
−C |
O |
|
O |
-H2 |
OH |
-H2 |
ONa |
|||||||
|
2 |
|
|
|
|
||||||
этаноат, |
|
|
|
|
|
|
ацетат натрия |
||||
|
|
|
|
|
|
|
|||||
ацетат цинка |
|
|
|
|
|
|
|
|
|
||
CH −C |
O |
K2O |
CH −C |
O |
KOH |
CH3−C |
O |
|
|
|
|
|
|
|
|||
3 |
OK |
-H2O |
3 |
OH |
-H2O |
|
OK |
|
|
|
|
||||||
ацетат калия |
ацетат калия |
|
132

|
O |
NaNH2 |
|
|
|
|
O Na2CO3 |
|
O |
||||
CH −C |
или NaH |
CH |
−C |
CH3−C |
|||||||||
|
|
|
|
|
|
|
|
||||||
3 |
ONa |
|
-NH3 |
|
3 |
|
|
OH -H2O,-CO2 |
|
ONa |
|||
|
|
|
или -H2 |
|
|
|
-C2H5OH |
|
|
||||
|
|
|
|
|
|
|
|
||||||
|
|
|
C H |
ONa |
|
|
|||||||
|
|
2 |
|
5 |
|
|
|
|
|
|
|
|
|
O
CH3−C  ONa
ONa
|
O |
NH3 |
|
|
|
|
O CH3-C≡C Na |
|
O |
||
CH −C |
|
|
|
CH |
−C |
|
|
|
CH3−C |
+ CH3-C≡CH ↑ |
|
|
|
|
|
|
|
||||||
3 |
O NH4 |
200C |
3 |
|
|
OH |
|
ONa |
|||
|
|
|
|
|
|
||||||
ацетат аммония |
|
CH3MgI |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
O |
+ CH4 ↑ |
|
|
||||
|
|
CH3−C |
OMgI |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
||
II. Реакции замещения ОН-группы
1. Реакция этерификации
Этерификация протекает в присутствии сильных и средних кислот, реакция обратима. В процессе реакции происходит замещение гидроксильной группы на алкокси группу и образование сложных эфиров.
|
|
|
O |
|
|
|
H |
CH3-C |
O |
+ H2O |
|
|
|
CH3C |
+ C2H5-O H |
|
|
OC2H5 |
|||||
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
этилэтаноат, |
|
|
|
|
|
|
|
|
|
|
|
этилацетат |
|
|
|
Механизм SN |
|
|
|
|
|
|
|
|
|
||
Nu - C2H5-O-H |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
O |
C2H5 |
|
|
O |
|
|
O-H |
|
|
|
|
H (Nu) |
|
CH |
-C |
H |
CH |
|
|
CH3-C O |
|
||||
OH |
|
-C |
|
|
|
|
|||||
3 |
|
|
3 |
OH |
-H2O |
|
|
|
|
||
|
|
|
O |
|
|
|
|
|
|||
|
|
CH3-C |
|
CH3-C |
O |
|
|
|
|
||
|
|
O-C2H5 |
|
OC2H5 |
|
|
|
||||
|
|
|
|
-H |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
||
H
133

2. Превращение в хлорангидриды и ангидриды а) синтез хлорангидридов
CH −C |
O |
+ PCl5 |
|
CH −C |
O |
+ POCl + HCl |
O-H |
|
Cl |
||||
3 |
|
3 |
3 |
|||
хлористый ацетил, хлорангидрид уксусной кислоты
В качестве реагентов можно также использовать SOCl2, PCl3.
Механизм SN
Nu - Cl
|
|
|
2 PCl5 |
|
|
|
|
|
|
|
|
PCl4 + PCl6 |
PCl6 |
|
|
|
|
|
|
PCl5 + Cl |
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-δ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
O |
|
|
PCl4 |
|
|
|
|
|
|
+δ |
|
O |
|
Cl |
|
|
|
|
|
|
|
|
|
|
O PCl4 |
|
|
|
O |
|
|||||
CH3 |
C |
|
|
CH3 |
C |
|
|
|
CH3 C |
|
|
|
|
|
CH3 C |
+ O PCl4 |
|||||||||||||||||||||
|
OH |
|
|
- H |
|
|
O-PCl4 |
|
|
|
|
|
|
Cl |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
б) синтез ангидридов |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O=PCl3 Cl |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
CH3−C |
O |
|
|
|
|
|
|
|
|
|
P2O5, t0C |
CH −C |
O |
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
O-H |
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
O + H2O |
|
|
|
|
|
|
|||||||||||||
CH3−C |
|
O-H |
|
|
|
|
|
|
|
|
|
CH3−C |
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
уксусный ангидрид |
|
|
|
|
|
|
|
|
|
|||||||||||||
4. Образование азотсодержащих производных |
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
а) синтез амидов |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
CH3−C |
O |
|
|
|
NH3 |
|
|
|
|
|
|
CH3−C |
O |
|
|
|
|
|
|
|
|
CH3−C |
O |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
O-H |
|
|
|
|
|
|
|
|
|
|
|
|
O NH4 |
|
|
|
|
|
|
|
|
NH2 |
|
|
|
||||||||||||
|
|
|
|
t0C |
|
|
|
|
|
|
|
|
-H2O |
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
или |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
амид уксусной кислоты |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ацетамид |
|
|
|
|||||
|
|
|
|
|
|
P2O5, t0C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
CH3-CH2-C |
O |
|
|
амид пропановой кислоты, пропиоамид |
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
б) синтез нитрилов |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
O |
|
|
|
|
P O |
5, |
t0C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
CH3−C |
|
|
|
|
2 |
|
|
|
|
CH3-C≡N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
NH2 |
|
-H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
нитрил уксусной кислоты |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
3 |
2 |
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ацетонитрил |
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
CH3-CH2-C≡N |
|
нитрил пропановой кислоты, пропионитрил |
|
|
|
|
|
|
|||||||||||||||||||||||||||||
134

4. Галоидирование по α - положению
а) хлорирование
CH3−COOH |
|
Cl2 |
CH2−C |
O |
|
|||
|
|
|
|
+ HCl |
||||
|
|
|
|
|||||
|
hν, 1170C |
Cl |
|
O-H |
|
|||
|
|
|
|
|
хлорэтановая, |
|
||
|
|
|
|
|
хлоруксусная кислота |
|||
R-CH2−COOH |
|
CuCl2 |
R-CH−COOH + HCl общий способ синтеза |
|||||
|
LiCl |
|
||||||
|
|
|
|
Cl |
|
|
||
|
|
|
ДМФА, t0C |
|
|
|||
|
|
|
|
|
|
|||
б) бромирование (реакция ГелляФольгарда – Зелинского)
R-CH2-COOH |
Br2 |
|
R-CH-COOH + HBr |
|
PBr3 |
||||
|
Br |
|||
5. Восстановление и окисление карбоновых кислот
а) восстановление
CH −COOH |
LiAlH4 |
(RCH2O)4AlLi |
4H2O |
4RCH |
OH + Al(OH)3 + LiOH |
|
|
|
|
||||
3 |
абс. ТГФ |
|
|
|
2 |
|
|
|
|
|
|
||
Используется для получения высших спиртов:
4 C11H23COOH |
1) LiAlH4 |
|
|
C11H23CH2OH + Al(OH)3 + LiOH |
|
|
||
додекановая, |
2) 4 H2O деканол-1, |
|
лауриловая |
|
лауриловый спирт |
кислота |
|
|
б) окисление
Карбоновые кислоты устойчивы к действию обычных окислителей, возможно окисление связи Сα - Н, если атом углерода в α - положении - третичный.
H |
KMnO4 |
OH |
|
α т. |
|||
|
|||
CH3 C COOH |
|
CH3 C COOH |
|
t0C |
|||
CH3 |
CH3 |
2-окси-2-метилпропановая кислота
135

ПРОИЗВОДНЫЕ ПРЕДЕЛЬНЫХ КИСЛОТ
Свойства и взаимные превращения
производные |
общая формула, |
примеры названий |
|
функциональная группа |
|
галогенангидриды
ангидриды
O
R -C Cl(Br)
-C Cl(Br) 
O
R -C O
-C O
R- C
C
O
CH3-C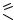 ClO
ClO
этаноил хлорид, хлорангидрид этановой (уксусной) кислоты, хлористый ацетил
O CH3-CH2-C Cl
пропаноил хлорид, хлорангидрид пропановой (пропионовой )кислоты, хлористый пропионил
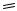 O
O
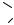 O
O
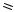 O
O
ангидрид этановой (уксусной) кислоты, уксусный ангидрид
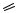 O
O
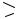 O
O
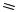 O
O
ангидрид пропановой (пропионовой) кислоты, пропионовый ангидрид
сложные эфиры |
R-C |
O |
O |
1 |
H-C |
OR |
|
OC2H5 |
|
|
|
|
этилметаноат, этиловый эфир метановой |
|
|
(муравьиной) кислоты, этилформиат |
|
|
CH3-C |
O |
|
OCH3 |
|
|
|
|
|
метилэтаноат, |
|
|
метиловый эфир этановой |
|
|
(уксусной) кислоты, |
|
|
метилацетат |
|
136
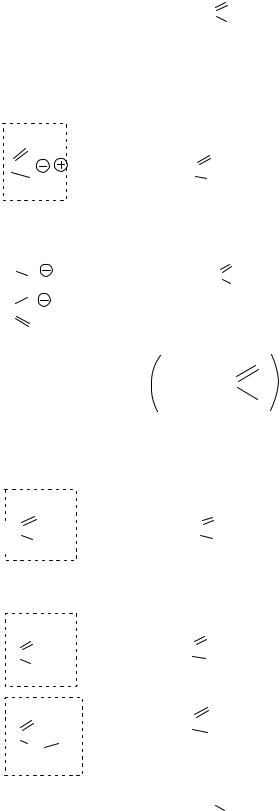
соли
амиды
O
R-C
O M M - металл
R-C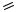 O
O
O M+2 O
R-C
O
O
R -C NH2
-C NH2
O
R-C
NH-R/
O
R-C N R/  R/
R/
O
CH3-CH2-C OC2H5
этилпропаноат, этиловый эфир пропановой (пропионовой) кислоты, этилпропионат
O H-C ONa
метаноат натрия, натриевая соль муравьиной кислоты, формиат натрия
O CH3-C ONa
этаноат натрия, натриевая соль уксусной кислоты, ацетат натрия
O |
|
CH3-CH2-C |
Ca |
O |
2 |
пропаноат кальция, кальциевая соль пропановой (пропионовой )кислоты
H-C
O
NH2
амид метановой (муравьиной) кислоты, формамид
O
H-C NH-CH3
N-метилформамид
O
H-C N(CH3)2
N,N-диметилформамид
CH3-C O NH2
O NH2
амид этановой (уксусной) кислоты, ацетамид
137
