
- •1.1. Ядерні сили та їх властивості. Ядерні реакції поділу і синтезу. Ланцюгова ядерна реакція. Ядерна енергетика та екологія.
- •1.2. Вивчення елементарних частинок та їх властивостей в школі.
- •1.3. Під яким кутом до поверхні Землі треба кинути тіло, щоб максимальна висота його підняття була рівна дальності польоту?
- •2.1. Радіоактивність, закон радіоактивного розподілу. Природа , , випромінювання. Правила зміщення.
- •2.2. Методика розв’язання задач з динаміки.
- •3.1. Перший принцип термодинаміки і його застосування. Оборотні ті необоротні процеси. Основні термодинамічні процеси.
- •3.2. Формування поняття про внутрішню енергію та способи її зміни.
- •4.1. Дослід Резерфорда і планетарна модель атома. Постулати Бора. Атом водню.
- •4.2. Методика введення поняття про електричний заряд в школі.
- •5.2.Методика введення фізичних величин в шкільному курсі фізики
- •5.3. До стелі ліфта, що рухається вертикально вгору з прискоренням 0,98 м/с2 , прикріплено пружний динамометр, на якому висить тягарець масою 1 кг. Яку силу показує стрілка динамометра?
- •7.1. Основні положення молекулярно-кінетичної теорії(мкт). Ідеальний газ. Основне рівняння мкт. Газові закони. Рівняння стану ідеального газу.
- •9.1. Методика формувань основних понять теми «Магнітне поле»
- •9.2. Стаціонарне магнітне поле у вакуумі, його вихровий характер. Закон Біо-Савара-Лапласа. Теорема про циркуляцію вектора напруженості магнітного поля.
- •9.3. Задача
- •12.1. Простір і час в нерелятив. Фізиці. Кінематика матеріальної точки. Системи відліку. Перетворення Галілея, їх кінематичні наслідки.
- •12.2. Формування основних понять кінематики в школі
- •2. Шлях і переміщення.
- •7. Рівномірний рух по колу.
- •Другий принцип термодинаміки. Теплові машини. Третій принцип термодинаміки. Ентропія: фіз. І стат. Зміст.
- •Методика вивчення теми: «Елементи теорії відносності»
- •14.2.Методика вивчення «Електричного струму в різних середовищах».
- •16.2 Вивчення теми «Світлові явища» в школі.
- •17.1 Поляризація світла. Поляризація при відбиванні та заломлені світла. Закон Брюстера та Малюса. Поляризаційні приклади та їх застосування.
- •17.3 Вісім однакових краплин, які мають однакові заряди, зливаються в одну велику краплину. Як зміниться її потенціал відносно потенціалу окремої краплини?
- •18.1 Робота, потужність, кінетична і потенціальна енергії. Збереження механічної енергії.
- •18.2. Лабораторна робота визначення теплоємності .
- •19.1. Геометрична оптика . Закони геометричної оптики. Тонкі лінзи . Фокусні лінзи.
- •19.2. Методика навчання явища електромагнітної індукції в 11 кл.
- •20.2.Формування основних понять обертального руху в школі.
- •22.2. Вивчення законів динаміки в школі.
- •23.1. Механічні коливання в ідеальних і реальних системах. Характеристики коливань і їх зв'язок з параметрами системи. Резонанс.
- •23.2. Методика формування основних понять коливального руху.
- •24.2. Вивчення алгебраїчних станів в шкф.
4.1. Дослід Резерфорда і планетарна модель атома. Постулати Бора. Атом водню.
Важливу роль у з’ясуванні будови атома зіграли досліди Е.Резерфорда щодо вивчення проходження альфа-частинок через тонкі плівки (фольги) золота та інших металів етапів.(мал.1) Досліди виявили, що деяка кількість α-частинок, розсіюючись атомами золота, відхилялась на великі кути (більші 900).
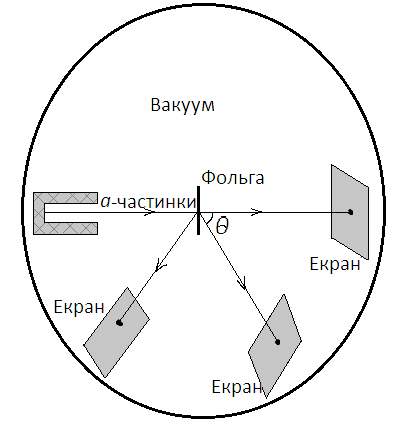
мал.1 мал.2 мал.3
Р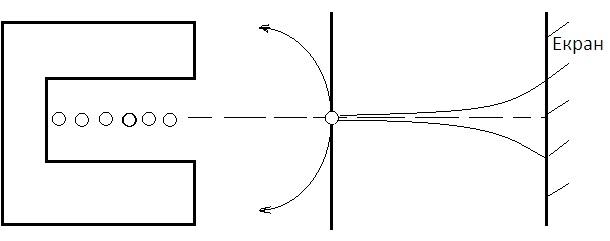 езерфорд
зрозумів, що весь позитивний заряд атома
зосереджений в центрі атома – ядрі, яке
займає дуже малий об’єм, порівняно з
усім об’ємом атома. Більшість α-частинок
визнає незначного розсіяння, бо
ймовірність влучення їх у ядро мала.
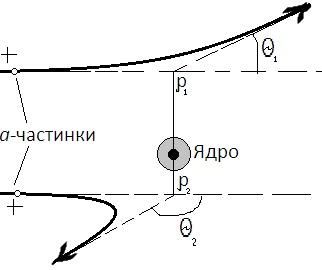
Однак α-частинки, що проходять поблизу
ядра, різко відхиляються бо на малих
відстанях діють дуже великі сили
відштовхування між позитивними
α-частинками і ядром (мал.2)
езерфорд
зрозумів, що весь позитивний заряд атома
зосереджений в центрі атома – ядрі, яке
займає дуже малий об’єм, порівняно з
усім об’ємом атома. Більшість α-частинок
визнає незначного розсіяння, бо
ймовірність влучення їх у ядро мала.
Однак α-частинки, що проходять поблизу
ядра, різко відхиляються бо на малих
відстанях діють дуже великі сили
відштовхування між позитивними
α-частинками і ядром (мал.2)
Навпроти
отвору в свинцевому контейнері на
екрані, покритому
![]() можна було помітити світлову пляму.
Резерфорд помістив на шляху рухомих
ядер тонку золоту пластинку (фольгу), і
помітив, що лише незначна частина ядер
відхиляється на значні кути і дуже мало
ядер відбивались назад. Узагальнивши
результати дослідів, Резерфорд зробив
висновки:
можна було помітити світлову пляму.
Резерфорд помістив на шляху рухомих
ядер тонку золоту пластинку (фольгу), і
помітив, що лише незначна частина ядер
відхиляється на значні кути і дуже мало
ядер відбивались назад. Узагальнивши
результати дослідів, Резерфорд зробив
висновки:
-
в цілому атом порожній. Майже вся його маса сконцентрована в ядрі діаметром
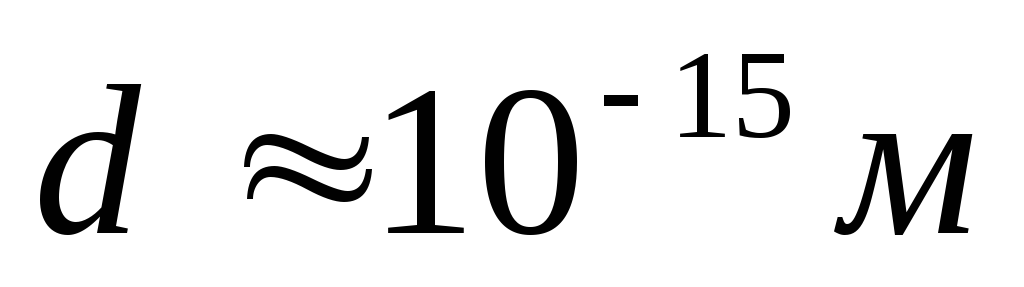 .
. -
Ядро несе в собі заряд
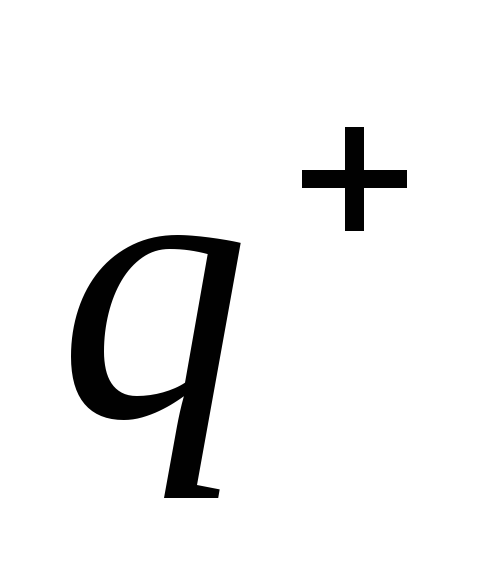 ,
величина якого за модулем дорівнює
заряду електрона, помноженому на
порядковий номер цього елемента в
таблиці Менделєєва.
,
величина якого за модулем дорівнює
заряду електрона, помноженому на
порядковий номер цього елемента в
таблиці Менделєєва. -
Оскільки атом електрично нейтральний, то позитивний заряд ядра компенсує заряд електронів, які мають рухатись навколо ядра, подібно до планет навколо Сонця.
На підставі результатів своїх дослідів Резерфорд запропонував ядерну (планетарну) модель будови атома.
Модель атома за Резерфордом припускає наступне:
1) весь
позитивний заряд атома і майже вся його
маса зосереджені в атомному ядрі –
області, яка займає дуже малий об’єм,
порівняно з усім об’ємом атома (лінійні
розміри ядра приблизно дорівнюють
![]() ,
а лінійні розміри атома -
,
а лінійні розміри атома -
![]() ).
).
Пізніше
було встановлено, що ядро атома завжди
містить ціле число позитивних елементарних
зарядів, тобто заряд ядра виражається
формулою
![]() ,
де
,
де
![]() - елементарний заряд;
- елементарний заряд;
![]() - номер хімічного елемента в таблиці
Менделєєва.
- номер хімічного елемента в таблиці
Менделєєва.
2) навколо ядра з великою шв-тю коловими орбітами рухаються електрони, подібно до планет навколо Сонця. Радіус колової орбіти самого далекого від ядра електрона і є радіус атома.
3) сумарний негативний заряд електронів дорівнює позитивному заряду ядра – атом в цілому нейтральний.
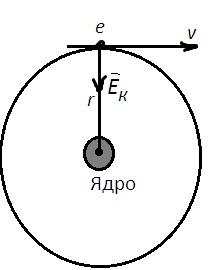
4) електрон утримується на орбіті Кулонівською силою притягання до ядра, яка надає електрону доцентрового прискорення (мал. 3).
ПОСТУЛАТИ БОРА
Запропонована
Резерфордом ядерна модель атома дозволила
пояснити результати дослідів з розсіювання
α-частинок у речовині, але зустрілася
з іншою принциповою перешкодою: закони
руху електронів у атомі Резерфорда
суперечили законам електродинаміки.
За цими законами електрон, рухаючись
по колу з прискоренням, повинен безперервно
випромінювати енергію у вигляді
електромагнітних хвиль. Внаслідок
випромінювання електрон повинен втрачати
енергію і, рухаючись по спіралі, за
короткий час (близько
![]() )
впасти на ядро. При цьому спектр
випромінювання повинен бути суцільним.
Насправді численні досліди показують,
що атоми – стійкі системи, які існують
десятки тисячоліть без змін і мають
лінійчасті, а не суцільні спектри
випромінювання.
)
впасти на ядро. При цьому спектр
випромінювання повинен бути суцільним.
Насправді численні досліди показують,
що атоми – стійкі системи, які існують
десятки тисячоліть без змін і мають
лінійчасті, а не суцільні спектри
випромінювання.
У 1913 р. датський учений Н.Бор зробив спробу пов’язати в єдине ціле ядерну модель атома водню і квантовий характер випромінювання й поглинання світла. Теорія Бора ґрунтується на трьох твердженнях:
Перший постулат Бора (умова стаціонарності орбіт): електрони в атомі можуть рухатися тільки певними (стаціонарними) орбітами, перебуваючи на яких вони, незважаючи на рух з прискоренням, не випромінюють енергії: при цьому атом перебуває в стійкому (стаціонарному) стані. Цей постулат по суті стверджує, що для опису руху електронів класична теорія неприйнятна.
Д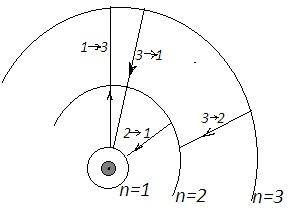 ругий
постулат Бора
(умова частот): випромінювання або
поглинання енергії атомами відбувається
тільки під час стрибкоподібної зміни
стану електрона, тобто під час його
переходу з однієї стаціонарної орбіти
з енергією
ругий
постулат Бора
(умова частот): випромінювання або
поглинання енергії атомами відбувається
тільки під час стрибкоподібної зміни
стану електрона, тобто під час його
переходу з однієї стаціонарної орбіти
з енергією
![]() на іншу енергію
на іншу енергію
![]() (мал.4). При цьому випромінюється чи
поглинається один фотон, енергія якого
визначається за формулою:
(мал.4). При цьому випромінюється чи
поглинається один фотон, енергія якого
визначається за формулою:
![]() .
.
Другий постулат Бора підтверджує експериментальне встановлений закон оборотності спектральних ліній – атоми поглинають лише ті спектральні лінії, які самі можуть випромінювати.
Третій
постулат Бора
(умова квантування): радіуси стаціонарних
орбіт (станів)
![]() мають такі значення, що їх добуток на
імпульс електрона
мають такі значення, що їх добуток на
імпульс електрона
![]() дорівнює цілому числу сталих Планка
дорівнює цілому числу сталих Планка
![]() ,
поділених на
,
поділених на
![]() :
:
![]() ,
,
![]() ,
де
,
де
![]() - маса електрона,
- маса електрона,
![]() - номер орбіти електрона,
- номер орбіти електрона,
![]() - його шв-ть на
- його шв-ть на
![]() й
орбіті,
й
орбіті,
![]() - радіус цієї орбіти.
- радіус цієї орбіти.
Гідроген. Хімічний знак Н.
Електрон рухається навколо ядра, утворюючи електронну оболонку. Негативний заряд електрона у атомі дорівнює позитивному заряду протона у ядрі атома.
Маса
всіх атомів приблизно кратні масі
найлегшого атома – атома Гідрогену.
Наприклад, маса наступного за масою
атома – атома Гелію в 4 рази більша за
масу атома Гідрогену, а маса атома
Карбону приблизно у 12 разів більша за
масу атома Гідрогену. Ми не випадково
згадали про Карбон: за атомну одиницю
маси (а.о.м.) прийнято саме
![]() маси атома Карбону.
маси атома Карбону.
