
- •Катаболизм липидов
- •Всасывание продуктов расщепления липидов
- •Транспорт липидов
- •Вопрос 15. Транспорт жирных кислот в митохондрии. Роль карнитина в этом процессе
- •Вопрос 16. Транспорт жирных кислот в митохондрии. Роль карнитина в этом процессе Транспорт ацил-СоА в митохондрии
- •Вопрос 17. Β-окисление насыщенных жирных кислот с четным числом углеродных атомов
- •Вопрос 18. Метаболизм кетоновых тел Образование кетоновых тел (кетогенез)
- •Вопрос 19. Два пути биосинтеза триацилглицеролов Биосинтез триацилглицеролов
- •Вопрос 20. Биосинтез холестерина. Роль гидроксиметилглутарил-СоА редуктазы в регуляции этого процесса Биосинтез холестерола
- •Вопрос 21. Расщепление белков в жкт
- •Вопрос 22. Характеристика ферментов вне- и внутриклеточного протеолиза
- •Вопрос 23. Транспорт аминокислот через мембраны. Γ-глутамильный цикл.
- •Вопрос 24, 25.
Вопрос 20. Биосинтез холестерина. Роль гидроксиметилглутарил-СоА редуктазы в регуляции этого процесса Биосинтез холестерола
Синтез ХС происходит в цитоплазме и микросомах. Исходным веществом для синтеза стеролов является ацетил-СоА, который транспортируется из митохондрий в цитоплазму (транспорт ацетил-СоА рассмотрен ранее, в лекции 23). 3-гидрокси-3-метилглутарил-СоА редуктазная (ГМГ-СоА редуктаза) реакция ‒ первая, практически необратимая реакция в цепи биосинтеза ХС. Она протекает со значительной потерей свободной энергии. Установлено, что данная реакция лимитирует скорость биосинтеза холестерина. Реакции фосфорилирования требуются для солюбилизации изопреноидных интермедиатов данного пути.
Биосинтез холестерола осуществляется в несколько этапов. I этап (рис.24.2) включает образование 3-гидрокси-3-метилглутарил-СоА (ГМГ-СоА) из ацетил-СоА и превращение ГМГ-СоА в мевалонат. В результате двух последовательно протекающих реакций (тиолазной и гидроксиметил-глутарил-СоА-синтазной) из трех молекул ацетил-СоА образуется одна молекула 3-гидрокси-3-метилглутарил-СоА.
Следующая реакция – превращение ГМГ-СоА в мевалонат. Она катализируется ГМГ-СоА редуктазой. Процесс восстановления требует затраты двух молекул NADPH. Источником NADPH является пентозофосфатный путь окисления глюкозы, а также NADP+-зависимые цитозольные малатдегидрогеназная и изоцитратдегидрогеназная реакции.

Рис.24.2. Первый этап биосинтеза холестерола
II этап (рис.24.3) – превращение мевалоната в фарнезилпирофосфат. Мевалонат дважды подвергается фосфорилированию по 5-ОН-группе при участии киназ. Донором фосфатных групп в этих реакциях служит АТР. Пирофосфомевалонат подвергается декарбоксилированию и дегидратированию, превращаясь в изопентенилпирофосфат (ИПФ, С5). Изопентенилпирофосфат ‒ активная изопреноидная единица, широко распространенная в природе и участвующая не только в синтезе ХС, но в смниезе каротиноидов, боковых цепей убихинонов, витаминов К и Е.
ИПФ изомеризуется в диметилаллилпирофосфат (ДПФ, С5). Взаимодействие ИПФ с молекулой диметилаллилпирофосфата, катализируемое изопентенилтрансферазой, приводит к образованию геранилпирофосфата (С10). Изопентенилтрансфераза осуществляет перенос диметилаллильного радикала на раскрывающуюся двойную связь в молекуле ИПФ. При этом происходит миграция двойной связи и потеря одной молекулы пирофосфата.

Рис. 24.3. Превращение мевалоната в фарнезилпирофосфат
К геранилпирофосфату вновь присоединяется ИПФ, в результате образуется фарнезилпирофосфат (С15) и освобождается пирофосфат, получающий атом водорода от близлежащей метиленовой группы. Эта конденсация является NADPН-зависимым процессом.
Этот же фермент катализирует реакцию переноса радикала геранила от геранилпирофосфата к следующей молекуле ИПФ. Освобождающийся в этой и в предыдущей реакции пирофосфат гидролизуется неорганической пирофосфатазой, что обеспечивает необратимость биосинтетического процесса. Продуктом данного этапа биосинтеза холестерола служит фарнезилпирофосфат (С15).
III этап (рис.24.4, рис. 24.5) ‒ образование сквалена из фарнезилпирофосфата и превращение сквалена в ланостерол.
|
|
|
|
Рис.24.4. Образование сквалена |
Рис.24.5.Превращение сквалена в ланостерол |
Две молекулы фарнезилпирофосфата, соединяясь «голова к голове» и теряя каждая свой пирофосфат, образуют сквален, содержащий 30 втомов углерода. Сквален образуется из прескваленпирофосфата под действием фермента скваленсинтазы, локализованной в эндоплазматическом ретикулуме. Источником атомов водорода в этой реакции является NADPH.
Сквален ‒ непредельный углеводород, состоящий их шести изопреноидных единиц (С30). Молекула сквалена легко принимает пространственную конфигурацию, близкую к пространственной конфигурации стеролов.
На стадии образования сквалена завершается анаэробная фаза биосинтеза ХС. Последующая фаза биосинтеза ХС является аэробной. На первом этапе при участии сквален-эпоксидазы, являющейся монооксигеназой, сквален легко окисляется с образованием сквален-2,3-эпоксида.
Ланостерол-синтаза осуществляет замыкание шести ‒ и пятичленных циклов в результате протонирования эпоксидной группы и смещения электронной плотности в системе двойных связей сквалена. По такому пути протекает образование ланостерола в клетках печени. У растений и других организмов в циклизации сквален-2,3-эпоксида принимают участие другие циклизующие ферментные системы с образованием продуктов иных, нежели ланостерол. Ланостерол уже имеет гидроксильную группу в положении 3 и три лишние по сравнению с ХС метильные группы. Они окисляются до карбоксильных, которые затем удаляются декарбоксилированием.
IV этап (рис.24.6) – превращение ланостерола в холестерол. Преобразование ланостерола ‒ многоступенчатый процесс, в ходе которого образуются разнообразные индивидуальные стеролы (зимостерол, десмостерол), характерные для животного и растительного мира.
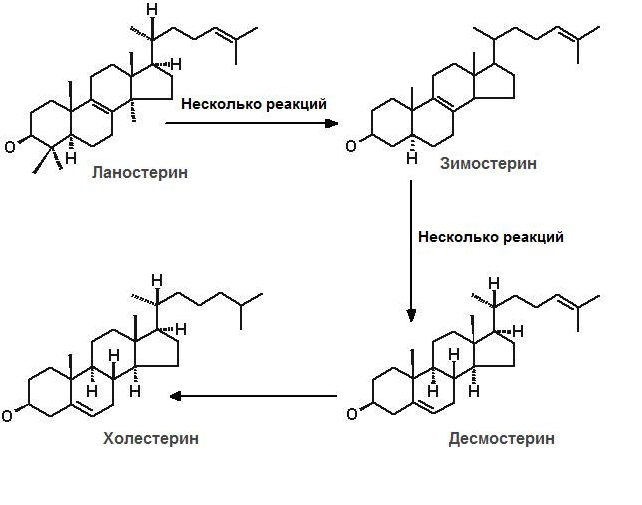
Рис.24.6. Трансформация ланостерола в холестерол
Хотя ланостерол и похож по структуре на холестерол, для его превращения в ХС требуется 20 дополнительных реакций. Ферменты, ответственные за эту трансформацию, локализованы в ЭПР. Преобразование ланостерола в ХС может идти двумя путями. Один из них ‒ восстановление десмостерола (приведен на рис. 24.6). Другой путь включает образование 7-дегидролхолестерола как предпоследнего интермедиата при синтезе холестерина.
Независимо от заключительного пути преобразования ланостерола, суммарный итог всех реакций биосинтеза ХС выглядит следующим образом:
18 СН3СОSСоА + 10 Н+ + ½ О2→ С27Н46О + 9СО2 + 18 HSСоА
Источником углеродного скелета холестерола служит ацетил-СоА, донором водорода являются вода и NADPН. Начиная со сквалена и заканчивая холестеролом, все промежуточные продукты биосинтеза нерастворимы в водной среде. Поэтому они участвуют в конечных реакциях биосинтеза ХС, будучи связанными со стеринпереносящими белками. Это обеспечивает их растворимость в цитозоле клетки и протекание соответствующих реакций. Стеринпереносящие белки обеспечивают также перемещение ХС внутри клетки, что имеет важное значение для вхождения его в клеточные мембраны, окисления в желчные кислоты, превращения в стероидные гормоны.
Эфиры холестерола ‒ принципиальная форма циркулирующего ХС ‒ образуются на цитоплазматической стороне ЭПР.

Рис. 24.7. Синтез ХС и его эфиров в эндоплазматическом ретикулуме
Биосинтез стеридов протекает путем переноса остатка высшей жирной кислоты от молекулы ацил-СоА на место водорода ОН-группы стерола. Катализирует этот процесс холестерол-ацилтрансфераза. Источником ацильных групп при биосинтезе стеридов могут выступать глицерофосфолипиды, в частности фосфатидилхолин. Он участвует в образовании эфиров холестерола лимфы и плазмы крови у человека при участии фосфатидилхолин-холестерол-ацилтрансферазы.


