
- •Введение
- •Нейромедиаторы центральной нервной системы
- •Синапс торможения
- •Седативно-снотворные средства
- •Нейростимуляторы и конвульсанты
- •Местные и общие анальгетики
- •Местные анальгетики
- •Опиатные анальгетики
- •Галлюциногены
- •Антипсихотические средства
- •Психотические средства
- •Введение ………………………………………………………… 3
-
Нейромедиаторы центральной нервной системы
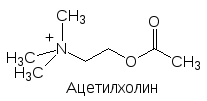
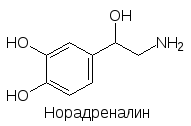
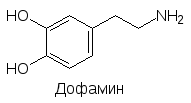
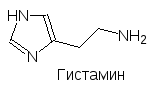
Головной мозг состоит из нескольких специализированных отделов, выполняющих особые функции. В лобной части расположена лимбическая система нервных клеток, выделяются таламус, гипоталамус, неостриатум, палеостриатум, средний мозг, продолговатый мозг, мост (три последних отдела связывают головной и спинной мозг). Кроме них есть чёрная субстанция (substantia nigra), голубое пятно (locus coerulans) и другие. Их согласованная работа обеспечивается многими нейромедиаторами и нейро-модуляторами, участвующими в межнейрональных взаимодействиях. Важнейшими нейромедиаторами ЦНС являются ацетилхолин, норадрена-лин, дофамин, серотонин, гистамин, глютаминовая кислота, ‑амино-масляная кислота (ГАМК), глицин и нейропептиды (энкефалины, динорфины, эндорфины (эндогенные морфины)):
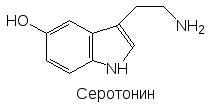
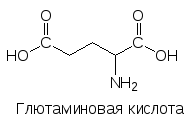
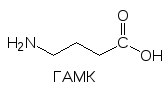
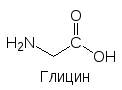
![]()
![]()
Однако этот перечень нельзя считать окончательным, так как совре-менные методы исследования позволяют находить новые нейромедиаторы. Так, ещё в 1965 году в клетках ЦНС был обнаружен ацетилированный дипептид из аспарагиновой и глютаминовой кислоты, но только в последние годы было показано, что он является третьим по важности нейромедиатором а головном мозге:
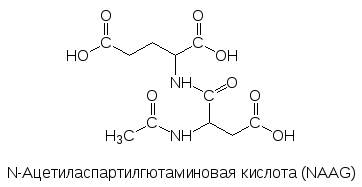
В последние годы накоплены убедительные данные о медиаторной роли производных жирных кислот, называемых нейролипинами (см. стр. ).
Если биосинтез ацетилхолина не связан с какой-либо конкретной группой клеток ЦНС, то дофамин синтезируется преимущественно в чёр-ной субстанции, норадреналин в голубом пятне, а серотонин в ядрах шва.
Ацетилхолин в головном мозге выполняет функции медиатора проме-жуточных нейронов, обеспечивающих переключение воздействий стволо-вой части мозга на кору больших полушарий. Многие отклонения в функционировании ЦНС системы связаны с пониженным уровнем ацетил-холина. В частности, к ним относятся миастения, некоторые виды пара-личей и болезнь Альцгеймера (старческое слабоумие). Для лечения таких болезней могут быть использованы как холиномиметики, так и ингиби-торы холинэтераз, разлагающих выполнивший медиаторную функцию ацетилхолин на холин и уксусную кислоту. При этом часто в одном препа-рате проявляются оба эти механизма биологической активности. Необра-тимыми ингибиторами холинэстераз являются многие органические производные кислот фосфора с фосфорилирующей способностью, напри-мер, смешанный этиловый и 4‑нитрофениловый эфир этилфосфоновой кислоты (армин):
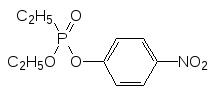
Этот препарат исследовался как средство для лечения глаукомы (повышенного внутриглазного давления). Достаточно давно применяется в медицине для лечения различных инвазий, например, при некоторых видах шистосомозов, метрифонат (известный как инсектицид хлорофос), но в последние годы он исследуется как ингибитор холинэстеразы, который также может найти применение для лечения болезни Альцгеймера. Вызванная действием фосфорилирующих агентов инактивация локализо-ванной в синапсах холинэстеразы носит необратимый характер, а биосинтез новых молекул этого фермента идет очень медленно. Вследствие этого эффект фосфорорганических препаратов оказывается достаточно продолжительным.
Обратимым ингибитором холинэстеразы является выделяемый из луковиц подснежника Воронова и других лилейных семейства амарили-совых алкалоид галантамин:
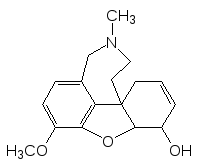
Его применяют в виде гидробромида при миастении, прогрессивной мышечной дистрофии и при других заболеваниях, в частности, при комплексном лечении последствий нарушения мозгового кровообращения и перенесенного полиомиэлита.
Эффективными средствами для лечения болезни Альцгеймера оказа-лись обратимые ингибиторы холинэстеразы, представляющие собой замещенные 4‑аминопиридины. В этой группе лекарственных соединений оптимальным сочетанием свойств выделяются отечественный препарат амиридин и разработанный в США такрин:
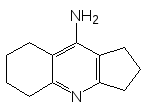 и
и

Амиридин менее токсичен для клеток печени. Замещенные 4‑амино-пиридины отличаются от обычных ингибиторов холинэстераз тем, что они блокируют также калиевую проницаемость мембран и в соответствии с этим стимулируют передачу нервного импульса в М‑холинэргических и ГАМК-эргических синапсах, увеличивая продолжительность потенциала действия. С влиянием на проведение сигнала торможения в ГАМК-эргических синапсах связано, очевидно, их седативное действие.
В настоящее время основными средствами для лечения болезни Альгеймера является донепезил (анцепт) и замещенный аминоадамантан (мемантан), соответственно (6,3 и 4,2 млн. рецептов в США в 2010 году):
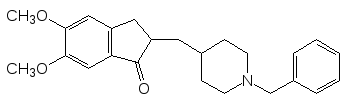
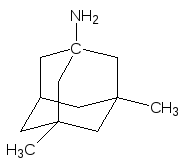
Нейромедиатором возбуждения в нейронах ЦНС является глютами-новая кислота. Её рецепторы представляют собой сложные образования, которые участвуют во многих процессах, в частности, в механизме форми-рования памяти, в развитии познавательных (когнитивных) функций. Избыточная активация глютаматных рецепторов является одним из факто-ров патогенеза эпилепсии. Эта аминокислота стабилизирует в клетках содержание калия и, кроме того, связывает токсичный метаболический аммиак. Установлено, что до 70% синапсов в центральной нервной системе являются глютаматэргическими.
При декарбоксилировании глютаминовой кислоты образуется ГАМК, которая в отличие от глютаминовой кислоты выполняет роль нейромедиа-тора в синапсах торможения. Функционирование ГАМК-эргических синапсов связано с нигростриатумной системой. Роль нейромедиатора торможения в спинном мозге выполняет глицин. Есть рецепторы на глицин и в нейронах головного мозга. Его применяют как мягкое снотворное и анксиолитическое средство, он усиливает действие многих психоактивных соединений с седативным эффектом.
Дофамин и норадреналин называют катехоламинами. Катехоламин-, гистамин- и серотонинэргические системы нейронов участвуют в регуляции двигательной активности, в эмоциональных реакциях, в формировании памяти, в процессах сна и бодрствования. Нарушения в работе этих систем лежат в основе патогенеза многих психических заболеваний.
Очень важная роль в осуществлении и регуляции нейромедиаторных процессов в головном мозге принадлежит нейропептидам. Они могут выполнять функции самостоятельных нейромедиаторов, но не исключено и их присутствие в нервных окончаниях вместе с «классическими» нейро-медиаторами в роли нейромодуляторов. Лучше других в этом ряду исследованы эндогенные опиаты – энкефалины, динорфины и эндорфины, например, Мет-энкефалин (Тир-Гли-Гли-Фен-Мет) и Лей-энкефалин (Тир-Гли-Гли-Фен-Лей). В составе полипетидных динорфинов и эндорфинов N‑концевая последовательность из пяти аминокислот всегда представлена энкефалинами. Эндогенные опиаты модулируют болевые ощущения, они могут участвовать в регуляции двигательной активности, в терморегуля-ции, в адаптации. Введение этих веществ вызывает эйфорию, чувство удовлетворения – это эффекторы внутреннего подкрепления, медиаторы морального вознаграждения, именно их выделение создает ощущение счастья. Есть данные о связи дофаминовых и энкефалиновых медиаторных путей. Так, например, блокаторы дофаминовых рецепторов снижают и двигательную активность, вызываемую энкефалином.
Рабочая гипотеза в области нейрохимии объясняет отклонения в психической деятельности нарушением баланса нейромедиаторов в синапсах ЦНС, например:
-
избыток дофамина в головном мозге вызывает шизофрению,
-
низкий уровень серотонина и норадреналина приводит к депрессии,
-
высокий уровень двух этих нейромедиаторов вызывает маниакально-депрессивные психозы (периодическая смена состояний повышенного возбуждения, беспокойства и апатии).
Такая упрощенная картина не совсем адекватно описывает все воз-можные отклонения в психической деятельности, но полной ясности во взаимоотношениях между разными нейромедиаторами пока нет.
Тяжёлая болезнь – паркинсонизм – является следствием недостатка дофамина в клетках мозга. В её основе лежит дегенеративное изменение клеток чёрной субстанции, которые его продуцируют. Сам дофамин не проходит через гематоэнцефалический барьер и поэтому его бесполезно использовать в качестве средства для лечения паркинсонизма, от которого чаще всего страдают пожилые люди. Паркинсонизм может также развить-ся у молодых людей в результате, например, вызванного травмой крово-излияния в области чёрной субстанции. Болезнь выражается в постоянном напряжении мышц, из-за чего любые движения даются с трудом, они плохо скоординированы, замедленны. Конечности у больных паркинсо-низмом находятся в постоянных колебательных движениях. В качестве средства для медикаментозного лечения паркинсонизма используется его биохимический предшественник – L‑3,4‑диоксифенилаланин (леводопа), превращающийся в дофамин в результате декарбоксилирования, и некото-рые его производные:
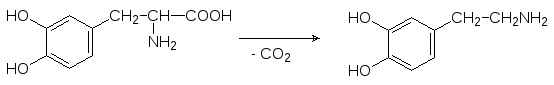
Конечно, обидно, что для образования оптически неактивного дофамина приходится принимать тщательно очищенный от D‑изомера препарат, но даже чистый леводопа не очень эффективен. Через несколько лет приёма это лекарство перестаёт помогать и наступает полная инвалид-ность, а примесь в нём D-изомера приводит к этому ещё скорее.
Картина взаимоотношений нейромедиаторов с их синтетическими или природными аналогами (со свойствами агонистов и антагонистов) ослож-нена ещё и тем, что на каждый нейромедиатор есть несколько типов рецепторов. В качестве примера можно привести норадреналин, который связывается с - и ‑адренорецепторами. Интересные данные получены на фторированных аналогах норадреналина:
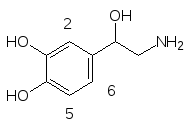
6-Фторнорадреналин является агонистом норадреналина в -адрено-рецепторах и практически не действует на -адренорецепторы. 2-Фторнор-адреналин связывается преимущественно с -адренорецепторами, тогда как 5-фторнорадреналин практически идентичен самому норадреналину и связывается с обоими типами адренорецепторов.
Обнаружено четыре типа рецепторов на гистамин; по крайней мере один из них связан с активностью аденилатциклазы. Если принять во внимание, что уже сейчас известно более двенадцати нейромедиаторов ЦНС, то становится понятной сложность картины взаимодействия психо-активных веществ с разными рецепторами в нейронах головного мозга, тем более, что различие в строении самих нейромедиаторов иногда не так уж и велико. Часто их избирательность основана не столько на структур-ных факторах, сколько на локализации, когда соответствующий синапс содержит определённый нейромедиатор и соответствующий рецептор, а попадание в этот синапс другого нейромедиатора исключено.
Различают ионотропные и метаботропные рецепторы. Первый тип рецепторов связан с ионными каналами, их активация вызывает ионный ток, оказывая таким образом непосредственное воздействие на иннерви-руемую клетку (чаще всего это нейрон). Метаботропные рецепторы пере-дают сигнал через G-белки, запускающие образование вторичных внутри-клеточных регуляторов – мессенджеров, которые активируют определён-ные метаболические процессы.
Связанные с ионными каналами глютаматные рецепторы, как и в дру-гих случаях, названы по наиболее активным агонистам. Два основных под-типа представлены NMDA-рецептором с селективным агонистом N-метил-D-аспарагиновой кислотой (NMDA) и АМРА-рецептором с 2-амино-3-(3-гидрокси-5-метилизоксазол-4-ил)пропановой кислотой (АМРА) в качестве селективного агониста:
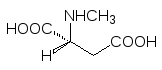 N-Метил-D-аспарагиновая
кислота
N-Метил-D-аспарагиновая
кислота
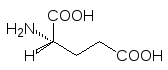 L-Глютаминовая
кислота
L-Глютаминовая
кислота
-
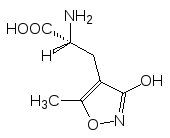
2-Амино-3-(3-гидрокси-5-метилиз-оксазол-4-ил)-пропановая кислота
Антагонисты глютаминовой кислоты на NMDA-рецепторах и АМРА-рецепторах интенсивно исследуются в фармакологическом отношении, так как они могут найти применение при лечении заболеваний, связанных с избыточной активацией этих рецепторов.
Важную роль в работе центральной нервной системы играют ГАМК-эргические синапсы, контролирующие прохождение сигналов возбужде-ния. Агонисты и антагонисты ГАМК, а также лиганды регуляторных сайтов в комплексе белков, обеспечивающих работу синапса торможения, представляют собой важную группу биологически активных веществ, используемых для корректировки сбоев в работе ЦНС. Принцип функцио-нирования синапса торможения достаточно важен для понимания меха-низма действия многих веществ седативно-снотворного, психости-мулирующего и конвульсантного направления и поэтому далее в самом общем виде будут представлены полученные в последние годы представ-ления о возможных путях вмешательства в работу этого важнейшего отдела нервной системы.
