
- •Лабораторна робота № 8 побудова кривих охолодження та діаграми подвійних сплавів
- •Короткі теоретичні відомості
- •Послідовність виконання роботи
- •Додаток для самостійної роботи Правило фаз (закон Гібса)
- •Питання для самоконтролю
- •Література
- •Лабораторна робота № 9 аналіз діаграми залізо – цементит
- •Короткі теоретичні відомості
- •Експериментальна побудова діаграм стану подвійних сплавів
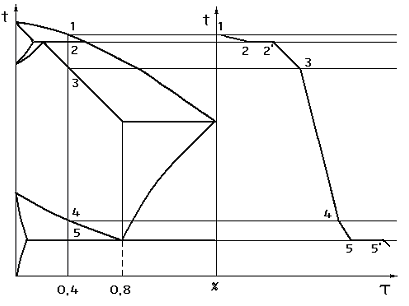
Рис. 9.2 Крива охолодження сталі 40.
В кожній з утворених точок відбудуться поліморфні перетворення, характер яких можна визначити правилом фаз. Так в точці 1 сплав починає кристалізуватись. З рідини виділяється ферит, тобто буде дві фази рідина-ферит. Тоді:
С1 = 2-2 + 1 = 1.
Значить С ≠ 0, що відповідає перегину на кривій охолодження (не нонваріантна система).
В точці 2 відбувається перитектичне перетворення. З рідини та фериту виділяється аустеніт, тобто система трифазна. Тоді:
С2 = 2 – 3 + 1 = 0.
Поскільки С = 0, то система є нонваріантною. Отже, на кривій охолодження буде полочка – температура не змінюється.
Наступна точка 3 лежить на лінії солідус, тобто сплав повністю кристалізувався, утворивши аустеніт. Тоді:
С3 = 2 – 1 + 1 = 2.
Отже, в точці 3 система не нонваріантна, що на кривій охолодження відображається перегином лінії.
128
Лабораторна робота № 8 побудова кривих охолодження та діаграми подвійних сплавів
Мета роботи: оволодіти методикою побудови кривих охолодження металів та сплавів методом термічного аналізу.
При виконанні роботи треба отримати такі знання та уміння:
Знання - особливості плавлення кристалічних тіл (металів), поліморфні перетворення в металах.
Уміння - готувати та проводити експеримент, за результатами експерименту будувати криві охолодження та діаграми подвійних сплавів.
Обладнання та матеріали: електрична пічка, термопара з вимірювальним приладом, олово, цинк, секундомір.
Короткі теоретичні відомості
Криві охолодження для металів і сплавів будуються в координатах температура-час. Розплавлений метал рівномірно охолоджують і фіксують зміну температури через певні проміжки часу. Зміни в стані металу чи сплаву, які відбуваються при їх охолодженні, супроводжуються поглинанням або виділенням тепла. Температури при яких відбуваються ці зміни називаються критичними.
При охолодженні металу та сплаву на графіку може бути одна або декілька критичних точок (температур). Це говорить про те, що метали та сплави можуть мати одне або декілька поліморфних перетворень. Наприклад, залізо має три поліморфні перетворення, а олово - одне.
П
113
внутрішньою енергією). На кривих охолодження це відображається для чистих металів поличкою, а сплавів переломом лінії. Наприклад на кривій охолодження заліза буде три полочки, а олова -одна.
При проведенні експерименту з'ясуйте при якій температурі у олова на кривій охолодження буде поличка.
Використовуючи криві охолодження металу та його сплавів можна побудувати діаграму подвійних сплавів у координатах температура - концентрація.
Для побудови діаграми сплаву олово-цинк треба використати чисті метали олово та цинк та їх сплави доевтектичний (4% Zn і 96% Sn), евтектичний (9% Zn і 91% Sn) і заевтектичний (30% Zn і 70% Sn). Для з'ясування порядку проведення експерименту скористайтесь підручником (1).
Для аналізу процесу кристалізації користуються правилом фаз (правило Гіббса) та правилом відрізків. З'ясуйте їх користуючись рекомендованою літературою (1)і(2).
Послідовність виконання роботи
1. Ознайомитись з лабораторною установкою, яка складається з електричної пічки, тигеля для металу і вимірювального приладу.
2. В тигель помістити олово та цинк у необхідному співвідношенні (за вказівкою викладача).
3. Включити електропічку у мережу.
4. Після розплавлення металу пічку виключити. Через рівномірні проміжки часу (10-15 с) фіксувати покази вимірювального приладу.
5. Користуючись градуйовочним графіком перевести зняті покази в температуру.
6. Побудувати криві охолодження.
7. Побудувати діаграму подвійного сплаву олово-цинк.
8. Скласти звіт про роботу.
т
114
Компонентами називають речовини, які входять до сплаву. Отже, чистий метал є однокомпонентним. Наприклад, залізо є однокомпонентним, а сталь двокомпонентною. Для двокомпонентної системи зміна рівноваги стану відбувається при зміні не тільки зовнішніх факторів (тиску, температури), але і від внутрішніх, поскільки з введенням в метал другого компоненту утворюється нова термодинамічна змінна – концентрація. За звичай в металах і сплавах всі перетворення відбуваються при постійному (атмосферному) тиску, тому в законі Гібса n=1.
Якщо С=0 (система нонваріантна), то зміна хоча б одного фактору приведе до порушення рівноваги системи і викличе зміну фазового стану. Наприклад, для чистого металу С=0 тільки при температурі кристалізації, тобто наявність рідкої і твердої фаз можлива лише при постійній температурі.
При температурах вище або нижче температури плавлення система буде моноваріантною(С=1), тобто існує одна степінь вільності. При цьому фазовий склад залишається постійним при зміні (в деяких межах) одного із змінних факторів (температури).
При побудові кривих охолодження це дає змогу перевірити правильність експериментальних даних. Крім того, можна користуючись правилом фаз побудувати криву охолодження будь-якого сплаву.
Д
127
