
- •Реферат
- •Тема: «Химические свойства оксидов»
- •Содержание
- •Введение
- •1. Оксиды
- •1.1. Определение
- •1.2. Классификация оксидов
- •1.3. Закономерности и изменения свойств оксидов
- •2. Химические свойства оксидов
- •2.1. Основные оксиды
- •2.2. Кислотные оксиды
- •2.3. Амфотерные оксиды
- •2.4. Общие химические свойства оксидов
- •Заключение
- •Список литературы
- •Приложение
1.3. Закономерности и изменения свойств оксидов
Увеличение степени окисления элемента и уменьшение радиуса его иона (при этом происходит уменьшение эффективного отрицательного заряда на этоме кислорода) делают оксид более кислотным. Это и объясняет закономерное изменение свойств оксидов от основных к амфотерным и далее к кислотным.
1) В одном периоде при увеличении порядкового номера происходит усиление кислотных свойств оксидов и увеличение силы соответствующих им кислот.


2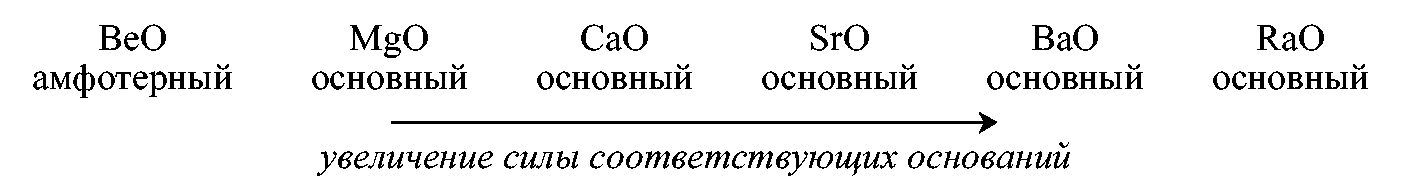 )
В главных подгруппах периодической
системы при переходе от одного элемента
к другому сверху вниз наблюдается
усиление новых свойств оксидов:
)
В главных подгруппах периодической
системы при переходе от одного элемента
к другому сверху вниз наблюдается
усиление новых свойств оксидов:
3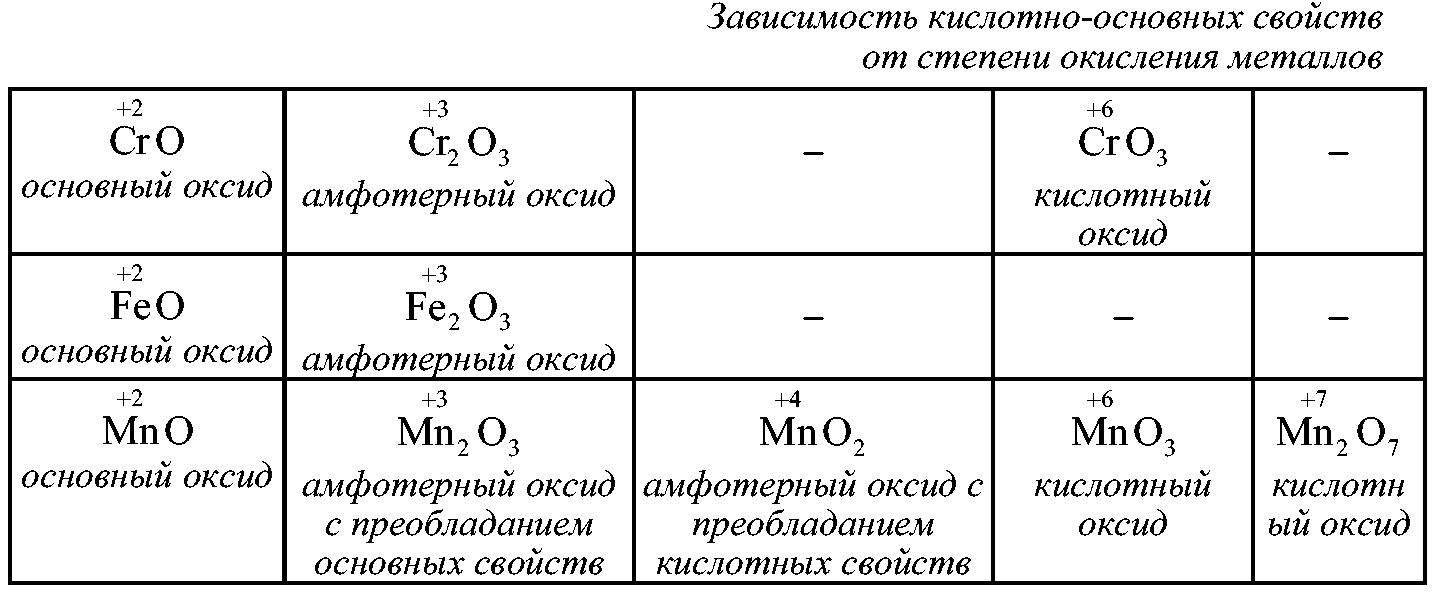 )
При повышении степени окисления элемента
усиливаются кислотные свойства оксида
и ослабевают основные
)
При повышении степени окисления элемента
усиливаются кислотные свойства оксида
и ослабевают основные
2. Химические свойства оксидов
2.1. Основные оксиды
К основным оксидам относятся:
- оксиды всех металлов главной подгруппы первой группы (щелочные металлы Li - Fr)
- главной подгруппы второй группы, начиная с магния (Mg - Ra)
- оксиды переходных металлов в низших степенях окисления, например, MnO, FeO.
Большинство основных оксидов представляет собой твердые кристаллические вещества ионного характера, в узлах кристаллической решетки расположены ионы металлов, достаточно прочно связанные с оксид-ионами О2-, поэтому оксиды типичных металлов обладают высокими температурами плавления и кипения.
Отметим одну характерную для оксидов особенность. Близость ионных радиусов многих ионов металлов приводит к тому, что в кристаллической решетке оксидов часть ионов одного металла может быть заменена на ионы другого металла. Это приводит к тому, что для оксидов часто не выполняется закон постоянства состава и могут существовать смешанные оксиды переменного состава.
Большинство основных оксидов не распадается при нагревании, исключение составляют оксиды ртути и благородных металлов:
to
2HgO = 2Hg + O2
to
2Ag2O = 4Ag + O2
Основные оксиды при нагревании могут вступать в реакции кислотными и амфотерными оксидами, с кислотами:
ВаО + SiO2 = ВаSiO3,
МgО + Аl2О3 = Мg(AlO2)2,
ZnО + Н2SО4 = ZnSО4 + Н2О.
Оксиды щелочных и щелочноземельных металлов непосредственно реагируют с водой:
Как и другие типы оксидов, основные оксиды могут вступать в окислительно-восстановительные реакции:
to
Fe2O3+2Al = Al 2O3 + 2Fe
to
3CuO+2NH3 = 3Cu + N2+3H2O
to
4FeO+O2 = 2Fe2 + O3
Основные оксиды наиболее активных металлов (щелочных и щелочноземельных, начиная с оксида кальция) при взаимодействии с водой (реакция гидратации) образуют соответствующие им гидроксиды (основания). Например, при растворении оксида кальция (негашёной извести) в воде образуется гидроксид кальция – сильное основание:
СаO + H2O → Са(OH)2
Основные оксиды взаимодействуют с кислотами, образуя соответствующие соли:
CaO + 2HCl → CaCl2 + H2O
К образованию солей также приводит реакция основных оксидов с кислотными оксидами:
Na2O + CO2 → Na2CO3
И с амфотерными оксидами:
Li2O+Al2O3 → 2LiAlO2
