
- •Затверджую
- •З дисципліни “ Хімія ”
- •Хімія та методи дослідження сировини та матеріалів
- •Тема 13. Галогени. Елементи VI- ііі груп періодичної системи
- •1. Загальна характеристика галогенів
- •2. Знаходження галогенів у природі
- •3. Властивості галогенів
- •4. Добування галогенів
- •5. Найважливіші сполуки галогенів та їх застосування
- •Питання для самоконтролю
- •1. Загальна характеристика р-елементів VI групи
- •2. Важливіші р-елементи: оксиген, сульфур
- •Сульфур – 2-й елемент VI групи
- •4. Важливіші сполуки р-елементів VI групи та їх застосування
- •5. Оксигеновмісні сполуки сульфуру, h2so4
- •Питання для самоконтролю
- •Елементи V групи періодичної системи д.І.Менделєєва
- •1. Загальна характеристика р-елементів V групи
- •2. Нітроген. Аміак
- •Застосування nh3
- •3. Нітратна кислота. Азотні добрива
- •Отримання hno3
- •4. Фосфор. Ортофосфатна кислота
- •Застосування h3po4
- •5. Важливі сполуки р-елементів та їх застосування
- •Питання для самоконтролю
- •1. Загальна характеристика р-елементів IV групи
- •2. Карбон, властивості карбону, оксидикарбону.
- •3. Силіцій. Силікатна кислота та її солі
- •4. Найважливіші сполуки р-елементів IV групи та їх застосування
- •Питання для самоконтролю
- •1. Загальна характеристика р-елементів ііі групи
- •2. Бор. Отримання та властивості бору і його сполук
- •3. Отримання та властивості а1 і його сполук
- •5. Важливіші сполуки р-елементів та їх застосування
- •Методи усунення твердості води
- •4. Найважливіші сполуки s-елементів іі групи та їх застосування
- •Питання для самоконтролю
- •1. Загальна характеристика s-елементів і групи
- •2. Гідроген. Вода. Отримання, властивості, застосування
- •3. Лужні метали: добування, властивості, застосування.
- •4. Найважливіші сполуки лужних металів та їх застосування
- •Питання для самоконтролю
- •Тема 14. Елементи IV- vі груп періодичної системи. Елементи VIII групи. Родина феруму План
- •1. Загальна характеристика d –елементів
- •Відношення металів до агресивних середовищ
- •9. Найважливіші сполуки d-елементів та їх застосування
- •Питання для самоконтролю
- •Елементи VIII групи. Родина феруму
- •1. Загальна характеристика елементів VIII групи
- •2. Розповсюдження у природі елементів родини феруму
- •3. Добування, властивості, застосування Fe, Co, Ni
- •4. Виготовлення чавуну та сталі
- •5. Важливіші сполуки елементів родини феруму та їх використання
- •Питання для самоконтролю
- •Cписок рекомендованої літератури Основна
- •Тема 15. Хімія конструкційних та ядерно-паливних матеріалів в енергетиці
- •Хімічні властивості урану та його сполук
- •Валентні стани урану
- •Найважливіші хімічні сполуки урану
- •Комплексоутворення і гідроліз
- •Контрольні питання
- •Ядерне паливо
- •1.2. Основні типи кристалічних решіток металів
- •Контрольні питання
1.2. Основні типи кристалічних решіток металів
Метали мають відносно складні типи кубічних решіток – об”ємно-центрована (ОЦК) і гранецент-рована (ГЦК) кубічна решітки. Основу ОЦК-решітки складає елементарна кубічна комірка (рис. 1.2, б), в якій позитивно заряджені іони металу знаходяться в вершинах кубу, і ще один атом в центрі його об”єму, тобто на перетині його діагоналей. Такий тип решітки в певних діапазонах температур мають залізо, хром, ванадій, вольфрам, молібден і інші метали. У ГЦК-решітки (рис. 1.2, в) елемен-тарною коміркою служить куб з центрованими гранями. Подібну решітку мають залізо, алюміній, мідь, нікель, свинець і ін. метали. Третім розповсюдженим різновидом щільноупакованих решіток є гексагональна щільноупакована (ГЩУ, рис. 1.2, г). ГЩУ-комірка складається з паралельних центри-рованих гексагональних основ, які відстоять одна від одної на параметр с. Три іона (атома) знаходя-ться на середній площині між основами. У гексагональних решіток відношення параметра с/а завжди більше одиниці. Таку решітку мають магній, цинк, кадмій, берилій, титан і ін.
Компактність кристалічної решітки або ступінь заповненості її об”єму атомами є важливою характеристикою. Вона визначається такими показниками, як параметр решітки, кількість атомів в кожній елементарній комірці, координаційне число і щільність упаковки.
Параметр решітки – це відстань між атомами по ребру елементарної комірки. Параметри кубічних решіток характеризуються довжиною ребра кубу (в нм) і позначаються літерою а. Для характеристи-ки гексагональної решітки приймають два параметри – сторону шостигранника а і висоту призми с.
Коли відношення с/а = 1,633, атоми упаковані найбільш щільно, - решітка називається гексагональ-
ною щільноупакованою (рис. 1.2, г). Метали з менш щільною упаковкою: с/а = 1,86 для цинку і 1,88
д
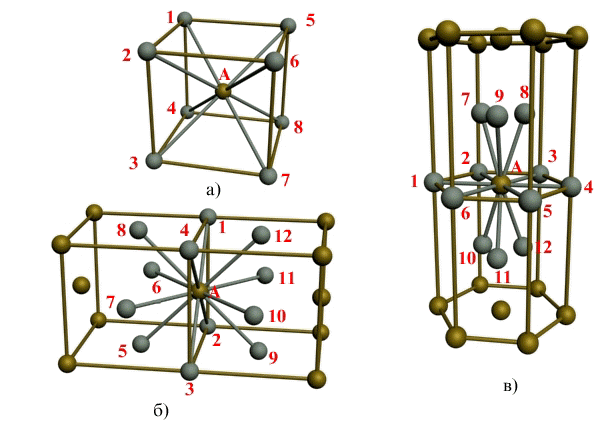
аналізу.
Рис. 1.3. Координаційне
число в різних
кристалічних
решітках для
атому А:
а) – об”ємноцентрована
кубічна
(К8); б) - гранецентрована кубічна
(К12); в) - гексагональна щільноупакована
(Г12)
Під координаційним числом треба розуміти кількість найближчих сусідів даного атому.
Для ГПУ-решітки координаційне число дорівнює 12 (Г12).
Щільність упаковки представляє собою відношення сумарного об”єму, що займають атоми в кристалічній решітці, до її повного об”єму. Різні типи кристалічних решіток мають різну щільність упаковки атомів. В ГЦК-решітці атоми займають 74% всього об”єму решітки, а міжатомні проміжки (пори) 26%. В ОЦК-решітці атоми займають 68% всього об”єму, а пори – 32%. Компактність решітки залежить від особливостей електронної структури металів і характеру зв”язку між атомами. Від типу кристалічної решітки сильно залежать властивості металу.
Упорядкованість кристалічної будови в просторовій решітці дозволяє виділити окремі кристало-графічні напрями і площини. Кристалографічні напрями – це характерні прямі лінії, що визодять із точки відліку, вздовж яких в кристалічній решітці розташовуються атоми. Точками відліку можуть слугувати вершини кубу, а кристалографічними напрямами – його ребра і діагоналі, а також діа-гоналі граней.
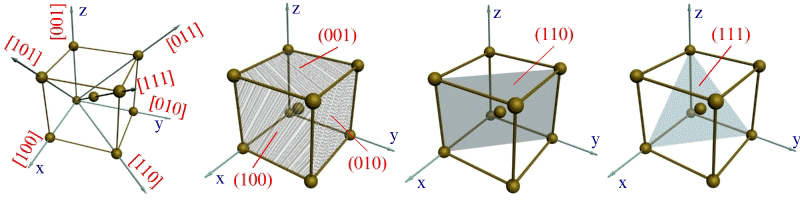
Рис. 1.4. Кристалографічні напрями і площини в кристалічній решітці: а) - основні напрями і
їх позначення; б), в), г) - основні площини і їх позначення
Під анізотропією треба розуміти неоднаковість механічних і інших властивостей в кристалічних тілах вздовж різних кристалографічних напрямах. Вона є природнім слідством кристалічної будови, бо на різних кристалографічних площинах і вздовж різних напрямів щільність атомів різна. Оскільки механічні, фізичні і хімічні властивості вздовж різних напрямів залежать від щільності розташованих на них атомів, то перераховані властивості вздовж різних напрямів в кристалічних тілах повинні бу-ти неоднаковими.
Анізотропія виявляється тільки в межах одного монокристалу або зерна-кристаліта. В полікриста-лічних тілах вона не спостерігається завдяки усередненню властивостей по кожному напряму для великої кількості зерен, що вільно орієнтовані одне відносно другого. Тому реальні метали є квазі-ізотропними, тобто псевдоізотропними.
|
|
|
Деякі метали, наприклад залізо, титан, олово і ін. здатні по досягненні певних температур змінювати кристалічну будову, тобто змінювати тип елементарної комірки своєї кристалічної ре-шітки. Це явище називається алотропією, або поліморфізмом, а самі переходи від одної кристаліч-ної будови до іншої – алотропні або поліморфні. Відоме на практиці немагнітне бета-залізо самостій-ною алотропічною формою не є, бо має таку ж як у альфа-заліза ОЦК-решітку і відрізняється від нього тільки відсутністю магнітних властивостей, які воно втрачає при 768°С (точка Кюрі).
В решітці реального металу можуть знаходитись різні дефекти. Вони бувають точкові, лінійні, по-верхневі і об”ємні. Точкові дефекти співрозмірні з розмірами атомів. До них відносяться вакансії, тобто незаповнені вузли решітки, міжвузлові атоми даного металу, домішкові атоми заміщення, тобто атоми, які за диаметром співрозмірні з атомами даного металу і т.д. Вплив цих дефектів на міцність металу може бути різним в залежності від їх кількості в одиниці об”єму і характеру.
Лінійні дефекти мають довжину, що значно перевищує їх поперечні розміри. До них відносяться дислокації, тобто дефекти, які утворюються в решітці в результаті зміщення кристалографічних площин. Дислокації бувають двох видів. Найбільш характерна крайова дислокація. Вона утворюється в результаті виникнення в решітці так званої напівплощини або екстраплощини (див. мал.).
Схема крайової дислокації
в ідеальному кристалі.
Другий тип дислокації – гвинтова
дислокація, яка представляє собою
умовну вісь в кристалі, навкруги якої
закручені атомні площини.
Висока рухомість дислокацій обумовлює
суттєве зменшення міцно-сті металу, бо
полугшує утворення зміщень в
зернах-кристалітах під дією напружень,
які додаються.
Дислокаційний механізм здвигової
пластичної деформації в кристалі може
призвести до руйнування виробу. Таким
чином, дислокації безпо-середньо
впливають на міцностні характеристики
металу.
Максимальна щільність
дислокацій може складати 1013
см-2.
При по-дальшому зростанні щільності
дислокацій метал руйнується.

Схема гвинтової
дислокації
Поверхневі дефекти включають в себе головним чином границі зерен (див. рис. нижче). На грани-
цях кристалічна решітка сильно деформована. В них накопичуються дислокації, які переміщуються зсередини зерен.

З практики відомо, що мілкозернистий метал міцніше крупнозернистого. Тому що у останнього менше сумарна довжина (міцність) границь, то можна зробити висновок, що поверхневі дефекти сприяють підвищенню міцності металу. Тому було створено декілька технологічних способів отримання мілкозернистих сплавів.
Об”ємні дефекти кристалічної решітки (тріщини, пори) зменшують
міцність металу.
Структура границі двох
сусідніх кристалічних
зерен
