- •Лекция № 1 предмет органической химии
- •Теории химического строения
- •Основные положения теории бутлерова:
- •1. Положение о химическом строении.
- •2. Положение о зависимости свойств от химического строения.
- •3. Положение о взаимном влиянии атомов.
- •Классификация органических соединений
- •Электронные представления о природе химической связи
- •Электронная структура Схема основного электронного состояния
- •Образование ковалентной связи
- •Гибридизация электронов углерода. - и - связи.
- •Основные характеристики ковалентных связей
- •1. Полярность
- •2. Поляризуемость
- •3. Направленность связей
- •4. Длина связи
- •5. Энергия связи
- •6. Классификация органических реакций по механизму
- •Лекция № 2
- •Алифатические соединения (жирные, ациклические)
- •Способы получения предельных углеводородов
- •Лабораторные способы получения алканов
- •Пространственное строение предельных углеводородов
- •Физические свойства предельных углеводородов
- •Химические свойства предельных углеводородов
- •Получение и свойства алифатических радикалов
- •I тип. Реакция замещения
- •II тип. Реакции окисления
- •III тип. Реакции термического расщепления предельных углеводородов
- •IV тип. Изомеризация предельных углеводородов
- •Лекция 3 этиленовые углеводороды
- •Номенклатура
- •Способы получения
- •Физические свойства олефинов
- •Химические свойства олефинов
- •1. Реакции присоединения
- •Эффект Караша
- •Свойства карбкатионов
- •2. Реакции окисления
- •3. Реакции полимеризации
- •4. Реакции аллильного замещения
- •Отдельные представители
- •Лекция 4 диеновые углеводороды
- •Способы получения
- •Особенности электронного строения диенов с сопряженными связями
- •Физические свойства
- •Химические свойства
- •1. Реакции присоединения
- •2. Реакции окисления
- •3. Реакции полимеризации
- •Натуральный и синтетический каучук
- •Лекция 5 ацетиленовые углеводороды
- •Лабораторные методы получения ацетиленовых углеводородов
- •II. Реакции окисления
- •III. Реакции полимеризации и конденсации
- •Реакции замещения водорода металлом – образование ацетиленидов
- •Изомерия
- •Номенклатура
- •Способы получения
- •Электронное строение
- •Физические свойства
- •Химические свойства
- •I.Реакции нуклеофильного замещения
- •Реакции отщепления галогена
- •III. Реакции отщепления галогеноводорода
- •Лекция 7 галогенопроизводные непредельных углеводородов
- •I. Галогенопроизводные винильного типа. Получение
- •Особенности свойств
- •II. Соединения аллильного типа Получение
- •Получение
- •Отличие в физических и химических свойствах фторуглеводородов
- •Лекция 8 спирты (оксисоединения)
- •Свойства
- •Отдельные представители
- •Многоатомные спирты
- •Способы получения (кроме общих)
- •Физические свойства
- •Химические свойства
- •Рациональная система названий
- •Номенклатура iupac
- •Гомологический ряд предельных монокетонов
- •Способы получения
- •Электронное и пространственное строение карбонильных соединений
- •Физические свойства
- •Химические свойства
- •Лекция 10
- •III. Реакции окисления и восстановления
- •Реакции восстановления
- •Классификация
- •Предельные одноосновные кислоты. Гомологический ряд
- •Изомерия
- •Номенклатура
- •Способы получения
- •1. Окисление углеводородов
- •3. Электронное строение
- •4. Физические свойства предельных одноосновных карбоновых кислот
- •5. Химические свойства карбоновых кислот
- •1) Кислотные свойства
- •4) Дегидратация кислот
- •5) Декарбоксилирование – отщепление со2.
- •Лекция 12 предельные двухосновные кислоты
- •Отличие в свойствах
- •Непредельные кислоты
- •Отличия в свойствах
- •Основные особенности геометрической изомерии
- •Номенклатура
- •Получение
- •Электронное строение нитросоединений
- •Физические свойства
- •Химические свойства
- •1.Определение и классификация
- •2. Изомерия, номенклатура
- •Номенклатура
- •Физические свойства
- •Химические свойства
- •Способы получения
- •Физические свойства
- •Химические свойства
- •Лекция 16 оптическая изомерия Оптическая активность
- •Динамическая стереохимия
- •Стереохимия нуклеофильного замещения
- •Стереохимия электрофильного присоединения
- •Стереохимия отщепления
Химические свойства предельных углеводородов
Предельные углеводороды имеют в составе
молекул только малополярные и
слабополяризующиеся
![]() -связи,
которые отличаются высокой прочностью,
поэтому в обычных условиях они являются
веществами мало химически активными
по отношению к полярным реагентам: не
взаимодействуют с концентрированными
кислотами, целочами, щелочными металлами,
окислителями. Это и послужило поводом
к их названию – парафины. Parumaffinus
по латыни малосродственный. Их химические
превращения протекают в основном при
повышенных температурах и под действием
УФ-облучения.
-связи,
которые отличаются высокой прочностью,
поэтому в обычных условиях они являются
веществами мало химически активными
по отношению к полярным реагентам: не
взаимодействуют с концентрированными
кислотами, целочами, щелочными металлами,
окислителями. Это и послужило поводом
к их названию – парафины. Parumaffinus
по латыни малосродственный. Их химические
превращения протекают в основном при
повышенных температурах и под действием
УФ-облучения.
Различают три основных типа реакций предельных углеводородов: замещение, окисление и отщепление. Эти реакции могут идти либо за счет разрыва связи С-С (энергия 83,6 ккал), либо за счет разрыва связи С-Н (энергия 98,8 ккал/моль). Реакции чаще идут с разрывом связи С-Н, т.к. она более доступна действию реагента, хотя связь С-С требует меньше энергии на расщепление. В результате таких реакций промежуточно образуются очень активные частицы – алифатические углеводородные радикалы.
Получение и свойства алифатических радикалов
1. Образование свободных радикалов при гомолитическом расщеплении связей С-С или С-Н происходит при температуре 300-700оС или под действием свободно-радикальных реагентов.
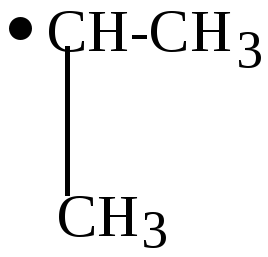
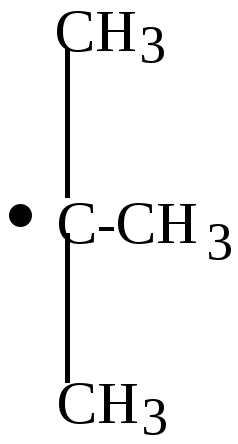
2. Продолжительность существования свободных радикалов (устойчивость) увеличивается от первичных радикалов к вторичным и третичным:
|
. СН3 |
< |
|
< |
|
3. Химические превращения свободных радикалов.
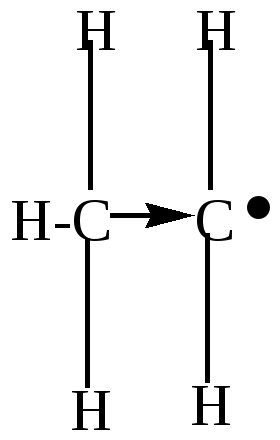
а) Взаимодействие с предельными соединениями – радикал отрывает Н и образуется новый радикал:
|
Cl . + |
|
|
|
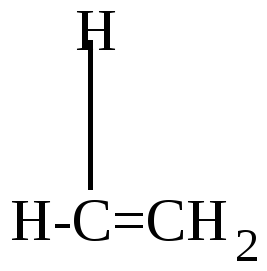
б) Взаимодействие с непредельными соединениями: происходит присоединение с образованием также нового радикала:
CH3.
+ CH2=СН2
![]() CH3-CH2-CH2.
CH3-CH2-CH2.
в) ![]() -распад
– радикалы с длинной углеродной цепью
распадаются с разрывом С-С связи в
-распад
– радикалы с длинной углеродной цепью
распадаются с разрывом С-С связи в
![]() -положении
к углероду с неспаренным электроном.
-положении
к углероду с неспаренным электроном.
CH3-
CH2 :
CH2-
CH2 .
![]() CH3-CH2.
+ CH2=CH2
CH3-CH2.
+ CH2=CH2
г) Диспропорционирование –
перераспределение водорода, связанное
с
![]() -распадом
по С-Н связи:
-распадом
по С-Н связи:
|
|
+ СН3-СН2.
|
|
+ СН3-СН3 |
д) Рекомбинация – соединение свободных радикалов друг с другом
СН3. + СН3.
![]() СН3-СН3
СН3-СН3
Зная особенности поведения свободных радикалов, легче уяснить основные закономерности конкретных реакций предельных углеводородов.
I тип. Реакция замещения
1. Реакции галоидирования. Самый энергичный реагент – фтор. Прямое фторирование приводит к взрыву. Наибольшее практическое значение имеют реакции хлорирования. Они могут протекать под действием молекул хлора на свету уже при комнатной температуре. Реакция протекает по свободно-радикальному цепному механизму и включает следующие основные стадии:
а) первая медленная стадия – инициирование цепи:
Cl : Cl
![]() Cl. +
Cl.
Cl. +
Cl.
R : H + . Cl
![]() HCl + R.
HCl + R.
б) развитие цепи – образование продуктов реакции с одновременным образованием свободных радикалов, продолжающих цепной процесс:
R.
+ Cl : Cl
![]() RCl + Cl.
RCl + Cl.
R : H + Cl.
![]() HCl + R.
HCl + R.
в) обрыв цепи:
R.
+ Cl.
![]() RCl
RCl
Так как СI. реагент активный, он может атаковать молекулу уже полученного хлорпроизводного, в результате образуется смесь моно- и полигалогенозамещенных. Например:
CH4
+ Cl2
![]() HCl + CH3Cl
HCl + CH3Cl
![]() CH2Cl2
CH2Cl2
![]() CHCl3
CHCl3
![]() ССl4
ССl4![]()
хлористый метил –HCl -HCl -HCl
хлористый метилен хлороформ четырех-
хлористый углерод
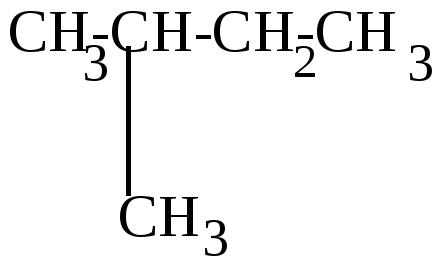
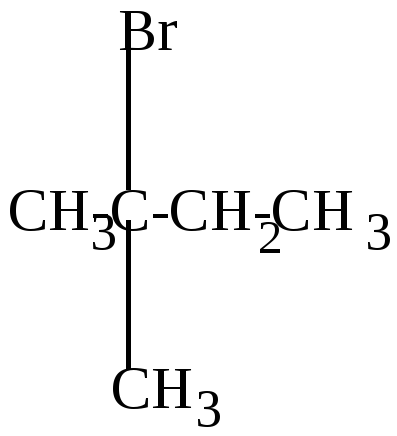
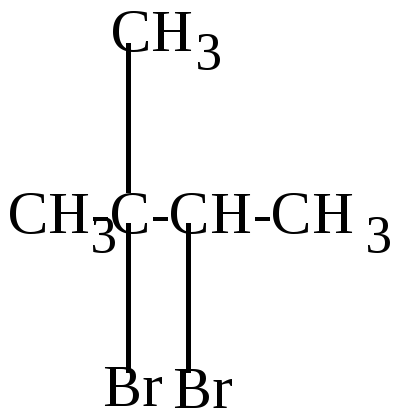
Реакция бромирования протекает значительно труднее, т.к. бром менее активен, чем хлор и реагирует в основном с образованием более устойчивых третичных или вторичных радикалов. При этом второй атом брома вступает обычно в соседнее с первым положение, преимущественно у вторичного углерода.
|
|
+ Br2
|
|
|
|
|
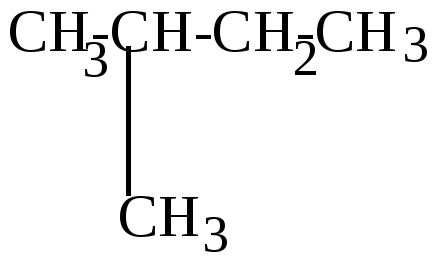
изопентан |
|
бромистый изопентан (2-бром-2-метилбутан) |
|
2,3-дибром-2-метилбутан |
Реакции иодирования практически не протекают, т.к. HI восстанавливает образующиеся йодистые алкилы.
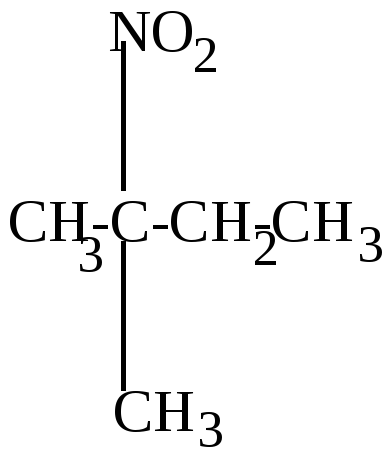
2. Нитрование – замещение атома Н на группу NО2 при действии азотной кислоты. Идет при действии разбавленной азотной кислоты (12%) при высокой температуре 150оС под давлением (реакция Коновалова). Легче реагируют парафины изостроения, т.к. замещение легче происходит у третичного атома углерода:
|
|
+ HONO2
|
|
|
изопентан |
|
2-нитро-2-метилбутан |
Механизм реакции нитрования связан с промежуточным образованием свободных радикалов. Инициированию способствует протекающий частично процесс окисления:
RH + HONO2
![]() ROH + HONO
ROH + HONO
азотистая кислота
HONO + HONO2
![]() HOH + 2 .
NO2
HOH + 2 .
NO2
|
|
+
. NO2
|
|
|
H .
CH3-C-CH3
+ . NO2
![]() CH3-C-CH3
+ HNO2
CH3-C-CH3
+ HNO2
CH3 CH3
. NO2
CH3-C-CH3
+ . NO2
![]() CH3-C-CH3
CH3-C-CH3
CH3 CH3
т.е. радикальная реакция нитрования углеводородов не имеет цепного характера.