
- •Лабораторний практикум
- •Івано-Франківськ
- •1 Загальні положення
- •2 Основні правила техніки безпеки
- •3 Звіт з роботи
- •4 Рекомендована література
- •Лабораторна робота №1 Абсорбція аміаку водою
- •Мета і задачі роботи
- •Теоретичні основи
- •1.2.1 Призначення і суть процесу
- •1.2.2 Параметри, які впливають на абсорбцію
- •Опис лабораторної установки
- •Порядок виконання роботи
- •1.5 Обробка результатів досліду
- •1.6 Контрольні питання
- •Лабораторна робота №2 Адсорбційна очистка олив
- •2.1 Мета і задачі роботи
- •2.2 Теоретичні основи
- •2.2.1 Призначення і суть процесу
- •2.2.2 Параметри, які впливають на адсорбцію
- •2.3 Опис лабораторної установки
- •2.4 Порядок виконання роботи
- •2.5 Обробка результатів досліду
- •2.6 Контрольні питання
- •Лабораторна робота №3 Ректифікація бінарної суміші
- •3.1 Мета і задачі роботи
- •3.2 Теоретичні основи
- •3.2.1 Призначення і суть процесу ректифікації
- •3.2.2 Параметри, які впливають на ректифікацію
- •3.3 Опис лабораторної установки
- •3.4 Порядок виконання роботи
- •3.5 Обробка результатів досліду
- •3.6 Контрольні питання
- •Лабораторна робота №4 Екстракція бензолу етиленгліколем
- •4.1 Мета і задачі роботи
- •4.2 Теоретичні основи
- •4.2.1 Призначення і суть процесу
- •4.2.2 Методи екстракції
- •4.2.3 Параметри, які впливають на процес
- •4.3 Опис лабораторної установки
- •4.4 Порядок виконання роботи
- •4.5 Обробка результатів досліду
- •4.6 Контрольні питання
- •Лабораторна робота №5 Каталітичний крекінг
- •5.1 Мета і задачі роботи
- •5.2 Теоретичні основи
- •5.2.1 Призначення, суть і механізм процесу
- •5.2.2 Сировина і одержувані продукти
- •5.2.3 Каталізатор
- •5.2.4 Параметри, що впливають на процес
- •5.2.4.1 Якість сировини
- •5.2.4.2 Температура в реакторі
- •5.2.4.3 Час контакту сировини і каталізатора
- •5.2.4.4 Кратність циркуляції каталізатора
- •5.2.4.5 Тиск в реакторі
- •5.3 Опис лабораторної установки
- •5.4 Порядок виконання роботи
- •5.5 Обробка результатів
- •5.6 Контрольні питання
- •Лабораторна робота №6 Підготовка сировини до каталітичного реформінгу
- •6. 1 Мета і задачі роботи
- •6.2 Теоретичні основи
- •6.2.1 Призначення, суть і хімізм процесу
- •6.2.2 Сировина і одержувані продукти
- •6.2.3 Каталізатори
- •6.2.4 Параметри, що впливають на процеси
- •6.2.4.1 Якість сировини
- •6.2.4.2 Температура на вході в реактори
- •6.2.4.3 Об’ємна швидкість подачі сировини
- •6.2.4.4 Тиск в реакторах
- •6.2.4.5 Кратність циркуляції водневмісного газу
- •6.2.4.6 Перепад температури по висоті реактора
- •6.2.4.7 Перепад тиску на каталізаторі
- •6.2.4.8 Температура стінок реактора
- •6.3 Опис лабораторної установки
- •6.4 Порядок виконання роботи
- •6.5 Обробка результатів досліду
- •6.6 Контрольні питання
- •Лабораторна робота №7 Карбамідна депарафінізація дизельного палива
- •7.1 Мета і задачі роботи
- •7.2 Теоретичні основи
- •7.2.1 Призначення і суть процесу
- •7.2.2 Сировина і одержувані продукти
- •7.2.3 Параметри, що впливають на процес
- •7.2.3.1 Якість сировини
- •7.2.3.2 Склад і концентрація карбаміду
- •7.2.3.3 Співвідношення карбамід-сировина
- •7.2.3.4 Температура
- •7.2.3.5 Склад і кількість активатора та розчинника
- •7.2.3.6 Час контакту сировини з карбамідом
- •7.3 Опис лабораторної установки
- •7.4 Порядок виконання роботи
- •7.5 Обробка результатів досліду
- •7.6 Контрольні питання
ІВАНО-ФРАНКІВСЬКИЙ
НАЦІОНАЛЬНИЙ
ТЕХНІЧНИЙ
УНІВЕРСИТЕТ НАФТИ І ГАЗУ
Кафедра
нафтогазового технологічного
транспорту і
теплотехніки
Гаєва Л.І.,
Дем’янчук Я.М.
ТИПОВІ
ТЕХНОЛОГІЧНІ ПРОЦЕСИ
І
ОБ’ЄКТИ ВИРОБНИЦТВ
ЛАБОРАТОРНИЙ
ПРАКТИКУМ
Для студентів
спеціальності „Автоматизація
технологічних процесів”
2003
МІНІСТЕРСТВО
ОСВІТИ І НАУКИ УКРАЇНИ
Івано-Франківський
національний технічний
університет
нафти і газу
Кафедра
нафтогазового технологічного
транспорту і
теплотехніки
Гаєва Л.І.,
Дем’янчук Я.М.
ТИПОВІ
ТЕХНОЛОГІЧНІ ПРОЦЕСИ
І
ОБ’ЄКТИ ВИРОБНИЦТВ
Для студентів
спеціальності „Автоматизація
технологічних процесів”
МВ 02070855-1020 -2003
2003
Гаєва
Л.І., Дем’янчук Я.М. Типові технологічні
процеси і об’єкти виробництв. Лабораторний
практикум. – Івано-Франківськ, Факел,
2003
. –
60с.
Лабораторний
практикум складений згідно з робочою
програмою курсу “Типові технологічні
процеси і об’єкти виробництв” для
студентів спеціальності 7.092501
”Автоматизація технологічних процесів”,
яка розроблена на основі навчального
плану, затвердженого Вченою Радою
університету 03 липня 2002 р. і призначений
для самостійної роботи при підготовці
до лабораторних робіт з вказаної
дисципліни студентами денної та заочної
форм навчання.
В
практикумі наведено 7 лабораторних
робіт з наступних розділів: абсорбція,
адсорбція, ректифікація, екстракція,
каталітичний крекінг, каталітичний
реформінг, карбамідна депарафінізація.
Наведені
загальні положення проведення
лабораторних робіт і основні правила
техніки безпеки, мета і зміст роботи,
теоретичні основи кожного із процесів,
порядок виконання роботи, обробка
результатів та складання звіту.
Рецензент:
Негрич
В.В. – канд. хім. наук, доцент кафедри
НГТТ і Т ІФНТУНГ
Дане
видання – власність ІФНТУНГ. Забороняється
тиражувати та розповсюджувати.
Зміст
1 Організація
проведення лабораторних робіт………………4
2 Основні правила
техніки безпеки…………………………..4
3 Звіт з
роботи……………………………………….………...
5
4 Рекомендована
література…………………………………. 6
Лабораторна
робота № 1
Абсорбція аміаку
водою…………………………...………… 7
Лабораторна робота
№ 2
Адсорбційна
очистка олив………………………………...…13
Лабораторна робота
№ 3
Ректифікація
бінарної суміші……………..…………………19
Лабораторна
робота № 4
Екстракція бензолу
етиленгліколем……………….………..29
Лабораторна
робота № 5 Каталітичний
крекінг……….………………………………..36
Лабораторна
робота № 6
Підготовка сировини
до каталітичного реформінгу……….45
Лабораторна
робота № 7
Карбамідна
депарафінізація дизельного палива……………54
Організація
проведення лабораторних робіт
Студент
допускається до виконання лабораторних
робіт тільки після інструктажу з техніки
безпечної роботи в лабораторії технології
переробки нафти і експлуатаційних
матеріалів.
Лабораторні роботи
виконуються за циклами. Перелік і
послідовність виконання робіт вказуються
викладачем на вступному занятті. Кожній
лабораторній роботі передує домашня
підготовка студента. В підготовку
входить:
- знання теоретичного
матеріалу з даної лабораторної роботи;
-
знання загального опису лабораторної
установки і призначення її окремих
елементів;
-
знання порядку виконання роботи і
методики обробки одержаних результатів;
- наявність
правильно підготовленого протоколу
роботи;
-
наявність повністю оформленого звіту
з попередньої лабораторної роботи.
Контроль
підготовленості студента з теоретичного
матеріалу здійснюється за допомогою
спеціальних тестів (карток), які містять
контрольні питання з даної роботи.
Допущений
до заняття студент отримує у викладача
індивідуальне завдання на виконання
роботи. Ознайомившись з лабораторною
установкою і розміщенням її основних
елементів, вказаних на принциповій
схемі, студент повідомляє викладачеві
послідовність виконання роботи, після
чого за його вказівкою приступає до
експерименту.
Дослідні
дані заносяться в таблицю і повинні
бути підписані викладачем на занятті.
Результати обробки дослідних даних
теж повинні бути представлені викладачеві
на занятті.
Після
закінчення роботи установку необхідно
вимкнути і привести в порядок робоче
місце, здати лаборанту прилади і
інструменти.
Непідготовлений
студент до заняття не допускається і
повинен виконати роботу в додатково
призначений час.
Усі
роботи в лабораторії виконуються тільки
під керівництвом викладача або лаборанта.
Не можна
загромаджувати робоче місце сторонніми
предметами, які не мають відношення до
роботи.
Не можна ходити
без потреби по лабораторії, рухати
прилади, реактиви, вузли установки та
інші предмети, які не відносяться до
даної лабораторної роботи.
Необхідно
користуватися тільки справними приладами
і інструментами.
Не можна
вмикати і вимикати без дозволу викладача
рубильники, прилади, лабораторні
установки та газові пальники.
Про всі
помічені неполадки потрібно негайно
повідомляти викладача.
Забороняється:
-
класти легко займисті речовини і
предмети на гарячі поверхні лабораторної
установки;
-
наливати і переливати горючі речовини,
нафтопродукти, розчинники поблизу
відкритого вогню;
- займатися ремонтом
установки без дозволу викладача;
- відволікати
студентів сторонніми розмовами;
-
виносити з лабораторії прилади,
інструмент, деталі установки, а також
вносити в лабораторію сторонні предмети.
Звіт
повинен відповідати встановленому
кафедрою зразку і бути виконаним з
врахуванням вимог стандартів ЕСКД і
СТП 02070855-03-99.
Звіт повинен бути
написаний особисто студентом, розбірливим
почерком, чорнилом (пастою) фіолетового,
синього чи чорного кольору.
Схеми
та таблиці повинні бути виконані за
допомогою креслярського приладдя.
Принципова
схема лабораторної установки і
експлікація виконуються на окремій
сторінці звіту олівцем чорного кольору.
Звіт з лабораторної
роботи повинен містити:
- номер і повну
назву лабораторної роботи;
- мету і задачі
роботи;
- принципову схему
лабораторної установки з експлікацією;
- порядок виконання
роботи;
- таблиці з
дослідними даними, результати їх
обробки;
- висновки з
лабораторної роботи.
1.Скобло А.И.,
Трегубова И.А., Молоканов Ю.К. Процессы
и аппараты нефтеперерабатывающей и
нефтехимической промышленности. – М.:
Химия,1982.-584с.
2. Смидович Е.В.
Технология переработки нефти и газа
- ч.2. – М.: Химия,1980. – 325с.
3. Черножуков Н.И.
Технология переработки нефти и газа.
– ч.3. – М.: Химия, 1978.
4. Справочник
нефтепереработчика / Под.ред.Г.А.Лас-товкина.-
Л.:Химия,1986.-648с.
5. Суханов В.П.
Каталитические процессы в нефтепереработке.
– М.: Химия, 1985. – 344с.
6. Касаткин А.Г,
Основные процессы и аппараты химической
технологии.– М.: Химия,1985. – 784с.
7. Павлов К.Ф.,
Романков П.Г., Носков А.А. Примеры и
задачи по курсу процессов и аппаратов
химической технологии. – М.:Химия,1987.
- 567с.
Мета: засвоєння
і закріплення теоретичних основ з
абсорбції; набуття експериментальних
навичок проведення процесу абсорбції
на лабораторній установці(на прикладі
розділення аміачно-повітряної суміші).
В результаті
виконання лабораторної роботи студент
повинен
знати:
-
призначення і суть процесу абсорбції;
використання процесу на підприємствах
нафтогазового комплексу; будову і
роботу різних типів абсорберів; роботу
системи абсорбер-десорбер; вплив
параметрів на процес абсорбції.
вміти:
-
вибирати необхідні параметри для
одержання продуктів необхідної якості;
проводити аналіз одержаних продуктів;
оцінювати результати проведення процесу
на лабораторній установці.
Процес абсорбції
служить для розділення суміші газів
на окремі компоненти. Він полягає в
тому, що газову суміш пропускають через
рідину – абсорбент. В якості абсорбенту
вибирається така рідина, яка поглинає
один із компонентів суміші і не поглинає
інші або поглинає частково. Як абсорбенти
використовуються наступні рідини:
вода, бензин, гас, дизельне паливо,
мінеральні оливи, гліколі та інші. При
змішуванні суміші газів з абсорбентом
компонент, який поглинається, переходить
з газової фази в рідку. Процес поглинання
газу рідиною називається абсорбцією.
Вона проводиться в апаратах – абсорберах,
які бувають тарільчатого, насадочного
і плівкового типів. По мірі проходження
газової суміші через абсорбент
концентрація компоненту, який
поглинається, в газовій фазі зменшується,
а в рідкій збільшується. Наступає момент
рівноваги. Рівновагою називається
такий стан системи, при якому кількість
компоненту, який переходить з газової
фази в рідку, рівна кількості компоненту,
який переходить зворотно з рідкої фази
в газову. Перехід поглинутого компоненту
з рідкої фази в газову називається
десорбцією. Процес абсорбції
використовується на підприємствах
нафогазового комплексу для осушення,
очищення природних і супутніх нафтових
газів від кислих сполук, розділення їх
на індивідуальні вуглеводні.
На
процес абсорбції впливають наступні
параметри: концентрація компоненту,
що поглинається, температура, тиск,
питома витрата абсорбенту, площа
контакту між газовою і рідкою фазами,
час контакту між ними.
Різниця між
концентраціями компоненту у вихідній
суміші і в газовій суміші в абсорбері
у момент рівноваги називається рушійною
силою абсорбції. Чим більша ця величина,
тим краще проходить процес абсорбції.
В процесі поглинання газу рідиною
виділяється теплота і температура в
абсорбері підвищується. З підвищенням
температури зростає хаотичний рух
молекул поглинутого компоненту і вихід
їх назад в газову фазу; тобто з підвищенням
температури процес абсорбції погіршується,
а десорбції покращується. Температура
в абсорбері регулюється кількістю
холодоагенту, який подається в
холодильник, де охолоджується абсорбент.
Чим
вищий тиск, тим краще дифузія молекул
компоненту, що поглинається, з газу в
рідину, що прискорює процес абсорбції.
Проте підвищення тиску в абсорбері
обмежується товщиною стінок апарату
і затратами на додаткове компреміювання
газу. Зниження тиску в апараті прискорює
зворотній процес виділення поглинутого
компоненту в газову фазу, тобто
прискорення процесу десорбції. Тиск в
абсорбері регулюється автоматично
клапаном, який встановлюється на лінії
виводу газової суміші з апарату.
Співвідношення
між витратою абсорбенту і витратою
газової суміші називається питомою
витратою абсорбенту. При збільшенні
її процес абсорбції прискорюється.
Проте, значне збільшення витрат
абсорбенту робить процес абсорбції не
економічним із-за зростання затрат
енергії на перекачку абсорбенту, витрати
теплоти на десорбцію поглинутого
компоненту в десорбері, витрати
холодоагенту на охолодження абсорбенту
перед абсорбцією. Питома витрата
абсорбенту регулюється кількістю
газової суміші, що подається в апарат.
Чим
більша площа контакту між газовою і
рідкою фазами, тим інтенсивніше проходить
абсорбція. Необхідна площа контакту
забезпечується при виготовленні
абсорберів. При зростанні часу контакту
між газовою і рідкою фазою повніше
проходить вилучення компоненту, але
при цьому зменшується продуктивність
абсорбера.
Схема
лабораторної установки наведена на
рис.1.1. Вона складається з балону 1, в
якому знаходиться аміачно-повітряна
суміш, вентиля 2, уловлювача крапель
абсорбенту 3, абсорбера 4, відвідної
трубки 5, колби для титрування 6, бюретки
7 з розчином соляної кислоти.
В
абсорбер 4 заливають мірним циліндром
100мл води. Повільно відкривають вентиль
2. Суміш аміаку і повітря буде проходити
через уловлювач 3, а пізніше через шар
води в абсорбері 4. При цьому аміак
поглинається водою, а повітря через
відвідну трубку 5 буде виходити в
атмосферу. Суміш пропускають через
воду на протязі 15хв, після чого вентиль
2 закривають. Аміак при проходженні
через воду вступає з нею
в
хімічну взаємодію. При цьому утворюється
розчин нашатирного спирту:
NH3+H2O=NH4OH
(1.1)
Заміряють
температуру рідини а абсорбері до і
після абсорбції і фіксують зростання
температури за час абсорбції. Титруванням,
утвореного в абсорбері нашатирного
спирту, розчином соляної кислоти
визначають його нормальність. В колбу
6 наливають 2мл утвореного розчину
нашатирного спирту з абсорбера 4 і
додають декілька крапель індикатора
– спиртового розчину фенолфталеїну.
Розчин нашатирного спирту, який має
лужне середовище забарвлюється в
рожевий колір. В бюретку 7 заливають
0,1н розчин соляної кислоти. Повільно
відкриваючи краник, на бюретці 7, краплями
добавляють розчин соляної кислоти в
колбу 6, весь час перемішуючи рідину в
колбі. В момент, коли розчин в колбі
обезбарвиться, подачу соляної кислоти
припиняють. Зміна забарвлення розчину
говорить про те, що весь нашатирний
спирт нейтралізований кислотою.
Нормальність
нашатирного спирту знаходять за
формулою:
де
Кількість
утвореного в абсорбері нашатирного
спирту визначають за формулою:
де 100 –
об’єм води в абсорбері, мл;
Дослідні
результати заносять в табл.1.1. За ними
роблять висновок про проходження
процесу абсорбції.
Таблиця
1.1 – Дослідні дані
Взято води в
абсорбері, мл Температура,
оС
Нормальність
НCl
Об’єм
НCl,
що пішов на титрування, мл
Об’єм
NH4OH,
взятого для титрування, мл
Кількість
утвореного NH4OH,г до
абсорбції після
абсорбції
1.Для чого призначений
процес абсорбції і в чому полягає його
суть? 2.Наведіть
приклади використання абсорбції на
підприємствах нафтогазового комплексу.
3.Як на процес
абсорбції впливає концентрація
компоненту у вихідній суміші?
4. Як на процес
абсорбції впливають температура і
тиск?
5. Як на процес
абсорбції впливає питома витрата
абсорбенту?
6. Як на процес
абсорбції впливають час і площа контакту
газової суміші та абсорбенту?
7. Опишіть лабораторну
установку для проведення абсорбції.
8. За
якими формулами визначають нормальність
і кількість утвореного нашатирного
спирту?
9. Який порядок
виконання роботи на лабораторній
установці?
Мета:
засвоєння і поглиблення теоретичного
матеріалу з адсорбції; набуття
експериментальних навичок проведення
процесу адсорбції на лабораторній
установці.
В результаті
виконання лабораторної роботи студент
повинен
знати:
- призначення і
суть процесу адсорбції, використання
його в нафтогазовій і нафтогазопереробній
промисловостях;
- вплив параметрів
на адсорбцію газів і рідин;
- роботу
системи адсорбер-десорбер періодичної
і безперервної дії;
вміти:
- правильно вибирати
параметри для одержання продуктів
необхідної якості та в заданій кількості;
- оцінювати
результати проведення процесу на
лабораторній установці;
-
виконувати розрахунки стадій адсорбції,
десорбції та регенерації адсорбенту.
Процес
адсорбції служить для розділення суміші
рідин або газів на окремі компоненти.
Прикладом використання процесу адсорбції
є: покращення кольору і зниження
коксує-мості олив шляхом вилучення з
них смол і поліциклічних ароматичних
вуглеводнів; підвищення октанового
числа бензинів шляхом вилучення з них
н-парафінових вуглеводнів; зниження
температури застигання дизельних палив
шляхом вилучення з них високоплавких
парафінових вуглеводнів; осушення і
очищення природного газу від кислих
сполук; розділення вуглеводневих газів
на компоненти; визначення складу газів
і рідин методом хроматографії.
Суть процесу
адсорбції полягає в тому, що суміш газів
або рідин, які необхідно розділити
пропускають через шар адсорбенту –
високопористу тверду речовину. В якості
адсорбенту можуть бути використані
наступні речовини: активоване дерев’яне
вугілля, деякі сорти глин, активований
оксид алюмінію, аморфні синтетичні
алюмосилікати, кристалічні синтетичні
алюмосилікати – цеоліти. Адсорбенти
завдяки високої пористості мають велику
питому поверхню.
Розглянемо
для прикладу суть адсорбції на
алюмосилікаті. Він складається в
основному з молекул Al2O3,
SiO2
та H2O.
На рис.2.1 наведені адсорбційна колонка
і гранули адсорбенту для пояснення
механізму адсорбції. Якщо розглядати
молекули Al2O3
чи SiO2,
то вони є нейтральні, так як позитивні
заряди катіонів компенсуються зарядом
аніонів О-2.
Але заряди катіонів Al+3
і
Si+4,
які лежать безпосередньо на поверхні
адсорбенту, не повністю компенсуються
аніонами О-2,
які знаходять в масі адсорбенту. Тому
навколо поверхні адсорбенту утворюється
слабке електричне поле. Під впливом
електричного поля в молекулах компоненту,
який вилучається з суміші, при проходженні
через адсорбент виникає дипольний
момент, тобто одна частина молекули
заряджається позитивно, а друга –
негативно.
Катіони
Al+3
і
Si+4
притягують до себе негативно заряджені
кінці молекул компоненту, який
вилучається, і утворюють з ними комплексні
сполуки. Це приєднання молекул одного
із компонентів суміші до поверхні
адсорбенту і називається процесом
адсорбції. Молекули інших компонентів
суміші не поляризуються і за цією
причиною проходять через шар адсорбенту,
не поглинаючись.
Чим
більший дипольний момент у молекул
компоненту, що знаходиться в суміші,
тим краще проходить його адсорбція.
Крім цього, на процес адсорбції впливають
діаметр пор адсорбенту і розмір молекул
компоненту, що адсорбується. Якщо
діаметр пор адсорбенту малий, а розмір
молекул, що адсорбуються, великий, то
молекули не зможуть заходити в пори і
адсорбція погіршується. Найбільшою
здатністю до адсорбції володіють
асфальто-смолисті речовини(АСР), потім
у порядку зменшення – поліциклічні
ароматичні, моноциклічні ароматичні,
нафтенові та парафінові вуглеводні.
Для
десорбції молекул компоненту з поверхні
адсорбенту на практиці використовують
наступні методи:
- нагрівання всієї
маси адсорбенту;
- продування
адсорбенту водяною парою;
-
промивання адсорбенту рідиною, яка має
більшу адсорбційну здатність порівняно
з речовиною, що знаходиться на поверхні
адсорбенту.
1
– гранула адсорбенту; 2 – катіони
алюмінію і кремнію на поверхні гранули
адсорбенту; 3 – молекула компоненту,
який вилучається; 4 – молекула компоненту,
який не вилучається; 5 – аніони кисню
Рисунок
2.1 – До пояснення механізму адсорбції
На процес адсорбції
впливають наступні параметри: температура,
тиск(для газової суміші), питома витрата
адсорбенту, якість адсорбенту і
властивості суміші.
Процес
адсорбції – екзотермічний, тобто
проходить з виділенням теплоти.
Збільшення температури призводить до
зростання хаотичного руху молекул і
зменшення швидкості адсорбції. Проте,
збільшення температури до певної межі
при розділення суміші рідин покращує
процес адсорбції. Це пояснюється тим,
що при зростанні температури знижується
в’язкість суміші і полегшується рух
молекул компоненту, що вилучається, із
суміші до поверхні адсорбенту. При
подальшому збільшення температури
починає зростати швидкість коливання
молекул у порах адсорбенту і їх відрив
від поверхні адсорбенту, тобто починається
зворотній процес – десорбція. Температура
при адсорбції регулюється кількістю
холодоагенту.
При
збільшенні питомої витрати адсорбенту
швидкість адсорбції зростає, так як
більша кількість молекул компоненту,
що поглинається, контактує з поверхнею
адсорбенту. Але при великій витраті
адсорбенту зростають експлуатаційні
затрати, зв’язані з регенерацією
адсорбенту і його охолодженням перед
стадією адсорбції. Питома витрата
адсорбенту регулюється кількістю
суміші, що подається в адсорбер.
Підвищення
тиску в процесі адсорбції компоненту
з газової суміші, аналогічно до абсорбції,
прискорює адсорбцію, так як покращується
дифузія молекул компоненту до поверхні
адсорбенту. Тиск при адсорбції регулюється
автоматично клапаном, який встановлюється
на лінії виводу з апарату непоглинутих
компонентів. При розділенні суміші
рідин, тиск на процес адсорбції не
впливає.
При
збільшення пористості адсорбенту і
адсорбційної здатності одного із
компонентів суміші, зростає швидкість
адсорбції.
Схема
лабораторної установки наведена на
рис.2.2. Вона складається з скляної
колонки 1 з електрообігрівом. В колонці
знаходиться шар адсорбенту 2. Швидкість
проходження оливи через адсорбент
регулюється краном 3. Олива стікає в
колбу 4. Температура оливи в колонці
заміряється термометром 5.
Зважують
100г попередньо просушеного при температурі
105…140оС
силікагелю або алюмосилікату, засипають
його в колонку 1. Після цього зважують
50г неочищеної оливи і заливають її в
колонку 1 при закритому крані 3. Через
ЛАТР включають обігрів колонки і при
досягненні температури оливи в колонці
80оС
витримують її на адсорбенті ще 15...20хв.
Відкривають кран 3 і оливу зливають в
колбу 4. Повторно заливають частково
очищену оливу в колонку і дають можливість
їй повністю стекти у попередньо зважену
колбу. На аналітичній вазі зважують
очищену оливу і адсорбент. Для неочищеної
і очищеної оливи визначають показник
заломлення і кінематичну в’язкість.
1-скляна
колонка; 2- шар адсорбенту; 3- скляний
кран; 4 - колба; 5- термометр; 6- ЛАТР
Рисунок
2.2 – Схема лабораторної адсорбційної
установки
Складають
матеріальний баланс очистки оливи у
вигляді табл.2.1.
Кінематичну
в’язкість оливи визначають за формулою:
де
Таблиця 2.1 –
Матеріальний баланс адсорбційної
очистки оливи Взято: Гра-ми % Одержано: Гра-ми % Неочищена
олива Адсорбент
50 100
Очищена
олива Адсорбент+АСР Втрати
Усього: 150 100 Усього: 150 100
За
кольором оливи (олива після очистки
повинна бути світлішою), за кольором
адсорбенту (адсорбент темніє від
відкладення на ньому АСР), за матеріальним
балансом, показ-ником заломлення
1. Що називається
процесом адсорбції?
2. Для чого служить
процес адсорбції?
3.
Наведіть приклади використання адсорбції
в нафтогазовій промисловості.
4. В чому полягає
суть адсорбції?
5. Які існують
методи десорбції адсорбованого
компоненту?
6. Як на процес
адсорбції впливає температура?
7. Як на процес
адсорбції впливає тиск?
8. Що
таке питома витрата адсорбенту і як
вона впливає на адсорбцію?
9. З яких
конструктивних елементів складається
лабораторна установка і який порядок
виконання роботи на ній?
Мета:
засвоєння і закріплення теоретичних
положень з процесу ректифікації; набуття
експериментальних навичок проведення
ректифікації бінарної суміші (гексану
і бензолу) на лабораторній установці.
В результаті виконання лабораторної
роботи студент повинен
знати:
- призначення і
суть процесу ректифікації;
- будову і роботу
простої та складної ректифікаційних
колон;
- використання
ректифікації на підприємствах
нафтогазового комплексу;
- вплив параметрів
на процес ректифікації;
вміти:
-
правильно вибирати параметри для
одержання продуктів необхідної якості
і в заданій кількості;
- оцінювати
результати проведення процесу на
лабораторній установці;
-
проводити розрахунок кількості тарілок
в колоні за дослідними даними.
Процес
ректифікації служить для розділення
суміші рідин, які мають різні температури
кипіння, на окремі компоненти. Компонент,
який кипить при нижчій температурі,
називається низькокиплячим (н.к.к.), а
другий, який кипить при вищій температурі,
називається висококиплячим (в.к.к.).
Суть ректифікації
полягає у багатократному контактуванні
нерівноважних парової і рідкої фаз, в
результаті якого протікають процеси
тепло- та масообміну і система досягає
стану рівноваги. При цьому проходить
вирівнювання температур і тисків у
фазах та перерозподіл компонентів між
ними. Процес ректифікації проводиться
в колонах, які представляють собою
вертикальні циліндричні апарати
всередині яких на різних висотах
змонтовані пристрої (тарілки або
насадки) для контакту парів з рідиною.
В залежності від кількості одержуваних
продуктів колони є прості і складні. У
простих колонах одержують один або два
цільових продукти, а в складних – три
і більше. В тарільчатих колонах контакт
між парою і рідиною проходить при
барботажі парів через шар рідини, яка
знаходиться на контактному пристрої.
В ректифікаційних колонах використовують
тарілки різних конструкцій: ковпачкові,
клапанні, S-подібні, струйні, провальні,
каскадні та інші. В насадочних колонах
контакт між фазами проходить на поверхні
насадочних тіл, а також у просторі між
ними. В якості насадок використовують
тверді тіла різної форми (кільця Рашига,
Палля, Лессінга, сідла Берлі, сітки,
пакети, складчаті кубики), які виготовлені
з металу, кераміки, пластмаси.
Прикладом
використання процесу ректифікації є:
стабілізація конденсату або бензину;
розділення суміші компонентів на окремі
продукти (блоки ректифікації) на
установках піролізу, коксування,
каталітичного крекінгу та реформінгу,
гідрокрекінгу; розділення суміші
вуглеводнів на метан, етан, пропан і
бутани на газофракціонуючій установці(ГФУ).
Розглянемо
більш детально суть процесу ректифікації.
Для розділення на компоненти суміш
рідин (сировина) в кількості G складу
xG
нагрівається звичайно в теплообміннику
Т-1 (рис.3.1) до температури кипіння н.к.к.
і у вигляді паро-рідинної суміші
вводиться в секцію живлення колони
К-1. У момент вводу в колону сировина
розділяється на парову у0
і рідку х0
фази. Пари в основному складаються з
н.к.к., але в них міститься і деяка
кількість в.к.к.. У подальшому задача
полягає в тому, щоб виділити з парів
в.к.к.. Це досягається пропусканням
парів через шар рідини на кожній тарілці
при проходженні їх вверх колони.
Розглянемо,
що проходить на одній із тарілок в
колоні (рис.3.2). На тарілці знаходиться
рідина, температура якої менше температури
парів. Ця рідина складається з в.к.к. і
н.к.к.. Пари, які проходять через рідину
на тарілці, охолоджуються. При цьому
частина в.к.к., який є у парах конденсується
і у вигляді рідини залишається на
тарілці. Рідина на тарілці нагрівається.
Низькокиплячий компонент, який є у
рідині на тарілці, випаровується і
піднімається вверх. Пари, які залишають
тарілку, містять більше н.к.к. порівняно
з парами, що піднімаються на тарілку.
При проходженні парів через ряд тарілок
наступає такий момент, коли практично
весь в.к.к. сконденсується і залишиться
у вигляді рідини на тарілках, а пари
будуть складатися тільки з н.к.к., які
відродяться з верху колони у вигляді
дистиляту в кількості D, складу
Рисунок
3.1 – Схема простої ректифікаційної
колони
Вернемося
до рідини на тарілці. Після конденсації
в.к.к. з парів, концентрація його в рідині
зростає. Після того, як рівень рідини
на тарілці 5 підніметься на висоту
зливної перегородки 7, рідина по склянці
4 зливається на тарілку, яка знаходиться
нижче. На ній конденсується нова порція
в.к.к. з парів, які проходять через
патрубки 3, прорізі в ковпачках 6 і
барботують через рідину, що знаходиться
на даній тарілці. В результаті цього
концентрація в.к.к. в рідині знову
зростає. Рідина, яка стікає з тарілки
на тарілку, називається зрошенням. По
мірі стікання рідини з тарілки на
тарілку наступає такий момент, коли
уся рідина практично буде складатися
з в.к.к., який у вигляді залишку R складу
1
– корпус колони; 2 – ковпачок; 3 –
патрубок для проходження парів; 4 –
зливна склянка; 5 – днище тарілки; 6 –
прорізи в ковпачках; 7 – зливна перегородка
Рисунок
3.2 – Схема ковпачкової тарілки
Для
створення достатньої кількості зрошення,
необхідно відводити теплоту з верхньої
частини колони, а для створення достатньої
кількості парів і забезпечення нормальної
роботи колони необхідно підводити
теплоту в низ колони.
На
процес ректифікації впливають наступні
параметри: температури верху і низу
колони, тиск, рівень рідини в низу
колони, постійність витрати і температури
сировини при вході в колону.
Температура
верху колони впливає на вихід і якість
дистиляту. Якщо температура верху
колони буде вище норми, то разом з н.к.к.
буде випаровуватися і в.к.к. Вихід
дистиляту при цьому зросте, але якість
його погіршиться. Виникає необхідність
повернення його в колону для повторної
ректифікації. Якщо ж температура верху
колони буде нижче норми, то не повністю
випаровується н.к.к. і виводиться з
верху колони. За рахунок цього знижується
продуктивність колони за дистилятором.
Температура верху колони регулюється
подачею гострого зрошення на першу
тарілку колони. При подачі зрошення на
верх колони воно випаровується. На
випаровування затрачується теплота і
температура верха колони знижується
до заданої.
Температура
низу колони впливає на вихід і якість
залишку. Якщо температура в низу колони
нижче норми, то неповністю з рідини
випаровується н.к.к. і він разом з
залишком виводиться з колони. Якість
залишку погіршується, хоча вихід його
зростає. Температура низу колони
регулюється кількістю теплоносія, який
подається у трубний змієвик або у
випарник. При подачі теплоносія вниз
колони залишок нагрівається і з нього
повністю випаровується н.к.к..
Тиск в
колоні впливає на якість продуктів і
вибирається залежно від температурного
режиму. Відомо, що зниження тиску
полегшує, а підвищення – погіршує
кипіння рідини. Тому, при зниженні тиску
в колоні при тих же температурах на
тарілках, рідина буде краще випаровуватись.
Це призведе до того, що разом з н.к.к. з
верху колони буде виводитись і в.к.к..
В результаті цього якість дистиляту
погіршиться. При підвищенні тиску не
весь н.к.к. випаровується і знижується
продуктивність колони за дистилятом.
Тиск в колоні регулюється клапаном,
який встановлюється на лінії виводу
повітря з ємності – сепаратора С-1. При
зростанні тиску в колоні клапан більше
відкривається, з колони виводиться
більша кількість парів і тиск знижується
до заданого. Після цього клапан
повертається в попереднє положення.
Рідина
в низу колони є гідрозатвором і
перешкоджає попаданню парів у трубопровід,
а пізніше в насос Н-2, який відкачує
залишок. Якщо рівень рідини не регулювати,
то вона повністю може вийти з колони.
При цьому пари з колони попадають у
відцентровий насос, він припинить
перекачувати рідину і почне працювати
“сам на себе”. А так як сировина
безперервно подається в колону, то
рівень рідини в ній буде зростати і
вона може повністю залити колону. Процес
ректифікації припиниться. Рівень рідини
в колоні регулюється кількістю залишку,
який виводиться з колони.
Витрата
і температура сировини впливають на
режим роботи колони. При збільшенні
витрати сировини зменшується температура
в колоні, що призводить до зниження її
продуктивності за дистилятом і погіршення
якості залишку. При зменшенні витрати
сировини в колону температура в ній
зростає, що призводить до одержання
неякісного дистиляту і зниження
продуктивності колони за залишком.
Витрата сировини регулюється автоматично
клапаном, який встановлюється на лінії
подачі її в колону. Температура входу
сировини в колону теж впливає на вихід
і якість одержуваних продуктів. Зростання
температури сировини призводить до
одержання неякісного дистиляту внаслідок
випаровування деякої частини в.к.к. і
відповідно зниження продуктивності
колони за залишком. Температура сировини
на вході в колону регулюється кількістю
теплоносія, що поступає в теплообмінник
Т-1.
Схема
лабораторної ректифікаційної установки
наведена на рис.3.3. Установка складається
з куба 2, до якого приєднана ректифікаційна
колонка 5 з електрообігрівом 4 і яка
заповнена кільцями Рашига 3. З верху
колонка закривається термометром 6.
Ректифікаційна колонка обладнана
дефлегматором 7, холодильником 9 і
приймачем дистиляту 10. Підігрів куба
проводиться колбонагрівачем 1.
Інтенсивність нагріву куба і колонки
регулюється ЛАТРами 11 і 12.
Циліндром
заміряють 50мл гексану(н.к.к.) і 50мл
бензолу (в.к.к.). Одержану суміш через
горловину заливають в куб 2. Горловину
закривають корком і для герметизації
замащують колоїдом або клеєм. До
холодильника 9 приєднують ємність 10
для дистиляту. Закривають кран 8 для
відводу дистиляту і включають подачу
води в дифлегматор 7 та холодильник 9.
Включають колбонагрівач 1 для нагріву
куба 2. Інтенсивність нагрівання куба
регулюють ЛАТРом 12. Після закипання
суміші і появи зрошення у нижній частині
колонки 5, включають електрообігрів
колонки, інтенсивність нагрівання якої
регулюють ЛАТРом 11 так, щоб пройшло
“захлинання” колонки, тобто поява над
насадкою 3 стовпа рідини. При “захлинанні”
уся поверхня насадки буде змочена
рідиною. Витримують цей режим на протязі
5…7хв. Після цього, зменшивши нагрів
куба і колонки, добиваються зникнення
стовпа рідини над насадкою, не допускаючи
припинення подачі зрошення верху
колонки (зрошення весь час повинно
стікати з дефлегматора 7 назад в колонку
5). У випадку припинення подачі зрошення
в колонку, необхідно знову відновити
режим “захлинання” і встановити режим
роботи установки заново. Режим, коли
дистилят не відбирається через кран 8
в ємність 10, а весь стікає назад в
колонку, називається повним зрошенням.
Витримують роботу колонки в даному
режимі 20…30хв. Після цього, повільно
відкривши кран 8, починають відбір
дистиляту з такою швидкістю, щоб на
одну краплю дистиляту в ємність 10 на
верх колонки поступало би 20…40 крапель
зрошення. При цьому слідкують, щоб
не було “захлинання” колонки. 1
– колбонагрівач; 2 – куб; 3 – кільця
Рашига; 4 – електроспіраль; 5 –
ректифікаційна колонка; 6 – термометр;
7 – диф-легматор; 8 – кран; 9 – холодильник;
10 – приймач дистиляту; 11,12 – ЛАТРи.
Рисунок
3.3 – Схема ректифікаційної установки
Коли в ємність 10
буде відібрано приблизно 50мл гексану,
записують температуру верха колонки.
Закривають кран 8, виключають нагрів
куба та колонки і дають можливість
повністю стекти рідині з насадки в куб.
На
рефрактометрі визначають показники
заломлення чистих компонентів (гексану
і бензолу), одержаних дистиляту і залишку
в кубі.
Склад
дистиляту і залишку визначають за
графіком, на осі ординат якого відкладають
показники заломлення гексану
За
одержаними значеннями складу дистиляту
де
Таблиця
3.1 – Дослідні дані Показники Продукти
Гексан
Бензол
Дистилят
Залишок Показник
заломлення,
Вміст
гексану, %об
Вміст
гексану, % об.
Рисунок 3.4- Графік
для визначення складу дистиляту і
залишку
Рисунок
3.5- Визначення кількості тарілок в
колоні графічним методом
1.
Для чого призначений процес ректифікації?
2. В чому полягає
суть ректифікації?
3.
Наведіть приклади використання
ректифікації на підприємствах
нафтогазового комплексу.
4. Як на процес
ректифікації впливає температура верху
колони?
5. Як на процес
ректифікації впливає температура низу
колони?
6. Як на процес
ректифікації впливає тиск?
7. Для чого в колоні
необхідно регулювати рівень залишку?
8. Чому необхідно
підтримувати постійними витрату і
температуру сировини на вході в колону?
9. З яких
конструктивних елементів складається
лабораторна установка?
10. Опишіть методику
проведення ректифікації на лабораторній
установці. 11.
Як визначаються склад дистиляту і
залишку?
12. Як визначається
кількість тарілок в колоні?
Мета:
засвоєння і поглиблення теоретичного
матеріалу з процесу екстракції; набуття
експериментальних навичок проведення
екстракції суміші рідин (гексан і
бензол). В результаті виконання
лабораторної роботи студент повинен
знати:
- призначення,
суть і методи екстракції;
- використання
екстракції на підприємствах нафтогазового
комплексу;
- будову і роботу
екстракційної колони;
- вплив параметрів
на процес екстракції;
вміти:
- правильно вибирати
параметри для оптимального проведення
процесу;
- оцінювати
результати проведення процесу на
лабораторній установці;
-
проводити розрахунок екстракції за
допомогою трикутної діаграми.
Процес
екстракції служить для розділення
суміші рідин, які мають однакову або
близькі температури кипіння, на окремі
компоненти за допомогою розчинника.
Екстракція полягає в тому , що суміш
рідин, що розділяється , змішується з
розчинником. В якості розчинника
вибирається рідина, яка розчиняє один
з компонентів суміші, а інші не розчиняє,
або розчиняє частково. Після відстоювання
уся маса розділяється на два шари з
границею розділу фаз. Нижній шар
складається з розчинника і розчиненого
в ньому одного з компонентів суміші.
Цей продукт називається екстрактним
розчином. Верх--ній шар складається з
непоглинутих компонентів суміші і
невеликої кількості розчинника. Цей
продукт називається рафінатним розчином.
Якщо у подальшому розділити екстрактний
і рафінатний розчини та відігнати від
них розчинник, то можна одержати чисті
компоненти, які складають вихідну
суміш.
Процес
екстракції проводиться в екстракційних
колонах або в системі апаратів типу “
зміщувач-відстійник ”. В нафтогазовому
комплексі процес екстракції
використовується для очистки олив
фенолом, фурфуролом або N-метилпіролідоном
від АСР,
деасфальтизації гудрону рідким
пропаном, вилучення ароматичних
вуглеводнів з реформатів (продукту
каталітичного реформінгу ) або конденсатів
за допомогою етиленгліколю.
В
залежності від кількості ступенів
екстракції і способів їх з’єднання
розрізняють наступні методи екстракції:
однократну, багатократну і протитічну.
При
однократній екстракції (рис.4.1а) вихідна
сировина G в один прийом обробляється
заданою кількістю розчинника L у
змішувачі 3-1. Утворену в результаті
змішування суміш розділяють у відстійнику
В-1 на рафінатний R і екстрактний S
розчини, які відводять з апарату в
ректифікаційні колони К-1 і К-2 для
відгонки розчинника і одержання
рафінату R0
і екстракту S0.
Розчинник знову повертається в процес.
При
багатократній
екстракції (рис. 4.1б) вихідна сировина
G і відповідні рафінатні розчини R1,
R2 обробляються
порцією свіжого розчинника L на кожній
ступені екстракції, де є змішувачі 3-1
... 3-3 і відстійники В-1...В-3. При цьому
рафінатний розчин з даної ступені
екстракції направляється в наступну
ступінь, а екстрактні розчини S1,
S2 ,
S3
після кожної ступені екстракції
виводяться з системи. При такому способі
обробки вихідна сировина G поступає на
першу ступінь екстракції, а кінцевий
рафінатний розчин R3
відбирається
з останньої ступені.
При
даній екстракції можна одержати кращу
якість рафінату порівняно з однократною,
але вихід кінцевого рафінату зменшується.
Протитічна
екстракція (рис.4.1в) характеризується
багатократним контактуванням у протитоці
відповідних рафінатних і екстрактних
розчинів. При цьому розчинник подається
тільки в останній змішувач 3-3, кінцевий
рафінатний розчин R3
виводиться
з відстійника В-3, а кінцевий екстрактний
розчин – з відстійника В-1.
Протитічна
екстракція забезпечує одержання
продуктів найвищої якості із максимальним
виходом.
З-1..З-3
– змішувачі; В-1..В-3 – відстійники;
К-1,К-2 – ректифікаційні колони; G –
сировина; L – розчинник; R,R1..R3
– рафінатні розчини; S,S1..S3
– екстрактні розчини; R0
– рафінат; S0
– екстракт
Рисунок 4.1 – Методи
екстракції: а – однократна ; б –
багатократна; в – протитічна
На
процес екстракції впливають наступні
параметри : температура, співвідношення
між витратою розчинника і витратою
вихідної суміші, якість розчинника.
При збільшенні температури зростає
розчинна здатність розчинника. При
цьому в одиниці об’єму розчинника буде
розчинятися більше компоненту, який
вилучається, і витрата розчинника в
процесі зменшиться. Але при збільшенні
температури знижується селективність
розчинника, і в ньому починають
розчинятися і інші компоненти суміші.
Крім того, при збільшенні температури
вище критичної, зникає границя розділу
фаз і неможливо буде розділити рафінатний
і екстрактний розчини.
При
зниженні температури спостерігається
зворотній процес. Так як розділення за
допомогою екстракції може проходити
лише при умові, що розчинник і сировина
утворюють гетерогенну систему, необхідно
вибирати таку температуру, яка забезпечу
достатньо високу селективність
(вибірковість) та розчинну здатність
розчинника. Температура екстракції
регулюється кількістю теплоносія, що
подається в теплообмінник для підігріву
розчинника.
Якщо
витрата розчинника буде недостатньою,
то не весь компонент, який вилучається,
перейде із сировини в розчинник. При
великій витраті розчинника починають
в ньому розчинятися й інші компоненти
суміші. За рахунок цього якість
одержуваних продуктів погіршується.
Крім того, зростають експлуатаційні
затрати зв’язані з перекачкою і
регенерацією розчинника. Співвідношення
розчинник/сировина складає 2,5...4,5 і
регулюються кількістю сировини, що
поступає в екстракційний апарат.
Якість
розчинника характеризується розчинною
здатністю і селективністю. Розчинна
здатність розчинника – це здатність
його розчиняти в одиниці маси певну
кількість компоненту. Селективність
або вибірковість – це здатність його
розчиняти тільки певний компонент
суміші, а інші не розчиняти. Чим вища
селективність розчинника, тим більш
чітко розділяються компоненти при
контакті з розчинником. Вищій розчинності
розчинника відповідає більший коефіцієнт
роз-приділення К. Коефіцієнт розприділення
– відношення концентрації компонента
в екстрактному розчинні Х1
до концентрації компоненту в рафінатному
розчині Х2
:
Він
визначається експериментально і
залежить від природи системи, її складу
та температури .
Чим
вища розчинна здатність розчинника,
тим більшу масу компоненту, який
вилучається, можна в ньому розчинити
і тим, відповідно, менша витрата
розчинника.
Селективність
і розчинність розчинника залежать від
температури. При підвищенні температури
селективність знижується, а розчинність
зростає.
Екстракцію
проводять в колбі 1, яка обладнана
механічною мішанкою 2, що приводиться
в рух електродвигуном 3. Кількість
обертів мішалки регулюється ЛАТРом 4.
Колба 1 має бокові горловини 5 і 6 для
термометра 7 і для заливу суміші та
розчинника. Відстоювання і розділення
рафінатного та екстрактного розчинів
проводять у ділильній лійці 8, яка
кріпиться на штативі 9. Відгонку від
розчинника екстракту проводять на
апараті , який складається з колби 10 з
відростком, термометра 11, холодильника
12, мірного циліндра 13, газового пальника
14 (рис. 4.2).
У мірному
циліндрі готовлять суміш з 15мл
бензолу і 15мл гексану.
Приготовлену суміш через горловину 5
заливають в колбу 1. Після цього в колбу
доливають 70 мл розчинника – етиленгліколю.
Включають в мережу ЛАТР 4 і плавним
поворотом ручки включають електродвигун
3 для обертання мішалки 2. Суміш перемішують
на протязі 20 –25 хвилин . При перемішуванні
бензол буде розчинятися в етиленгліколі.
За час перемішування продуктів визначають
рефрактометром коефіцієнт заломлення
бензолу і гексану.
Після закінчення
перемішування суміш переливають з
колби 1 в ділильну лійку 8. В ділильній
лійці вся маса продуктів розділяється
на два шари з чіткою границею розділу
між ними. Нижній шар – екстрактний
розчин – етиленгліколь з розчиненим
в ньому бензолом; верхній шар – рафінатний
розчин – гексан з невеликою кількістю
етиленгліколю. Зливають нижній шар (
екстрактний розчин) з ділильної лійки
і заливають його в колбу 10 для відгону
бензолу. Колбу 10 під’єднують до
холодильника 12 , закривають корком з
термометром 11 і нагрівають газовим
пальником 14. Бензол випаровується з
розчину, конденсується в холодильнику
14 і у вигляді рідини стікає в мірний
циліндр 13. При відгонці бензолу від
розчинника необхідно слідкувати за
температурою. Як тільки весь бензол
випарується, то пари його не будуть
омивати ртутний стовпчик термометра
11, і температура різко буде зменшуватися.
Після цього припиняють нагрівання
колби і відключають газовий пальник.
Заміряють об’єм
відігнаного бензолу, етиленгліколю і
гексану, що залишився в ділильній лійці.
Визначають
коефіцієнти заломлення одержаних
рафінату-гексану і екстракту-бензолу.
1
– колба; 2 – механічна мішалка; 3 –
електродвигун; 4 – ЛАТР; 5,6 – бокові
горловини; 7 – термометр; 8 – ділильна
лійка; 9 – штатив; 10 – колба з екстрактним
розчином; 11 – термометр; 12 – холодильник;
13 – мірний циліндр; 14 – газовий пальник.
Рисунок 4.2 –
Лабораторні установки для проведення
екстракції
Значення показників
заломлення чистих гексану і бензолу,
а також одержаних рафінату і екстракту
та об’єми одержаних продуктів заносять
в таблицю 4.1. Таблиця
4.1- Дослідні дані Взято,
мл Одержано,
мл Коефіцієнт
заломлення,
Гексану
Бензолу
Розчинника
Рафінату
Екстракту
Розчинника
Гексану
Бензолу
Рафінату
Екстракту
За даними таблиці
будують графік залежності коефіцієнту
заломлення гексану і бензолу від складу
продуктів (рис.4.3) та визначають склади
рафінату і екстракту. Роблять висновок
про якість розділення вихідної суміші.
Вміст гексану, %
об
Рисунок 4.3 – Графік
для визначення складу рафінату і
екстракту
1.Для чого служить
процес екстракції?
2.В чому полягає
суть процесу екстракції ?
3.Наведіть приклади
використання екстракції в нафтогазовому
комплексі.
4.Опишіть однократну
екстракцію.
5.Намалюйте і
опишіть багатократну екстракцію.
6.Намалюйте і
опишіть протитічну екстракцію.
7.Як на процес
екстракції впливає температура?
8.Як на процес
екстракції впливає співвідношення
розчинник/сировина?
9.Що таке селективність
і що таке розчинність розчинника?
10.Як на процес
екстракції впливає якість розчинника?
11.З яких конструктивних
елементів складається лабораторна
установка для проведення екстракції?
12.Як одержують
рафінат і екстракт?
13.Як визначити
склади рафінату і екстракту?
Мета:
засвоєння і закріплення теоретичних
положень з процесу каталітичного
крекінгу; набуття експериментальних
навичок проведення каталітичного
крекінгу вакуумного газойлю на
лабораторній установці.
В результаті
виконання лабораторної роботи студент
повинен
знати:
- призначення,
суть і механізм реакцій процесу
каталітичного крекінгу;
- характеристику
сировини і одержуваних продуктів;
- вплив параметрів
на процес каталітичного крекінгу;
вміти:
-
правильно вибирати параметри для
одержання продуктів необхідної якості
і в заданій кількості;
- оцінювати
результати проведення процесу на
лабораторній установці.
Каталітичний
крекінг служить для одержання компонентів
моторних палив, сировини для нафтохімії,
виробництва технічного вуглецю і коксу
із важких нафтових фракцій з межами
википання 350...5000С
.
Суть
процесу полягає в тому, що сировина в
реакторі змішується з гарячим
каталізатором. Молекули сировини при
контакті з поверхнею каталізатора
розриваються (крекуються) з утворенням
більш легких продуктів порівняно з
вихідною сировиною. В умовах каталітичного
крекінгу (температура 450...5100С,
тиск 0,1...0,3 МПа, каталізатор-аморфний
або кристалічний алюмосилікатний)
протікає велика кількість реакцій,
серед яких визначаючими є: розрив
вуглець-вуглецевого зв’язку, перерозподіл
водню, ароматизація, ізомеризація,
розрив і перегрупування вуглеводневих
кілець, конденсація, полімеризація і
коксоутворення. Механізм більшості
реакцій каталітичного крекінгу найбільш
задовільно пояснюється карбокатіонною
теорією, згідно якої активними проміжними
частинками є карбокатіони. Вони
утворюються при гетеролітичному розриві
зв’язків у молекулі вуглеводнів під
впливом каталізатора або при приєднанні
до вуглеводню електрондефіцитних
кислотних груп каталізатора.
У
схематичному вигляді основні напрями
перетворення вуглеводнів при каталітичному
крекінгу можна представити наступним
чином:
Таким
чином, найбільш активними вуглеводнями
в умовах контакту з алюмосилікатним
каталізатором є олефінові. Це пояснюється
в першу чергу їх високою адсорбційною
здатністю по відношенню до каталізатора.
Реакції перерозподілу водню нарівні
з розщепленням та ізомеризацією в
значній мірі визначають якість продуктів
крекінгу.
Основною
сировиною каталітичного крекінгу є
вакуумні дистиляти парафінових відносно
смолистих і сірчаних нафт з межами
википання 350 - 500 (540)0С.
В окремих випадках до сировини додають
більш легкі прямогонні фракції,
гасово-газойлеві фракції термічних
процесів і коксування, напівпродукти
виробництва олив, мазути нафт з невисоким
вмістом металів.
Продуктами
установки каталітичного крекінгу є
наступні:
-
вуглеводневий газ C1-C4,
який містить 25...35% пропан-пропілену і
30...50% бутан-бутиленів. Він направляється
на ГФУ. Після розділення сухий газ С1-С2
використовується в якості палива для
заводських печей, пропан-пропіленова
і бутан-бутиленова фракції (ППФ і ББФ)
– в якості сировини для установок
полімеризації і алкілювання;
-
бензинова фракція з межами википання
n.к.-1950С
має октанове число 87...95 за дослідним
методом (78...85 за моторних методом),
використовується як базовий компонент
автомобільних бензинів;
- фракції,
які википають вище 1950С
розділяються на фракції 195-3500С
і залишок вище 3500С
при роботі установки за паливним
варіантом або на фракції 195-2700С;
270-4200С
і залишок вище 4200С
при роботі установки за нафтохімічним
варіантом;
- гасова
фракція 195-2700С
використовується як флото-реагент або
як сировина для одержання ароматичних
вуглеводнів;
- фракція
легкого газойлю 195-3500С
має цетанове число 35...40, температуру
застигання -20...-500С.
Використовується як компонент дизельних
палив;
-
газойлева фракція 270-4200С
використовується як сиро-вина для
виробництва технічного вуглецю;
-
фракції важкого газойлю, що википають
вище 3500С
і вище 4200С
мають температуру застигання 10...250С,
коксуємість 5...10%. Використовуються як
компоненти котельного палива або як
сировина для одержання високоякісного
коксу.
Сучасні каталізатори
крекінгу представляють собою складні
системи, які складаються з 10...25% цеоліту
типу У в рідкоземельній обмінній формі,
яка рівномірно розподіляється в 75...90%
аморфного алюмосилікатного каталізатора.
Хімічний склад цеолітвмістного
каталізатора можна записати у вигляді
емпіричної формули:
Ме2/nО·Aℓ2О3·mSiО2·xН2О,
де
Ме – метал; n – валентність катіона; m
= 2...15. Каталізатор випускається у вигляді
мікросферичних частинок діаметром
(6...6,5) ·10 -5м
або кульок діаметром (3...5) ·10 -3м.
Вміст окремих компонентів у каталізаторі
наступний, % мас.: оксид алюмінію –
35...40; оксиди рідкоземельних металів –
2...4; оксид натрію – 0,3...0,4. Насипна густина
цеолітних каталізаторів складає
800...900 кг/м3,
стабільна активність - 55...60%. Активним
компонентом в каталізаторах є цеоліт.
Аморфна матриця забезпечує оптимальну
межу міцності, стабілізуючу дію на
цеоліт, оптимальну пористу структуру
для дифузії реакційної суміші при
крекінгу і регенерації, відвід теплоти
від цеолітного компоненту.
В
результаті крекінгу вуглеводневої
сировини поверхня каталізатора
покривається смолисто-коксовими
відкладами. Для відновлення активності
ці відклади випалюють шляхом контакту
гарячого каталізатора з киснем повітря
при температурах 630...6700С
в апаратах-регенераторах.
До
основних параметрів, що впливають на
вихід і якість продуктів каталітичного
крекінгу відносяться: якість сировини,
температура в реакторі, час контакту
сировини і каталізатора, кратність
циркуляції каталізатора.
Найбільш
типова сировина каталітичного крекінгу
– вакуумні газойлі первинної перегонки
нафти, які википають в межах
350-(500...540)0С.
Рідше як сировина використовуються
дистиляти коксування, рафінати процесів
деасфальтизації мазутів і гудронів,
напівпродукти виробництва олив, мазути
з невисоким вмістом металів. На результати
крекінгу впливають як фракційний так
і хімічний склади сировини. По мірі
облегшення сировини зростає вихід
вуглеводнів С3-С4
і бензину при одночасному зниженні
виходу водню і коксу на каталізаторі.
Обважнення сировини до певної межі
призводить до підвищення октанового
числа бензину і його виходу. Обмежуючим
фактором кінця кипіння сировини є вміст
у ній асфальто-смолистих речовин,
металів і висока коксуємість, які є
причиною коксоутворення і швидкої
дезактивації каталізатора. За хімічним
складом найбільш сприятливою є сировина
нафтенової основи, так як в результаті
реакцій дегідрування і перерозподілу
водню продукти крекінгу більш стабільні
і містять більше ароматичних вуглеводнів,
а бензини мають вище октанове число.
Небажаним
компонентом сировини є поліциклічні
ароматичні вуглеводні, які мають
підвищену адсорбційну здатність по
відношенню до поверхні каталізатора,
блокують його активні центри і є джерелом
коксоутворення на каталізаторі. Сировина
вторинного походження містить у своєму
складі більше ненасичених та поліциклічних
ароматичних вуглеводнів, тому її важче
переробляти за прямогонну. На практиці
до прямогонної сировини додають не
більше 20...25% вторинної.
Для
підготовки сировини до каталітичного
крекінгу досить часто проводять її
облагородження методами деасфальтизації,
селективного очищення і гідроочищення.
При цьому значно знижується вміст у
сировині асфальто-смолистих речовин,
олефінових вуглеводнів, сірчаних,
азотних і кисневих сполук та важких
металів, а також зменшується її
коксуємість. При каталітичному крекінгу
підготовленої сировини утворюється
менше коксу на каталізаторі та
вуглеводневого газу і більше бензину
з вищою стабільністю.
Промислові
процеси каталітичного крекінгу проводять
в інтервалі температур 450...5100С.
З ростом температури в реакторі
знижуються виходи коксу і важкого
газойлю, що пояснюється посиленням
десорбції і видалення важких парів з
поверхні каталізатора. При цьому помітно
зростає вихід газу при незначному
зменшенні виходу світлих продуктів
(бензину і легкого газойлю). Октанове
число бензину збільшується за рахунок
ароматизації вуглеводнів. Температура
в реакторі регулюється кількістю
палива, яке подається в піч, де
підігрівається сировина і залежить
від температури регенерації каталізатора.
Висока
активність цеолітвмістних каталізаторів
у поєднанні з їх швидкою дезактивацією
в ході протікання реакцій обумовила
створення прямотічних ліфт-реакторів
з висхідним потоком сировинно-каталізаторної
суміші. Для ліфт-реактора масова
швидкість подачі сировини є умовним
показником і фізичний зміст має час
контакту сировини і каталізатора. При
цьому час контакту сировини і каталізатора
в ліфт-реакторі знижується до 4...8с проти
180...190с в реакторі з псевдозрідженим
шаром каталізатора. Для формування
якості кінцевих продуктів і співвідношення
між ними в бажаному напрямі на виході
із ліфт-реактора організовується
додаткова зона крекінгу у форсованому
киплячому шарі. Час контакту сировини
і каталізатора регулюються швидкістю
подачі сировини і каталізатора.
Кратність
циркуляції каталізатора – це маса
каталізатора, що приходиться на 1 тонну
сировини, яка подається в реактор. Вона
зв’язана з допустимою величиною
коксовідкладення, яка не перевищує
1,0…1,5% мас. на каталізатор (3,5...4,5% мас.
на сировину). Крім того, кратність
циркуляції каталізатора визначається
температурним режимом реактора і
регенератора. Збільшення кратності
циркуляції каталізатора зменшує час
його перебування в зоні реакції.
Кількість коксу на кожній частині
каталізатора зменшується, а це в свою
чергу сприяє зростанню степені
перетворення сировини, тобто підвищенню
виходу газу, бензину та коксу. Збільшення
виходу коксу пояснюється зниженням
ефективності відпарювання відпрацьованого
каталізатора. Зміною кратності циркуляції
каталізатора можна регулювати кількість
теплоти, яку необхідно підводити ззовні,
степінь перетворення сировини, степінь
закоксованості каталізатора. З іншого
боку зростання кратності циркуляції
каталізатора збільшує енергетичні
затрати на експлуатацію установок
каталітичного крекінгу. При цьому також
зростають розміри реакторно-регенеративного
блоку. Кратність циркуляції каталізатора
на установках каталітичного крекінгу
з киплячим шаром каталізатора становить
8...12, а в реакторах ліфтного типу -
2,5...7. Кратність циркуляції каталізатора
регулюється кількістю сировини, що
подається в реактор.
Процес
каталітичного крекінгу ведуть при
невеликому надлишковому тиску 0,07...0,18
МПа. Підвищення тиску мало впливає на
процес, оскільки він відбувається на
поверхні каталізатора. При підвищенні
тиску незначно зростає вихід коксу,
оскільки збільшується кількість
компонентів, які адсорбуються на
поверхні каталізатора. При цьому вихід
бензину і його октанове
число
зменшується. Тиск в реакторі підтримується
дещо вищим атмосферного для проштовхування
пароподібних продуктів реакції з
реактора в ректифікаційну колону. Тиск
в реакторі регулюється автоматично
клапаном, який встановлюється на лінії
виводу газоподібних продуктів з нього.
Схема лабораторної
установки наведена на рис. 5.1. Установка
складається з реактора 1, заповненого
алюмосилікатним каталізатором, який
знаходиться в циліндричній вертикальній
електричній печі 2, лабораторного
автотрансформатора 3 для регулювання
електронагрівання, ділильної лійки
для сировини 4, термопари 5 і потенціометра
6 для вимірювання температури в реакторі,
колби 7 для збирання рідких продуктів
крекінгу, холодильника 8 і збірника
конденсату 9.
Включають
електричну піч 2, при цьому ручку
лабораторного автотрансформатора
встановлюють на позначку 220 В. Зважують
100 г сировини і заливають її у ділильну
лійку 4, після чого включають подачу
води в холодильник 8. Коли потенціометр
6 покаже температуру в реакторі
450...4600С,
відкривають кран на ділильній лійці з
сировиною і подають її з швидкістю 10
мл/хв (при більшій швидкості подачі
сировини різко зменшується температура
в реакторі, що призводить до сповільнення
реакцій крекінгу). При контакті сировини
і каталізатора проходить крекінг
сировини. Рідкі продукти крекінгу
стікають з реактора 1 в колбу 7. Газоподібні
продукти і частина бензину у вигляді
парів проходять через холодильник 8,
частково конденсуються і збираються
в збірнику конденсату 9. Вуглеводневі
гази через гумову трубку викидуються
в атмосферу.
Після
того, як сировина з лійки 4 стече в
реактор 1 і припиниться поступлення
продуктів в колбу 7, виключають нагрівання
реактора, для цього ставлять ручку на
ЛАТРі в положення „0” і виймають вилку
з розетки. Рідкі продукти крекінгу
переливають із
1-реактор;
2-циліндрична вертикальна електрична
піч; 3-лабора-торний автотрансформатор;
4-ділильна лійка; 5-термопара;
6-потен-ціометр; 7-конічна колба;8-холодильник;
9- збірник конденсату
Рисунок
5.1 – Схема лабораторної установки
каталітичного крекінгу
колби
7 і збірника 9 у попередньо зважену
конічну колбу. Колбу з продуктами
зважують на аналітичній вазі і визначають
масу рідких продуктів крекінгу-бензину
і газойлей. Для визначення кількості
одержаного бензину, його відганяють
від легкого і важкого газойлів на
апараті Енглера(рис.5.2). Для цього рідкі
продукти крекінгу зливають в колбу 1.
Її закривають корком з термометром 2.
Встановлюють колбу на азбестову
прокладку 6. Відвідну трубку вставляють
в трубку 8 холодильника 3, після чого
колбу закривають металевим кожухом 7.
Мірний циліндр 4 ставлять під нижній
загнутий кінець трубки холодильника.
Під час перегонки циліндр закривають
ватою, щоб не було втрат парів. Включають
газовий пальник 5 і регулюють нагрівання
колби так, щоб перша крапля бензину при
перегонці впала з кінця трубки
холодильника не раніше 5 хвилин і не
пізніше 15 хвилин від початку нагрівання.
Після падіння першої краплі бензину в
циліндр, збільшують нагрівання і ведуть
перегонку з швидкістю 20...25 крапель за
10 секунд, що відповідає 4...5 мл/с. Кінцем
перегонки бензину рахується момент,
коли термометр покаже температуру
1950С.
Нагрівання припиняють, зважують циліндр
з бензином.
1-колба з боковим
відводом; 2-термометр; 3-ванна холодильника;
4-мірний циліндр; 5-газовий пальник;
6-азбестова прокладка; 7-металевий кожух;
8-трубка холодильника; 9,10-патрубки для
вводу і виводу води
Рисунок 5.2 – Прилад
для відгону бензину від газойлів
Результати
зважування рідких продуктів крекінгу
заносять в таблицю 5.1. Складають
матеріальний баланс і за ним роблять
висновок про те, як пройшов процес
каталітичного крекінгу.
Таблиця 5.1 -
Матеріальний баланс каталітичного
крекінгу Взято:
Грами %
мас Одержано: Грами %
мас
Сировина
100
100 Бензин Газойлі Вуглеводневий газ
+ кокс Втрати
1,0
При
проведенні каталітичного крекінгу
сировини на аморфному алюмосилікатному
каталізаторі вихід бензину складає
28...32% мас., на кристалічному алюмосилікатному
(цеолітному) каталізаторі – 50% мас. і
більше.
1.Для чого призначений
процес каталітичного крекінгу?
2.В чому полягає
суть процесу каталітичного крекінгу?
3.Наведіть у
схематичному вигляді механізм реакцій
каталітичного крекінгу.
4.Які вуглеводні
сировини є найбільш активними і чому?
5.Що використовується
в якості сировини каталітичного
крекінгу?
6.Назвіть продукти
крекінгу і дайте їх характеристику.
7.Що
представляють собою каталізатори
каталітичного крекінгу і яка роль
кожного з компонентів в ньому?
8.Як впливає на
процес каталітичного крекінгу якість
сировини?
9.Які існують
методи підготовки сировини і в чому
вони полягають?
10.Як на
процес каталітичного крекінгу впливає
час контакту сировини і каталізатора?
11.Як на процес
каталітичного крекінгу впливає
температура?
12.Що таке кратність
циркуляції каталізатора і як вона
впливає на процес крекінгу?
13.Як на процес
каталітичного крекінгу впливає тиск?
14.З яких
конструктивних елементів складається
лабораторна установка каталітичного
крекінгу?
15.Який
порядок виконання роботи на лабораторній
установці каталітичного крекінгу?
16. На
якому апараті проводиться розділення
рідких продуктів крекінгу і з яких
конструктивних елементів він складається?
Мета:
засвоєння і поглиблення теоретичного
матеріалу з процесу каталітичного
реформінгу, набуття експериментальних
навичок проведення підготовки сировини
до каталітичного реформінгу на
лабораторній установці АРН –2.
В результаті
виконання лабораторної роботи студент
повинен
знати:
-
призначення, суть і хімізм процесу
каталітичного реформінгу;
- характеристику
сировини і одержуваних продуктів;
-
опис технологічної схеми установки
каталітичного реформінгу;
-
параметри контролю і регулювання на
установці каталітичного реформінгу;
вміти:
-
оцінювати результати одержання сировини
для каталітичного реформінгу на
лабораторній установці;
-
правильно вибирати параметри процесу
для одержання якісних продуктів і в
заданій кількості.
Процес
каталітичного реформінгу служить для
підвищення детонаційної стійкості
(октанового числа) бензинів і одержання
ароматичних вуглеводнів, головним
чином, бензолу, толуолу і ксилолів.
Суть
процесу реформінгу полягає в тому, що
сировина змішується з водневмісним
газом, нагрівається до температури
біля 500оС
і у вигляді парів проходить через шар
каталізатора. Під дією температури і
каталізатора відбувається зміна
хімічної структури молекул сировини.
Процес
каталітичного реформінгу включає три
основні типи реакцій перетворення
вуглеводнів: ароматизацію, ізомеризацію
і гідрокрекінг. Найбільш важливими є
реакції, які призводять до утворення
ароматичних вуглеводнів. До них
відносяться реакції дегідрування
шестичленних нафтенових вуглеводнів
і дегідроциклізація парафінових
вуглеводнів:
В
той час, коли реакція (6.1) протікає з
найбільшою швидкістю, то реакція (6.2) –
з найменшою. Парафінові вуглеводні
нормальної будови в умовах каталітичного
реформінгу можуть також вступати в
реакцію ізомеризації:
СН3
– (СН2)3
– СН3
І
СН3
н
– пентан ізопентан
П’ятичленні
нафтени, що містяться у сировині,
безпосередньо не гідруються, але в
присутності каталізаторів реформінгу
вони ізомеризуються з утворенням
відповідних шестичленних нафтенів,
які вже здатні до дегідрування:
Високі
температури процесу викликають реакції
крекінгу. Утворені осколки молекул
можуть насичуватися воднем або вступати
в реакції ущільнення. Насичення осколків
молекул воднем називається гідрокрекінгом.
Він призводить до утворення вуглеводневих
газів і може бути представлений у
вигляді наступної реакції:
С8Н18
+ Н2
октан
пропан пентан
Це
небажана реакція процесу каталітичного
реформінгу, оскільки в результаті її
зменшується вихід цільового продукту
– високооктанового бензину. Реакції
ущільнення призводять до утворення
коксу на каталізаторі і його дезактивації,
тому теж є небажаними в процесі. Щоб
запобігти цьому реформінг проводять
в атмосфері водню при високому тиску.
Сировиною
каталітичного реформінгу є бензинові
фракції прямої перегонки нафти, а також
бензинові фракції вторинного походження:
коксування, гідрокрекінгу, термокрекінгу.
Для одержання високооктанового бензину
найчастіше використовують широку
бензинову фракцію 85-180оС,
а для одержання індивідуальних
ароматичних вуглеводнів: бензолу –
фракцію 62-85оС,
толуолу – фракцію 85-105оС,
ксилолів та етилбензолу – фракцію
105-140оС.
Основною вимогою до сировини каталітичного
реформінгу є мінімальна кількість
сірки
Продуктами
установки каталітичного реформінгу є
вуглеводневий газ, головка стабілізації,
водневмісний газ і каталізат (реформат).
Вуглеводневий
газ С1
– С2
використовують як паливо для заводських
печей. Головка стабілізації містить
насичені вуглеводні пропан і бутани.
Її направляють на розділення (ГФУ) або
відвантажують безпосередньо з установки
як зріджений газ для комунально-побутового
споживання та газобалонних двигунів.
Каталізат
реформінгу – це бензинова фракція з
октановим числом 85…88 за моторним
методом (95…97 за дослідним методом)
містить 50…70% ароматичних вуглеводнів.
Каталізат використовують як базовий
компонент автомобільних і авіаційних
бензинів. При одержанні індивідуальних
ароматичних вуглеводнів їх виділяють
з каталізату методом екстракції.
Водневмісний
газ (ВВГ) містить 75…90% об. водню і
вуглеводні С1
– С4.
ВВГ частково використовують для
поповнення втрат водневмісного газу
на установці реформінгу, а основну його
частину направляють на установки
гідроочистки, гідрокрекінгу, ізомеризації
та гідродеалкілювання нафтопродуктів.
Промислові
процеси каталітичного реформінгу
проводять на біфункціональних
каталізаторах, що складаються з активного
носія
Існує
три типи каталізаторів реформінгу:
моно-, бі- і поліметалеві. Першим
промисловим каталізатором реформінгу
був алюмоплатиновий, від чого і одержав
назву процес – платформінг. Платинові
каталізатори містили 0,5…0,65%мас. платини,
нанесеної на оксид алюмінію. Каталізатори
цієї серії (АП-56, АП-64) достатньо ефективні
в процесі реформінгу, але нестійкі до
дії гетероорганічних сполук і дуже
дорогі.
Біметалеві
каталізатори реформінгу містять уже
два активні елементи. Найчастіше це
платина і реній. Платино-ренієві
каталізатори містять до 0,4%мас. платини
та 0,4…0,6%мас. ренію. Промисловий процес
на каталізаторах цього типу називають
реніформінгом. Порівняно з платиновими
каталізаторами платино-ренієві
(КР-101,КР-102, КР-104) мають більшу активність
і стабільність та меншу вартість.
Каталізаторами
нового покоління є поліметалеві, які
містять три і більше металів (
Регенерацію
каталізаторів реформінгу здійснюють
випалюванням коксу з наступним
окислювальним хлоруванням каталізатора.
Промисловий
процес реформінгу проводять у середовищі
водневмісного газу (70…90% об.) при таких
умовах: темпе-ратура – 470…520оС,
тиск – 1,5…4,0 МПа, об’ємна швидкість
подачі сировини – 1,0…2,0 год –1,
кратність циркуляції ВВГ – 900…1500 м3/м3.
Основними
параметрами, які впливають на показники
роботи установки каталітичного
реформінгу є наступні: якість сировини,
температура сировини на вході в реактори,
об’ємна швидкість подачі сировини,
тиск і кратність циркуляції ВВГ.
На
промислових установках реформінгу
контролюють перепад температури по
висоті реактора, перепад тиску на
каталізаторі і температуру стінок
реактора.
На
показники реформінгу великий вплив
мають вуглеводневий і фракційний склади
сировини. Вихід каталізату і водневмісного
газу, стабільність роботи каталізатора
зростають при збільшенні у сировині
нафтенових і ароматичних вуглеводнів.
Гетероорганічні сполуки та олефінові
вуглеводні знижують працездатність
каталізатора, тому їх вилучають
гідроочищенням. Щодо фракційного
складу, то оптимальною є фракція 85-180оС
при одержанні високооктанового
компоненту бензину. Фракцію п.к. – 85оС
переробляти недоцільно, так як при
цьому збільшується вихід вуглеводневого
газу за рахунок реакцій гідрокрекінгу.
Помітного ж збільшення октанового
числа бензину не проходить із-за
відсутності у цій фракції нафтенів С6.
Кінець кипіння сировини обмежується
тим, що вище 180оС
у сировині містяться поліциклічні
вуглеводні, які викликають інтенсивне
закоксовування каталізатора і його
дезактивацію, внаслідок чого зменшується
тривалість міжрегенераційного періоду
в роботі установки реформінгу. Вміст
нафтенових і ароматичних вуглеводнів
у сировині визначається аналізатором,
а фракційний склад – розгонкою на
апараті Енглера.
Температуру
сировинно-водневої суміші на вході в
реактори встановлюють на початку
реакційного циклу на рівні, який
забезпечує задану якість каталізату
– октанове число або концентрацію
ароматичних вуглеводнів. Звичайно,
початкова температура знаходиться в
межах 470…500оС.
По мірі закоксовування каталізатора,
температуру на вході в реактори
підвищують, підтримуючи постійну якість
каталізату. Зниження температури при
інших рівних умовах призводить до
збільшення виходу бензину, зниження
виходу газів, зменшення коксоутворення,
але водночас і до зменшення октанового
числа бензину. При надмірному підвищенні
температури посилюється коксоутворення
на каталізаторі, а також збільшується
вихід газів внаслідок проходження
реакцій гідрокрекінгу. Температура
сировини на вході в реактори регулюється
подачею палива в трубчату піч, де
підігрівається сировина.
Об’ємна
швидкість подачі сировини – це відношення
об’єму сировини, що подається в реактор
за одну годину до об’єму каталізатора,
який знаходить в зоні реакції. Зазвичай,
вона становить 1,0…2,0год –1.
Зменшення об’ємної швидкості сировини
при інших рівних умовах дає той самий
ефект, що і підвищення температури:
зменшення виходу каталізату, підвищення
його октанового числа, збільшення
виходу газу та коксу. Дуже низькі об’ємні
швидкості подачі сировини економічно
невигідні, оскільки при цьому значно
збільшуються розміри реакторів або
зменшується продуктивність установки.
Об’ємна швидкість сировини регулюється
кількістю сировини, що подається на
установку.
Тиск
в реакторах залежить від типу каталізатора
і складає до 4 МПа для алюмоплатинового
каталізатора та 1,5…2,0 МПа для бі- і
поліметалевих каталізаторів. При
підвищенні тиску різко знижується газо
- та коксоутворення. Водночас, збільшення
тиску сповільнює реакції ароматизації,
що призводить до зниження октанового
числа бензинів. Тиск в реакторах
регулюється автоматично клапаном, який
встановлюється на лінії виводу
газоподібних продуктів із реакторів.
Кратність
циркуляції ВВГ – це об’єм водневмісного
газу, що подається на одиницю об’єму
сировини за нормальних умов. Кратність
циркуляції ВВГ коливається в межах
900…1500 м3/м3.
Розбавлення парів сировини воднем
запобігає закоксовуванню каталізатора
і сприяє збільшенню тривалості роботи
каталізатора. З іншого боку, збільшення
кратності циркуляції ВВГ пов’язане
із зростанням енергетичних затрат на
експлуатацію установки реформінгу.
Кратність циркуляції ВВГ регулюється
об’ємом ВВГ, що додається до сировини.
Температурний
перепад по висоті реактора служить
характеристикою активності каталізатора.
По мірі відпрацювання каталізатора,
відкладенню коксу на ньому, зниженню
концентрацію водню у циркулюючому ВВГ
перепад температур по висоті реактора
зменшується. Перепад температури
підтримується в межах 10оС
і контролюється п’ятьма термопарами.
На
шарі каталізатора існує завжди перепад
тиску, який викликаний гідравлічним
опором каталізатора. Зменшення або
відсутність перепаду тиску свідчить
про те, що в шарі каталізатора утворилися
канали по яких рухаються пари
сиро-винно-водневої суміші. Ця суміш
проходить через каталізатор без суттєвої
зміни структури, що є небажаним. Перепад
тиску на каталізаторі контролюється
дифманометром.
За
допомогою термопар проводиться постійний
контроль температури стінок реактора.
Це пов’язано з тим, що при температурі
вище 260оС
водень починає розчинятися у металі і
змінює його структуру. Внаслідок цього
матеріал стінок реактора втрачає свої
початкові властивості і можливе
утворення мікротріщин, через які
проходить водневмісний газ.
Схема
лабораторної установки наведена на
рис.6.1. Установка складається з електричної
печі 1 для нагрівання сировини, куба 2,
ректифікаційної колонки з насадкою 3,
холодильника 4 для конденсації і
охолодження бензинових фракцій, збірника
5, резервної ємності 6, трансформатора
7 для регулювання нагріву печі,
трансформатора 8 для регулювання нагріву
ректифікаційної колонки, термопари 9
і потенціометра 10 для вимірювання
температури верху колонки.
Заливають
в куб 2 300мл бензину первинної перегонки
нафти. Поміщають куб в піч 1, подають
воду в холодильник 4 і включають
нагрівання печі та ректифікаційної
колонки 3, регулюючи інтенсивність
нагрівання трансформаторами 7 і 8.
По
мірі нагрівання куба і колонки легка
бензинова фракція випаровується; її
пари піднімаються вверх колонки.
Проходячи через холодильник 4, більш
важкі вуглеводні конденсуються і у
вигляді рідини (зрошення) повертаються
в колонку. Сконденсована і охолоджена
легка фракція стікає у збірник 5. Після
того, як потенціометр 10 покаже температуру
верху колонки 85оС,
закривають кран збірника 5 і зливають
легку фракцію п.к. – 85оС
у резервну ємність 6. Нагрівання куба
та колонки продовжують і в збірник 5
відбирають широку бензинову фракцію
85-180оС.
Коли температура верху колонки досягне
180оС,
виключають нагрівання куба і колонки.
Для цього встановлюють ручки на ЛАТРах
7 і 8 в положення “0”, опускають піч і
виключають установку. Легку і широку
бензинові фракції із збірника зливають
у мірні циліндри для визначення їх
об’єму. В кубі установки залишається
важка бензинова фракція 180оС
– к.к. Для одержаної сировини каталітичного
реформінгу (фракції 85-180оС)
визначають фракційний склад на апараті
Енглера (рис.5.2). Опис апарату Енглера
і методика визначення фракційного
складу бензину наведені в лабораторній
роботі №5.
1-
електрична піч; 2-куб; 3- ректифікаційна
колонка з насадкою; 4- холодильник; 5-
збірник; 6- резервна ємність; 7,8 –
трансформатори; 9- термопара; 10-
потенціометр
Рисунок
6.1 – Схема лабораторної установки
(АРН-2) для підготовки сировини до
каталітичного реформінгу
Об’єми
бензинових фракцій, одержаних на
лабораторній установці та фракційний
склад сировини каталітичного реформінгу
заносять в табл.6.1.
За фракційним
складом широкої бензинової фракції
роблять висновок про якість підготовки
сировини для реформінгу.
1.
Для чого призначений процес каталітичного
реформінгу? 2.
В чому полягає суть каталітичного
реформінгу? 3.
Наведіть основні реакції перетворення
вуглеводнів, які мають місце при
каталітичному реформінгу? 4.
Що використовуються в якості сировини
реформінгу? 5.
Назвіть продукти реформінгу і дайте
їх характеристику. 6.
Дайте характеристику промислових
каталізаторів реформінгу. 7.Як
впливає на процес реформінгу якість
сировини? 8.
Як впливає на результати реформінгу
температура входу сировини в реактори? 9.
Як впливає на процес реформінгу об’ємна
швидкість подачі сировини? Таблиця
6.1 – Дослідні дані
Взято сировини,мл
Одержано
бензинової фракції, мл
Фракційний
склад сировини реформінгу, оС
легкої
широкої
важкої
t
п.к.
t
10%
t
50%
t
90%
t
к.к.
10.
Як впливає на процес реформінгу тиск
в реакторі? 11.
Що таке кратність циркуляції ВВГ і як
вона впливає на процес реформінгу? 12.
Чому необхідно контролювати температуру
по висоті реактора? 13.
Чому необхідно контролювати перепад
тиску на каталізаторі? 14.
Чому необхідно контролювати температуру
стінок реактора? 15.
З яких конструктивних елементів
складається лабораторна установка для
підготовки сировини до реформінгу? 16.
Який порядок виконання роботи на
лабораторній установці підготовки
сировини до реформінгу? 17.
Якими показниками оцінюється якість
сировини каталітичного реформінгу в
лабораторній роботі?
Мета:
закріплення і поглиблення теоретичного
матеріалу з процесу карбамідної
депарафінізації; набуття експериментальних
навичок проведення карбамідної
депарафінізації дизельного палива на
лабораторній установці.
В результаті
виконання лабораторної роботи студент
повинен
знати:
-
призначення і суть процесу карбамідної
депарафінізації нафтопродуктів;
- характеристику
сировини і одержуваних продуктів;
-
опис технологічної схеми установки
карбамідної депарафінізації дизельного
палива;
-
параметри контролю і регулювання на
установці карбамідної депарафінізації;
вміти:
- оцінювати
результати проведення процесу на
лабораторній установці;
-
правильно вибирати необхідні параметри
для одержання якісних продуктів і в
заданій кількості.
Процес
карбамідної депарафінізації служить
для вилучення високоплавких твердих
парафінових вуглеводнів із дизельних
палив та олив з метою зниження їх
температури застигання.
Суть
процесу полягає в тому, що сировину
змішують з карбамідом (сечовиною),
етиловим спиртом і розчинником. Хімічна
формула карбаміду H2NCONH2.
За зовнішнім виглядом це білий
кристалічний порошок. В кожний кристал
карбаміду входить чотири молекули. При
цьому молекули орієнтовані так, що між
ними немає вільного простору. Така
структура кристалу називається
тетрагональною. При контакті зі спиртом
структура кристалу карбаміду змінюється
на гексагональну і між молекулами
утворюється канал діаметром 5…6А. В
утворенні канали заходять молекули
твердих парафінових вуглеводнів,
діаметри яких є меншими. Утворюється
комплексна сполука карбаміду з
парафіном. Розчинник додають для
зниження в’язкості реакційної суміші
і покращення контакту між сировиною
та карбамідом. В якості розчинника
використовуються легкий бензин,
дихлоретан та інші продукти. У подальшому
комплексна сполука відокремлюється
від депарафінізованого продукту і
розкладається гарячою водою. Парафіни,
які входять в комплексну сполуку легко
відокремлюються від водного розчину
карбаміду. Розчинник відганяється від
депарафінізованого продукту. На цьому
процес закінчується.
Сировиною
установки карбамідної депарафінізації
є фракції дизельного палива прямої
перегонки нафти або рафінати селективної
очистки олив.
Продуктами
установки є депарафінізоване дизельне
паливо, що використовується як компонент
зимового дизельного палива и(tзаст.<
-25oC)
або депарафінізована олива, що
направляється на доочистку та м’які
парафіни. Що використовуються як
сировина для одержання синтетичних
жирних спиртів і кислот. Їх, в свою
чергу, використовують для виробництва
миючих і поверхнево-активних речовин.
До
основних параметрів, що впливають на
якість і вихід продуктів карбамідної
депарафінізації відносяться: якість
сировини, склад і концентрація карбаміду,
співвідношення карбамід –сировина,
температура, склад і кількість активатора
та розчинника, час контакту сировини
з карбамідом.
Ефективність
карбамідної депарафінізації залежить
від фракційного і хімічного складів
сировини. Найкращою для процесу є
сировина з межами википання > 150oC
i < 420oC,
тобто гасові, дизельні фракції і фракція
легкої оливи парафінової основи.
Використання в якості сировини бензинової
фракції недоцільно тому, що в ній не
містяться парафінові вуглеводні з
кількістю атомів вуглецю 9 і з якими
карбамід утворює нестійкий комплекс.
Поганою є і дуже важка сировина. В ній,
як правило, знаходяться вуглеводні
ізобудови і ароматичні вуглеводні.
Розміри їх молекул більші діаметру
каналів в карбаміді і тому вони не
утворюють комплексної сполуки, а
залишаються в депарафінізаті. Крім
того, в такій сировині містяться
асфальто-смолисті речовини і сірчані
сполуки, які адсорбуються на поверхні
карбаміду та ізолюють канали від
сировини, в результаті чого утворення
комплексу погіршується. Фракційний
склад сировини контролюється на апараті
Енглера.
Карбамід
може використовуватися у кристалічному
вигляді або у вигляді насиченого водного
чи спиртового розчинів. У кристалічному
стані карбамід є більш активним і
дозволяє одержувати швидше і добре
промитий комплекс.
Оптимальне
співвідношення між карбамідом і
сировиною залежить від виду сировини.
Для депарафінізації легкої сировини
необхідно менше карбаміду, для важкої
– більше. Кратність карбамід-сировина
знаходиться в межах (0,7…1,2):1 для
реактивного і дизельного палив,
(1,0…3,0):1 для депарафінізації олив. При
збільшення карбаміду зростає кількість
вилученого парафіну із сировини,
температура застигання депарафінізату
знижується, але якість парафіну
погіршується із-за наявності в ньому
ароматичних вуглеводнів. Кратність
карбамід-сировина регулюється кількістю
сировини, що подається на установку.
Температура
процесу залежить від якості сировини,
а саме від її фракційного складу. При
збільшенні молярної маси і температурних
меж википання фракції температура
депарафінізації зростає. При цьому
зменшується в’язкість, покращується
контакт між карбамідом і сировиною,
але рівновага комплексоутворення
зсувається вліво. Тому температуру
процесу необхідно вибирати оптимальною,
яка сприяє максимальному виходу
депарафінізату з мінімальною температурою
застигання. При депарафінізації
реактивних і дизельних палив температура
підтримується в межах 20…35оС,
а при депарафінізації олив - +30…50оС.
При більших температурах починається
зворотній процес – руйнування комплексної
сполуки. При нижчих температурах,
внаслідок зростання в’язкості реакційної
суміші, сповільнюється швидкість
комплексоутворення. Крім того, для
охолодження продуктів необхідні
додаткові експлуатаційні витрати.
Температура реакційної суміші у
промислових умовах регулюється кількістю
холодоагента, що подається в холодильник,
через який циркулює реакційна суміш.
Активатор
послаблює зв’язки парафінів з іншими
вуглеводнями сировини, сприяє підвищенню
активності карбаміду за рахунок
перебудови кристалічної структури з
тетрагональної в гексагональну,
послаблює дію смолистих речовин. В
якості активатора використовуються
вода, спирти, кетони. Для реактивного
і дизельного палив кращим активатором
є етиловий і пропіловий спирти, для
олив - ацетон. Кількість активатора
складає 2…10% і залежить від складу
сировини і самого активатора.
Розчинник
покращує контакт реагуючих речовин,
знижуючи в’язкість нафтопродукту, а
також полегшує розділення депарафінізованого
продукту і комплексу. В якості розчинника
використовуються органічні речовини:
бензол, дихлоретан, бензин. Кількість
розчинника складе 10...30% і залежить від
виду сировини.
При
збільшенні часу контакту сировини з
карбамідом зростає ймовірність
проникнення твердих парафінів у канали
кристалів карбаміду. Час контакту
сировини і карбаміду складає 30-60хв та
залежить від виду сировини. Збільшення
часу їх контакту покращує якість
депарафінізату, але знижує продуктивність
установки. Утворенню комплексу сприяє
і перемішування реакційної суміші, яке
проводиться механічним способом.
Схема
лабораторної установки карбамідної
депарафінізації наведена на рис.7.1.
Установка складається з фарфорового
стакана 1, механічної мішалки 2, яка
з’єднана з електродвигуном 3, ЛАТРа 4
для регулювання обертів мішалки.
У
фарфоровий стакан 1 заливають 100г
сировини - фракції дизельного палива,
100г розчинника – бензину, 8мл активатора
– етилового спирту і засипають 75г
кристалічного карбаміду. Включають
мішалку 2 плавним поворотом ручки ЛАТРа
4 і перемішують реакційну суміш на
протязі 30хв при кімнатній температурі.
В процесі перемішування суміші
утворюється комплекс карбаміду з
твердими парафіновими вуглеводнями.
Після цього мішалку виключають. Для
відокремлення комплексу від рідких
продуктів суміш із стакана 1 виливають
у фільтрувальну лійку 5, яка з’єднана
корком із конічною плоскодонною колбою
8. Для відсмоктування рідкої фази колбу
під’єднують до вакуум-насоса. Комплексну
сполуку 6, яка залишилася на фільтрі
промивають розчинником для вилучення
з її поверхні залишків сировини. Комплекс
переносять у склянку і заливають 200мл
гарячої води, яка нагріта до температури
80…90оС.
Комплекс при цьому руйнується і парафіни
спливають вверх. Відокремлення парафінів
від водного розчину карбаміду проводиться
у ділильній лійці. Водний розчин
карабміду зливають у склянку, а пізніше
в каналізацію. Парафіни 7 зливають у
колбу ємністю 50мл і зважують. Рідкі
продукти з конічної колби переливають
у круглодонну колбу з відростком
установки, схема якої наведена на
рис.4.2. Бензин відганяють до температури
180оС.
Після відгонки активатора і розчинника
депарафінізат охолоджують і зважують.
1
- фарфоровий стакан; 2 - механічна мішалка;
3 - електродвигун; 4-ЛАТР; 5 - лійка для
фільтрування; 6 - комплекс; 7 - парафіни;
8-фільтрат;9-штатив
Рисунок
7.1 – Лабораторне устаткування для
карбамідної депарафінізації
Визначають
температури застигання сировини і
одержаного депарафінізату на установці
7.2. Для цього паливо заливають у пробірку
1 з подвійними стінками до мітки 2.
Пробірку закривають корком 5, в якому
закріплені термометр 3 і дротяна мішалка
4. Пробірку з паливом встановлюють в
охолоджуючу суміш, яка складається з
льоду (снігу) і хлориду натрію (калію)
у співвідношенні 2:1. Починають випробування
при безперервному перемішуванні палива
мішалкою. Через кожні 5оС
зниження температури палива проводять
спостереження за його станом. Для цього
швидко виймають пробірку і дивляться
на світло чи не помутніло паливо. Коли
досліджуване паливо помутніє, виймають
з пробірки мішалку і продовжують
випробування до застигання палива.
Пробірку з паливом виймають періодично
з охолоджуваної суміші (з інтервалом
2оС
зниження температури), нахиляють її на
45о
і дивляться чи не змінився меніск палива
на протязі 1хв. Якщо меніск не змістився,
то фіксують температуру і на цьому
закінчують випробування. Якщо ж меніск
палива змістився, то знову вставляють
пробірку в охолоджуючу суміш і продовжують
дослідження до моменту застигання
палива.
Результати
зважування парафіну і депарафінованого
дизельного палива та значення температур
застигання сировини і депарафінізату
заносять в табл.7.1. За матеріальним
балансом, температурами застигання
сировини і продукту роблять висновок
про ефективність проведення процесу
карбамідної депарафінізації дизельного
палива.
1-пробірка з
подвійними стінками; 2-кільцева мітка;
3-термометр; 4-дротяна мішалка; 5-корок
Рисунок 7.2 – Прилад
для визначення температури застигання
дизельного палива
1
Для чого призначений процес карбамідної
депарафінізації? 2
В чому полягає суть комплексоутворення? 3
Назвіть сировину і продукти карбамідної
депарафінізації і дайте їх характеристику. 4
Як на процес депарафінізації впливає
якість сировини? 5
Що представляє собою карбамід і в якому
вигляді він може використовуватися в
процесі? 6
Як на результат депарафінізації впливає
співвідношення карбамід-сировина? 7
Що використовується в якості активатора
і яка його роль при депарафінізації? 8
Які речовини використовуються в якості
розчинника і яка його роль у процесі
депарафінізації? Таблиця
7.1 – Результати досліду
Взято: Одержано: Температура
застигання, оС
сировини
депарафі-нізату
парафінів
втрати
сировини
депарафіні-зату г % г % г % г %
9
Як впливає на процес депарафінізації
температура? 10
Як впливає на процес депарафінізації
час контакту сировини з карбамідом? 11
З яких конструктивних елементів
складаються установки для проведення
процесу, відокремлення та розкладання
комплексу і відгонки розчинника? 12
Який порядок виконання лабораторної
роботи з процесу карбамідної
депарафінізації? 13
Як проводиться визначання температури
застигання сировини і депарафінізату? 14
Якими показниками оцінюється ефективність
процесу карбамідної депарафінізації?
Лабораторний практикум
Івано-Франківськ
1 Загальні положення
2 Основні правила техніки безпеки
3 Звіт з роботи
4 Рекомендована література
Лабораторна робота №1 Абсорбція аміаку водою
Мета і задачі роботи
Теоретичні основи
1.2.1 Призначення і суть процесу
1.2.2 Параметри, які впливають на абсорбцію
Опис лабораторної установки
Порядок виконання роботи
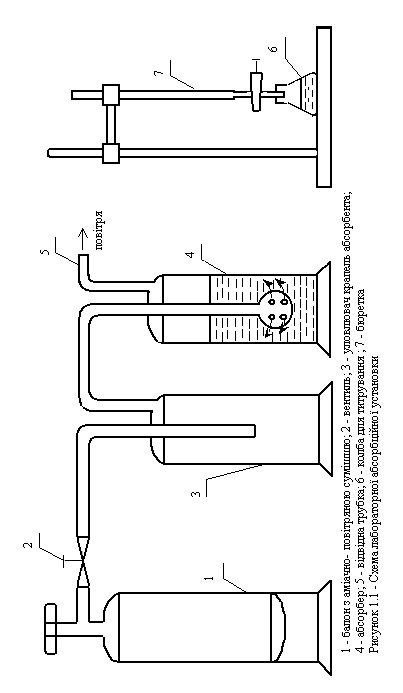
1.5 Обробка результатів досліду
![]() ,
(1.2)
,
(1.2)![]() - нормальність розчину кислоти;
- нормальність розчину кислоти;![]() - об’єм кислоти, що пішов на титрування,
мл;
- об’єм кислоти, що пішов на титрування,
мл;![]() - об’єм нашатирного спирту, взятого
для титрування, мл.
- об’єм нашатирного спирту, взятого
для титрування, мл.![]() ,
(1.3)
,
(1.3)![]() -
молярна маса нашатирного спирту, г/моль;
1000 – об’єм води, необхідний для
приготування 0,1н розчину нашатирного
спирту, мл.
-
молярна маса нашатирного спирту, г/моль;
1000 – об’єм води, необхідний для
приготування 0,1н розчину нашатирного
спирту, мл.
1.6 Контрольні питання
Лабораторна робота №2 Адсорбційна очистка олив
2.1 Мета і задачі роботи
2.2 Теоретичні основи
2.2.1 Призначення і суть процесу

2.2.2 Параметри, які впливають на адсорбцію
2.3 Опис лабораторної установки
2.4 Порядок виконання роботи

2.5 Обробка результатів досліду
![]() ,
(2.1)
,
(2.1)![]() -
кінематична в’язкість оливи при заданій
температурі t,
сСт (мм2/с);
с-стала віскозиметра, мм2/с2;
-
кінематична в’язкість оливи при заданій
температурі t,
сСт (мм2/с);
с-стала віскозиметра, мм2/с2;
![]() -
час витікання певного об’єму оливи
через капіляр віскозиметра, с.
-
час витікання певного об’єму оливи
через капіляр віскозиметра, с.
![]() та кінематичною в’язкістю
та кінематичною в’язкістю
![]() неочищеної і очищеної оливи роблять
висновок про ефективність процесу
адсорбції.
неочищеної і очищеної оливи роблять
висновок про ефективність процесу
адсорбції.2.6 Контрольні питання
Лабораторна робота №3 Ректифікація бінарної суміші
3.1 Мета і задачі роботи
3.2 Теоретичні основи
3.2.1 Призначення і суть процесу ректифікації
![]() .
Пари дистиляту конденсуються та
охолоджуються в холодильнику-конденсаторі
ХК-1 і відокремлюються від повітря в
сепараторі С-1. Частина дистиляту в
кількості g повертається в колону на
першу тарілку в якості гострого зрошення.
.
Пари дистиляту конденсуються та
охолоджуються в холодильнику-конденсаторі
ХК-1 і відокремлюються від повітря в
сепараторі С-1. Частина дистиляту в
кількості g повертається в колону на
першу тарілку в якості гострого зрошення.
![]() відкачується
з низу колони К-1 насосом Н-2. І так,
вирішена технологічна задача –
суміш(сировина), розділена на компоненти:
н.к.к. у вигляді парів дистиляту відведений
з верху колони, а в.к.к. у вигляді залишку
відведений з низу колони.
відкачується
з низу колони К-1 насосом Н-2. І так,
вирішена технологічна задача –
суміш(сировина), розділена на компоненти:
н.к.к. у вигляді парів дистиляту відведений
з верху колони, а в.к.к. у вигляді залишку
відведений з низу колони.
3.2.2 Параметри, які впливають на ректифікацію
3.3 Опис лабораторної установки
3.4 Порядок виконання роботи

3.5 Обробка результатів досліду
![]() і бензолу
і бензолу
![]() ,
а також дистиляту
,
а також дистиляту
![]() і залишку
і залишку
![]() ;
на осі абсцис – вміст гексану у
%об.(рис.3.4). Показники заломлення чистих
компонентів суміші з’єднують прямою
лінією. Зі значень
;
на осі абсцис – вміст гексану у
%об.(рис.3.4). Показники заломлення чистих
компонентів суміші з’єднують прямою
лінією. Зі значень
![]() і
і
![]() проводять
горизонталі до перетину з цією лінією.
З точок перетину 1 і 2 опускають
перпендикуляри на вісь абсцис і одержують
вміст гексану в залишку
проводять
горизонталі до перетину з цією лінією.
З точок перетину 1 і 2 опускають
перпендикуляри на вісь абсцис і одержують
вміст гексану в залишку
![]() та дистиляті
та дистиляті
![]() .
Одержані значення показників заломлення
і склади продуктів заносять в таблицю
3.1.
.
Одержані значення показників заломлення
і склади продуктів заносять в таблицю
3.1.![]() і залишку
і залишку
![]() графічним методом визначають теоретичну
і фактичну кількість тарілок в
експериментальній колоні. Графічний
метод визначення теоретичної кількості
тарілок в колоні наведений на рис.3.5.
Спочатку будують криву рівноваги фаз
за рівноважними концентраціями парової
і рідкої фаз. Пізніше будують робочі
лінії верху і низу колони. Координати
т.К(
графічним методом визначають теоретичну
і фактичну кількість тарілок в
експериментальній колоні. Графічний
метод визначення теоретичної кількості
тарілок в колоні наведений на рис.3.5.
Спочатку будують криву рівноваги фаз
за рівноважними концентраціями парової
і рідкої фаз. Пізніше будують робочі
лінії верху і низу колони. Координати
т.К(![]() )
і т.L(
)
і т.L(![]() )
для побудови робочої лінії верху колони.
Координати т.М (
)
для побудови робочої лінії верху колони.
Координати т.М (![]() ),
а т.S знаходиться на перетині ординати
),
а т.S знаходиться на перетині ординати
![]() з робочою лінією верху колони . З’єднують
точки М і S та одержують лінію концентрації
низу колони. Між кривою рівноваги фаз
і лініями концентрації верху і низу
колони проводять ступінчату лінію,
починаючи від т.К і закінчуючи т.М.
Кількість горизонтальних площадок
дорівнює кількості теоретичних тарілок
в колоні. Фактична кількість тарілок
в колоні визначається за формулою:
з робочою лінією верху колони . З’єднують
точки М і S та одержують лінію концентрації
низу колони. Між кривою рівноваги фаз
і лініями концентрації верху і низу
колони проводять ступінчату лінію,
починаючи від т.К і закінчуючи т.М.
Кількість горизонтальних площадок
дорівнює кількості теоретичних тарілок
в колоні. Фактична кількість тарілок
в колоні визначається за формулою:![]() ,
(3.1)
,
(3.1)![]() -
теоретична кількість тарілок в колоні,
шт;
-
теоретична кількість тарілок в колоні,
шт;
![]() -
коефіцієнт корисної дії тарілки (для
більшості тарілок
-
коефіцієнт корисної дії тарілки (для
більшості тарілок
![]() =
0,5).
=
0,5).
![]()

3.6 Контрольні питання
Лабораторна робота №4 Екстракція бензолу етиленгліколем
4.1 Мета і задачі роботи
4.2 Теоретичні основи
4.2.1 Призначення і суть процесу
4.2.2 Методи екстракції

4.2.3 Параметри, які впливають на процес
![]() (4.1)
(4.1)4.3 Опис лабораторної установки
4.4 Порядок виконання роботи
4.5 Обробка результатів досліду
![]()

4.6 Контрольні питання
Лабораторна робота №5 Каталітичний крекінг
5.1 Мета і задачі роботи
5.2 Теоретичні основи
5.2.1 Призначення, суть і механізм процесу
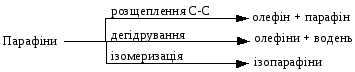

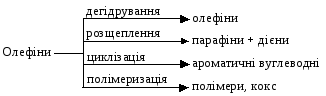
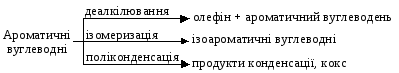
5.2.2 Сировина і одержувані продукти
5.2.3 Каталізатор
5.2.4 Параметри, що впливають на процес
5.2.4.1 Якість сировини
5.2.4.2 Температура в реакторі
5.2.4.3 Час контакту сировини і каталізатора
5.2.4.4 Кратність циркуляції каталізатора
5.2.4.5 Тиск в реакторі
5.3 Опис лабораторної установки
5.4 Порядок виконання роботи

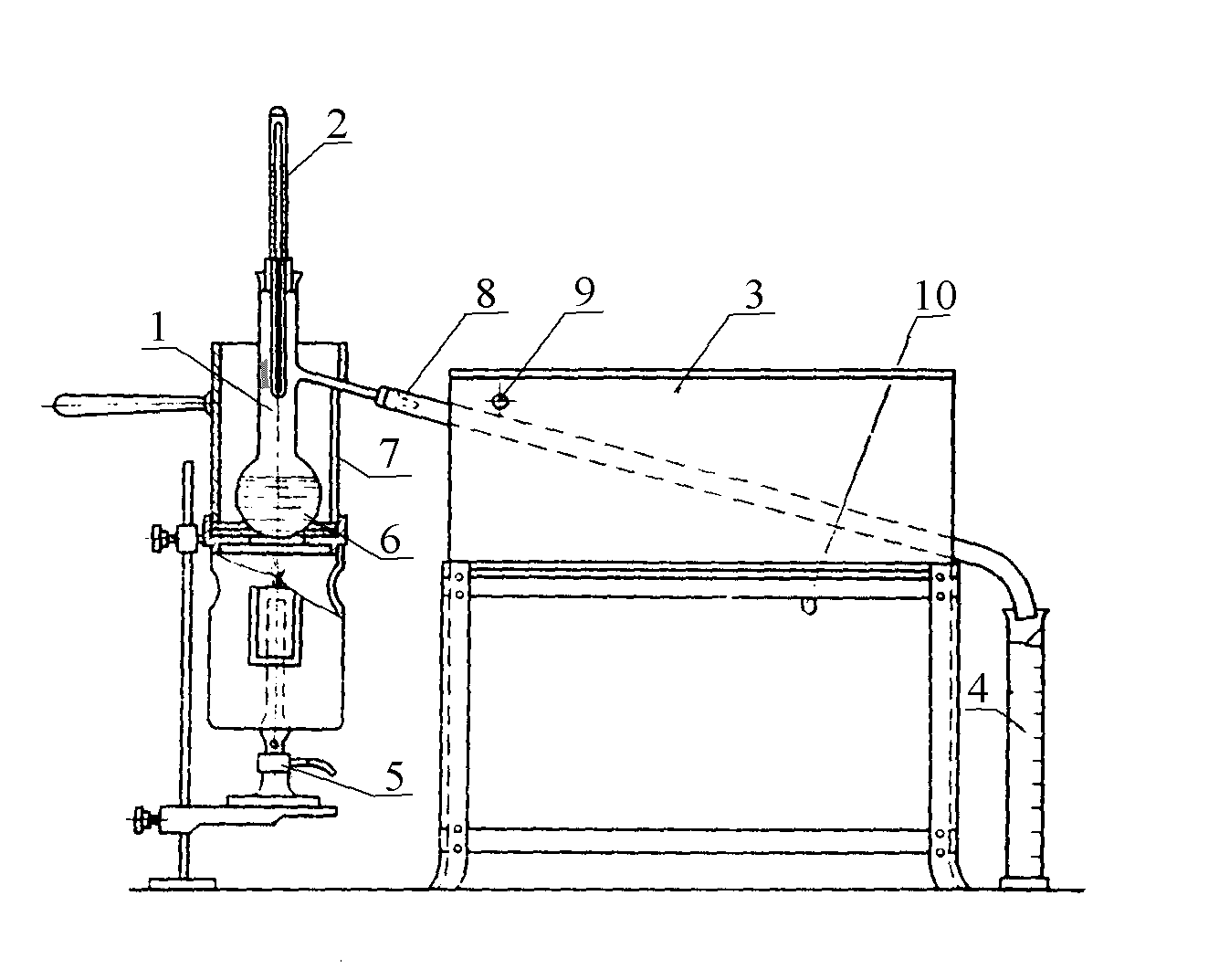
5.5 Обробка результатів
5.6 Контрольні питання
Лабораторна робота №6 Підготовка сировини до каталітичного реформінгу
6. 1 Мета і задачі роботи
6.2 Теоретичні основи
6.2.1 Призначення, суть і хімізм процесу
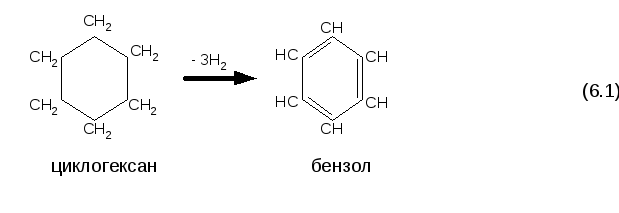
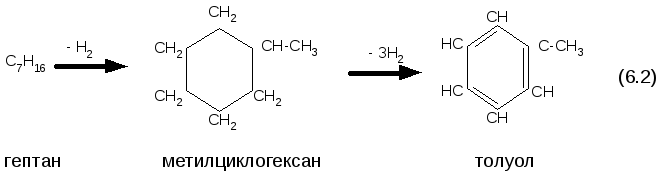
![]() СН3
– СН – СН2
–СН3
(6.3)
СН3
– СН – СН2
–СН3
(6.3)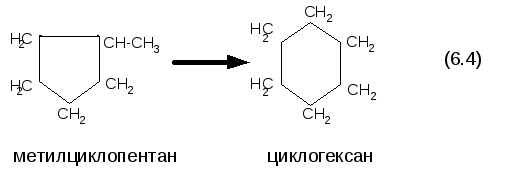
![]() С3Н8
+ С5Н12
(6.5)
С3Н8
+ С5Н12
(6.5)6.2.2 Сировина і одержувані продукти
![]() %мас.
і азоту
%мас.
і азоту
![]() %
мас. Тому сировину перед реформінгом
направляють попередньо на гідроочищення
від гетероорганічних сполук.
%
мас. Тому сировину перед реформінгом
направляють попередньо на гідроочищення
від гетероорганічних сполук.
6.2.3 Каталізатори
![]() ,
який має кислотні функції та нанесених
на нього одного чи декількох активних
елементів (
,
який має кислотні функції та нанесених
на нього одного чи декількох активних
елементів (![]() тощо)
з гідруючо-дегідруючими властивостями.
Активність носія підсилюють шляхом
підведення до його поверхні галогеновмісних
сполук (
тощо)
з гідруючо-дегідруючими властивостями.
Активність носія підсилюють шляхом
підведення до його поверхні галогеновмісних
сполук (![]() ).
Вміст гідруючих компонентів на поверхні
носія складає 0,5…0,8%мас.
).
Вміст гідруючих компонентів на поверхні
носія складає 0,5…0,8%мас.
![]() ).
Ці каталізатори (КР-108, КР-110) мають
найвищу активність та стабільність
(на протязі 6…7років). Крім цього, перехід
від моно- до бі – і поліметалевих
каталізаторів дозволив дещо знизити
температуру та суттєво зменшити тиск
цього процесу, що привело до зменшення
енергетичних затрат на експлуатацію
промислових установок каталітичного
реформінгу.
).
Ці каталізатори (КР-108, КР-110) мають
найвищу активність та стабільність
(на протязі 6…7років). Крім цього, перехід
від моно- до бі – і поліметалевих
каталізаторів дозволив дещо знизити
температуру та суттєво зменшити тиск
цього процесу, що привело до зменшення
енергетичних затрат на експлуатацію
промислових установок каталітичного
реформінгу.
6.2.4 Параметри, що впливають на процеси
6.2.4.1 Якість сировини
6.2.4.2 Температура на вході в реактори
6.2.4.3 Об’ємна швидкість подачі сировини
6.2.4.4 Тиск в реакторах
6.2.4.5 Кратність циркуляції водневмісного газу
6.2.4.6 Перепад температури по висоті реактора
6.2.4.7 Перепад тиску на каталізаторі
6.2.4.8 Температура стінок реактора
6.3 Опис лабораторної установки
6.4 Порядок виконання роботи

6.5 Обробка результатів досліду
6.6 Контрольні питання
Лабораторна робота №7 Карбамідна депарафінізація дизельного палива
7.1 Мета і задачі роботи
7.2 Теоретичні основи
7.2.1 Призначення і суть процесу
7.2.2 Сировина і одержувані продукти
7.2.3 Параметри, що впливають на процес
7.2.3.1 Якість сировини
7.2.3.2 Склад і концентрація карбаміду
7.2.3.3 Співвідношення карбамід-сировина
7.2.3.4 Температура
7.2.3.5 Склад і кількість активатора та розчинника
7.2.3.6 Час контакту сировини з карбамідом
7.3 Опис лабораторної установки
7.4 Порядок виконання роботи

7.5 Обробка результатів досліду

7.6 Контрольні питання
60
59
3 58
4 57
5 56
6 55
7 54
8 53
9 52
10 51
11 50
12 49
13 48
14 47
15 46
16 45
17 44
18 43
19 42
20 41
21 40
22 39
23 38
24 37
25 36
26 35
27 34
28 33
29 32
30 31
