
- •Валентные состояния атомов углерода (sp3-, sp2- и sp-гибридизация). Образование σ- и π-связей. Тип гибридизации и геометрия молекул.
- •2. Оценка распределения электронной плотности в молекулах органических веществ. Способы передачи электронного влияния атомов (±I и ±m-эффекты).
- •3. Реагенты, субстраты, свободные радикалы, электрофилы и нуклеофилы. Классификация органических реакций:
- •4.Структурная и пространственная изомерия органических веществ.
- •5.Алканы и алкены. Сравнительная характеристика строения и свойств.
- •5) Полимеризация алкенов и их производных в присутствии кисло протекает по механизму ае:
- •6.Электронное строение бензола. Раскройте значение термина «ароматические свойства».
- •7.Влияние ориентантов I и II рода на протекание реакций sе.
- •12.Углеводы. Опишите строение моносахаридов, восстанавливающих и невосстанавливающих дисахаридов, таких полисахаридов как крахмал, гликоген, клетчатка. Расскажите о роли углеводов в живой природе.
- •13.Нуклеиновые кислоты. Общая характеристика днк и рнк, особенности строения и биологическая роль. Репликация днк. Передача генетической информации (транскрипция) и синтез белков (трансляция).
-
Валентные состояния атомов углерода (sp3-, sp2- и sp-гибридизация). Образование σ- и π-связей. Тип гибридизации и геометрия молекул.
Атом С им-т заряд +6.
1s22s22px12py12pz0
Возбужденный углерод: 1s22s12px12py12pz1
Гибридизация – явление взаимод-я м\у собой молекулярных орбиталей, близких по энергии и имеющих общие элементы симметрии, с обр-ем гибридных орбиталей с более низкой энергией.
sp3-гибридизация(1 валентное состояние углерода): харак-на для гомологического ряда метана.
 Угол
109,28.
Угол
109,28.
σ-связи м\у углеродом и водородом обр-ны sp3-гибридными облаками углерода и облаками водорода. Главное отличие σ-связей от др состоит в том,что перекрывание орбиталей осущ-ся вдоль линии,соединяющей ядра атомов.
sp2-гибридизация (2 валентное состояние атома углерода):обр-ся при взаимод-и двух р-орбиталей (рx и py) и s-орбитали, причем образовавшиеся sp2-орбитали лежат в одной плоскости и обр-т угол 120°. Харак-на для гомологического ряда этилена.
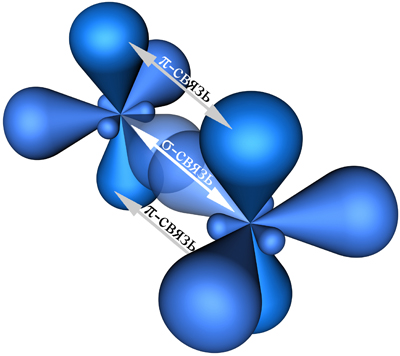
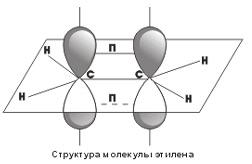
Двойная связь обр-на гибридизованными sp2-орбиталями, а п-связь обр-на негибридизованными р-орбиталями.
sp-гибридизация (3 валентное состояние атома углерода): обр-ся при взаимод-и s-орбитали с px-орбиталью.
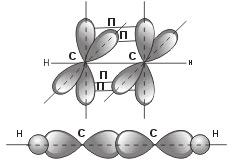
Для sp-гибридизации хар-на линейная ориентация молекулярных орбиталей. Хар-на для гомолог-го ряда ацетилена. σ-связь обр-на гибридным sp-облаком углерода в одной плоскости, а 4 p-электронных облака обр-т две п-связи во взаимоперпендикулярных плоскостях.
2. Оценка распределения электронной плотности в молекулах органических веществ. Способы передачи электронного влияния атомов (±I и ±m-эффекты).
Все составляющие молекулу атомы нах-ся во взаимосвязи и испытывают взаимное влияние. Это влияние передается, в основном, ч\з систему ковалентных связей, с пом\ю т.н. электронных эффектов. Электронными эффектами наз-т смещение электронной плотности в мол-ле под влиянием заместителей.
Атомы, связанные полярной связью, несут частичные заряды, обозначаемые греческой буквой "дельта" (δ). Смещение электронной плотности по цепи простых С-С связей наз-ся индуктивным эффектом и обозначается I.
Индуктивный эффект передается по цепи с затуханием. Направление смещения электронной плотности всех s -связей обозначается прямыми стрелками.
В завис-ти от того, удаляется ли электронная плотность от рассматриваемого атома углерода или приближается к нему, индуктивный эффект называют отрицательным (-I) или положительным (+I). Знак и величина индуктивного эффекта определяются различиями в электроотрицательности между рассматриваемым атомом углерода и группой, его вызывающей.
Атом, "оттягивающий" электронную плотность s-связи в свою сторону, приобретает отрицательный заряд δ-. При рассмотрении пары атомов, связанных ковалентной связью, более электроотрицательный атом, оттягивающий на себя атомы наз-ют акцептором, он обладает отрицательным индуктивным эффектом. Его партнер по s-связи соответственно будет иметь равный по величине дефицит электронной плотности, т.е. частичный положительный заряд δ+, будет наз-ся донором, обладает положительным индуктивным эффектом.
+I-эффект проявляют алифатические углеводородные радикалы, т.е. алкильные радикалы (метил, этил и т.д.). Большинство функциональных групп проявляют -I-эффект: галогены, аминогруппа, гидроксильная, карбонильная, карбоксильная группы.
Индуктивный эффект проявляется и в случае, когда связанные атомы углерода различны по состоянию гибридизации.
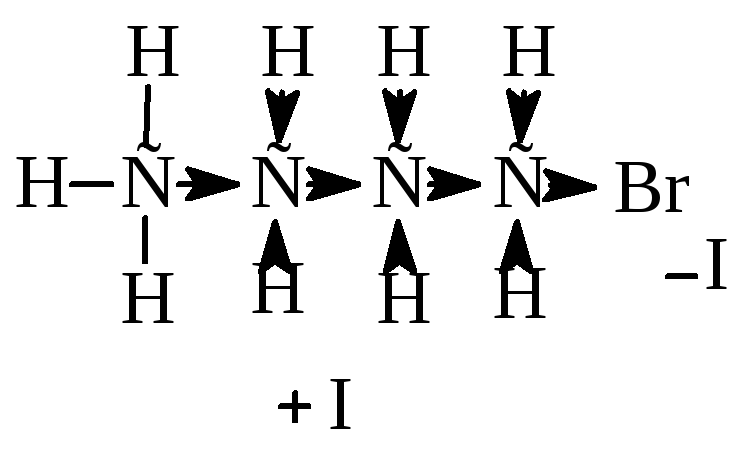
Влияние заместителя на распределение электронной плотности, передаваемое по p-связям, называют мезомерным эффектом (М). Мезомерный эффект также может быть отрицательным и положительным. В структурных формулах его изображают изогнутой стрелкой, начинающейся у центра электронной плотности и завершающейся в том месте, куда смещается электронная плотность.
Сопряжение-явление обр-я з-электронного облака, общего для 3 или более С атомов.

