
- •Рибосома
- •Биосинтез белка это центральный процесс живой клетки: именно через него « мертвые «
- •Общая схема биосинтеза белков в клетке (ДНК—РНК— белок ).
- •Т Р А Н С К Р И П Ц И Я: Отдельные
- •АКТИВИРОВАНИЕ И АКЦЕПТИРОВАНИЕ АМИНОКИСЛОТ
- •Т Р А Н С Л Я Ц И Я : Рибосомы являются
- •Формирование функционального белка : По мере синтеза полипептидной цепи она частично высовывается из
- •Рибосома это компактная частица,
- •Методом рассеяния нейтронов установлено, что каждая рибосомная субчастица содержит одну молекулу высокополимерной рибосомной
- •Рибосому разделяет борозда, которая сильно расширяется в одном месте, обнажая « глаз» рибосомы.
- •Обе « шеи» находятся напротив друг друга
- •Центр Р рибосомы занимает пептидил-тРНК, и рибосома может связывать молекулу аминоацил-тРНК, соответствующую кодону,
- •В итоге А-участок освобождается, и в нем
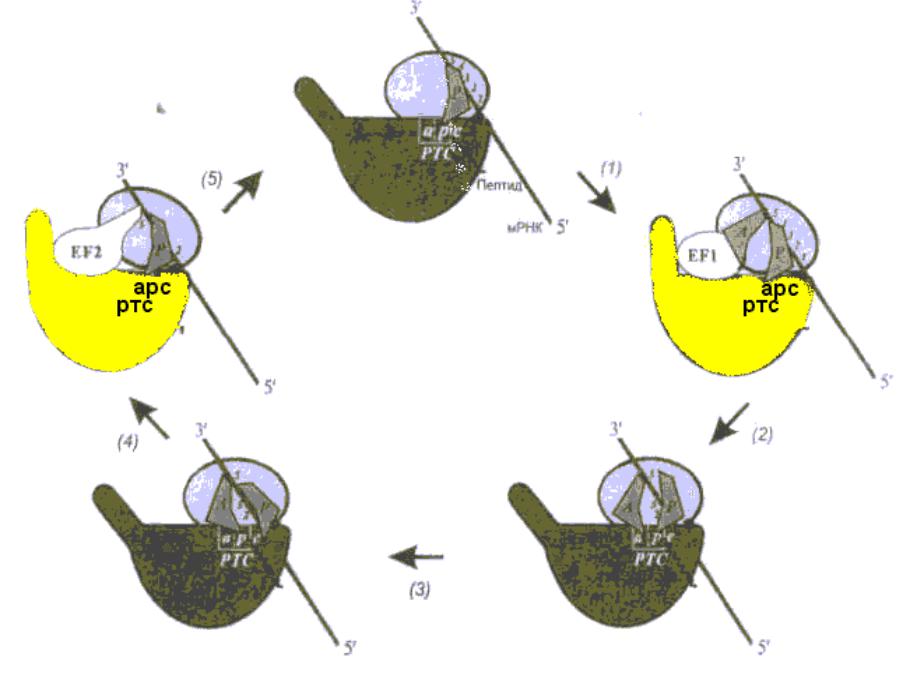
- •Цикл Элонгации в рибосоме рассматривается с точки зрения модели смыкания- размыкания (1),
- •Реакция транспептидации происходит в « закрытой « рибосоме между группами двух субстратов- пептидил—тРНК
- •Антибиотики- вещества, синтезируемые микроорганизмами и подавляющие размножение бактерий, других микробов, а также вирусов
- •Интеркаляторы такие как рифамицин, рубомицин и актиномицин D встраиваются в двойную спираль ДНК,
- •Эритромицин нарушает нормальную функцию большой рибосомной субцастицы. Хлорамфеникол- является одним из немногих природных

Рибосому разделяет борозда, которая сильно расширяется в одном месте, обнажая « глаз» рибосомы. Эта особенность отражает реальный факт существования полости между рибосомными субчастицами. Именно в этой полости размещаются основные субстраты рибосомы—молекулы пептидил-тРНК и аминоацил-тРНК, участвующие в образовании полипептидной цепи. Это –тРНК—связывающий центр рибосомы.
Малая субъединица рибосомы имеет « головку» и « тело»., образуемые глубокой бороздой. Последняя выполняет функцию « шеи « -- место, в котором размещается участок связывания мРНК и через которое цепь протягивается от одного конца к другому. У большой рибосомной субцастицы в « шее « размещается главный каталитический центр

Обе « шеи» находятся напротив друг друга
имежду ними располагается «глаз». Важной характерной чертой рибосомы
является подвижный палочкообразнвй выступ большой субъединицы, справа от «головки».
Генетические функции малой рибосомной субчастицы:
Именно малая субъединица рибосомы, и только она, связывается с мРНК, т.е. служит первичным приемником генетической информации для белок- синтезирующего аппарата. Удержание мРНК на рибосоме есть функция малой субчастицы, в то время как большая в
этом не участвует.


Центр Р рибосомы занимает пептидил-тРНК, и рибосома может связывать молекулу аминоацил-тРНК, соответствующую кодону, установленному в данный момент в А-участке..
( шаг I ).
В результате удерживаемая рибосомой пептидил-тРНК и вновь связанная аминоацил- тРНК, оказываются в рибосоме в состоянии – бок— о -- бок ( состояние II ). Рибосома катализирует р-цию транспептидации между двумя субстратами рибосомы—пептидил-тРНК и аминоацил –тРНК: пептидильный остаток переносится от « своей» тРНК на аминогруппу аминоацил-тРНК, удлиняясь на одну аминокислоту с С-конца. ( шаг II). В Р-участке осталась деацилированная тРНК, а в А- участке помещается остаток тРНК, удлиненной пептидил-тРНК
( состояние III ). Деацилированная тРНК

В итоге А-участок освобождается, и в нем
устанавливается следующий кодон мРНК. Цикл завершен.
Факторы элонгации FЕ-1 и ЕF-2.
Таким образом, большая субъединица рибосомы выступает как фермент, ответственный за образование пептидных связей. Это главная энзиматическая функция рибосомы. В рибосоме есть четкое разделение труда: малая субъчастица выполняет генетические функции, являясь ответственной за прием и декодирование генетической
информации. Большая частица участвует в энзиматических реакциях в процессе

Цикл Элонгации в рибосоме рассматривается с точки зрения модели смыкания- размыкания (1),
а фактор элонгации ЕF- 1 с ГТФ открывает рибосому. (2) После расщепления ГТФ, фактор элонгации ЕF-1 покидает рибосому, а аминоацильный конец-тРНК взаимодействует с пептидил- трансферазным центром большой субчастицы, и способствует смыканию субчастиц и запиранию рибосомы. (3)

Реакция транспептидации происходит в « закрытой « рибосоме между группами двух субстратов- пептидил—тРНК и аминоацил —тРНК. (4).Размыкание пре- транслокационной рибосомы промотируется фактором элонгации ЕF-2 с ГТФ. Это приводит к выходу деацилированной тРНК и смещению остатка тРНК молекулы пептидил-тРНК вместе с мРНК. (5) Гидролиз ГТФ и уход фактора элонгации ЕF-2 снова дает возможность рибосоме сомкнуться. В ходе элонгационного цикла рибосома осциллирует между сомкнутым и разомкнутым состояниями.

Антибиотики- вещества, синтезируемые микроорганизмами и подавляющие размножение бактерий, других микробов, а также вирусов и клеток. Большинство антибиотиков продуцируются микроорганизмами из рода актиномицетов ( Streptomyces sp. ) и определенными грибами. Однако существуют и синтетические антимикробные вещества, такие как сульфаниламиды и ингибиторы гираз.

Интеркаляторы такие как рифамицин, рубомицин и актиномицин D встраиваются в двойную спираль ДНК, таким образом препятствуя репликации и транскрипции. Интеркаляторы токсичны и для эукариот, поэтому их применение в качестве цитостатиков ограниченно. Синтетические ингибиторы ДНК- топоизомераз, так называемые –Ингибиторы гираз воздействуют на репликацию, и тем самым подавляет репродукцию бактерий. К ингибиторам трансляции относится большая группа антибиотиков, воздействующих на рибосому ( Аминогликозиды, Тетрациклины, Эритромицин, Пуромицин, Хлорамфеникол). Тетрациклины- антибиотики широкого спектра действия. Аминогликозиды, воздействуют на все фазы трансляции.
