- •Управляемая самостоятельная работа студентов
- •Содержание
- •Введение
- •1.Биосинез гистидина
- •2.Пути обмена гистидина
- •4.Использование гистидина как радиопротектора и антиоксиданта.
- •4.1 Использование гистидина как радиопротектора
- •4.2 Использование гистидина как антиоксиданта.
- •5.Биосинтез аргинина
- •6.Основные пути обмена аргинина. Биологическое значение
- •Заключение
- •Лист для замечаний Литература
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ БЕЛАРУСЬ
УЧРЕЖДЕНИЕ ОБРАЗОВАНИЯ
«ГОМЕЛЬСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ»
Кафедра общей, биоорганической и биологической химии
Управляемая самостоятельная работа студентов
по теме:
«. Гистидин и аргинин. Биосинтез, основные пути обмена, их биологическая роль».
Выполнила студентка группы Л-231
Повчиник Дарья Анатольевна Проверил преподаватель
Ассистент кафедры
Скрыпникова Любовь Петровна
Гомель, 2018
Содержание
1.Биосинез гистидина 3
1.2.Пути обмена гистидина 7
4.Использование гистидина как радиопротектора и антиоксиданта. 9
4.1 Использование гистидина как радиопротектора 9
4.2 Использование гистидина как антиоксиданта. 10
5.Биосинтез аргинина 11
6.Основные пути обмена аргинина. Биологическое значение 13
Заключение 15
Лист для замечаний 16
Литература 17
Введение
Гистиди́н
(L-α-амино-β-имидазолилпропионовая
кислота) — гетероциклическая
альфа-аминокислота, одна из 20 протеиногенных
аминокислот. По современным представлениям
также является незаменимой кислотой
как для детей, так и для взрослых. 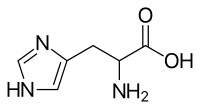
Остаток гистидина входит в состав активных центров множества ферментов. Гистидин является предшественником в биосинтезе гистамина. Одна из незаменимых аминокислот, способствует росту и восстановлению тканей. В большом количестве содержится вгемоглобине; используется при лечении ревматоидных артритов, язв и анемии. Недостаток гистидина может вызвать ослабление слуха.
Гистидином богаты такие продукты как тунец, лосось, свиная вырезка, говяжье филе, куриные грудки, соевые бобы, арахис, чечевица. Кроме того, гистидин включается в состав многих витаминных комплексов и некоторых иных медикаментов.
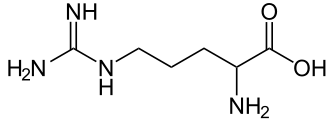
Аргини́н (2-амино-5-гуанидинпентановая кислота) — алифатическая основная α-аминокислота. Оптически активна, существует в виде L- и D- изомеров. L-Аргинин входит в состав пептидов и белков, особенно высоко содержание аргинина в основных белках — гистонах и протаминах (до 85 %). Новое исследование позволяет предположить, что чрезмерное потребление аргинина иммунными клетками, которые обычно защищают мозг, является причиной возникновения болезни Альцгеймера
Аргинин — частично-заменимая аминокислота. У взрослого и здорового человека аргинин вырабатывается организмом в достаточном количестве. В то же время, у детей и подростков, у пожилых и больных людей уровень синтеза аргинина часто недостаточен. Биосинтез аргинина осуществляется из цитруллина под действием аргининсукцинатсинтазы и аргининсукцинатлиазы.
Аргинин является одним из ключевых метаболитов в процессах азотистого обмена (орнитиновом цикле млекопитающих и рыб).
Аргинин является субстратом NO-синтаз в синтезе оксида азота NO, являющегося локальным тканевым гормоном с множественными эффектами — от противоспалительного до сосудистых эффектов и стимуляции ангиогенеза.
1.Биосинез гистидина
Все сведения о биосинтезе гистидина почерпнуты из опытов на микроорганизмах. Броквист и Снелл доказали, что различные бактерии могут превращать р-имидазолпировиноградную кислоту в гистидин при наличии в среде пиридоксальфосфата. Эти данные показывают, что имидазолпировиноградная кислота является предшественником гистидина, но в настоящее время при истолковании этих наблюдений следует учитывать и другие возможности.
Биосинтез гистидина очень сложен, это каскад из 9 реакций.
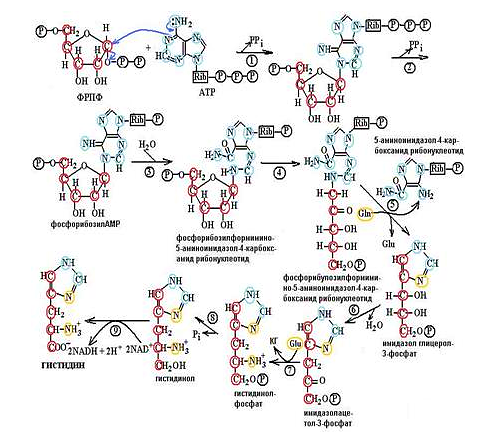
Начальными соединениями для синтеза гистамина выступают: аденозин-трифосфорная кислота (АТФ) и 5-фосфорибозил-1-пирофосфат (ФРПФ).
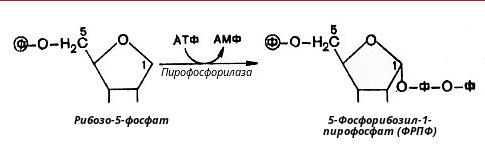
К молекуле 5-фосфорибозил -1- пирофосфата (ФРПФ) присоединяется молекула АТФ.
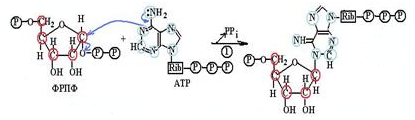
При этом от молекулы ФРПФ отрывается пирофосфатный хвост, а пуриновое ядро азотистого основания АТФ присоединяется к углероду пятичленного сахара рибозы в молекуле ФРПФ.
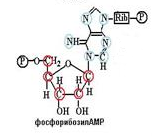
2.На втором этапе от образовавшегося соединения отщепляются еще два фосфорных остатка, которые на начальном этапе принадлежали АТФ.Образуется соединение фосфорибозилАМФ.
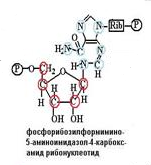
3.Третий этап. Гидролиз, т.е. присоединение воды к пуриновому ядру, принадлежащему изначально молекуле АТФ. Углеродное кольцо разрывается, кислород воды присоединяется к углероду, а пара водородов отходит к соседним азотам.
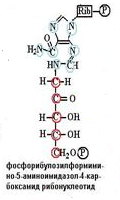
4.Четвертый этап. Кольцо пятичленного сахара рибозы размыкается, при этом отщепляется молекула воды.
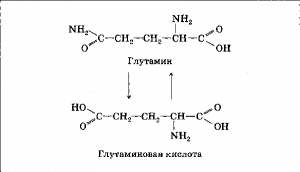
5.На пятом этапе происходит метаморфоза. В реакцию вступает глутамин, который отдает азотистый остаток, а забирает гидроксильный остаток — ОН, превращаясь в глутаминовую кислоту (глутамат).
Глутаминовая кислота и глутамин – два соединения, постоянно обменивающиеся азотными головами. Аммиак, образующийся при работе, захватывается глутаминовой кислотой, которая превращается в глутамин – транспортную форму переноса азотистой группы. Глутамин используется в разнообразных реакциях синтеза, вот и для образования имидазольного кольца гистидина пригодился.
Реакция обмена азотистой головой глутамина с глутаминовой кислотой выглядят так:
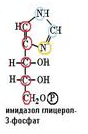
Соединение, идущее на синтез гистидина, перегруппировывается, от него отщепляется рибонуклеотид — 5-аминоимидазол-4-карбоксамид – промежуточный продукт синтеза АТФ. На синтез АТФ оно и направится.
Другой продукт расщепления содержит пять атомов углерода из первоначального скелета сахара рибозы, один атом углерода и один атом азота, отщепленные от первоначально вступившей в реакцию молекулы АТФ, и один атом азота, принесенный глутамином. Одновременно замыкается имидазольное кольцо.
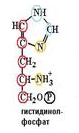
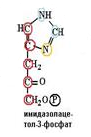
6.На шестом этапе отщепляется еще одна молекула воды
7.На седьмом этапе глутамат превращается в а-кетоглутарат, отдав аминную часть, которая приращивается к предыдущему соединению.
8.Дальше
идет потеря фосфорного остатка, который
заменяется на водород. Образуется
спирт.
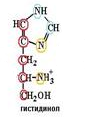
На
заключительном этапе образовавшийся
спирт окисляется молекулой НАД, и спирт
превращается в аминокислоту.