
6 Молекулярная физика и термодинамика
Тест 6 – 1
 На
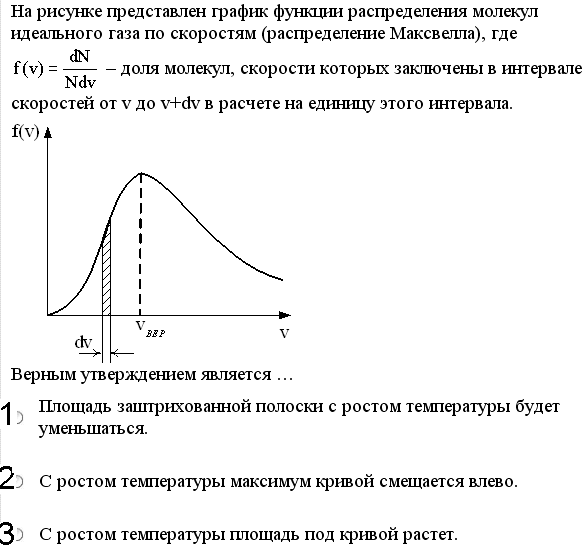
рисунке представлен график функции
распределения молекул идеального
газа по скоростям (распределение
Максвелла), гдеf
(v)
= dN
/ (N·dv)
- доля
молекул, скорости которых заключены в
интервале скоростей
от v
до (v+dv)
в расчете на единицу этого интервала.
Верным утверждением является ...
На
рисунке представлен график функции
распределения молекул идеального
газа по скоростям (распределение
Максвелла), гдеf
(v)
= dN
/ (N·dv)
- доля
молекул, скорости которых заключены в
интервале скоростей
от v
до (v+dv)
в расчете на единицу этого интервала.
Верным утверждением является ...
Варианты ответов: 1) Площадь заштрихованной полоски с ростом температуры будет уменьшаться. 2) С ростом температуры максимум кривой смещается влево.
3) С ростом температуры площадь под кривой растет.
Решение.
Начнём с анализа третьего утверждения. Площадь, ограниченная графиком функции распределения f(v) и осью абсцисс, численно равна единице, так как функция распределения удовлетворяет условию нормировки. Следовательно, с изменением температуры площадь остается постоянной, поэтому третье утверждение является неверным.
Проанализируем
второе утверждение. Максимум функции
распределения приходится на значение
скорости, называемой наиболее вероятной,
которая равна: v
вер
= ![]() ,
где k - постоянная Больцмана, Т – абсолютная
температура,
,
где k - постоянная Больцмана, Т – абсолютная
температура, ![]() -
масса молекулы. Из этой формулы следует,
что с ростом температуры максимум кривой
смещается вправо, а не влево. Поэтому
второе утверждение также неверно.
-
масса молекулы. Из этой формулы следует,
что с ростом температуры максимум кривой
смещается вправо, а не влево. Поэтому
второе утверждение также неверно.
Рассмотрим первое утверждение. Площадь заштрихованной полоски приблизительно равна площади параллелограмма, которая равна произведению основания на высоту, т.е. f(v)·dv. Но значение f(v) уменьшается с ростом температуры, так как эта функция удовлетворяет условию нормировки, а значение dv остаётся неизменным, поэтому их произведение уменьшается, и площадь заштрихованной полоски с ростом температуры будет уменьшаться. Следовательно, утверждение 1 является верным.
Ответ: вариант 1.
Тест 6 – 2
На рисунке теста 6 – 1 представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где f (v) =dN / (N·dv) - доля молекул, скорости которых заключены в интервале скоростей от v до (v+dv) в расчете на единицу этого интервала.
Если, не меняя температуры и числа молекул, взять другой газ с большей молярной массой, то...
Варианты ответов:
1) площадь под кривой увеличится; 2) максимум кривой сместится вправо в сторону больших скоростей; 3) максимум кривой сместится влево в сторону меньших скоростей.
Решение.
Начнём с анализа первого утверждения. Площадь, ограниченная графиком функции распределения f(v) и осью абсцисс, численно равна единице, так как функция распределения удовлетворяет условию нормировки. Следовательно, с изменением массы молекулы площадь остается постоянной, поэтому первое утверждение является неверным.
Рассмотрим
два других утверждения. Максимум функции
распределения приходится на значение
скорости, называемой наиболее вероятной.
Наиболее вероятная скорость равна: v
вер
= ![]() ,
где
,
где ![]() - постоянная Больцмана, Т – абсолютная
(или термодинамическая) температура,
- постоянная Больцмана, Т – абсолютная
(или термодинамическая) температура,
![]() -
масса молекулы. Эту формулу можно
записать в другом виде: v
вер
=
-
масса молекулы. Эту формулу можно
записать в другом виде: v
вер
=![]() ,
где R
– газовая постоянная, μ – молярная
масса. Из этой формулы следует, что с
ростом молярной массы максимум кривой
смещается влево, а не вправо. Поэтому
второе утверждение также неверно.
Следовательно, верным является третье
утверждение.
,
где R
– газовая постоянная, μ – молярная
масса. Из этой формулы следует, что с
ростом молярной массы максимум кривой
смещается влево, а не вправо. Поэтому
второе утверждение также неверно.
Следовательно, верным является третье
утверждение.
Ответ: вариант 3.
