

Оглавление
Предисловие . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . |
5 |
Глава 1. Тканевая принадлежность сосудистого эндотелия . . . . . . . . . . . . . . . |
7 |
1.1. Строение эндотелия . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 9 1.2. Тканевая специфичность эндотелия . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 15 1.3. Функции эндотелия. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 17 1.4. Строение микрососудов . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 21
Глава 2. Строение микроциркуляторного русла в норме . . . . . . . . . . . . . . . . . . 23
2.1. Микроциркуляторное русло сердца . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 28 2.1.1. Тканевая мозаика эндотелия кровеносных
и лимфатических сосудов сердца. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 32 2.2. Микроциркуляторное русло органов дыхания . . . . . . . . . . . . . . . . . . . . . . . . . . . . 33 2.3. Микроциркуляторное русло органов брюшной полости . . . . . . . . . . . . . . . . . . . 36 2.3.1. Брюшина и сальник . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 36 2.3.2. Слюнные железы. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 42 2.3.3. Желудок . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 42 2.3.4. Тонкая кишка. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 43 2.3.5. Толстая кишка . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 45 2.3.6. Прямая кишка . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 46 2.3.7. Печень и желчный пузырь. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 47 2.3.8. Поджелудочная железа. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 51 2.3.9. Селезенка . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 52 2.4. Микроциркуляторное русло почки и мочевого пузыря . . . . . . . . . . . . . . . . . . . . 53 2.5. Микроциркуляторное русло щитовидной железы. . . . . . . . . . . . . . . . . . . . . . . . . 57 2.6. Микроциркуляторное русло внутренних женских половых органов . . . . . . . . . 61 2.7. Микроциркуляторное русло кожи . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 63 2.8. Микроциркуляторное русло мышц . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 64 2.9. Крово- и лимфообращение в лимфатическом узле . . . . . . . . . . . . . . . . . . . . . . . . 64 2.9.1. Кровоснабжение лимфатического узла. . . . . . . . . . . . . . . . . . . . . . . . . . . . . 64 2.9.2. Синусы лимфатического узла . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 67
Глава 3. Механизмы регуляции микроциркуляции . . . . . . . . . . . . . . . . . . . . . . 70
3.1. Местная регуляция кровотока в капилляроне . . . . . . . . . . . . . . . . . . . . . . . . . . . . 70 3.1.1. Миогенная ауторегуляция . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 70 3.2. Гуморальная регуляция микроциркуляции . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 71 3.3. Нервная регуляция микроциркуляции . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 73
Глава 4. Общая патология микроциркуляции . . . . . . . . . . . . . . . . . . . . . . . . . . 75
4.1. Внутрисосудистые нарушения . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 75 4.1.1. Расстройства реологии и вязкости крови . . . . . . . . . . . . . . . . . . . . . . . . . . . 75 4.1.2. Нарушение коагуляции и фибринолиза крови . . . . . . . . . . . . . . . . . . . . . . 76 4.1.3. Изменение скорости кровотока . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 77 4.2. Сосудистые нарушения . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 77 4.2.1. Диапедез форменных элементов через капилляры . . . . . . . . . . . . . . . . . . . 78 4.2.2. Микрокровоизлияния . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 78 4.3. Внесосудистые нарушения. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 78
4 |
Коррекция микроциркуляции в клинической практике |
Глава 5. Способы коррекции нарушений микроциркуляции . . . . . . . . . . . . . . 79
5.1. Терапия лекарственными препаратами . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 79 5.2. Терапия лазерным излучением . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 89 5.3. Озонотерапия . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 91 5.4. Терапия экзогенным оксидом азота . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 95
5.4.1. Влияние оксида азота на пролиферативную активность эндотелия микрососудов кожи в условиях гнойной раны . . . . . . . . . . . . . 98
Глава 6. Нарушения микроциркуляции при различных заболеваниях и их коррекция . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 103
6.1. Нарушения микроциркуляции в условиях экспериментального инфаркта миокарда . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 103
6.2. Эндотелий лимфатических микрососудов сердца в условиях экспериментального инфаркта миокарда . . . . . . . . . . . . . . . . . . . . . 108
6.3. Нарушения микроциркуляции при патологии органов дыхания . . . . . . . . . . . 112 6.3.1. Радионуклидные методы . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 121 6.3.2. Конъюнктивальная биомикроскопия . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 122 6.3.3. Лазерная доплеровская флоуметрия . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 126
6.4. Коррекция микроциркуляторных нарушений при патологии органов дыхания . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 130
6.4.1. Пневмония . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 130 6.4.2. Атрофический бронхит . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 131 6.4.3. Легочное кровотечение . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 134 6.4.4. Эрозивный трахеобронхит. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 138 6.5. Нарушения микроциркуляции брюшины при перитоните . . . . . . . . . . . . . . . . 147
6.6. Нарушение микроциркуляции тонкой кишки при кишечной непроходимости и перитоните . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 149
6.7. Нарушение микроциркуляции при язвенной болезни желудка и двенадцатиперстной кишки . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 152
6.7.1. Антигипоксантная региональная лимфатическая терапия . . . . . . . . . . . 154 6.7.2. Терапия лазерным излучением . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 158 6.8. Нарушения микроциркуляции при желудочно-кишечном кровотечении . . . 161 6.8.1. Влияние оксида азота на ангиогенез при желудочном кровотечении . . 164
6.9.Функциональная морфология кровеносных микрососудов, желчных капилляров и клеток печени в условиях экспериментального
воспаления желчного пузыря . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 166 6.10. Нарушения микроциркуляции при гнойном холангите . . . . . . . . . . . . . . . . . . . 168 6.11. Нарушения микроциркуляции при остром панкреатите и панкреонекрозе . . . 171 6.12. Нарушения микроциркуляции щитовидной железы
при некоторых ее заболеваниях . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 173 6.13. Нарушение микроциркуляции при остром сальпингоофорите. . . . . . . . . . . . . 178 6.14. Нарушения микроциркуляции в условиях огнестрельной раны . . . . . . . . . . . . 179 6.15. Нарушения микроциркуляции у больных с хронической венозной
недостаточностью нижних конечностей и их коррекция лимфологическими методами . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 181
6.16. Нарушения микроциркуляции и образование отеков. . . . . . . . . . . . . . . . . . . . . 191
Заключение . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . |
204 |
Список литературы . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . |
205 |

ПРЕДИСЛОВИЕ
Термин «микроциркуляция» появился лишь в 1954 г., когда в США была созвана первая конференция по физиологии и патологии микроциркуляции (Гальвестон, Техас). Он появился в связи с необходимостью выделения специальной области знаний о механизмах и путях движения жидкостей в тканях. Этот раздел науки возник на основе накопления новых фактов и совершенствования техники, сделавшей возможными комплексные морфофизиологические исследования. Однако применяемые морфологами методы изучения микроциркуляторного русла на аутопсийном и биопсийном материале имели ряд недостатков, обусловленных определением состояния интрамуральных сосудов преимущественно на поперечных и косых срезах, большими трудностями при исследовании одновременно сосудов гемо- и лимфоциркуляции.
Широкие возможности для изучения микроциркуляции представились патологоанатомам при внедрении в практику безинъекционного исследования серозных оболочек по методике В.В. Куприянова. Метод позволяет изучить все звенья микроциркуляторной системы на значительном протяжении
вих сложных взаимоотношениях, судить о состоянии лимфатических терминалей, внутрисосудистых нарушениях, изменении проницаемости. Опыт клинико-морфологических сопоставлений состояния микроциркуляторного русла при различных заболеваниях позволил считать, что именно серозные оболочки являются для морфологов «окном» в микроциркуляцию всего организма. Наряду со стереотипными реакциями развиваются структурные изменения микроциркуляторного ложа, которые обусловлены определенным заболеванием.
Значительный качественный скачок в познании морфологических основ микроциркуляции произошел в связи с применением метода сканирующей электронной микроскопии коррозионных препаратов, который основан на заполнении сосудистого русла специальными быстротвердеющими пластмассами, растворении тканей в щелочи или кислоте и изучении полученного слепка
всканирующем электронном микроскопе, сочетающем в себе большую глубину фокуса, что дает «трехмерность» изображения, широкий диапазон увеличений, высокую разрешающую способность.
Под термином микроциркуляция мы понимаем движение биологических жидкостей с содержащимися в них веществами по микроскопическим
6 |
Коррекция микроциркуляции в клинической практике |
сосудам, через стенки сосудов и по тканевым (межклеточным) пространствам. Чтобы понять все аспекты микроциркуляции, надо знать структуру и функцию не только микрососудов, но также крови и лимфы, их заполняющих, не говоря уже о канонах распределения жидкости за пределами стенки сосуда. В свете современных достижений науки микроциркуляторное русло следует рассматривать как отдел (подсистему) сердечно-сосудистой системы. Микроциркуляторное русло обслуживает микроциркуляцию (как процесс). В то же время систему микроциркуляции невозможно вычленить из комплекса других систем организма – она взаимодействует с ними и формировалась в связи с развитием самого организма.

Глава 1
ТКАНЕВАЯ ПРИНАДЛЕЖНОСТЬ СОСУДИСТОГО ЭНДОТЕЛИЯ1
Сердечно-сосудистая система играет важнейшую роль
вобеспечении нормального течения всех процессов жизнедеятельности организма. Это диктует необходимость обстоятельного изучения транспорта крови и механизма переноса веществ через стенки сосудов. Данный процесс осуществляется при участии эндотелия, от состояния которого зависит проницаемость сосудистых стенок.
В1945 г. австралийский патолог Г. Флори, работавший в Оксфорде вместе с А. Флеммингом и Э. Чейном, получил Нобелевскую премию за пенициллин. Однако остались малоизвестными его последующие работы по изучению эндотелия. Используя электронную микроскопию, Г. Флори установил, как макромолекулы диффундируют сквозь стенки артерий и вен различных органов. Он впервые обнаружил мембранные микроструктуры эндотелия и межклеточные соединения, участвующие в транспортных процессах; выяснил его роль
вобразовании атеросклеротических изменений сосудов. Работы Г. Флори послужили основой сегодняшних представлений об эндотелии – ткани, ответственной за сопряжение множества процессов в системе кровообращения. Эти исследования привели к пониманию молекулярных причин патогенеза многих сосудистых заболеваний: атеросклероза, гипертонии, сердечной и почечной недостаточности, отеков. Возникло особое понятие, по сути, новая клиническая форма – эндотелиальные дисфункции, объединяющее огромный спектр нарушений сердечно-сосудистой системы в целом.
Говоря о сосудистой системе, было бы примитивным упрощением иметь
ввиду только крупные и мелкие пронизывающие тело «трубочки», которые служат механическим «кровепроводом». Кровь, за 40–60 с обегающая все уголки живого тела, помимо эритроцитов – главных носителей кислорода и углекислоты, содержит многие другие компоненты. Среди них – тромбоциты, похожие на миниатюрные лепешечки – клетки, начиненные биологическим материалом, который необходим для «ремонтных работ» в сосудистой стенке. Не соответствуя общей стремительности потока, лениво перекатываясь по внутренней стенке, движутся лейкоциты. Они выполняют охранную миссию, обладая особой чувствительностью ко всему чужеродному. Здесь же находятся
1 Глава написана совместно с д-ром мед. наук В.Г. Андреевым.
8 |
Коррекция микроциркуляции в клинической практике |
макрофаги, похожие на растрепанные цветочные бутоны, – клетки иммунной защиты. А также системы белков, ферментов, гормонов, низкомолекулярных продуктов – целый сонм биологически активных веществ, синтезируемых или выбрасываемых в кровь из тканей.
Для сохранения равновесия в системе гемодинамики и для поддержания транскапиллярного обмена есть несколько условий, в реализации которых участвуют как химические факторы сосудистой стенки, так и перечисленные клетки крови:
•должен поддерживаться определенный уровень гидростатического давления в сосуде, без чего невозможны непрерывное движение крови и обменная функция между кровью и тканями;
•кровоток должен быть непрерывным. Спазм сосуда, образование микротромбов, скопление клеток в каком-то участке микроциркуляторного ложа должны устраняться незамедлительно;
•репарация поврежденной сосудистой стенки; включение биохимических и физических механизмов; активация тромбоцитов и фермента тромбина, образование «заплаток» из фибриновых волокон, спазм микрососудов;
•регуляция транскапиллярной проницаемости. Существовавшее долгое время представление о пассивной роли микрососудов в обменных процессах рухнуло под лавиной новых фактов. В словаре нынешних специалистов фигурируют такие понятия, как «микровезикуляция», «пиноцитоз», «интерстициальный градиент», «скаффелдинг» (создание
строительного каркаса), «ремоделирование мембран» и др.
Эти условия формулируются как единое правило поддержания равновесия между тонусом сосуда, его физической целостностью и свойствами текущей крови, что некогда было определено как «гемоваскулярный гомеостаз». Если свойства крови меняются (увеличивается число микроагрегатов, растет ее вязкость и, следовательно, возникает опасность нарушения транскапиллярной функции), в дело вступают биохимические системы, регулирующие течение транспортируемой жидкости и адаптивные изменения мышечного тонуса сосудов. Так постулировалась в 70-х годах роль калликреин-кининовой системы крови.
Эндотелий – мономерный слой пограничных клеток между кровью и мышечным слоем сосуда, оказывается важнейшей тканевой структурой, причастной к регуляции и реализации всех перечисленных функций.
По современным представлениям, эндотелий – не просто барьер или фильтр. Это активный эндокринный орган, самый большой в теле, диффузно рассеянный по всем тканям. Он синтезирует субстанции, важные для контроля свертывания крови, регуляции тонуса и артериального давления, фильтрационной функции почек, сократительной активности сердца, метаболического обеспечения мозга. Контролирует диффузию воды, ионов, продуктов метаболизма. Реагирует на механическое воздействие текущей жидкости, кровяное давление и ответное напряжение, создаваемое мышечным слоем сосуда. Эндотелий чувствителен к химическим и анатомическим повреждениям, которые могут приводить к повышенной агрегации и адгезии циркулирующих клеток,
Глава 1. Тканевая принадлежность сосудистого эндотелия |
9 |
развитию тромбоза, оседанию липидных конгломератов. «Маэстро кровообращения» — так именовал его нобелевский лауреат, британский фармаколог Дж. Вейн.
По выражению лауреата Нобелевской премии G.E. Palade (1968), паспортный возраст человека соответствует состоянию сосудистого эндотелия.
1.1. Строение эндотелия
Термин «эндотелий» (от греч. Endon – внутри и thele – сосок) предложил в 1865 г. W. His как дополнительный к термину «эпителий». До 30-х годов XX века им обозначали выстилку сердца, кровеносных и лимфатических сосудов, серозных, синовиальных и мозговых оболочек, задней камеры глаза, респираторных путей.
Влитературе высказываются разные взгляды о месте эндотелия в системе тканей: его относят либо к эпителиям, либо рассматривают как одну из форм клеточной организации соединительной ткани. Наиболее обоснованной представляется точка зрения, высказанная Н.Г. Хлопиным, о том, что сосудистый эндотелий является тканью эпителиоморфного типа (специфическая разновидность однослойного плоского эпителия). Логическим развитием взглядов Н.Г. Хлопина следует считать выделение системы эндотелия, что также созвучно представлениям о самостоятельном значении тканевых систем на уровне организма, обоснованным в дискуссионной статье Н.Н. Кочетова.
Внастоящее время термин «эндотелий» (синоним – сосудистый эндотелий) применяется только для обозначения внутренней клеточной выстилки кровеносного и лимфатического русла.
Эндотелий – это однослойный пласт специализированных клеток, выстилающих изнутри все сердечно-сосудистое дерево. Для человека среднего веса – это ткань весом около 1,8 кг и один триллион клеток со сложнейшим устройством, включающим системы синтеза белков и низкомолекулярных веществ, рецепторы, ионные каналы.
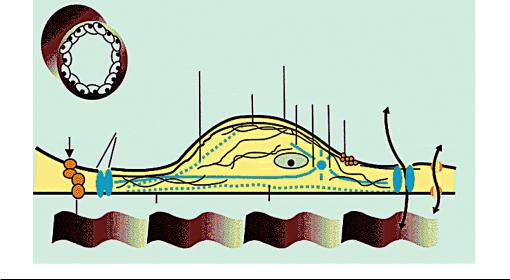
Для эндотелия, как и для типичных эпителиев, является характерным пограничное положение, отсутствие межклеточного вещества, наличие сходной по строению базальной мембраны (содержит коллаген IV типа), полярность строения клеток, наличие системы межклеточных контактов, формирующих непрерывный клеточный пласт; общность механизмов роста в культуре и при репаративной регенерации (рис. 1.1). С помощью специфических клеточных маркеров показано, что первоначальным источником развития сосудистого эндотелия, как и мезотелия, являются клеточные элементы мезодермы листков спланхнотома.
Эндотелиальное дерево не однородно в своей архитектуре. Его гетерогенность, соответствующая гетерогенности сосудистого ложа, зависит от размера, структуры, биохимической организации, функции данного органа. Эндотелиальная тканевая система обладает рядом специфических функций организменного значения и к тому же занимает в организме вполне определенное положение, являясь непрерывной внутренней выстилкой кровеносных
10 |
Коррекция микроциркуляции в клинической практике |
люминальные кортикальная мембрана
|
каркасные |
(актин, спектрин и др.) |
|
|
|
|
|
волокна |
|
|
|
||
|
|
|
|
|
|
|
|
интермедиальные |
|
|
транспорт |
|
|
|
миофиламенты |
микротрубочки |
|
воды, |
|
|
|
межклеточные |
|
макромолекул |
|
||
|
|
|
|
|||
трансцелюлярная |
соединения из |
|
кавеолы |
трансцеллюлярная |
||
диффузия |
активных филаментов |
|
диффузия Н2 |
О |
||
|
|
|
||||
белков |
(актин, миозин и др.) |
|
|
|
ионы, органические |
|
соединения
базальная мембрана |
базальные каркасные волокна |
вазальные гладкомышечные клетки
Рис. 1.1. Поперечный срез сосуда (вверху слева)
имикроструктура эндотелиальной клетки
илимфатических сосудов и сердца. Однако даже при таком компромиссном
подходе перед исследователями при анализе многочисленных функций эндотелия и его органоспецифичности встает вопрос, является ли эндотелиальная клетка одной из самых плюрипотентных клеток в организме, или же существует чрезвычайно большое многообразие эндотелиальных клеток со строго закрепленными индивидуальными функциями.
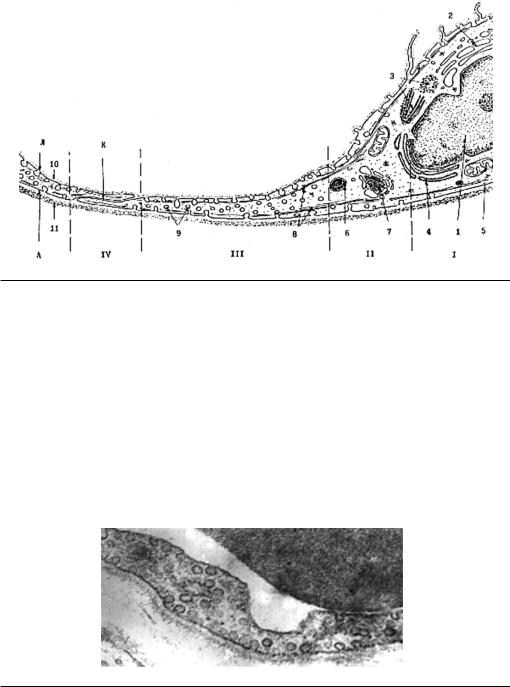
Электронно-микроскопически в каждом эндотелиоците выделяют (рис. 1.2) четыре структурно-функциональные зоны: ядерную, органелл, периферическую и контактную, а также три стороны поверхности: люминальную, аблюминальную и контактную.
Ядро находится в центральной (ядерной) зоне и содержит, как правило, одно ядрышко. Форма ядер овальная или лопастная, с многочисленными инвагинациями кариолеммы в зависимости от растяжения сосудистой стенки. Пластинчатый комплекс расположен над ядром, состоит из уплощенных мешочков и цистерн, крупных вакуолей и мелких везикул; рядом находится клеточный центр.
В зоне органелл сконцентрированы элементы гранулярной эндоплазматической сети, митохондрии со светлым матриксом и малым числом крист, первичные лизосомы. Некоторые эндотелиоциты (чаще артериальных сегментов) содержат осмиофильные гетерогенные структуры – специфические тельца Вейбеля–Паладе, являющиеся, очевидно, производными пластинчатого комплекса. В периферической зоне в основном локализованы специализированные транспортные структуры: микропиноцитозные везикулы, трансэндотелиальные каналы, фенестры, поры-люки. Микропиноцитозные везикулы –
Глава 1. Тканевая принадлежность сосудистого эндотелия |
11 |
Рис. 1.2. Строение эндотелиоцита (схема). Структурно-функциональные зоны: I – ядерная, II – органелл, III – периферическая, IV – контактная (вертикальные штриховые линии – условные границы зон). Поверхности клетки: Л – люминальная, А – аблюминальная, К – контактная. Ультраструктурные компоненты: 1 – ядро, 2 – пластинчатый комплекс, 3 – клеточный центр, 4 – гранулярная эндоплазматическая сеть, 5 – митохондрия, 6 – лизосома, 7 – тельце Вейбеля–Паладе, 8 – элементы цитоскелета, 9 – микропиноцитозные везикулы, 10 – гликокаликс (параплазмолеммальный слой), 11 – базальная мембрана
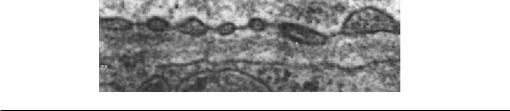
наиболее характерная структура эндотелиоцитов, занимающая до 30–40% объема цитоплазмы (рис. 1.3).
В 70% встречаются прикрепленные микропиноцитозные везикулы, закрытые однослойной диафрагмой, реже – открытые инвагинации плазмолеммы и свободные везикулы. Окантованные микропиноцитозные пузырьки обеспечивают транспорт веществ, рецепторно связывающихся с поверхностью
Рис. 1.3. Капилляр миокарда взрослой крысы. Периферическая зона эндотелиоцита. Иммерсионная фиксация, ×24 000
12 |
Коррекция микроциркуляции в клинической практике |
эндотелиоцитов, неокантованные везикулы специализируются на переносе анионных белков. При слиянии нескольких микропиноцитозных везикул могут формироваться временные трансэндотелиальные каналы.
Фенестры и поры сближаются специализацией по трансэндотелиальному переносу веществ преимущественно конвекционным способом. Фенестры (рис. 1.4) – редуцированные трансэндотелиальные каналы диаметром от 30 до 80 нм, закрытые однослойными диафрагмами, локализуются кластерами в истонченных до 0,1 мкм частях клетки и занимают до 20% площади поверхности.
Поры являются сквозными отверстиями истонченных участков эндотелиоцитов, непосредственно соединяющими просвет сосуда с периэндотелиальным пространством. Их размеры обеспечивают прохождение растворов с микро- и макромолекулами и клеток крови.
Цитоскелет эндотелиоцитов представлен комплексом механохимических белков (тубулин, актин, виментин и др.), обеспечивающих поддержание формы, подвижность клеток и контактное торможение. Состоит из варьирующих по распределению и ориентации микротрубочек, микрофиламентов, якорных фибрилл, соединяющих фибриллярные элементы цитоплазмы с цитолеммой и ядерной оболочкой.
Люминальная поверхность включает три слоя: параплазмолеммальный (гликокаликс), плазмолемму и подмембранный (кортикальный); обеспечивает рецепцию и селекцию переносимых соединений, регуляцию транспортных свойств эндотелиоцита, определяет изменение конфигурации поверхности клетки. Образует микровыросты, складки и микроворсинки, которые могут быть связаны с захватом материала из просвета сосуда или иметь реактивный характер.
Латеральные поверхности эндотелиоцитов (контактная зона) заполнены цементирующим веществом параплазмолеммального слоя и содержит специализированные межклеточные контакты (рис. 1.5) – простые, сложные (интердигитационные), плотные и щелевые, на которые приходится до 10% объема клеточного пласта. Они являются интегрирующими структурами монослоя эндотелиоцитов в ткань, обеспечивают устойчивость пласта движению крови или лимфы и возможность транспорта веществ. Контакты – динамичные структуры, способные за счет ремоделирования цитоскелета изменять размеры межклеточных щелей в течение минут.
Рис. 1.4. Капилляр околощитовидной железы с эндотелием фенестрированного типа. Иммерсионная фиксация, ×28 000
