
ГОУ ВПО УГМА Росздрава
кафедра биохимии
Утверждаю
Зав. каф. проф., д.м.н.
Мещанинов В.Н.
_____‘’_____________2008 г
МЕТОДИЧЕСКАЯ РАЗРАБОТКА
К ПРАКТИЧЕСКОМУ ЗАНЯТИЮ. ФАКТОРЫ
ВНЕШНЕЙ СРЕДЫ И МЕТАБОЛИЗМ (для преподавателей).
Факультет: медико-профилактический.
Курс: 2
1. ТЕМА ЗАНЯТИЯ: факторы внешней среды и метаболизм.
2. УЧЕБНАЯ ЦЕЛЬ ЗАНЯТИЯ: обьяснить
3. ЗАДАЧИ ЗАНЯТИЯ:
3.1.Рассмотреть
3.2.Обобщить
3.3.Рассмотреть
3.4.
4. ПРОДОЛЖИТЕЛЬНОСТЬ ЗАНЯТИЯ: 3 акад. часа.
5. МЕСТО ПРОВЕДЕНИЯ ЗАНЯТИЯ: учебная комната
6. ОСНАЩЕНИЕ ЗАНЯТИЯ
6.1.набор для тест - контроля знаний студентов.
6.2.Микроплакаты, отражающие характер нарушений.
6.3.Наборы химических реактивов для определения ацетальдегида, молонового диальдегида, пролина и фенола.
6.4.Химическая посуда, автодозаторы, штативы для пробирок.
6.5.Термостат,
7. ПЛАН ПРОВЕДЕНИЯ ЗАНЯТИЯ И БЮДЖЕТ УЧЕБНОГО ВРЕМЕНИ
7.1. Организационные вопросы 5 мин.
7.2. Введение. Актуальность, цели и задачи учебного занятия 10 мин.
7.3. Проведение тест - контроля знаний студентов 20 мин.
7.4. Рассмотрение теоретических вопросов темы 80 мин.
7.5. Перерыв 10 мин.
7.6. Самостоятельное выполнение студентами лабораторной работы - 50 мин.
7.7. Подведение итогов занятия 5 мин.
8. МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ПРОВЕДЕНИЮ ЗАНЯТИЯ.. КОНТРОЛЬНЫЕ ВОПРОСЫ ПО ТЕМЕ ЗАНЯТИЯ.
8.1. Охарактеризуйте комплекс важнейших повреждающих факторов внешней среды
8.2. Каково влияние ионов тяжелых металлов (Pb, Cd, Hg) на метаболизм.
8.3. Каково влияние ионов Al, Cr на метаболизм.
8.4. Охарактеризуйте нарушение обмена веществ клетки при отравлениях нитратами и нитритами.
8.5.Дайте понятие химического СПИДА. Каково влияние токсических ароматических соединений, хлорорганических соединений - пестицидов, ДГ, гербицидов, диоксинов.
8.6.Каково влияние различных видов излучений: радиоактивного, рентгеновского, магнитного, ультрафиолетового на организм.
Дайте оценку по схеме: - характеристика излучения
- область применения
- особенности поражения
8.7.Дайте определение и характеристику пневмокониозам.
8.8.Каковы причины повреждающего действия этанола и ацетальдегида?
8.9.Назовите важнейшие пути метаболизма этанола в организме. Дайте им характеристику.
СОДЕРЖАНИЕ ЗАНЯТИЯ.
В настоящее время природные экологические катастрофы дополняются антропологическими(заводские взрывы, аварийные выбросы ядовитых веществ, хронение и переработка радиоактивных отходов). Кроме того недоброкачественная питьевая вода, загрязненные пищевые продукты, шум, загазованность, электромагнитные, радиоактивные загрязнения, широкое применение компьютеров, внедрение сотовой связи - все это способствует ухудшению экологической обстановки; поэтому одна из важнейших задач врача – гигиениста знать основу повреждающего действия этих факторов и уметь бороться с ними.
Влияние неорганических токсинов.
1. Свинец.
1.1. Источники: электрические кабели, свинцовые аккумуляторы, атомная промышленность, пигменты (сурик), свинцовые белила, глазурь.
Ежегодно: в воду 500-600 тыс. Тонн
в почву 400 тыс. тонн
в воздух, в виде аэрозолей солей 260 тыс. тонн
1.2. Характер поражения:
а) ионы Pb2+ комплексообразователи взаимодействуют и блокируют SH группы белков
2R – SH + Pb2+→ R-S-Pb-S-R + 2H+
б) образование гелеобразующих ??????? , что затрудняет проникновение микроорганизмов.
Pb2+ + 2R- COOH → Pb (R-COO)2 + 2H+
в) разобщение окислительного фосфорилирования.
г) накапливается в костях, вытесняя другие металлы.
д) физиологические эффекты: нарушение психики, агрессивность, ухудшение памяти, головокружение, раздражительность.
е) мышечная гипотония.
2. Кадмий (Cd2+).
2.1. Источники: сжигание топлива ТЭЦ, внесение с минеральными удобрениями, промышленные стоки.
2.2. Характер поражения: а) Cd2+ замещает Zn во всех цинксодержащих ферментах, блокируя их.
б) Cd замещает Ca2+, вызывая нарушения фосфорно – кальциевого обмена.
в) взаимодействует с SH группами белков.
г) усиливает активность аргиназы и уреазы.
3. Ртуть.
3.1. Источники: жидкий электрод в ртутных выпрямителях тока, лабораторных приборах.
3.2. Характер поражения:
а) микромеркуризм проявляется как и первых двух металлов.
б) психические нарушения.
4. Алюминий.
4.1. Источники: промышленные производства, полезные ископаемые.
4.2. Характер поражения:
а) хрупкость костей
б) анемия
в) накапливается в мозге: нарушения речи, провалы в памяти, нарушение ориентации, помутнение рассудка, конвульсии – болезнь Альцгеймера, старческий маразм.
г) Al образует хелатные комплексные соединения.
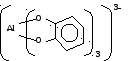
5. Хром.
5.1. Источники: промышленное производство.
5.2. Характер поражения:
а) в крови связан с трансферрином, вступая в конкуренцию с Fe3+; накапливается в печени и почках, в ядре; выделяется с мочой.
б) в природе распространены Cr3+ Cr6+.
в) особенно опасны соединения Cr6+, вызывая различные ОВР; возникновение дефектов лизилоксидазы и нарушения в соединительной ткани.
Отравление нитратами и нитритами.
Происходит при накоплении этих солей свежими овощами и фруктами (губительно внесение органических удобрений) при добавлении нитратов как консервантов в мясные и рыбные продукты.
Токсичность NO3-, NO2- проявляется: а) NO3- способствует окислению аминогрупп в азотистых основаниях нуклеиновых белков, теряется способность к образованию водородных связей; повреждение процессов транскрипции и редупликации.
R-NH2 + NO3- + НАДH + H+ + H+ → R-OH + 2H2O + НАД+ + N2
б) NO2- воздействует на гемоглобин, превращая его в метгемоглобин (гипоксия).
HbFe2+ + NO2- → HbFe3+ + NO
в) нитраты → нитриты → нитрозамины
NO3- → NO2-
R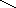 1R2-NH
+ HNO2
→ R1
1R2-NH
+ HNO2
→ R1
(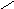 вторичный N-N=O
+ H2O
вторичный N-N=O
+ H2O
амин) R2 (вторичный нитрозамин)
R-NH2 + HNO2 → R1-NH-N=O ↔ [R1-(N=N)-OH] → R-OH + N2
первичный амин первичный нитрозамин
Нитрозамины являются канцерогенами, окисляя NH2 группы азотистых оснований.
г) NO2, NO3 образуют свободные радикалы, способствуя разрушению мембран.
2NO3- → 2NO2- + O2
O2 + ē → O2-˙
д) алкил нитрозамины способны алкилировать белки, нуклеиновые кислоты и нитрозировать ароматические аминокислоты, вызывая канцерогенез. Особенно быстро метилируют гистоновые белки, ДНК, по седьмому положению гуанина.
C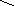 H3
H3
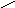 N-N-N=O
→ CH2=N+=N-
+ H-R
→ CH3-R
+ N2
N-N-N=O
→ CH2=N+=N-
+ H-R
→ CH3-R
+ N2
CH3
диметилнитрозамин диазометан гистоновый белок
Пневмокониозы – пылевые болезни. Характеризуются развитием в легких склеротических изменений при попадании промышленных пылей.
Выделяют:
1. Силикозы. Возникают при длительном вдыхании SiO2. В легких SiO2 растворяется в H2SiO3, H2SiO4, вызывая гибель клеток. Si2O3 фагоцитируется макрофагами, которые выделяют фактор синтеза коллагена фибробластами, кроме того выделяется интерлейкин – 1, вызывающий деление фибробластов. Возникает силикотический фиброз, образование узелковой ткани.

 OH OH
OH OH
R
 1-O-Si-O-Si-O-R2
1-O-Si-O-Si-O-R2
OH OH
R1-OH - полисахариды
R2-OH – полисахариды
Кислоты образуют комплекс с полисахаридами, увеличивая вязкость межклеточного матрикса.
2. Асбестозы. Возникают при запылении легких асбестовой пылью – силикатом магния. Важнейшим является хризотил Mg3[Si2O5](OH)4. Вызывает диффузное разростание диффузной ткани в межальвеолярных перегородках, бронхах, сосудах. Гиперкератоз возникает на пальцах рук, ног, подошвах ног возникают асбестовые бородавки.
3. Антрактозы. Возникают при длительном вдыхании угольной пыли. Поражающее действие оказывает угольная кислота, образуясь в легочной ткани. При фагоцитировании макрофагами образуются антрактические узлы с последующей антрокотической индурацией легких. Узлы расподаются и образуются коверны – «черная чахотка».
Для всех пневмокониозов характерно:
1. Увеличение о-пролина в легочной ткани и лимфатических узлах, моче.
2. Увеличение продуктов перикисного окисления липидов в легких и крови.
Органические вещества токсичные для человека вырабатываются бактериями, микроорганизмами, насекомыми, рыбами. Наиболее токсичны: HCN, алколоиды, ботулинистический и дифтерийный токсины. Однако наибольшую опасность представляют органические, рукотворные вещества. Это отходы производства нефтехимической, целлюлозно – бумажной, металлургической промышленности.
Влияние на организм ароматических углеводородов.
1. Ароматические углеводороды всасываются из кишечника, метаболизируют в печени и выделяются с калом.
Механизм действия на клетку:
Образуют донорно – акцепторные комплексы с пуриновыми основаниями ДНК и РНК, что нарушает процесс репликации, транскрипции и трансляции
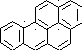
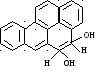
печень
перерождение
нормальной клетки
в рковую
эпоксидирование


компонент любого
??? бензпирен
2. Ароматические амины (анилиновые красители и ??????????): анилин, α нафтиламин, β нафтиламин. Механизм канцерогенного действия заключается в образовании продуктов трансформации: гидроксиламинов, аминобензолов.

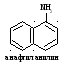
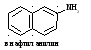
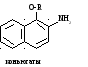
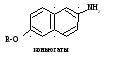
R: C6H9O6
SO3H
CO – CH3
3. Диоксины – объединение химически различных веществ по одному свойству – политоксичности. Их действие вызывает канцерогенез, гибель плода в матке, рождение детей с врожденными уродствами, потеря фертильности мужской спермы, психические нарушения.
Примеры:
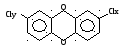

Через атом Cl идет соединение с белками, нуклеиновыми кислотами.
Механизм действия диоксинов: активация монооксигеназы и образование свободных радикалов, гидроксилированных продуктов не образуется.
Синергизм – токсическое действие диоксинов и других экотоксинов оказывается выше суммы их действия.
q + радиация
u + нитраты
o + S(II) соединения
k + Pb, Cd, Hg
c + хлорфенолы
u
НП
Выведение диоксинов происходит в результате почечной фильтрации. Выводятся медленно, накапливаются в жировой ткани. Распад диоксина в почве, воде, воздухе не происходит т.к. является ядом для всех аэробов. Диоксины адсорбируются в саже, аэрозольных частицах.
Действие ионизирующего излучения на человека.
Ионизирующее излучение: рентгеновское – получают с помощью электронного аппарата
гамма лучи – испускаются нестабильными радиоактивными изотопами.
Количественная характеристика излучения – доза : величина энергии поглощенная тканями, более универсальна эквивалентная доза – это величина поглощенной дозы умноженная на переводной коэффициент. Измеряется в Берах (Бер) или зивертах (Зв).
1Зв = 100Бер
Эффекты ионизирующего излучения:
1. Действие на воду(60-70 массы тела) 50% энергии поглощенной дозы приходится на Н2О, другие 50% на клеточные органеллы и растворенные вещества.
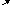 Н˙
Н˙
а )
возбуждение Н2О
→ Н2О*
)
возбуждение Н2О
→ Н2О*
ОН˙
б )
ионизация Н2О
→ Н2О+
+ ē
)
ионизация Н2О
→ Н2О+
+ ē
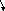
Н+ ОНׁ
Н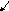
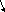 2О
+ ē → Н2О-
2О
+ ē → Н2О-
Н ׁ ОН-
Далее возникшие ионы взаимодействуют между собой, с О2, активными формами кислорода
О2 + ē → О2-˙ ОН˙ + ОН ˙→ Н2О2
 ОН˙
ОН˙
О2 + Н˙ → НО2˙ НО2 ˙+ Н ˙→ Н2О2
 ОН˙
ОН˙
НО2˙ + НО2˙ → Н2О2 + О2
Возникшие радикалы ведут к образованию вторично радикальных продуктов из растворенных в воде соединений.
2. Действие ионизирующего излучения на белки, ферменты, аминокислоты.
а) образование – S-S - мостиков между аминокислотами, белками.
R1-SH + R2-SH → R1-S-S-R2 + 2H˙
Изменение уровня свободных аминокислот: на 75% метионина, на 26% триптофана.
Начальная инактивация SH групп вызывается короткоживущими радикалами. Наиболее чувствительна система окислительного фосфорилирования. Генерирование АТФ повреждается.
3. Действие на углеводы.
Ионизирующее излучение производит распад углеводов, образуются органические кислоты и формальдегид, понижается вязкость мукополисахаридов, в частности, гиалуроновая кислота; гепарин теряет антикоагуляционные свойства.
4. Действие на липиды.
Образуется комплекс радиотоксинов, перекиси, эпоксиды, альдегиды, кетоны.
ROOH → ROO˙ + H˙
ROO˙ + R1H → ROOH + R1˙
R1˙ + O2 → ROO˙
Образуются липидные токсины, вызывающие образование других биологически активных веществ: хонона, холина, гистамина, вызывающие распад белков.
Этапы радиоактивного поражения (по Рудину А. И.):
а) физическая стадия – действие на сложные макромолекулы. Образование ДНК, белков, сложных липидов.
б) химическая стадия. Образовавшиеся радикалы действуют на клеточные структуры – мембраны. Идет образование перекисей, усиливается неврологический эффект.
в) биохимическая стадия. Выход факторов из поврежденных клеток и органелл.
Защита клетки от радиоактивного поражения:
а) радиопротекторы – вещества синтетического происхождения, при введении их перед облучением уменьшают поражающее действие ионизирующего излучения.
-
серосодержащие соединения
-
индолилаениламины
б) природные противолучевые вещества:
-
зоопрепараты: яды змей, насекомых (пчелы, пауки). Самые перспективные яды скорпиона, каракурта.
-
трефоны – трофические факторы в экстрактах, выделяемы из тканей животных (тимус, селезенка). Особенно среднеазиатская черепаха. Testudo hossfieldi.
-
эстрогены: этродиолы, эстриолы, эстроны эффект «колокола» - противолучевое действие снижается не только с увеличением, но и с уменьшением дозы облучения.
-
иммуномодуляторы – цитокины (интерлейкины, интерферон) хорошо сочетаются с витаминами (А, В1, В2, В6, С, Д3, Е, РР).
-
фитопрепараты – алкалоиды (капуста огородная, брюква, горчица, редька, бобовые), фитополисахариды.
Все остальные виды излучения действуют подобно ионизирующему излучению, только с менее выраженным эффектом.
ПРАКТИЧЕСКАЯ ЧАСТЬ:
Работа № 1. Качественное определение ацетальдегида в моче при отравлении этанолом.
Согласно современным представлениям этанол окисляется с участием фермента алкогольдегидрогеназы до ацетальдегида.
Ацетальдегид производит неблагоприятное действие на организм ингибирует биосинтез белка, нарушает обмен аминокислот в головном мозге.
Ацетальдегид обезвреживается в печени, а при алкогольной интоксикации может выводиться с мочой.
Ход работы: в пробирку с 1 мл мочи добавляют 1 мл фуксинсернистой кислотой. Раствор окрашивается в фиолетовый цвет.
Работа № 2. Качественное определение фенола в моче при отравлении.
Отравление лекарственными препаратами - салицилатами, производными ПАСК, ароматическими углеводородами - часто вызывают нарушения метаболизма.
Выделение препаратов происходит с мочой в виде коньюгатов, либо в неизменном виде при отравлениях лекарственными веществами; ароматическими углеводородами. Качественная реакция на фенольный радикал - наличие продуктов метаболизма этих веществ.
Ход работы: В пробирку помещают 2 капли раствора фенола, добавляют 3 капли воды и каплю раствора хлорного железа. Появляется интенсивное красно - фиолетовое окрашивание.
Работа № 3. Количественное определение молонового диальдегида с помощью тиобарбитуровой кислоты.
Аутоокисление липидов, протекающее в организме, называют липидной пероксидацией. Известно, что одной из причин активизации этого процесса является ионизирующее излучение; так как оно способно инициировать образование радикалов, течение цепных, радикальных процессов. При активном, протекающем процессе образовавшиеся липидные гидроперекиси распадаются с образованием молонового альдегида. Определение его производится для оценки перекисного окисления липидов.
Ход работы: к 1 мл цельной крови добавляют 6 мл 5,7 % трихлоруксусной кислоты. К 2 мл безбелкового экстракта добавляют 1 мл 0,8 % раствора тиобарбитуровой кислоты, полученный раствор помещают в кипящую водяную баню на 10 мин. Полученный раствор фотоколориметрируют (светофильтр . . . . ).
Расчет по формуле:
Концентрация МДА= [ E * 6,73*10-5] ммоль/литр крови
где Е – экстинкция раствора
6,73*10-5 -
Клиническое значение: увеличение концентрации молонового диальдегида наблюдается при возрастании перекисного окисления липидов в тканях. Это может происходить при различных воспалительных реакциях: пневмониях, бронхитах, диффузных поражениях соединительной ткани и т. д.
Работа № 4. Качественное определение пролина в моче.
Характерной особенностью коллагена является присутствие в его молекуле аминокислот пролина и оксипролина.
Содержание пролина и оксипролина в моче является одним из показателей степени фиброзного процесса в органах и тканях.
Ход работы: Фильтровальную бумагу, смоченную в гуотиновом растворе (9,6 мл гуатинового реактива и 0,4 мл уксусной кислоты). Бумагу высушивают при комнатной температуре, наносят по 1 капле мочи каждого образца. Образцы помещают в сушильный шкаф 100ºС на 10 мин. Далее промывают 1М HCl и дистиллированной водой.
Интерпретация: ярко - голубая окраска, оставшаяся после промывания, свидетельствует о повышении концентрации пролина. Нижняя граница чувствительности теста 0,1 мг/мл. Фенилаланин дает серо - голубую окраску, трептофан - коричневую.
Клиническое значение: тест на пролин положителен при гиперпролинемии I и II типов, синдром Вилсона Джоджера.
Норма пролина в моче 4-15 мг в сутки
9. ЭТАЛОНЫ ОТВЕТОВ НА ЗАДАЧИ, тестовые вопросы, используемые при контроле знаний на занятии (можно в виде приложения)
10. ХАРАКТЕР И ОБЪЕМ ВОЗМОЖНОЙ УЧЕБНО-ИССЛЕДОВАТЕЛЬСКОЙ РАБОТЫ ПО ТЕМЕ
(Указать конкретно характер и форму УИРС: подготовка реферативных выступлений, проведение самостоятельных исследований, имитационная игра, оформление истории болезни с использованием монографической литературы и др. формы)
11. ЛИТЕРАТУРА ДЛЯ ПОДГОТОВКИ К ЗАНЯТИЮ ПРЕПОДАВАТЕЛЯМ:
