
- •Контрольные вопросы к экзамену учебной дисциплины «Биохимия»
- •2.Уровни структурной организации белков: первичная, вторичная, третичная, четвертичная, домены, надмолекулярные структуры
- •3. Связь свойств, функций и активности белков с их структурной организацией (специфичность, видовая принадлежность, эффект узнавания, динамичность, эффект кооперативного взаимодействия).
- •4. Факторы повреждения структуры и функции белков, роль повреждений в патогенезе заболеваний. Протеинопатии.
- •5. Первичная структура белков. Зависимость свойств и функций белков от их первичной структуры. Изменения первичной структуры, протеинопатии.
- •6. Роль протеомики в оценке патологических состояний
- •7.Миоглобин и гемоглобин. Конформационные изменения и кооперативные взаимодействия субъединиц гемоглобина. Эффект Бора. Роль 2,3 –бифосфоглицерата.
- •9. Кинетика ферментативных реакций. Уравнение Михаэлиса – Ментона. Преобразование Лайнуивера – Бэрка
- •10. Строение ферментов. Кофакторы и коферменты. Активный центр, строение, функции, связь со специфичностью действия ферментов. Возможность изменения специфичности (трансформация).
- •11. Международная классификация и номенклатура ферментов. Шифр ферментов. Классификация ферментов по их локализации в органах и клетках (компартментализация).
- •12. Ингибирование активности ферментов: обратимые, необратимые, конкурентные, неконкурентное. Принцип применения лекарственных препаратов, основанный на ингибировании ферментов (примеры).
- •1. Конкурентное ингибирование
- •2. Неконкурентное ингибирование
- •1. Специфические и неспецифические
- •2. Необратимые ингибиторы ферментов как
- •13. Изоферменты. Особенности строения и функционирования (рассмотреть на примере лдг). Значение определения изоферментного спектра ферментов в диагностике заболеваний.
- •14. Аллостерическая регуляция. Ингибирование по принципу обратной связи.
- •15. Регуляция активности и количества ферментов (аллостерическая, регуляция путем фосфорилирования и дефосфорилирования, ограниченного протеолиза проферментов)
- •16. Первичные и вторичные ферментопатии. Биохимические механизмы развития патологий. Примеры заболеваний.
- •17. Энзимодиагностика и энзимотерапия. Ингибиторы ферментов как лекарственные препараты
- •18. Зависимость скорости ферментативных реакций от температуры, рН, концентрации субстратов (индукция и репрессия ферментов). Индукция к лекарственным веществам.
- •19. Кофакторы и коферменты. Водорастворимые витамины, как предшественники коферментов. Металлоферменты и ферменты, активируемые металлами
- •1. Роль металлов в присоединении субстрата
- •2. Роль металлов в стабилизации третичной
- •3. Роль металлов в ферментативном
- •4. Роль металлов в регуляции активности
- •1. Механизм "пинг-понг"
- •2. Последовательный механизм
- •Модуль II. Введение в обмен веществ. Биологическое окисление
- •20. Основные пищевые вещества. Суточная потребность. Незаменимые факторы питания
- •21.Переваривание основных пищевых веществ (жиров, белков, углеводов), ферменты пищеварительных соков. Наследственная непереносимость пищевых веществ.
- •22. Витамины. Классификация, функции. Алиментарные и вторичные авитаминозы и гиповитаминозы, их следствия, подходы к профилактике.
- •1. Образование и роль соляной кислоты
- •2.Механизм активации пепсина
- •3.Возрастные особенности переваривания белков в желудке
- •4. Нарушения переваривания белков в желудке
- •1. Активация панкреатических ферментов
- •2. Специфичность действия протеаз
- •24. Биологическое окисление. Особенности, функции. Макроэргические соединения. Синтез атф. Аэробный и субстратный типы окислительного фосфорилирования Превращение метаболической энергии в тепло.
- •25. Характеристика мультиферментных комплексов цепи переноса электронов. Структурная организация дыхательной цепи, ее функции (энергетическая, терморегуляторная) и место в системе дыхания
- •28. Микросомальное окисление, его организация, биологическая роль, связь с условиями внешней среды. Возможные побочные эффекты.
- •30. Механизм защиты от токсического действия кислорода. Антиоксидантная система
- •2. Антиоксидантная система
- •32. Нарушения энергетического обмена, причины. Гипоэнергетические (энергодефицитные) состояния, их причины и последствия.
- •Гипоэнергетические состояния
- •33. Окислительное декарбоксилирование пировиноградной кислоты. Строение пируватдегидрогеназного комплекса, роль витамина в-1
- •34. Цикл лимонной кислоты (цикл Кребса), последовательность реакций, характеристика окислительных ферментов, связь с цепью переноса электронов, энергетическая и пластическая функции.
- •Модуль III. Обмен и функции углеводов
- •35. Метаболизм фруктозы и галактозы, связь с онтогенезом. Галактоземия, фруктозурия.
- •36. Основные углеводы пищи. Общая схема источников и путей расходования глюкозы в организме.
- •37. Гликолиз, последовательность реакций, связь с общими путями катаболизма (полное аэробное окисление глюкозы). Физиологическая роль процесса.
- •38. Анаэробное окисление глюкозы (анаэробный гликолиз), последовательность реакций, физиологическое значение, регуляция. Судьба молочной кислоты.
- •39. Метаболизм фруктозы и галактозы, связь с онтогенезом. Галактоземия, фруктозурия.
- •40. Пентозофосфатный путь превращения глюкозы, окислительные реакции, энергетическая функция, образование восстановительных эквивалентов и рибозы.
- •41. Глюконеогенез. Ключевые реакции, роль пирувата, лактата, аминокислот. Значение процесса, регуляция. Роль биотина.
- •42. Синтез и распад гликогена: биологическое значение процесса. Зависимость от ритма питания. Регуляция. Гликогенозы и агликогенозы.
- •43. Поддержание физиологического уровня глюкозы в крови. Цикл Кори и глюкозо-аланиновый цикл.
- •44. Гипо- и гипергликемия, почечный порог для глюкозы, глюкозурия. Толерантность к глюкозе.
- •45. Особенности обмена глюкозы в различных тканях (мышцы, эритроциты, мозг, жировая ткань, печень). Зависимость путей использования глюкоза от ритма и характера питания.
- •Модуль IV. Структура, функция и обмен липидов. Биологические мембраны, строение, функции
- •47. Повреждение мембран, связь с развитием болезней. Основные повреждающие факторы. Перекисное окисление липидов (пол). Роль неблагоприятной экологической обстановки в активации этого процесса.
- •49. Ненасыщенные и полиненасыщенные (пнжк) жирные кислоты. Зависимость их концентрации от питания. W-3 и w-6 жирные кислоты как предшественники синтеза эйкозаноидов, простагландинов и лейкотриенов.
- •50. Транспортные липопротеины крови, особенности строения, функции. Апобелки. Роль липопротеинлипазы и лецитин-холестерин-ацилтрансферазы (лхат).
- •51.Метаболизм плазменных липопротеинов. Атерогенные и антиатерогенные липопротеины. Дислипопротеинемии, гиперлипопротеинемии. Атеросклероз. Коэффициент атерогенности.
- •52. Различия синтеза триацилглицеринов (таг) в печени и жировой ткани. Взаимопревращение глицерофосфолипидов. Жировое перерождение печени. Липотропные факторы.
- •53. Депонирование и мобилизация жиров, биологическая роль процессов, зависимость от ритма питания и физической нагрузки. Гормональная регуляция липолиза и липогенеза.
- •55. Синтез и использование кетоновых тел. Гиперкетонемия, кетонурия, ацидоз при сахарном диабете и голодании.
- •56. Синтез и функции холестерина. Образование мевалоновой кислоты. Регуляция процесса, гмг-КоА-редуктаза. Транспорт и выведение холестерина из организма.
- •57. Обмен полиненасыщенных жирных кислот. Образование эйкозаноидов, строение, номенклатура, биосинтез, биологическая роль.
- •58. Желчь, желчные кислоты (первичные и вторичные). Желчные мицеллы их образование и роль Применение хенодезоксихолевой кислоты для лечения болезни.
- •59.Синтез жирных кислот, пальмитат синтетазный комплекс, строение, последовательность реакций. Источники восстановительных эквивалентов. Микросомальная система удлинения жирных кислот.
- •Модуль V. Обмен белков и аминокислот
- •2. Оксидаза l-аминокислот
- •3. Оксидаза d-аминокислот
- •3. Биологическое значение трансаминирования
- •2. Органоспецифичные аминотрансферазы ант и act
- •1. Реакции синтеза мочевины
- •2. Энергетический баланс процесса
- •3. Биологическая роль орнитинового цикла
- •Модуль VI. Обмен и функции нуклеиновых кислот. Матричные биосинтезы.
- •Модуль VII. Гормоны. Гормональная регуляция метаболических процессов
- •81. Гормоны поджелудочной железы. Строение, образование, механизм действия инсулина и глюкагона.
- •82. Кальций и фосфор. Биологические функции, распределение в организме. Регуляция обмена, участие паратгормона, кальцитонина и активных форм витамина d.
- •83. Гормоны коры надпочечников: минерало - и глюкокортикоиды. Строение, синтез. Влияние на водно-солевой обмен, обмен белков, липидов и углеводов.
- •84. Йодсодержащие гормоны, строение, биосинтез, Влияние на обмен веществ. Изменения обмена при гипертиреозе и гипотиреозе.
- •85. Адреналин. Строение, биосинтез, биологическая роль.
- •86. Гормоны передней доли гипофиза, строение, место в системе регуляции. Биологическая роль.
- •87. Гормоны задней доли гипофиза (вазопрессин и окситоцин), строение, биологическая роль.
- •88. Половые гормоны: мужские и женские, влияние на обмен веществ.
- •89. Гипер- и гипопродукция гормонов (разобрать на примерах гормонов щитовидной железы, надпочечников). Модуль VIII. Биохимия крови и мочи
- •90. Общий белок и белковый спектр плазмы крови. Альбумины и глобулины их функции, гипо - и гиперпротеинемия, диспротеинемии, парапротеинемии.
- •92.Каликреин-кининовая система, синтез кининов, биологическая роль.
- •93. Форменные элементы крови. Особенности метаболизма в эритроцитах и лейкоцитах. Биохимические механизмы, обеспечивающие резистентность эритроцита.
- •94. Синтез гема и гемоглобина. Регуляция этих процессов. Вариации первичной структуры и свойств гемоглобина. Гемоглобинопатии.
- •95. Железо. Транспорт, депонирование, функции, обмен. Нарушения обмена: железодефицитная анемия, гемосидероз, гемохроматоз.
- •96.Дыхательная функция крови. Молекулярные механизмы газообмена в легких и тканях. Факторы, влияющие на насыщение гемоглобина кислородом. Карбоксигемоглобин, метгемоглобин.
- •97.Ферменты крови «собственные» и поступающие при повреждении клеток. Диагностическая ценность анализа белков и ферментов крови
- •98. Белки и ферменты крови. Белки «острой фазы». Физиологически активные пептиды (кининовая система).
- •99. Распад гема, образование, обезвреживание и выделение билирубина. Конъюгированный и неконъюгированный билирубин. Гипербилирубинемии.
- •100. Виды желтух (гемолитическая, паренхиматозная, обтурационная, новорожденных). Диагностическое значение определения билирубина в крови и моче.
- •101. Буферные системы крови: бикарбонатная, фосфатная, белковая, гемоглобиновая. Причины развития и формы ацидоза и алкалоза. Возможные последствия этих отклонений.
- •102. Состав мочи. Нормальные и патологические компоненты. Исследование мочи с целью диагностики болезней.
- •103. Клиническое значение биохимического анализа крови (белки, ферменты, глюкоза, мочевина, железо, кальций и др.).
- •Модуль iх. Биохимии отдельных органов и тканей: соединительной, мышечной, нервной
- •113. Биохимические основы проведения нервного импульса. Роль ферментов, медиаторов, атф, мембранных белков, кальция, калия и натрия.
95. Железо. Транспорт, депонирование, функции, обмен. Нарушения обмена: железодефицитная анемия, гемосидероз, гемохроматоз.
Николаев стр. 491-493
Гемосидероз — избыточное отложение гемосидерина в тканях организма. Возникает при усиленном распаде эритроцитов, нарушении утилизации этого пигмента в процессе эритроцитопоэза, усиленном всасывании его в кишечнике, при нарушении обмена железосодержащих пигментов.В организме взрослого человека содержится 4—5 г железа, в основном в составе гемопротеидов и соединений резервного железа — ферритина и гемосидерина, являющихся белковыми комплексами. Основной представитель гемопротеидов — гемоглобин клеток эритроидного ряда. При избытке железа в организме гемосидерин накапливается в тканях, что сопровождается повреждением лизосом.
Гемохроматоз (пигментный цирроз, бронзовый диабет) - HLA-ассоциированное полисистемное заболевание, наследуемое по аутосомно-рецессивному типу, обусловленное генетическим дефектом, который приводит к повышенному всасыванию железа в желудочно-кишечном тракте и с избыточным накоплением железа в организме, что проявляется поражением печени, поджелудочной железы, сердца, кожи, суставов, гипофиза.
Транспорт железа в плазме крови и его поступление в клетки
В плазме крови железо транспортирует белок трансферрин. Трансферрин - гликопротеин, который синтезируется в печени и связывает только окисленное железо (Fe3+). Поступающее в кровь железо окисляет фермент ферроксидаза, известный как медьсодержащий белок плазмы крови церулоплазмин. Одна молекула трансферрина может связать один или два иона Fe3+, но одновременно с анионом СО32- с образованием комплекса трансферрин-2 (Fe3+-CO32-). В норме трансферрин крови насыщен железом приблизительно на 33%.
Трансферрин взаимодействует со специфическими мембранными рецепторами клеток. В результате этого взаимодействия в цитозоле клетки образуется комплекс Са2+-кальмодулин-ПКС, который фосфорилирует рецептор трансферри-на и вызывает образование эндосомы. АТФ-зависимый протонный насос, находящийся в мембране эндосомы, создаёт кислую среду внутри эндосомы. В кислой среде эндосомы железо освобождается из трансферрина. После этого комплекс рецептор - апотрансферрин возвращается на поверхность плазматической мембраны клетки. При нейтральном значении рН внеклеточной жидкости апотрансферрин изменяет свою конформацию, отделяется от рецептора, выходит в плазму крови и становится способным вновь связывать ионы железа и включаться в новый цикл его транспорта в клетку. Железо в клетке используется для синтеза железосодержащих белков или депонируется в белке ферригине.
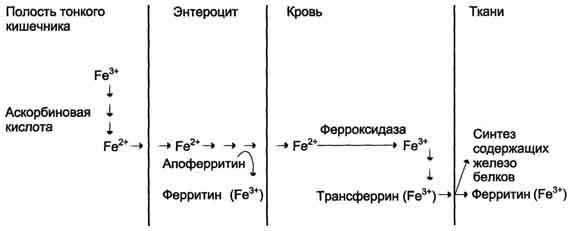
Рис. 13-7. Поступление экзогенного железа в ткани. В полости кишечника железо освобождается из белков и солей органических кислот пищи. Усвоению железа способствует аскорбиновая кислота, восстанавливающая железо. В клетках слизистой оболочки кишечника избыток поступившего железа соединяется с белком апоферритином с образованием ферритина, при этом ферритин окисляет Fe2+ в Fe3+. Поступление железа из клеток слизистой оболочки кишечника в кровь сопровождается окислением железа ферментом сыворотки крови ферроксидазой. В крови Fe3+ транспортирует белок сыворотки крови трансферрин. В тканях Fe2+ используется для синтеза железосодержащих белков или депонируется в ферритине.
Ферритин - олигомерный белок с молекулярной массой 500 кД. Он состоит из тяжёлых (21 кД) и лёгких (19 кД) полипептидных цепей, составляющих 24 протомера. Разный набор прогомеров в олигомере ферритина определяет образование нескольких изоформ этого белка в разных тканях. Ферритин представляет собой полую сферу, внутри которой может содержаться цо 4500 ионов трёхвалентного железа, но обычно содержится менее 3000. Тяжёлые цепи ферритина окисляют Fe2+ в Fe3+, Железо в виде гидроксидфосфата находится в центре сферы, оболочка которой образована белковой частью молекулы. Оно поступает внутрь и освобождается наружу через каналы, пронизывающие белковую оболочку апоферритина, но железо может откладываться и в белковой части молекулы ферритина. Ферритин содержится почти во всех тканях, но в наибольшем количестве в печени, селезёнке и костном мозге. Незначительная часть ферритинаэкскретируется из тканей з плазму крови. Поскольку поступление ферэитина в кровь пропорционально его содержанию в тканях, то концентрация ферритина в крови - важный диагностический показатель запасов железа в организме при железодефидитной анемии. Метаболизм железа в организме представлен на рис. 13-8.
В. Регуляция поступления железа в клетки
Содержание железа в клетках определяется соотношением скоростей его поступления, использования и депонирования и контролируется двумя молекулярными механизмами. Скорость поступления железа в неэритроидные слетки зависит от количества белков-рецепторов трансферрина в их мембране. Избыток железа в клетках депонирует ферритин. Синтез шоферритина и рецепторов трансферринарегулируется а уровне трансляции этих белков и зависит от содержания железа в клетке.
На нетранслируемом 3'-конце мРНК рецептора трансферрина и на нетранслируемом 5'-конце мРНКапоферритина имеются шпилечные петли - железочувствительные элементы IRE (рис. 13-9 и 13-10). Причём мРНК рецептора трансферрина имеет 5 петель, а мРНКапоферритина - только 1.
Эти участки мРНК могут взаимодействовать с регуляторным IRE-связывающим белком. При низких концентрациях железа в клетке IRE-связывающий белок соединяется с IRE мРНКапоферритина и препятствует присоединению белковых факторов инициации трансляции (рис. 13-9, А). В результате этого снижаются скорость трансляции апоферритина и его содержание в клетке. Вместе с тем при низких концентрациях железа в клетке IRE-связывающий белок связывается с железочувствительным элементом мРНК рецептора трансферрина и предотвращает её разрушение ферментом РНК-азой (рис. 13-10, А). Это вызывает увеличение количества рецепторов трансферрина и ускорение поступления железа в клетки.
При повышении содержания железа в клетке в результате его взаимодействия с IRE-связывающим белком происходит окисление SH-групп активного центра этого белка и снижение сродства к железочувствительным элементам мРНК. Это приводит к двум последствиям:
во-первых, ускоряется трансляция апоферритина (рис. 13-9, Б);
во-вторых, IRE-связывающий белок освобождает шпилечные петли мРНК рецептора трансферрина, и она разрушается ферментом РНК-азой, в результате снижается скорость синтеза рецепторов трансферрина (рис. 13-10, Б). Ускорение синтеза апоферритина и торможение синтеза рецепторов трансферрина вызывают снижение содержания железа в клетке.
В целом эти механизмы регулируют содержание железа в клетках и его использование для синтеза железосодержащих белков.
ОБМЕН ЖЕЛЕЗА
В гемсодержащих белках железо находится в составе гема. В негемовых железосодержащих белках железо непосредственно связывается с белком. К таким белкам относят трансферрин, ферритин, окислительные ферменты рибонук-леотидредуктазу и ксантиноксидазу, железофлавопротеины NADH-дегидрогеназа и сукцинат-дегидрогеназа.
В организме взрослого человека содержится 3 - 4 г железа, из которых только около 3,5 мг находится в плазме крови. Гемоглобин имеет примерно 68% железа всего организма, ферритин - 27%, миоглобин - 4%, трансферрин - 0,1%, На долю всех содержащих железо ферментов приходится всего 0,6% железа, имеющегося в организме. Источниками железа при биосинтезе железосодержащих белков служат железо пищи и железо, освобождающееся при постоянном распаде эритроцитов в клетках печени и селезёнки.
В нейтральной или щелочной среде железо находится в окисленном состоянии - Fe3+, образуя крупные, легко агрегирующие комплексы с ОН-, другими анионами и водой. При низких значениях рН железо восстанавливается и легко диссоциирует. Процесс восстановления и окисления железа обеспечивает его перераспределение между макромолекулами в организме. Ионы железа обладают высоким сродством ко многим соединениям и образуют с ними хелатные комплексы, изменяя свойства и функции этих соединений, поэтому транспорт и депонирование железа в организме осуществляют особые белки. В клетках железо депонирует белок ферритин, в крови его транспортирует белок трансферрин.
А. Всасывание железа в кишечнике
В пище железо в основном находится в окисленном состоянии (Fe3+) и входит в состав белков или солей органических кислот. Освобождению железа из солей органических кислот способствует кислая среда желудочного сока. Наибольшее количество железа всасывается в двенадцатиперстной кишке. Аскорбиновая кислота, содержащаяся в пище, восстанавливает железо и улучшает его всасывание, так как в клетки слизистой оболочки кишечника поступает только Fe2+. В суточном количестве пищи обычно содержится 15 - 20 мг железа, а всасывается только около 10% этого количества. Организм взрослого человека теряет около 1 мг железа в сутки.
Количество железа, которое всасывается в клетки слизистой оболочки кишечника, как правило, превышает потребности организма. Поступление железа из энтероцитов в кровь зависит от скорости синтеза в них белка апоферритина. Апоферритин "улавливает" железо в энтероцитах и превращается в ферритин, который остаётся в энтероцитах. Таким способом снижается поступление железа в капилляры крови из клеток кишечника. Когда потребность в железе невелика, скорость синтеза апоферритина повышается (см. ниже "Регуляция поступления железа в клетки"). Постоянное слущивание клеток слизистой оболочки в просвет кишечника освобождает организм от излишков железа. При недостатке железа в организме апоферритин в энтероцитах почти не синтезируется.елезо, поступающее из энтероцитов в кровь, транспортирует белок плазмы крови трансферрин (рис. 13-7).
Нарушения метаболизма железа
Железодефицитная анемия может наблюдаться при повторяющихся кровотечениях, беременности, частых родах, язвах и опухолях ЖКТ, после операций на ЖКТ. При железодефицитной анемии уменьшается размер эритроцитов и их пигментация (гипохромные эритроциты малых размеров). В эритроцитах уменьшается содержание гемоглобина, понижается насыщение железом трансферрина, а в тканях и плазме крови снижается концентрация ферритина. Причина этих изменений - недостаток железа в организме, вследствие чего снижается синтез гема и ферритина в неэритроидных тканях и гемоглобина в эритроидных клетках.
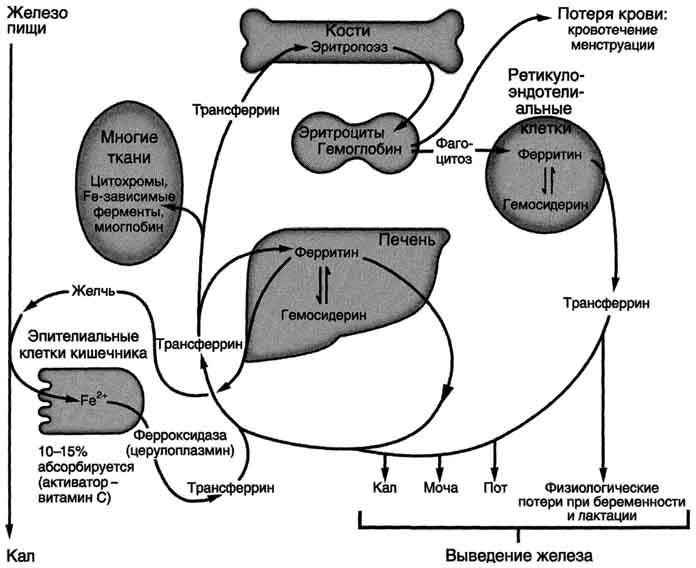
Рис. 13-8. Метаболизм железа в организме.
