
- •ПРЕДИСЛОВИЕ ПЕРЕВОДЧИКА
- •ПРЕДИСЛОВИЕ
- •СПИСОК СОКРАЩЕНИЙ
- •1. Введение
- •1.1. Освещение по Кёлеру
- •1.1.1. Принципы метода
- •1.1.2. Предварительная проверка оборудования
- •1.2. Установка света по Кёлеру
- •2.1. Преломление
- •2.1.1. Числовая апертура
- •2.2. Отражение, поглощение и пропускание
- •2.3. Флуоресценция/фосфоресценция
- •2.4. Поляризация
- •2.5. Дифракция
- •2.5.1. Тестовые пластинки Аббе
- •2.5.2. Формирование первичного изображения
- •2.5.3. Разрешающая способность
- •2.5.4. Роль конденсора в разрешении микроскопа
- •2.5.5. Увеличение
- •2.5.6. Увеличение и разрешение
- •4. Поле зрения
- •5. Резюме
- •6. Литература для дальнейшего чтения
- •1. Введение
- •1.1. Определение контраста
- •2. Светлопольная микроскопия
- •3. Фазовый контраст
- •3.2. Дифрагированный свет в фазовом контрасте
- •4. Темнопольная микроскопия
- •4.1. Освещение по Рейнбергу
- •4.2. Темнопольные конденсоры высокого разрешения
- •4.3. Темнопольное изображение
- •5. Поляризованный свет
- •5.1. Использование одиночного поляризатора
- •5.2. Использование скрещенных поляризаторов
- •5.2.2. Направление двулучепреломления
- •6.3. Интерференционная отражательная микроскопия
- •6.3.2. Физические основы метода
- •6.3.3. Интерпретация результатов
- •7.1. Красители
- •7.2. Использование светофильтров
- •7.3. Срезы
- •7.4. Качество препарата
- •8. Другие методы
- •8.1. Дисперсионное окрашивание
- •10. Благодарности
- •11. Литература
- •ФИКСИРОВАНИЕ ИЗОБРАЖЕНИЯ
- •1. Введение
- •2. Рисование
- •3. Фотомикрография
- •4.1. Разрешение
- •4.2. Разрешающая способность и размер отпечатка
- •4.4. Освещение
- •5. Микроскоп для фотомикрографии
- •5.1. Штатив микроскопа
- •5.2. Оптика
- •5.2.1. Числовая апертура и увеличение объективов
- •5.2.2. Исправление аберраций
- •5.2.4. Иммерсионные объективы
- •5.2.5. Глубина резкости
- •5.2.6. Кривизна поля зрения
- •5.2.7. Типы конденсоров
- •5.2.8. Чистка линз
- •6. Камера для фотомикрографии
- •6.1. Выбор размера пленки
- •6.3. Специальная фотомикрографическая камера
- •6.4. Микроскопы со встроенными фотосистемами
- •6.5. Камера с мехами
- •7. Наведение на фокус и определение экспозиции
- •7.1. Наведение на фокус
- •7.2. Определение экспозиции
- •7.3. Контроль экспозиции
- •8. Выбор условий для фотомикрографии
- •8.1. Фотографический процесс
- •8.1.1. Чувствительность пленки
- •8.1.2. Зернистость
- •8.1.3. Контрастность
- •8.2. Черно-белая фотомикрография
- •8.3. Цветная фотомикрография
- •8.3.1. Цветные отпечатки или слайды
- •8.3.2. Печать со слайдов
- •8.3.3. Цветовая температура
- •8.3.4. Коррекция цветовых искажений
- •8.3.6. Выбор чувствительности пленки
- •8.4. Поляроидные клетки
- •8.4.2. Камера Поляроид SX70
- •8.4.3. Поляроидные слайды
- •8.5. Хранение неэкспонированной пленки
- •9. Фотомакрография
- •9.1.1. Стереомикроскопы для фотомикрографии
- •9.1.2. Макроскопы
- •9.1.3. Фотомакрографические объективы
- •9.2. Освещение для фотомакрографии
- •9.3. Определение экспозиции при фотомакрографии
- •10. Завершение процесса фотомикрографии
- •10.1. Содержание записей
- •10.2. Хранение негативов
- •10.3. Хранение слайдов
- •10.4. Монтаж слайдов
- •10.5. Хранение отпечатков
- •10.6. Определение и указание увеличения
- •11. Практическое руководство
- •11.2. Начальная калибровка экспонометра
- •12. Литература для дальнейшего чтения
- •ИММУНОГИСТОХИМИЯ
- •1. Введение
- •2. Антитела
- •2.1. Структура иммуноглобулинов
- •2.2. Поликлональная антисыворотка
- •2.3. Моноклональные антитела
- •2.4. Очистка антител
- •2.5. Специфичность реакций антител
- •2.6. Хранение антител
- •3.1. Выбор условий обработки ткани
- •3.2. Выявление скрытых антигенов
- •4. Выбор способа мечения
- •4.1. Флуоресцентные метки
- •4.2. Ферментные метки
- •4.2.1. Пероксидаза хрена
- •4.2.2. Щелочная фосфатаза
- •4.2.3. Глюкозооксидаза
- •4.2.4. Галактозидаза
- •4.3. Коллоидное золото
- •4.4. Выбор метки
- •5. Методы окраски
- •5.1. Прямой метод
- •5.2. Непрямой метод
- •5.4. Системы с использованием биотин — авидина
- •5.5. Другие методы
- •6. Экспериментальные методы
- •6.1. Общее описание метода
- •6.2. Выбор правильного разведения антител
- •6.3. Флуоресцентные метки
- •6.4. Пероксидаза
- •6.4.1. Ингибирование эндогенного фермента
- •6.5. Щелочная фосфатаза
- •6.5.1. Блокирование эндогенного фермента
- •6.5.2. Мера предосторожности
- •6.6. Глюкозооксидаза
- •6.7. Галактозидаза
- •6.9. Некоторые общие процедуры
- •6.9.1. Покрытие предметных стекол
- •6.9.2. Дополнительное окрашивание
- •7.1. Контрольные препараты
- •7.2. Решение проблем
- •9. ДНК-зонды для гибридизации in situ
- •9.1. Принцип метода гибридизации
- •9.2. Экспериментальная процедура
- •9.2.1. Выявление Y-хромосомы
- •9.2.2. Выявление цитомегаловируса
- •10. Цитологические препараты
- •11. Количественная оценка
- •12. Оборудование
- •13. Благодарности
- •14. Литература
- •ГИСТОХИМИЯ И СВЕТОВАЯ МИКРОСКОПИЯ
- •1. Введение
- •1.1. Объекты для гистохимического окрашивания
- •1.1.1. Что такое окрашивание?
- •2. Приготовление и хранение срезов препаратов
- •2.1. Необходимые характеристики препарата
- •2.2. Методы приготовления и хранения препаратов
- •2.2.1. Получение тонких слоев
- •3. Что можно выявлять? Некоторые примеры
- •3.1. Выявление химических свойств
- •3.1.1. Химические фрагменты
- •3.1.2. Специфические вещества
- •3.1.3. Классы веществ
- •3.2. Выявление биологических объектов
- •3.2.1. Биологические объекты
- •3.2.2. Биологические процессы
- •3.3. Морфологические исследования
- •4. Выбор методов
- •5.1. Оценка селективности методов
- •5.2. Оценка локализации окрашивания
- •5.4. Оценка чистоты реагентов
- •5.5. Номенклатура реагентов
- •6. Что необходимо для гистохимической работы
- •6.1. Оборудование и материалы
- •6.2. Как научиться работать?
- •7. Почему используются гистохимические методы
- •8. Благодарности
- •ФЛУОРЕСЦЕНТНАЯ МИКРОСКОПИЯ
- •1. Введение
- •2. Флуорохромы
- •3. Флуоресцентный микроскоп
- •3.1. Способы освещения
- •3.1.1. Освещение проходящим светом
- •3.1.2. Освещение падающим светом
- •3.2. Источники света
- •3.3. Домики для ламп
- •3.4. Фильтры
- •3.4.1. Возбуждающие фильтры
- •3.4.2. Запирающие фильтры
- •3.4.3. Цветные светоделительные зеркала
- •3.5. Объективы и окуляры
- •4. Применение флуоресцентных красителей
- •4.1. Нуклеиновые кислоты
- •4.1.1. Прижизненное окрашивание флуорохромами
- •4.2. Иммунофлуоресценция
- •4.3. Флуоресценция нейромедиаторов
- •4.4. Двойное окрашивание
- •5. Микрофлуориметрия
- •5.1. Введение
- •5.2. Стандарты флуоресценции
- •5.3. Оборудование
- •5.3.1. Инвертированные микрофлуориметры
- •5.3.2. Сканирующие микрофлуориметры
- •5.4. Измерения содержания ДНК
- •5.4.1. Оборудование
- •5.4.2. Подготовка материала
- •5.4.3. Процедура окрашивания
- •5.4.4. Проведение измерений
- •6. Анализ изображения при флуоресценции
- •7. Сканирующая лазерная микроскопия
- •8. Литература
- •МИКРОМЕТРИЯ И АНАЛИЗ ИЗОБРАЖЕНИЯ
- •1. Введение
- •2. Простая микрометрия
- •2.1. Измерения длины
- •2.1.3. Окуляр-микрометр сдвига
- •2.1.4. Другие методы измерения длины
- •2.2 Измерения углов
- •2.3. Измерение толщины
- •2.4. Счетные камеры
- •2.4.2. Техника работы с гемоцитометром
- •3.1.1. Определение АA в двухфазном препарате
- •3.2. Принципы измерения площади поверхности
- •4. Измерения с использованием дигитайзера
- •5.2. Измерения с помощью компьютера
- •6. Приборы и математическое обеспечение работ
- •7. Литература
- •ВИДЕОМИКРОСКОПИЯ
- •1. Видеомикроскопия и оборудование для нее
- •1.1. Введение
- •1.1.1. Видеоусиление
- •1.1.2. Видеоинтенсификация
- •1.1.3. Цифровая обработка изображения
- •1.2.1. Условия ограниченного числа фотонов
- •1.3. Различные методы видеомикроскопии
- •1.3.1. Видеомикроскопия с усилением
- •1.3.2. Аналоговое усиление контраста
- •1.3.3. Цифровая обработка изображения
- •1.4.1. Камеры и контроллеры камер
- •1.4.5. Видеопроцессорные платы
- •1.4.6. Монофункциональные процессоры
- •1.4.7. Взгляд в будущее
- •1.5. Условия, налагаемые на микроскоп
- •1.6. Как соединить телекамеру с микроскопом
- •2.1. Различные виды VEC-микроскопии
- •2.2. Приготовление препаратов
- •2.3. Получение изображения
- •2.4. Интерпретация изображений
- •2.5. Типичные применения и ограничения метода
- •2.5.1. Светлопольная микроскопия
- •2.5.2. Темнопольная микроскопия
- •2.5.4. Фазовый контраст
- •2.5.5. Поляризационная микроскопия
- •2.5.7. Отражательная контрастная микроскопия
- •2.5.8. Флуоресцентная микроскопия
- •2.5.9. Примеры применения в биологии и биохимии
- •3.1. Введение
- •3.2. Процесс формирования изображения
- •3.2.1. Условия, касающиеся микроскопа
- •3.2.2. Получение статических изображений
- •3.2.3. Получение изображений подвижных объектов
- •3.3. Типичные приложения
- •3.3.2. Картирование отношений
- •3.3.4. Визуализация молекул
- •3.3.6. Люминесценция
- •3.3.7. Нейробиология
- •4.1. Пространственные измерения
- •4.2. Измерения по интенсивности
- •5.1. Видеозапись и редактирование
- •5.1.1. Стандарты видеотехники
- •5.1.2. Форматы видеопленок
- •5.1.3. Качество видеопленок
- •5.1.4. Видеомагнитофоны
- •5.1.5. Видеомагнитофоны с цейтраферной записью
- •5.1.6. Запись при видеомикроскопии
- •5.1.8. Копирование и редактирование видеозаписей
- •5.2.1. Оборудование
- •5.3. Перенос видеозаписей в видеофильм
- •5.4. Рисование с монитора
- •6. Благодарности
- •7. Литература
- •1. Введение
- •2. Классификация сегментов хромосом
- •2.1. Гетерохроматиновые сегменты
- •2.2. Эухроматиновые сегменты
- •2.3. Ядрышковые организаторы
- •2.4. Кинетохоры
- •4.2. G-окрашивание
- •4.2.1. ASG-метод
- •4.2.3. Метод Галлимора и Ричардсона
- •4.3. R-окрашивание
- •4.4. Q-окрашивание
- •4.4.1. Q-окрашивание с помощью акрихина
- •4.5.2. Процедура окраски
- •5.1. Окрашивание ДАФИ/дистамицином
- •5.2.1. Метод культивирования клеток
- •5.2.2. Методика окраски
- •5.3.2. Синхронизация с помощью БУДР [39]
- •5.3.3. Синхронизация с помощью ФУДР [13, 40]
- •6. Наблюдение и регистрация сегментов хромосом
- •6.3. Фотографирование сегментированных хромосом
- •6.4.1. Получение профилей сегментов
- •6.4.2. Отражательная микроскопия
- •6.4.3. Измерение полиморфизма хромосом
- •7. Благодарности
- •8. Литература
- •9. Литература для дальнейшего чтения
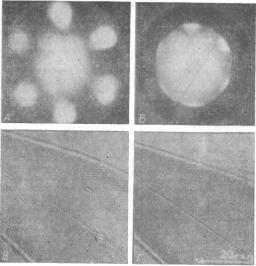
Рис. 1.6. Связь изображения с дифракционной картиной
взадней фокальной плоскости объектива. Использован масляно-иммерсионный объектив Planapo (Zeiss), NA 1,3—0,8, Х100. Препарат диатомовой водоросли P. angulatum (шкала — 20 мкм). А. З.ф.п. объектива при полностью открытой диафрагме объектива. На рисунке виден свет нулевого порядка в центре и дифракционный спектр первого порядка от диатомовой водоросли, который собран объективом. Б. З.ф.п. при закрытой диафрагме объектива. Дифракционный спектр первого порядка почти полностью исключен. В. Изображение, получаемое в ситуации А, где различные дифракционные спектры участвуют в формировании изображения. Г. Изображение, получаемое в ситуации Б, где дифракционный спектр первого порядка не участвует
вформировании изображения. Обратите внимание, что в случае В разрешается гексагональная структура, а в Г — нет.
Угол отклонения дифрагированного светового луча определяется формулой sin6 = X/A:, где к — период образца.
Таблица 1.8. Метод нахождения диска Рамсдена и определения его размера
1.Используя матовое стекло или кусочек бумаги, можно наблюдать диск Рамсдена, держа стекло под прямым углом на расстоянии около 3 мм от вершины окуляра и сфокусировав микроскоп на препарат. Диск Рамсдена в этой точке будет иметь вид слабо освещенного кружка.
2.Отметьте его диаметр и расстояние от поверхности глазной линзы окуляра.
3.Окуляры, используемые людьми, носящими очки, имеют достаточное расстояние, чтобы очковая линза могла поместиться между поверхностью окуляра и глазом. Величина диска Рамсдена пропорциональна апертуре объектива и обратно пропорциональна общему увеличению микроскопа, как следует из уравнения 4.
Объектив собирает свет, рассеянный образцом. Число порядков дифракции, собранное объективом, определяется его отверстным углом (sin а), а более точно — числовой апертурой, в которой учитывается показатель преломления среды, находящейся между препаратом и объективом.
Если из микроскопа вынуть окуляр, то с помощью фазового телескопа можно наблюдать з. ф. п. объектива. Она содержит множество изображений источника света, число которых соответствует числу порядков дифрагированного света, собранных объективом. Таким образом, з. ф. п. выступает в роли оптического преобразователя образца.
Свет, выходящий из з. ф. п., распространяется в виде серии конусов, вершины которых представляют собой дифракционный спектр, видимый в з. ф. п. Поскольку лучи в каждом из этих конусов происходят из одного источника, то они способны интерферировать. Интерференционная картина, возникающая в плоскости первичного изображения, есть результат взаимодействия света нулевого и первого порядков. Эта интерференционная картина является первичным изображением и представляет собой увеличенную репродукцию образца.
Можно показать, что если перекрыть свет нулевого порядка, заслонив центральную часть з. ф. п., то в результате получится изображение с обратным контрастом. Если аналогичным образом удалить первый дифракционный максимум, то изображение, получающееся в результате интерференции нулевого максимума и второго максимума, будет нести удвоенное количество информации. Взаимооднозначное соответствие между деталями образца и изображения достигается только тогда, когда в формировании изображения участвует первый дифракционный максимум. Все остальные дифракционные максимумы, попадающие в изображение, улучшают его качество, давая более резкие границы деталей и лучшее разрешение изображения по интенсивности. Первичное изображение само по себе есть Фурье-преобразование, которое реализуется в з. ф. п. объектива, и, таким образом, к нему приложимы многочисленные термины, описывающие данный процесс. Если дифракционный максимум первого порядка не участвует в построении изображения, то микроскоп не может разрешить детали препарата, дающие такую дифракцию.
3. ф. п. объектива будет еще раз обсуждаться в гл. 2 применительно к фазово-контрастной микроскопии.
2.5.3. Разрешающая способность
Эксперименты с тестовой пластинкой Аббе и с диатомовыми водорослями показывают, как строится
15
изображение в микроскопе из света, который проходит через з. ф. п. объектива. Если мы видим деталь изображения, то это значит, что микроскоп разрешил соответствующую деталь и построил ее изображение. Мы уже видели, что разрешение деталей возможно только в том случае, если объектив собирает первый дифракционный максимум достаточно хорошо для того, чтобы в результате интерференции возникло первичное изображение. Данная возможность объектива определяется его NA.
Величина NA не имеет размерности, так как она является отношением двух величин. Мы уже видели, что синий свет собирается легче, чем красный, при любом значении NA. Таким образом, разрешающая сила пропорциональна NA и обратно пропорциональна длине волны освещающего препарат света. Разрешающая сила может быть выражена как способность разрешать отрезок (между двумя точками), и этот отрезок
называется разрешением. Оно задается формулой: |
|
Разрешение = 0,61 X λ/NА. |
(2) |
Подставляя в данную формулу длину волны зеленого света, например, 500 нм, и NA 1,3, мы получаем разрешение объектива около 250 нм. Таким образом, теоретически микроскоп позволяет исследователю наблюдать раздельно две точки, находящиеся на расстоянии 250 нм. Их невозможно будет разрешить, если они будут находиться друг к другу ближе, чем на расстоянии 250 нм.
2.5.4. Роль конденсора в разрешении микроскопа
В уравнении (2) используется NA объектива, однако на практике конденсор также играет определенную роль в достижении максимального разрешения. Во всех экспериментах, о которых говорилось выше, использовался очень узкий пучок света, чтобы наблюдать угол дифракции. Однако на самом деле конденсор освещает объект широким конусом света. При освещении по Кёлеру этот конус составляет примерно 66% от конуса, воспринимаемого объективом. Так, объектив с апертурой 1,3 требует конденсора с апертурой 0,9. Это означает, что некоторые лучи будут выходить из препарата под углом около 70° к вертикали. Эти лучи будут давать первый и более высокие дифракционные максимумы на стороне, обращенной к объективу, а те же максимумы со стороны предметного стекла будут потеряны. Если конденсор вообще не имеет числовой апертуры, то свет не попадает на образец. Таким образом, в формуле для разрешающей способности должен учитываться конденсор. На практике она имеет следующий вид:
Разрешение = 0,61 х λ /(NAoб. + NАконд.)/2. (3)
Глаз человека имеет предел разрешения порядка 2-х угловых минут у людей с ослабленным зрением и порядка 1-й минуты у людей с острым зрением. Таким образом, разрешение микроскопа должно быть таким, чтобы для глаза угловые размеры достигали вышеуказанной величины. Эта проблема будет обсуждаться в следующем разделе.
2.5.5. Увеличение
Схема светового микроскопа, выполненная на основании геометрической оптики, показывает (рис. 1.7), что увеличение есть двустадийный процесс.
Во-первых, увеличенное действительное изображение (Н) препарата (h) создается объективом в плоскости первичного изображения. Математически увеличение есть отношение размеров изображения к размерам препарата (когда оба они находятся на одинаковом расстоянии от глаза или экрана). Это первичное увеличение, которое часто бывает выгравировано на объективе. Создаваемое объективом изображение оказывается в микроскопе внутри окуляра и является перевернутым. Если поместить маленький кружочек матового стекла на то место окуляра, где обычно располагается измерительная шкала, то, в случае контрастного образца, можно увидеть первичное изображение.
Во-вторых, проходя через окуляр, свет меняет свое направление таким образом, что в глаз попадает конус света со значительно большим углом. Это вторичное увеличение, которое обычно выгравировано на окуляре. Конечное изображение, наблюдаемое при этой величине угла, будет иметь размер Н'. Общее увеличение микроскопа (У. М.) есть результат первичного увеличения объектива и вторичного увеличения окуляра.
Увеличение объектива, -как правило, очень тесно связано с его апертурой. Так, апертуре 0,65 соответствует увеличение
Dp= (2 X Dя X NA)/У.М., |
(4) |
где Dя — расстояние ясного зрения, которое полагается равным 250 мм. Для практических целей диаметр диска Рамсдена (Dp) может быть принят равным 1—3 мм. Эти параметры ограничивают отношение увеличения к числовой апертуре в пределах от 170 до 1000.
Практическое правило, приведенное выше, должно быть скорректировано в соответствии с размером зрачка глаза наблюдателя. С оптической точки зрения зрачок наблюдателя — это входной зрачок (глаз), а диск Рамсдена — выходной зрачок (микроскоп). Они работают совместно лучше всего тогда, когда их размеры совпадают и они правильно расположены друг относительно друга. Для определения положения и размеров диска Рамсдена см. табл. 1.8.
16

Рис. 1.7. Геометрическая оптика светового микроскопа: fOK — фокусное расстояние окуляра; foe — фокусное расстояние объектива; Т — длина тубуса; h — размеры препарата; Н — размеры первичного изображения; Н' — размеры конечного изображения; £>я — расстояние ясного зрения (250 мм).
Х40, а апертуре 1,3 соответствует увеличение около ХЮО. Окуляры имеют увеличение 10 или 6,3, но могут быть и другие увеличения. В некоторых микроскопах имеется система, позволяющая изменять увеличение, даваемое окулярами. Однако существует определенное соответствие между общим увеличением микроскопа и числовой апертурой используемого объектива:
Таблица 1.9. Демонстрация пустого (избыточного) увеличения
1.Рассмотрите диатомовую водоросль, например Navicula lyra, с помощью объектива Х40 с NA 0,65 и окуляра Х6, дающих общее увеличение Х240. Отметьте, что в изображении, полученном с помощью данного объектива, можно различить точки, расстояние между которыми равно примерно 500 нм.
2.Повторите наблюдение с объективом ХЮ, NA 0,25 и окуляром Х25, которые вместе дадут вам примерно то же увеличение. Контур клеток виден, но детали их поверхности не видны.
3.Можно сделать вывод, что во втором случае имеется избыточное увеличение. Объектив способен разрешить детали размером не менее, чем 1200 нм, а детали строения диатомовой водоросли значительно мельче. Таким образом, в данном случае имеется избыточное, или пустое увеличение.
2.5.6.Увеличение и разрешение
Дальнейшее увеличение лимитируется пределом разрешения объектива (см. разд. 2.5.3). Функция увеличения состоит в том, чтобы сделать угловые размеры деталей изображения достаточными для того, чтобы глаз мог их различать. Искомый угол лежит в пределах 1—2-х угловых минут. При стандартном расстоянии 250 мм от глаза под таким углом виден отрезок длиной 0,1 мм. Таким образом, разрешение объектива должно соответствовать этому уровню. Например, для того, чтобы достичь разрешения деталей в 500 нм, минимальное увеличение микроскопа при использовании объектива с числовой апертурой 0,65 нм теоретически должно быть 200. На практике используется увеличение, которое в несколько раз превышает расчетное. Эти величины могут быть получены из приведенных выше формул. Можно видеть, что для получения общего увеличения 400 при использовании объектива с числовой апертурой 0,65 и первичным увеличением Х40 необходимо использовать окуляр с увеличением не менее Х5 (см. табл. 1.9).
Любое дополнительное увеличение сверх минимального называется пустым (бесполезным) увеличением. Оно несколько ухудшает изображение, не добавляя к нему никаких новых деталей.
2.5.7. Резюме; о роли дифракции в световой микроскопии
В разд. 2.5.1—2.5.6 было уже достаточно сказано об отдельных сторонах данного явления, теперь необходимо только свести их все вместе. Дифракция— это лишь один из путей рассеяния света образцом, однако было показано, что она находится в количественном соответствии с латеральной разрешающей способностью микроскопа. Разрешающая сила объектива определяется его способностью собирать дифрагированный свет; соответствующий параметр объектива называется его числовой апертурой. Предел разрешения объектива доводится до предела разрешения глаза наблюдателя с помощью увеличения, величина которого оговаривалась выше. Любое дополнительное увеличение не дает дополнительной информации, однако оно может быть полезно, чтобы избежать излишнего напряжения глаз.
Разрешение, о котором мы говорили до сих пор, — это разрешение по осям х и у препарата. Теперь нам
17
предстоит рассмотреть разрешение по оси z. Оно также зависит от NA объектива и будет обсуждаться в следующем разделе.
3. Глубина поля зрения (глубина резкости)
Рассмотрение оптических причин появления глубины резкости (г. р.) не входит в задачу настоящей книги, но на практике пределы глубины в микроскопии очень важны. Большая г. р. является наиболее привлекательной чертой сканирующей электронной микроскопии, однако сканирующая световая микроскопия еще не достигла такого же совершенства и не имеет столь же широкого употребления. Очень малая г. р. объективов с большим увеличением используется для того, чтобы получать информацию в каждый данный момент времени только с одной плоскости на оси z внутри препарата. (В настоящее время разработана методика использования изображений с очень малой глубиной резкости, получаемых на лазерных сканирующих микроскопах.) Повышение контраста изображения достигается за счет удаления расфокусированного света, исходящего из плоскостей, лежащих выше и ниже плоскости, находящейся в фокусе. Данная техника рассмотрена в разд. 3.1.
При визуальной микроскопии г. р. зависит от трех факторов: разрешающей способности объектива по оси г; геометрической г. р. и аккомодационной способности глаза [1]. Эти факторы объединены в уравнении (5). Г. р. прямо пропорциональна длине волны используемого света, обратно пропорциональна не просто апертуре объектива, а квадрату ее и также обратно пропорциональна увеличению. Джеймс [1] рассчитал г. р. прибора, которая есть видимая г. р. минус фактор глаза. Некоторые значения ее приведены в табл. 1.10.
Таблица 1.10. Общая глубина резкости (мкм) в зависимости от объектива и общего увеличения (п=1,5) [1]
Числовая |
|
Общее увеличение микроскопа |
|
|||
Х10 |
Х50 |
Х100 |
Х500 |
X1000 |
||
апертура |
||||||
объектива |
|
|
|
|
|
|
0,05 |
1187 |
371 |
|
|
|
|
0,3 |
|
|
22 |
8 |
|
|
0,65 |
|
|
|
3 |
2 |
|
0,85 |
|
|
|
2 |
1 |
|
1,3 |
|
|
|
1 |
0,6 |
|
г.р. = n[λ/2 X (NА)2]+[0,34/(У. M. X NA)]. |
|
(5) |
||||
Величины, приводимые в табл. 1.10, являются ориентировочными, но можно видеть, что они очень малы для объективов с большой NA и что если величина г. р. является критической, то в некоторых случаях лучше использовать объективы с малой NA и небольшим первичным увеличением в комбинации с окулярами с большим увеличением. Такая комбинация, разумеется, скажется на латеральном разрешении, как показано в разд. 2.5. Измерение глубины поля зрения описано в гл. 7, разд. 2.3.
При визуальном наблюдении опытный исследователь постоянно двигает фокус вверх и вниз с тем, чтобы составить себе представление об изображении по всей глубине. Будущие разработки в области видеозаписи и вывода на экран собранных изображений, как упоминалось выше, смогут избавить людей от такого запоминания. Фотография поля зрения очень хорошо показывает пределы г. р. при фиксированной фокусировке. Малая глубина фокуса является преимуществом в том случае, когда необходимо использовать оптическое сечение по оси z.
3.1. Тандемная или конфокальная сканирующая микроскопия
В последнее время с целью обойти ограничение, налагаемое в световой микроскопии малой глубиной фокуса, была предложена сканирующая техника. В ней препарат сканируется серией очень маленьких полей зрения, изображения этих полей •собираются по отдельности, затем полное изображение восстанавливается из них, как мозаика. В одном из таких микроскопов используется вращающийся диск Нипкова диаметром 100 мм, содержащий 48000 отверстий, через которые освещается препарат. При отражательной микроскопии тот же диск используется для пропускания света. Частота сканирования составляет 12 000 линий через изображение, прибор дает 20 полных изображений в секунду, составленных из 400 частичных изображений. Эта система была названа тандемным сканирующим отражательным световым микроскопом (ТСОСМ). Петран и др. [3] использовали эту технику для исследования деталей строения костей в крупных объектах, таких, как черепа, и для исследования малопрозрачных трехмерных препаратов, таких, как ткани растений или животных.
Несколько лазерных сканирующих микроскопов было разработано с целью улучшения качества
18
