
XAXANINA
.pdfКаждую колбу закрывают пробкой, взбалтывают в течение нескольких минут и оставляют выстаиваться на сутки. Для определения pH пригодна только отстоявшаяся,
совершенно прозрачная вытяжка. Поэтому перед измерением pH раствор над почвой целесообразно отфильтровать. Прозрачный раствор вытяжки (фильтрат) переливают в стакан на 100 мл, опускают электроды и измеряют pH на иономере.
По полученному значению pH почвы рассчитывают нормы внесения известняка,
гашеной извести, золы на земельный участок в 500 м2.
71

Работа № 12
Ионоселективное определение примесей различных ионов в природной и питьевой воде
А. Определение хлорид-ионов
В последнее время в потенциометрии широко применяются так называемые ионо-
селективные электроды, позволяющие избирательно измерять активную концентрацию определяемых ионов в растворе в присутствии посторонних ионов, мешающих определе-
нию.
Помимо высокой избирательности ионоселективные электроды отличаются боль-
шой чувствительностью (10–4 - 10–5 моль/л, а в некоторых случаях и 10–7 моль/л). С их по-
мощью проводят экспрессные определения, автоматический непрерывный химико-
аналитический контроль производства и т.п. Ионоселективные электроды обеспечивают избирательное определение многих типов ионов. В табл.12 приведены основные характе-
ристики ионоселективных электродов.
Ионометрический анализ природной и питьевой воды на содержание ионов осно-
ван на измерении величины равновесного потенциала ионоселективного мембранного электрода, погруженного в раствор анализируемого иона. Потенциал измеряют относи-
тельно электрода сравнения, снабженного солевым мостиком, заполненного 1 М раство-
ром нитрата калия, с помощью иономера (рис.7).
Рис.7. Внешний вид иономера
72
|
|
|
|
|
Таблица 12 |
|
|
|
Основные характеристики ионоселективных электродов |
||||
|
|
|
|
|
||
|
Определяемые |
Состав мембраны |
Чувствительность, |
|
||
|
ионы |
|
моль/л |
|
||
|
|
|
|
|||
|
F |
|
LaF3 |
10–6 - 10–7 |
|
|
|
Cl |
|
Ag2S - AgCl |
10 |
–5 |
|
|
|
|
|
|
||
|
Br |
|
Ag2S - AgBr |
10–6 |
|
|
|
I |
|
Ag2S - AgI |
5 10–7 |
|
|
|
CN |
|
Ag2S - AgI |
5 10–6 |
|
|
|
NO |
|
Жидкий ионообменник - четвер- |
10–5 |
|
|
|
3 |
|
тичные аммониевые соли |
|
|
|
|
|
|
|
|
|
|
|
ClO |
|
Жидкий ионообменник - четвер- |
10–5 |
|
|
|
4 |
|
тичные аммониевые соли |
|
|
|
|
|
|
|
|
|
|
|
S2 |
|
Ag2S |
10–7 |
|
|
|
SCN , S O2 |
Ag2S - AgSCN |
10–5 |
|
||
|
2 |
3 |
|
|
|
|
|
|
|
Жидкий ионообменник - каль- |
|
|
|
|
Ca 2 |
|
циевая соль додецилфосфорной |
10–4 |
|
|
|
|
|
кислоты |
|
|
|
|
Cu 2 |
|
Ag2S - CuS |
10–6 |
|
|
|
Pb2 |
|
Ag2S - PbS |
10–6 |
|
|
|
Cd2 |
|
Ag2S - CdS |
10–6 |
|
|
|
K |
|
Жидкий ионообменник - валино- |
10–5 |
|
|
|
|
|
мицин |
|
|
|
При потенциометрических измерениях, проводимых для определения концентра-
ций отдельных веществ методом прямой потенциометрии или методом потенциометри-
ческого титрования, монтируют ячейку, состоящую из индикаторного электрода и элек-
трода сравнения. Как правило, она представляет собой обычный химический стакан.
Раствор в ячейке перемешивают с помощью механической или магнитной мешалки.
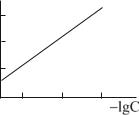
Концентрацию анализируемого иона находят по калибровочному графику, который строят в координатах Е - (–lgC) (рис.8).
E, мВ |
|
|
325 |
|
|
225 |
|
|
125 |
|
|
2 |
4 |
6 |
Рис.8. Калибровочный график |
||
73
Оборудование и реактивы
Иономер.
Ионоселективный электрод на Сl–.
Электрод сравнения хлоридсеребряный.
Пипетки мерные на 10 мл.
Стаканы стеклянные на 100 и 250 мл.
Бумага фильтровальная.
Хлорид калия.
Нитрат калия, 1 М раствор.
Описание определения
По точной навеске готовят серию стандартных растворов хлорида калия (10–1 - 10–5
М) с постоянной ионной силой, создаваемой 1 М раствором нитрата калия. Снимают за-
висимость потенциала ионоселективного электрода от концентрации хлорида калия и строят градуировочный график. Измерения проводят в порядке возрастания концентра-
ции. После каждого измерения электроды промывают дистиллированной водой и осуша-
ют фильтровальной бумагой.
Измеряют значения равновесных потенциалов анализируемых растворов. Опреде-
ляют концентрацию хлорид-ионов в питьевой и природной воде, пользуясь построенным
калибровочным графиком.
Концентрацию хлорид-ионов вычисляют в граммах по формуле
X(г) = С(моль/л)∙МСl–.
Результаты измерений заносят в форму табл.13.
Форма таблицы 13
Результаты ионометрического определения ионов в воде
|
|
Эталоны |
|
|
Исследуемые |
|
|||
Параметры |
|
|
|
растворы |
|
||||
|
|
|
|
|
|
||||
|
1 |
2 |
3 |
4 |
1 |
|
2 |
|
3 |
Концентрация |
|
|
|
|
|
|
|
|
|
С, моль/л |
|
|
|
|
|
|
|
|
|
Потенциал Е, В |
|
|
|
|
|
|
|
|
|
74

Б. Определение фторид-ионов
Селективность электродов на твердых мембранах связана с возможностью перено-
са через мембрану только определяемого иона.
Мембрану фторселективного электрода изготавливают из фторида лантана, в кото-
рый с целью снижения электрического сопротивления вводят ионы Eu2+. Такой электрод имеет высокую селективность по отношению к ионам фтора, причем зависимость потен-
циала от логарифма концентрации линейна. Зависимость потенциала такого мембранного электрода (индикаторный электрод) от активности фторид-ионов описывается уравнением Нернста:
|
|
RT |
|
|
|
|
и.э и.э |
|
ln aF |
или и.э и.э 0,059 ln aF . (1) |
|||
nF |
||||||
|
|
|
|
|
||
Для измерения потенциала ионоселективного электрода собирают схему:
Электрод сравнения |
Исследуемый раствор Индикаторный электрод |
||||
Ag | Ag Cl| KCl |
F− |
LaF3 |
|
|
|
ЭДС Е этого гальванического элемента: |
|
|
|
||
|
E эл.с и.э . |
|
|
(2) |
|
Решая уравнения (1) и (2), получают: |
|
|
|
||
|
−lg aF− = |
E K' |
, |
|
|
|
|
|
|
||
|
0,059 |
|
|
|
|
где K' - константа, включающая постоянные величины |
, |
. |
|||
|
|
|
эл.ср |
и.э |
|
Для учета общей константы K' проводят градуировку ионоселективного электрода,
т.е. устанавливают зависимость ЭДС от активности (или концентрации при постоянной ионной силе) фторид-ионов.
При анализе природных и производственных объектов следует помнить, что F–-ион в кислых растворах или в присутствии ионов Fe3+ и Al3+ находится в виде слабодиссоции-
рующей кислоты HF и фторидных комплексов указанных металлов. Поэтому в растворе доводят рН до значения 5 - 7, а также добавляют цитрат натрия, который образует с иона-
ми железа и алюминия более прочные комплексы.
Оборудование и реактивы
Иономер.
Индикаторный электрод - ионоселективный электрод на F–-ион. Перед работой вы-
держивают электрод в 0,001 М NaF в течение суток. Перед измерением промывают и ос-
75
тавляют на 10 - 20 минут в дистиллированной воде, затем осушают фильтровальной бума-
гой.
Электрод сравнения - хлоридсеребряный.
Стаканы полиэтиленовые емкостью от 50 мл.
Колбы мерные на 100 мл, 6 шт.; на 1000 мл, 1 шт.
Цилиндры на 50, 100, 1000 мл.
Пипетки мерные на 10 и 25 мл.
Стандартный раствор фторида натрия 0,1 М (навеску 4,200 г растворяют в мерной колбе емкостью 1000 мл).
Фоновый раствор - сульфат натрия 1 М (навеску 142 г Na2SO4 или 322 г Na2SO410H2O (технические весы) растворяют в мерной колбе емкостью 1000 мл).
Азотная кислота, 0,01 М раствор (готовят разбавлением 0,7 мл концентрированной
HNO3 до объема 1000 мл).
Аммиак, 0,01 М водный раствор (готовят разбавлением 0,75 мл концентрированно-
го NH3 до объема 1000 мл).
Бидистиллированная вода.
Описание определения
Необходимо изучить инструкцию по работе на иономере.
Для калибровки фторселективного индикаторного электрода надо построить график зависимости φ и.э. от концентрации фторид-иона CF При построении графика в стандарт-
ные и анализируемые растворы вводят одинаковый избыток фонового электролита. В
этом случае можно полагать, что во всех растворах ионная сила постоянна и одинакова и поэтому φ и.э = const + 0,059lg CF.
Из основного стандартного раствора с концентрацией фторид-иона 10–1 М приготовьте последовательным разбавлением его раствором 1 М Na2SO4 шесть растворов с концентрацией
NaF (M): 10–1, 10–2, 10–3, 10–4, 10–5, 10–6. Для этого отберите пипеткой 10 мл 10–1 М раствора
NaF в мерную колбу на 100 мл и доведите фоновым раствором (1 М Na2SO4) объем до метки.
Из полученного раствора 10–2 M Na2SO4 последовательным разбавлением фоновым раство-
ром приготовьте остальные растворы.
При определении концентрации фторид-иона в анализируемом растворе необходи-
мо приготовить раствор с той же ионной силой. Для этого 5 мл исследуемого раствора раз-
ведите 1 М Na2SO4 в колбе на 50 мл.Индикаторной бумагой проверьте рН и доведите его
0,01 М HNO3 или NН4OH до значения 5,0 - 5,5. 76
Измерьте потенциал фторселективного электрода в этом растворе.
По градуировочному графику определите значение pX = –lgCF– в любом анализи-
руемом растворе.
В иономере с ионоселективным электродом градуировочный график строится мик-
ропроцессором автоматически на основе измеренных значений ЭДС электродной системы стандартных растворов NaF. Также автоматически выдается значение pX = –lgCF– в анали-
зируемом растворе, исходя из ранее построенного градуировочного графика.
Определите содержание фторид-иона в контрольных задачах, проверьте результат у преподавателя и вычислите относительную погрешность измерений.
В. Определение примесей железа
Содержание железа в поверхностных водах суши составляет десятые доли милли-
грамма в одном литре, вблизи болот - единицы миллиграммов в одном литре. Повышен-
ное содержание железа наблюдается в болотных водах, в которых железо находится в ви-
де комплексов с солями гуминовых кислот - гуматами. Наибольшие концентрации железа
(до нескольких десятков и сотен миллиграммов в одном литре) наблюдаются в подземных водах с низкими значениями рН.
Являясь биологически активным элементом, железо в определенной степени влияет на интенсивность развития фитопланктона и качественный состав микрофлоры в водо-
емах.
Концентрация железа подвержена заметным сезонным колебаниям. Обычно в во-
доемах с высокой биологической продуктивностью в период летней и зимней стагнации заметно увеличение концентрации железа в придонных слоях воды. Осенне-весеннее пе-
ремешивание водных масс (гомотермия) сопровождается окислением Fe (II) в Fе (III) и
выпадением последнего в виде Fe(OH)3.
Поскольку соединения железа в воде могут существовать в различных формах (как в растворе, так и во взвешенных частицах), более точные результаты могут быть получе-
ны только при определении суммарного железа во всех его формах, так называемого об-
щего железа.
Перевод железа в растворимую форму, пригодную для анализа, проводят, добавляя
кпробе определенное количество сильной кислоты (HNO3, HCl, H2SO4) до рН 1 - 2.
Вкислой среде (рН < 5) ионы железа (III) образуют с комплексоном ЭДТА прочный комплекс (рКнест = 25,1):
77

Fe3+ + H2Y2‾ FeY‾ + 2H+.
При титровании с ионоселективным и хлоридсеребряным электродами скачок по-
тенциала в точке эквивалентности связан с практическим исчезновением окисленной формы окислительно-восстановительной системы Fe3+/Fe2+.
Для получения устойчивых значений потенциалов титруемый раствор должен содер-
жать сопряженную форму окислительно-восстановительной пары: Fe2+-ионы, образующие прочный комплекс с H2Y2–.
Оборудование и реактивы
Иономер.
Электрод ионоселективный на железо (III).
Электрод сравнения хлоридсеребряный.
Вода бидистиллированная.
Пипетки на 10 мл.
Стаканы стеклянные на 100, 250 мл.
Бумага фильтровальная.
Соль Мора, 1%-ный раствор.
Ацетат натрия, 10%-ный раствор.
ЭДТА 0,05 М раствор.
Описание определения
В стакан емкостью 100 мл пипеткой перенесите аликвотную часть (25 мл) анализи-
руемого раствора, разбавьте ее 50 мл воды, опустите мешалку и установите стакан на площадке магнитной мешалки. Добавьте 10%-ный раствор ацетата аммония до момента,
пока раствор не окрасится в желто-оранжевый цвет вследствие гидролиза соли железа.
Добавьте 5 - 10 капель 1%-ного раствора соли Мора. В раствор поместите ионоселектив-
ный электрод и хлоридсеребряный электрод сравнения, заполненный насыщенным рас-
твором хлорида калия.
Схема ГЭ будет иметь следующий вид:
Ag, AgCl |
|
KClнас Исследуемый |
Ионоселективный |
|
|||
|
|
раствор |
электрод Fe3+ |
|
|
78
После включения магнитной мешалки начните титрование, прибавляя по 2 мл 0,05
М раствора ЭДТА и измеряя ЭДС. Вблизи точки эквивалентности титрант прибавляйте по
1 мл.
Результаты титрования запишите в форму табл.14 и постройте графики в коорди-
натах E-V и (ΔЕ/ΔV - V).
|
|
|
|
|
|
Форма таблицы 14 |
|
|
Результаты титрования |
|
|
|
|
||
|
|
|
|
|
|
|
|
Номер опыта |
Объем добавляемого |
Измеренная ЭДС, В |
|
E |
|
Концентрация |
|
титранта V, мл |
|
V |
|
железа, г |
|
||
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
Вычислите содержание Fe3+ в граммах во всем объеме анализируемого раствора по формуле
m(г) (V N)ЭДТА ЭFe n 10 3 ,
где N - нормальная концентрация; V - объем раствора ЭДТА; ЭFe - эквивалент же-
леза; n - число аликвотных частей.
Г. Определение нитрат-ионов
Ионометрический анализ природной и питьевой воды на содержание нитрат-ионов основан на измерении величины равновесного потенциала ионоселективного мембранно-
го электрода, погруженного в раствор анализируемого иона. В состав мембраны входят жидкий ионообменник с четвертичными аммониевыми солями. Потенциал измеряют на иономере относительно хлоридсеребряного электрода, заполненного насыщенным рас-
твором хлорида калия.
Оборудование и реактивы
Иономер.
Ионоселективный электрод на NO3.
Электрод сравнения хлоридсеребряный.
Вода бидистиллированная.
Пипетки на 10 мл.
Стаканы стеклянные на 100 и 250 мл.
Бумага фильтровальная.
79
Хлорид калия.
Нитрат калия, 10–1 М раствор.
Сульфат калия, 1 М раствор.
Описание определения
По точной навеске готовят стандартный раствор нитрата калия 10–1 М. Последова-
тельным разбавлением исходного стандартного раствора готовят растворы 10–2 - 10–5 М с постоянной ионной силой, создаваемой 1 М раствором сульфата калия (фон А). Снимают зависимость потенциала ионоселективного электрода от концентрации нитрата калия и строят калибровочный график. Измерения проводят в порядке возрастания концентрации.
После каждого измерения электроды промывают дистиллированной водой и осушают фильтровальной бумагой.
Измеряют значения равновесных потенциалов анализируемых растворов. Опреде-
ляют концентрацию нитратов в питьевой и природной воде, пользуясь построенным ка-
либровочным графиком.
Концентрацию нитрат-ионов вычисляют в граммах по формуле
Х(г) С(моль / л) МNO3 .
Результаты измерений заносят в форму табл.15.
Форма таблицы 15
Результаты ионометрического определения ионов в воде
Параметры |
|
Эталоны |
|
Исследуемые растворы |
||||
1 |
2 |
3 |
4 |
1 |
2 |
3 |
||
|
||||||||
Концентрация С, моль/л |
|
|
|
|
|
|
|
|
Потенциал Е, В |
|
|
|
|
|
|
|
|
80
