
- •Биохимия Электронный дидактический комплекс (эдк)
- •Физическая химия вода
- •Активная реакция водных растворов
- •Ионное произведение воды. Водородный показатель
- •Методы определения рН среды
- •Роль активной реакции среды в биологических процессах
- •Буферные pacтворы, состав, механизм действия
- •Буферная емкость
- •Биологическое значение буферных систем
- •Коллоидная химия
- •Классификация дисперсных систем
- •Поверхностные явления
- •Адсорбция
- •Коллоидные растворы (золи) Методы получения
- •Строение коллоидных частиц
- •Коагуляция. Седиментация. Пептизация
- •Молекулярно-кинетические свойства коллоидных растворов
- •Осмотическое давление
- •Биологическое значение явления осмоса
- •Механизмы, участвующие в сохранении изоосмии:
- •Оптические свойства коллоидных систем
- •Растворы высокомолекулярных соединений
- •Свободная и связанная вода в коллоидных pacтвopax
- •Свойства растворов вмс
- •Денатурация
- •2. Белки; биологическая роль Аминокислоты
- •Содержание белков в организме и тканях
- •Методы выделения белков
- •Методы фракционирования и очистки белков
- •Физико-химические свойства белков
- •Аминокислоты
- •Ациклические аминокислоты
- •Структура белковой молекулы
- •Классификация белков
- •Химия сложных белков
- •3. Нуклеиновые кислоты
- •Нуклеотиды и нуклеозиды
- •Структура днк
- •Рибонуклеиновые кислоты
- •4. Ферменты
- •Биосинтез и клеточная локализация ферментов
- •Химическая природа ферментов
- •Строение ферментов
- •Активный центр фермента
- •Регуляция активности ферментов
- •Механизм действия ферментов
- •Основные свойства ферментов
- •2. Зависимость активности ферментов от рН среды.
- •Факторы, определяющие активность ферментов
- •Активирование и ингибирование ферментов
- •Типы ингибирования
- •Классификация и номенклатура ферментов
- •Применение ферментов.
- •Использование иммобилизованных ферментов для производства биологических соединений
- •Иммуноферментный анализ и его использование в ветеринарии
- •5. Химия витаминов
- •Классификация и номенклатура витаминов
- •I. Жирорастворимые витамины
- •II. Витамины, растворимые в воде
- •Витамин d, антирахитический, кальциферол
- •Витамин e, антистерильный, токоферолы
- •Витамин к, антигеморрагический (филлохинон)
- •Витамин q (убихинон)
- •Водорастворимые витамины
- •Витамин b1, антиневритный, тиамин
- •Витамин b2, рибофлавин
- •Витамин b3, пантотеновая кислота
- •Витамин b5, pp, никотинамид, ниацин, антипеллагрический
- •Витамин b6, адермин, пиридоксол
- •Витамин b12, кобаламин, антианемический
- •Фолиевая кислота
- •Витамин с (аскорбиновая кислота)
- •Биотин, витамин h
- •6. Гормоны
- •Гормоны гипофиза
- •Поджелудочная железа
- •Гормоны щитовидной железы
- •Гормоны надпочечников
- •Гормоны коры надпочечников
- •Гормоны половых желез
- •Гормоны тимуса (вилочковой железы)
- •Гормоны местного действия
- •7. Обмен веществ и энергии
- •Основные этапы обмена веществ
- •Биологическое окисление
- •Окислительное фосфорилирование
- •Токсичность кислорода
- •8. Химия и обмен углеводов
- •Моносахариды
- •Производные моносахаридов.
- •Полисахариды (гликаны)
- •Гетерополисахариды (гетерогликаны)
- •Обмен углеводов
- •Катаболизм глюкозы
- •Гликогенолиз
- •Биосинтез углеводов
- •Биосинтез гликогена (гликогенез)
- •Регуляция углеводного обмена.
- •9. Химия и обмен липидов
- •Химическое строение нейтральных жиров
- •Жирные кислоты.
- •Нейтральные гликолипиды
- •Фосфолипиды (фосфатиды)
- •Сфинголипиды
- •Двойной липидный слой мембран
- •Обмен липидов
- •Переваривание липидов в желудочно-кишечном тракте
- •Промежуточный обмен липидов
- •Энергетический баланс β-окисления жирных кислот
- •Метаболизм ацетил-коэнзима а
- •Пути образования кетоновых тел
- •Биосинтез липидов
- •Метаболизм стеринов и стеридов
- •Липосомы
- •10. Обмен белков
- •Биологическая ценность белков
- •Нормы белка в питании животных
- •Белковые резервы организма
- •Обмен простых белков
- •Переваривание белков в желудочно-кишечном тракте моногастричных животных
- •Переваривание белков в кишечнике.
- •Особенности переваривания белков у жвачных животных
- •Дезаминирование аминокислот
- •Трансаминирование – непрямой путь дезаминирования аминокислот
- •Декарбоксилирование аминокислот
- •Окислительное расщепление аминокислот
- •Особенности обмена отдельных аминокислот
- •11. Биосинтез белка
- •Генетический код
- •Этапы синтеза белка
- •Мультиферментный механизм синтеза белка
- •12.Обмен нуклеиновых кислот Переваривание нуклеиновых кислот в желудочно-кишечном тракте
- •Промежуточный обмен нуклеиновых кислот Распад нуклеиновых кислот в тканях
- •Пиримидиновые основания
- •Биосинтез нуклеиновых кислот
- •Рекомбинантные молекулы и проблемы генной инженерии
- •Клонирование животных
- •Метод молекулярной гибридизации
- •Принцип метода
- •Способы гибридизации
- •Метод блоттинга по Саузерну
- •Полимеразная цепная реакция (пцр)
- •Необходимые приборы и реактивы
- •13. Обмен воды и солей
- •Вода, ее содержание и роль в организме
- •Потребность животного организма в минеральных веществах, их поступление и выделение
- •Микроэлементы
- •14. Биохимия крови
- •Физико-химические свойства крови
- •Буферные системы крови
- •Плазма крови и ее химический состав
- •Белки плазмы и сыворотки крови
- •Небелковые азотистые вещества крови
- •Форменные элементы крови
- •15. Биохимия мышечной ткани
- •Механизм сокращения мышцы
- •Азотистые экстрактивные вещества мышц
- •Минеральные вещества
- •Окоченение мышц
- •16. Биохимия молока и молокообразования
- •17. Биохимия почек и мочи
- •Патологические компоненты мочи
- •Особенности мочи птиц
- •18. Биохимия кожи и шерсти
- •19. Биохимия яйца
- •Биосинтез компонентов яйца
- •Предметный указатель
- •Приложения
- •Рекомендуемая литература
- •Тесты для проверки биохимических
- •Глава 8. Химия обмена углеводов
- •24. Сложноэфирные связи в молекулах триацилглицеролов подвергаются ферментативному гидролизу при участии:
Клонирование животных
Под клоном понимают генетически однородные потомки одной исходной особи, образующиеся в результате бесполого размножения.
Для создания генетических копий сельскохозяйственных животных методом клеточной инженерии разрабатываются способы клонирования: пересадка ядер соматических клеток в яйцеклетку с предварительно удаленным ядром. Для этого берут от донора стволовые (не прошедшие дифференцировку) клетки. Ядро стволовых клеток in vitro вводят в энуклеированные яйцеклетки реципиента. Полученные таким способом зиготы крупного рогатого скота можно культивировать in vitro до 8-, 16-ти даже 32-клеточной стадии. Таких эмбрионов, достигших завершающих стадий предимплантационного развития, можно не только трансплантировать коровам-реципиентам или замораживать для длительного хранения, но использовать для последующего клонирования. Таким образом, можно в условиях in vitro получать неограниченное количество эмбрионов. Метод клонирования животных является очень привлекательным для получения неограниченно большого количества копий от высокопродуктивных особей, а потому разрабатывается очень интенсивно.
Достижения молекулярной биологии по изучению роли нуклеиновых кислот в процессах жизнедеятельности привели к разработке совершенно новых методов диагностики болезней животных и человека на основе уникальных свойств ДНК и РНК. Это – методы молекулярной гибридизации и полимеразной цепной реакции.
Метод молекулярной гибридизации
Метод молекулярной гибридизации (ДНК-гибридизация, ДНК-зонды) широко применяется для диагностики инфекционных болезней, в генетике, криминалистике и т.д. Метод основан на уникальном свойстве генетического материала организма – молекулы ДНК –, состоящей из мононуклеотидов, образовывать двойную спираль с комплементарно соединенными азотистыми основаниями. Известно, что молекула ДНК представляет полимер, состоящий из четырех видов дезоксирибонуклеотидов (dAMP, dGMP, dTMP, dCMP), соединенных между собой 3'- и 5'-фосфодиэфирными связями дезоксирибоз. Молекула ДНК образует двойную спираль, при которой азотистые основания первой цепи строго комплементарно соединяются водородными связями с азотистыми основаниями второй цепи, при этом аденин соединяется с тимином, гуанин с цитозином.
Принцип метода
Структуру двойной спирали ДНК (или РНК), скрепленную водородными связями, можно разрушить нагреванием, поскольку спаренные, не связанные между собой ковалентно, две полинуклеотидные цепи ДНК после разрыва всех водородных связей полностью разделяются.
Процесс разделения цепей называют денатурацией или плавлением ДНК. Денатурация происходит в узком интервале температур и сопровождается гиперхромным эффектом, т.е. при этом происходит возрастание поглощения ультрафиолетовых лучей. Температуру, при которой происходит разделение цепей ДНК, называют точкой плавления (Т пл.), которая в зависимости от состава ДНК имеет величину примерно 85-95о C. Процесс денатурации ДНК обратимый, т.е. при снижении температуры происходит восстановление водородных связей – отжиг – образование двойной спирали. Это явление называют ренатурацией (рис. 12.2.). Ренатурация связана со специфичностью спаривания азотистых оснований между комплементарными цепями. Реакция происходит в две стадии: вначале короткие комплементарные последовательности двух цепей случайно соединяются друг с другом и образуют двухспиральный участок, затем образуется длинная двухцепочечная структура с восстановлением первоначальных свойств, утраченных при денатурации.
В ренатурации участвуют две комплементарные последовательности. Если при этом взяты цепочки молекулы ДНК из различных источников, то говорят о гибридизации, например при отжиге ДНК и РНК.
В основе гибридизации лежит тот же принцип спаривания комплементарных оснований, который обеспечивает репликацию ДНК или ренатурацию молекул. Способность к гибридизации двух препаратов нуклеиновых кислот является строгим тестом на комплементарность их последовательностей.
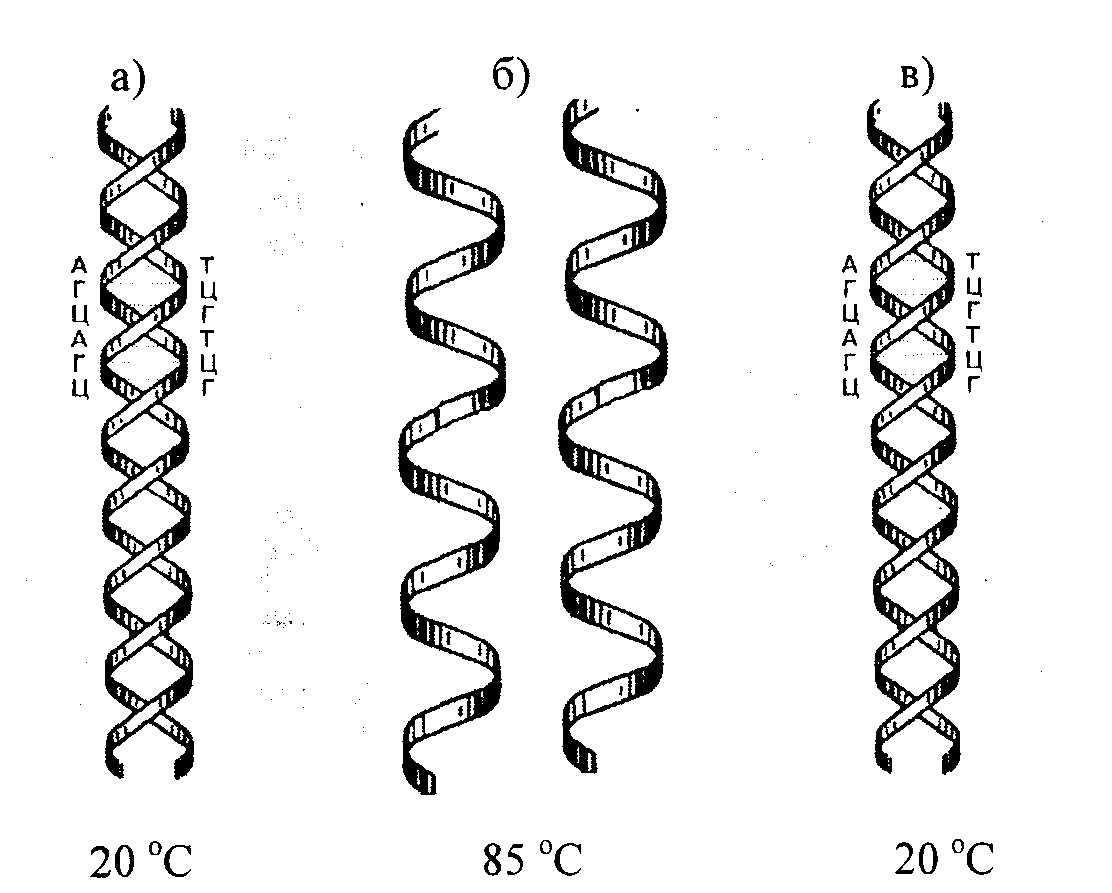
Рис. 12.2. Схема денатурации и ренатурации ДНК; двойная спираль образуется по принципу комплементарности азотистых оснований.
а) нативная молекула ДНК,
б) денатурированная молекула ДНК,
в) ренатурированная молекула ДНК.
