
- •Биохимия Электронный дидактический комплекс (эдк)
- •Физическая химия вода
- •Активная реакция водных растворов
- •Ионное произведение воды. Водородный показатель
- •Методы определения рН среды
- •Роль активной реакции среды в биологических процессах
- •Буферные pacтворы, состав, механизм действия
- •Буферная емкость
- •Биологическое значение буферных систем
- •Коллоидная химия
- •Классификация дисперсных систем
- •Поверхностные явления
- •Адсорбция
- •Коллоидные растворы (золи) Методы получения
- •Строение коллоидных частиц
- •Коагуляция. Седиментация. Пептизация
- •Молекулярно-кинетические свойства коллоидных растворов
- •Осмотическое давление
- •Биологическое значение явления осмоса
- •Механизмы, участвующие в сохранении изоосмии:
- •Оптические свойства коллоидных систем
- •Растворы высокомолекулярных соединений
- •Свободная и связанная вода в коллоидных pacтвopax
- •Свойства растворов вмс
- •Денатурация
- •2. Белки; биологическая роль Аминокислоты
- •Содержание белков в организме и тканях
- •Методы выделения белков
- •Методы фракционирования и очистки белков
- •Физико-химические свойства белков
- •Аминокислоты
- •Ациклические аминокислоты
- •Структура белковой молекулы
- •Классификация белков
- •Химия сложных белков
- •3. Нуклеиновые кислоты
- •Нуклеотиды и нуклеозиды
- •Структура днк
- •Рибонуклеиновые кислоты
- •4. Ферменты
- •Биосинтез и клеточная локализация ферментов
- •Химическая природа ферментов
- •Строение ферментов
- •Активный центр фермента
- •Регуляция активности ферментов
- •Механизм действия ферментов
- •Основные свойства ферментов
- •2. Зависимость активности ферментов от рН среды.
- •Факторы, определяющие активность ферментов
- •Активирование и ингибирование ферментов
- •Типы ингибирования
- •Классификация и номенклатура ферментов
- •Применение ферментов.
- •Использование иммобилизованных ферментов для производства биологических соединений
- •Иммуноферментный анализ и его использование в ветеринарии
- •5. Химия витаминов
- •Классификация и номенклатура витаминов
- •I. Жирорастворимые витамины
- •II. Витамины, растворимые в воде
- •Витамин d, антирахитический, кальциферол
- •Витамин e, антистерильный, токоферолы
- •Витамин к, антигеморрагический (филлохинон)
- •Витамин q (убихинон)
- •Водорастворимые витамины
- •Витамин b1, антиневритный, тиамин
- •Витамин b2, рибофлавин
- •Витамин b3, пантотеновая кислота
- •Витамин b5, pp, никотинамид, ниацин, антипеллагрический
- •Витамин b6, адермин, пиридоксол
- •Витамин b12, кобаламин, антианемический
- •Фолиевая кислота
- •Витамин с (аскорбиновая кислота)
- •Биотин, витамин h
- •6. Гормоны
- •Гормоны гипофиза
- •Поджелудочная железа
- •Гормоны щитовидной железы
- •Гормоны надпочечников
- •Гормоны коры надпочечников
- •Гормоны половых желез
- •Гормоны тимуса (вилочковой железы)
- •Гормоны местного действия
- •7. Обмен веществ и энергии
- •Основные этапы обмена веществ
- •Биологическое окисление
- •Окислительное фосфорилирование
- •Токсичность кислорода
- •8. Химия и обмен углеводов
- •Моносахариды
- •Производные моносахаридов.
- •Полисахариды (гликаны)
- •Гетерополисахариды (гетерогликаны)
- •Обмен углеводов
- •Катаболизм глюкозы
- •Гликогенолиз
- •Биосинтез углеводов
- •Биосинтез гликогена (гликогенез)
- •Регуляция углеводного обмена.
- •9. Химия и обмен липидов
- •Химическое строение нейтральных жиров
- •Жирные кислоты.
- •Нейтральные гликолипиды
- •Фосфолипиды (фосфатиды)
- •Сфинголипиды
- •Двойной липидный слой мембран
- •Обмен липидов
- •Переваривание липидов в желудочно-кишечном тракте
- •Промежуточный обмен липидов
- •Энергетический баланс β-окисления жирных кислот
- •Метаболизм ацетил-коэнзима а
- •Пути образования кетоновых тел
- •Биосинтез липидов
- •Метаболизм стеринов и стеридов
- •Липосомы
- •10. Обмен белков
- •Биологическая ценность белков
- •Нормы белка в питании животных
- •Белковые резервы организма
- •Обмен простых белков
- •Переваривание белков в желудочно-кишечном тракте моногастричных животных
- •Переваривание белков в кишечнике.
- •Особенности переваривания белков у жвачных животных
- •Дезаминирование аминокислот
- •Трансаминирование – непрямой путь дезаминирования аминокислот
- •Декарбоксилирование аминокислот
- •Окислительное расщепление аминокислот
- •Особенности обмена отдельных аминокислот
- •11. Биосинтез белка
- •Генетический код
- •Этапы синтеза белка
- •Мультиферментный механизм синтеза белка
- •12.Обмен нуклеиновых кислот Переваривание нуклеиновых кислот в желудочно-кишечном тракте
- •Промежуточный обмен нуклеиновых кислот Распад нуклеиновых кислот в тканях
- •Пиримидиновые основания
- •Биосинтез нуклеиновых кислот
- •Рекомбинантные молекулы и проблемы генной инженерии
- •Клонирование животных
- •Метод молекулярной гибридизации
- •Принцип метода
- •Способы гибридизации
- •Метод блоттинга по Саузерну
- •Полимеразная цепная реакция (пцр)
- •Необходимые приборы и реактивы
- •13. Обмен воды и солей
- •Вода, ее содержание и роль в организме
- •Потребность животного организма в минеральных веществах, их поступление и выделение
- •Микроэлементы
- •14. Биохимия крови
- •Физико-химические свойства крови
- •Буферные системы крови
- •Плазма крови и ее химический состав
- •Белки плазмы и сыворотки крови
- •Небелковые азотистые вещества крови
- •Форменные элементы крови
- •15. Биохимия мышечной ткани
- •Механизм сокращения мышцы
- •Азотистые экстрактивные вещества мышц
- •Минеральные вещества
- •Окоченение мышц
- •16. Биохимия молока и молокообразования
- •17. Биохимия почек и мочи
- •Патологические компоненты мочи
- •Особенности мочи птиц
- •18. Биохимия кожи и шерсти
- •19. Биохимия яйца
- •Биосинтез компонентов яйца
- •Предметный указатель
- •Приложения
- •Рекомендуемая литература
- •Тесты для проверки биохимических
- •Глава 8. Химия обмена углеводов
- •24. Сложноэфирные связи в молекулах триацилглицеролов подвергаются ферментативному гидролизу при участии:
Структура днк
Нуклеиновые кислоты – высокомолекулярные соединения из нуклеотидов. Чем сложнее клетка, тем больше генетической информации, следовательно, больше ДНК. Например, вирусы содержат одну молекулу ДНК или РНК, сравнительно небольшого размера. Фаги (вирусы бактерий) также содержат одну молекулу ДНК из 40-200 тыс. пар нуклеотидов. Бактериальные клетки имеют более сложную структуру и больше ДНК. Так, клетка кишечной палочки (E.coli) имеет генетический материал из 4-106 пар нуклеотидов (Мм 26-109 кДа) длиной 1,4 мм, что в 700 раз больше самой клетки. Клетка человека содержит 3-109 нуклеотидов в 46 хромосомах. Общая длина молекулы ДНК составляет около 2 метров. Одна хромосома содержит 1 молекулу ДНК. Основная масса ДНК находится в клеточном ядре в хромосомах. Однако небольшая часть ДНК (около 0,1%) обнаруживается в митохондриях. Количество ДНК в пикограммах на 1 клетку составляет у человека 6,8, у курицы – 2,3, дрожжевых клеток – 0,05, E.coli – 0,01. Нуклеотидный состав ДНК изучен Чаргаффом (1949 г.) и установлено, что нуклеотидный состав из различных тканей одного вида животных одинаков, не зависит от возраста, условий питания и внешней среды. Определены правила Чаргаффа для ДНК:
Сумма пуриновых нуклеотидов равна сумме пиримидиновых нуклеотидов: А+Г=Т+Ц.
Молярное содержание аденина равно молярному содержанию тимина (A=T или А/Т=1).
Молярное содержание гуанина равно молярному содержанию цитозина (Г=Ц или Г/Ц=1).
Количество аденина и цитозина равно количеству гуанина и тимина (А+Ц=Г+Т или А+Ц/Г+Т=1).
В ДНК из различных источников неодинаково соотношение нуклеотидов: у одних преобладает содержание аденина над гуанином, тимина над цитозином (А+Т<Г+Ц), у других преобладает гуанин и цитозин над аденином и тимином (Г+Ц>А+Т), т.е. имеется видовая специфичность ДНК по нуклеотидному составу. Благодаря применению различных методов электорофореза, а так же ферментов рестриктаз («генных ножниц»), меченых соединений, методов секвенирования и других современных методов молекулярной биологии изучена последовательность нуклеотидов – первичная структура нуклеиновых кислот.
Первичная структура ДНК – последовательность нуклеотидов, образуется благодаря сложноэфирной связи, возникающей между остатками фосфорной кислоты у 3' углерода дезоксирибозы одного мононуклеотида с 5'углеродом дезоксирибозы другого мононуклеотида (рис.3.4.).
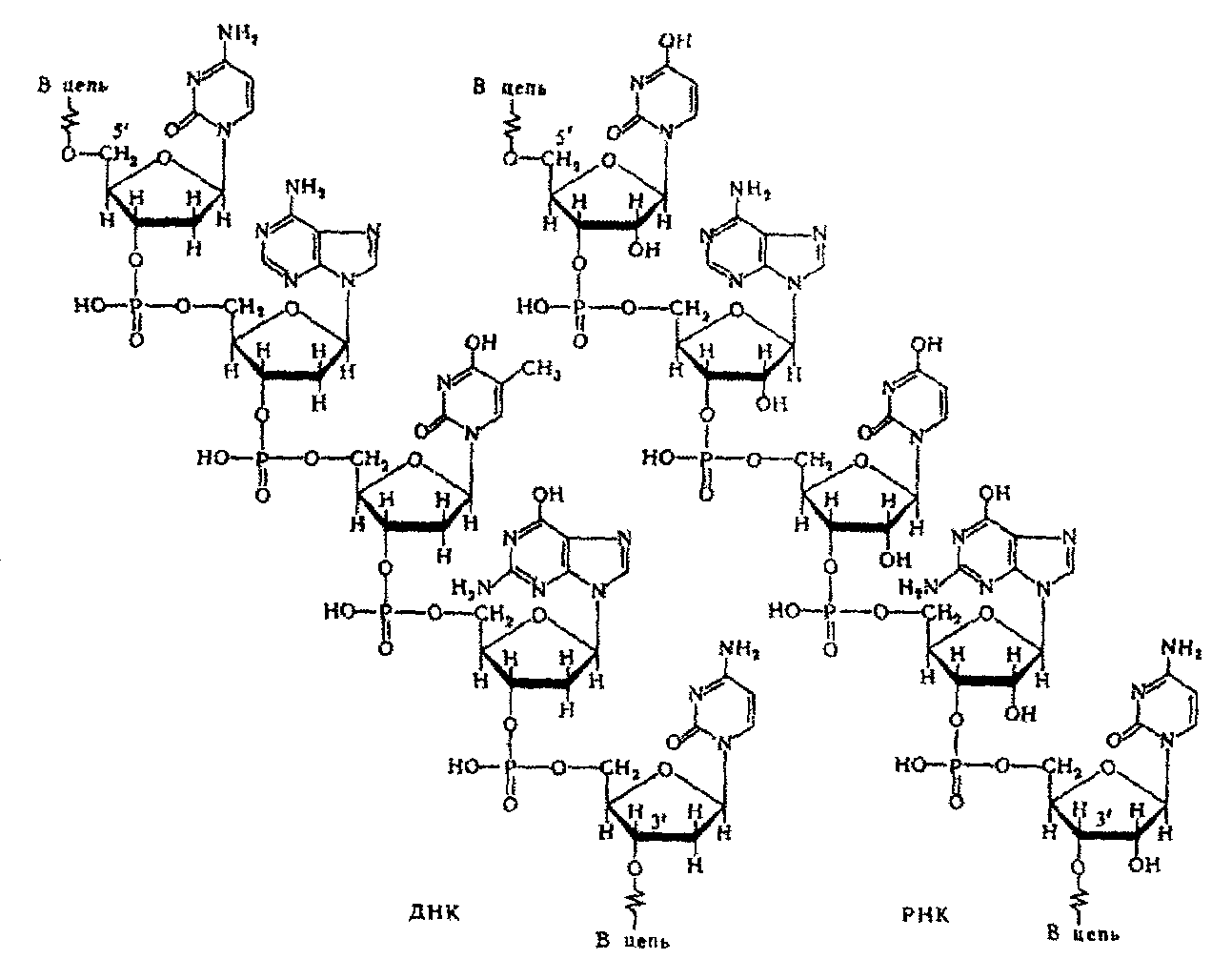
ДНК РНК
а) строение фрагментов молекул ДНК и РНК.
Сверхспиральная Релаксированная
кольцевая ДНК кольцевая ДНК

Рис. 3.4. Строение молекул ДНК и РНК (а); (б) - кольцевидная ДНК
Вторичная структура – спирализация полидезоксирибо-нуклеотидной цепи, вернее двух цепей. Выяснение вторичной структуры ДНК – это одно из крупнейших открытий в биологии, так как при этом был раскрыт молекулярный механизм передачи генетической информации в ряду поколений. В 1953 году Д.Уотсон и Ф.Крик установили, что ДНК представляет собой двойную спираль, состоящую из двух антипараллельных полинуклеотидных цепей. Полинуклеотидная цепь расположена в форме спирали с одним оборотом (шагом) 10 пар нуклеотидов, что составляет 3,4 нм и расстоянием между плоскостями оснований 0,34 нм, при этом между амино- и кетогруппами азотистых оснований образуются водородные связи. Две нуклеотидные цепи образуют правую спираль, при этом углеводно-фосфатные группы располагаются снаружи, а азотистые основания – внутри, где аденин первой цепи соединяется двумя водородными связями с тимином второй цепи, а гуанин с цитозином тремя водородными связями. Связь A=T и Г=Ц называется комплементарной. Связь между указанными азотистыми основаниями является строго специфичной. Так, если в одной цепи последовательность нуклеотидов составляет АТГЦ, то во второй цепи будет комплементарно ТАЦГ. Таким образом, последовательность нуклеотидов в одной цепи автоматически определяет последовательность нуклеотидов в другой комплементарной цепи.
Исследования показали, что кроме указанной выше В-формы ДНК (репликативной формы), в зависимости от влажности и ряда других условий, могут быть: А-форма молекулы при транскрипции (1 виток насчитывает 11 пар нуклеотидов, цепь короче на 25%); С-формы надмолекулярных структур (1 виток имеет 9,3 пар оснований), Z-формы (левая спираль, на 1 виток приходится 12 нуклеотидов). Известны и другие формы (бок о бок форма, кольцевидная форма, одноцепочечная и т.д.).
Из физико-химических свойств, кроме большой длины молекулы, следует отметить денатурацию молекулы ДНК, которая происходит при повышении температуры свыше 800C. При этом происходит разрыв водородных связей между азотистыми соединениями, двухцепочечная молекула «расщепляется» на составляющие цепи. Полная денатурация ДНК - это расхождение комплементарных цепей. При охлаждении раствора денатурированной ДНК цепи до комнатной температуры (или несколько ниже 800C) происходит восстановление нативной структуры. Этот прием называется отжигом. Восстановление первоначальной структуры нуклеиновой кислоты называется ренатурацией. Образование двойной спирали ДНК по принципу комплементарности широко применяется для диагностики инфекционных болезней животных методом молекулярной гибридизации, ДНК-зондированию, полимеразной цепной реакции, для генетических исследований. Принцип комплементарности обеспечивается при синтезе новой молекулы ДНК, когда происходит удвоение молекулы - репликация ДНК, что очень важно для передачи генетических особенностей организма (рис.3.5).
М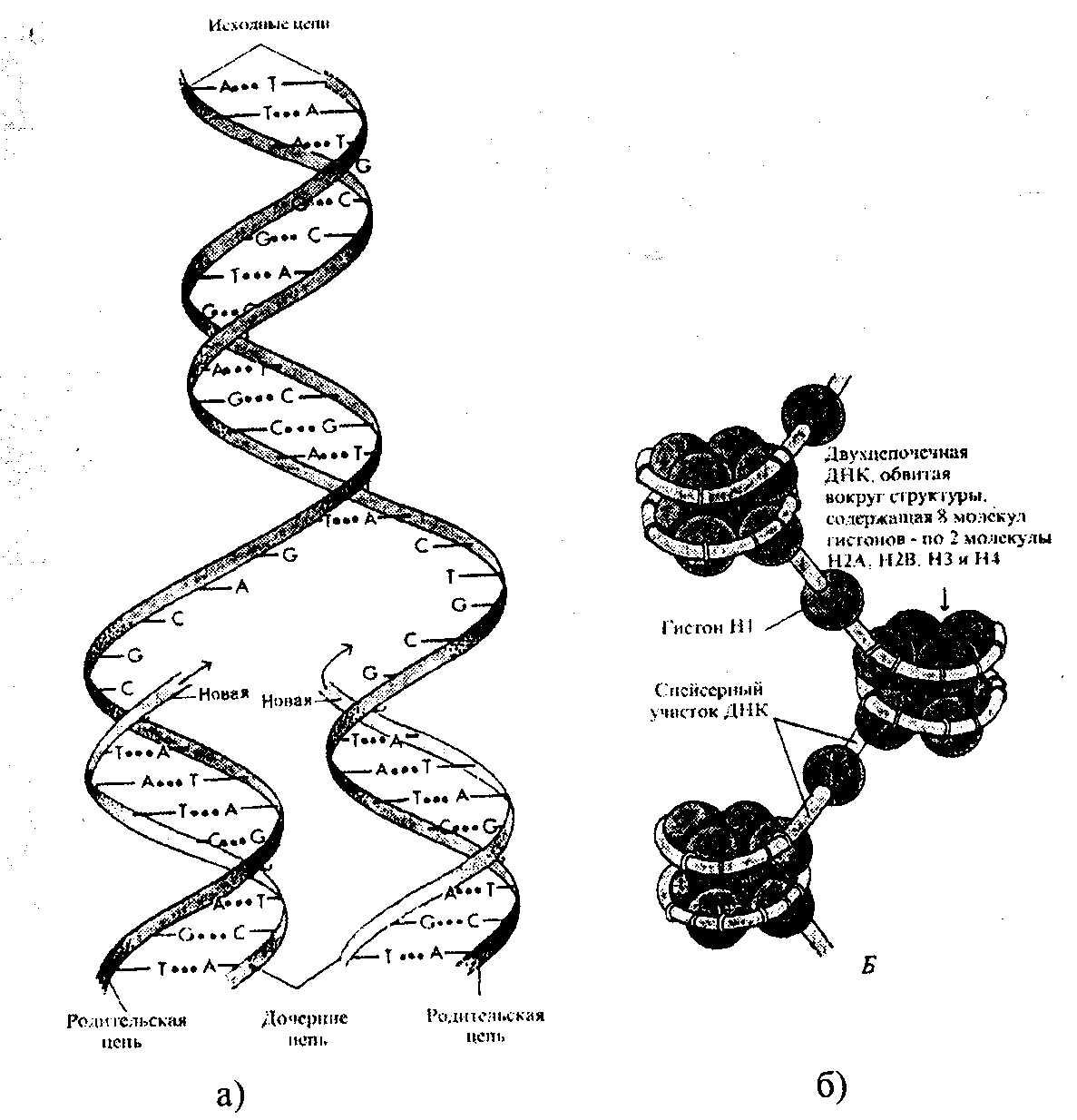 одель
репликации ДНК, предложенная Уотсоном
и Криком. Комплементарные цепи родительской
ДНК разделяются, и каждая из них служит
матрицей для биосинтеза комплементарной
дочерней цепи.
одель
репликации ДНК, предложенная Уотсоном
и Криком. Комплементарные цепи родительской
ДНК разделяются, и каждая из них служит
матрицей для биосинтеза комплементарной
дочерней цепи.
Рис.3.5. Модель молекулы ДНК (а), нуклеосом (б).
Третичная структура ДНК и организация хроматина в клетках животных. Молекула ДНК является очень длинной, поэтому в клетке плотно «упакована» путем сверхспирализации с участием белков основного характера. ДНК клетки в основном находится в составе хромосом ядер и лишь небольшая часть ее находится в митохондриях. Суммарный материал хромосом – хроматин – содержит ДНК, гистоны, негистоновые белки и небольшое количество РНК.
До 50% хроматина составляют гистоны. Гистоны богаты основными аминокислотами – аргинином и лизином, на долю которых приходится до 25% аминокислотных остатков белка. Радикалы этих аминокислот при рН 7,0 протонированы (NH3+), несут положительный заряд. Гистоны соединяются с отрицательно заряженной (за счет остатка фосфорной кислоты) двухцепочечной ДНК с образованием ДНК-гистонового комплекса. Различают пять видов гистонов: Hl - богатый лизином, Н2А, Н2В - богатые лизином и аргинином, НЗ и Н4 – богатые аргинином. Все гистоны подвергаются модификациям – метилированию, ацетилированию, фосфорилированию и поли-АДФ-рибозилированию. При этом в их молекулах изменяется распределение электронной плотности, что меняет характер их связи с ДНК. Считают, что таким образом осуществляется механизм регуляции активности генов. Упаковка молекулы ДНК начинается с образования нуклеосом. Нуклеосома – это комплекс двухцепочечной молекулы ДНК с гистонами, где около 200 пар нуклеотидов делает два оборота вокруг 8 молекул гистонов (Н2А, Н2В, НЗ и Н4 по две молекулы). Между нуклеосомами расположена соединительная (линкерная) ДНК из 20-120 пар нуклеотидов, связанная с гистоном Hl (рис.3.5.(б)). Нуклеосомы обеспечивают плотную упаковку молекулы ДНК. Они упорядоченно расположены в пространстве и образуют толстые фибриллы в виде соленоидов. Такая упаковка ДНК в хроматине обеспечивает уменьшение линейных размеров ДНК в 10000 раз.
Цитоплазматическая ДНК содержится в митохондриях – 0,1% от общего количества ДНК клетки. Это двухцепочечные кольцевые молекулы, сравнительно небольшого размера (мм ≈106). В цитоплазме бактериальных клеток кроме хромосомной ДНК имеются добавочные кольцевидные молекулы ДНК, их называют плазмидами. Плазмиды способны автономно размножаться, стабильно наследуются. Мелкие плазмиды содержат генетическую информацию для 2-3 белков, а крупные могут кодировать до 200 белков. Количество их в клетке может быть различное: мелких – несколько десятков, крупных – 1-2. Плазмиды могут обуславливать вирулентность бактерии, устойчивость к отдельным антибиотикам: тетрациклину, стрептомицину и т.д. Плазмиды широко используются в генетической инженерии.
Молекула ДНК является материальным носителем генетической информации. Геном – это совокупность генов данного организма. Ген (цистрон) – участок ДНК, несущий информацию для синтеза одного белка (полипептида). Различают структурные гены, они кодируют полипептиды и РНК; регуляторные гены выполняют регуляторные функции. Количество генов в одной хромосоме зависит от сложности организма: у мелких вирусов несколько десятков, вируса оспы – около 200, бактериальных клеток несколько тысяч, генома человека около 35000.
