
- •1.1. Массовый, объемный и мольный состав реакционной смеси
- •1.2. Характеристики газовых смесей
- •1.3. Основные критерии стадий химического превращения
- •1.4. Элементы расчетов химических реакторов
- •1.5. Тепловые расчеты химико-технологических процессов
- •1.6. Соотношение единиц измерения
- •1.7. Справочные сведения
- •1.8. Примеры и задачи к главе 1
- •Пример 1.1
- •Решение
- •Пример 1.2
- •Решение
- •Пример 1.3
- •Решение
- •Задача 1.1
- •Задача 1.2
- •Задача 1.3
- •Задача 1.4
- •2.1. Получение полиэтилена
- •2.2. Полиэтилен высокого давления
- •2.2. Полиэтилен низкого давления
- •2.3. Полиэтилен среднего давления
- •2.4. Получение полипропилена в промышленности
- •Особенности полимеризации пропилена
- •Промышленное производство полипропилена
- •2.5. Производство полиизобутилена
- •Особенности полимеризации изобутилена
- •Производство полиизобутилена
- •2.6. Примеры и задачи к главе 2
- •Пример 2.1
- •Решение
- •Пример 2.2
- •Решение
- •Пример 2.3
- •Решение
- •Пример 2.4
- •Решение
- •Пример 2.5
- •Решение
- •Пример 2.6
- •Решение
- •Пример 2.7
- •Решение
- •Пример 2.8
- •Решение
- •Пример 2.9
- •Решение
- •Пример 2.10
- •Решение
- •Пример 2.11
- •Решение
- •Пример 2.12
- •Решение
- •Пример 2.13
- •Решение
- •Пример 2.14
- •Решение
- •Пример 2.15
- •Решение
- •Пример 2.16
- •Решение
- •Пример 2.17
- •Решение
- •Задача 2.1
- •Задача 2.2
- •Задача 2.3
- •Задача 2.4
- •Задача 2.5
- •Глава 3. Получение синтетических каучуков
- •3.1. Каучуки общего назначения
- •3.2. Каучуки специального назначения
- •3.3. Примеры и задачи к главе 3
- •Пример 3.1
- •Решение
- •Пример 3.2
- •Решение
- •Пример 3.3
- •Решение
- •Пример 3.4
- •Решение
- •Задача 3.1
- •Задача 3.2
- •Задача 3.3
- •Глава 4. Получение поливинилацетата
- •4.1. Производство растворов ПВА
- •4.2. Производство полимеров и сополимеров винилацетата эмульсионным методом
- •4.3. Производство поливинилацетата суспензионным методом
- •4.4. Примеры и задачи к главе 4
- •Пример 4.1
- •Решение
- •Пример 4.2
- •Решение
- •Задача 4.1
- •Задача 4.2
- •Глава 5. Производство полимеров и сополимеров стирола
- •5.1. Производство полистирола, ударопрочного полистирола и сополимеров акрилонитрила, бутадиена и стирола в массе
- •5.2. Производство полимеров и сополимеров стирола суспензионным способом
- •5.3. Производство полимеров и сополимеров стирола эмульсионным способом
- •5.4. Примеры и задачи к главе 5
- •Пример 5.1
- •Решение
- •Пример 5.2
- •Решение
- •Пример 5.3
- •Решение
- •Пример 5.4
- •Решение
- •Пример 5.5
- •Решение
- •Пример 5.6
- •Решение
- •Задача 5.1
- •Задача 5.2
- •Задача 5.3
- •Глава 6. Полимеры и сополимеры хлористого винила
- •6.1. Полимеризация хлористого винила в массе
- •6.2. Технология получения суспензионного ПВХ
- •6.3. Технология производства латексного ПВХ
- •6.4. Примеры и задачи к главе 6
- •Пример 6.1
- •Решение
- •Пример 6.2
- •Решение
- •Пример 6.3
- •Решение
- •Пример 6.4
- •Решение
- •Пример 6.5
- •Решение
- •Задача 6.1
- •Задача 6.2
- •Задача 6.3
- •Задача 6.4
- •Задача 6.5
- •Задача 6.6
- •Задача 6.7
- •Задача 6.8
- •Глава 7. Акриловые полимеры
- •7.1. Получение полиметилметакрилата в массе мономера
- •7.2. Полимеризация в суспензии
- •7.3. Производство акриловых полимеров эмульсионным способом
- •7.4. Примеры и задачи к главе 7
- •Пример 7.1
- •Решение
- •Пример 7.2
- •Решение.
- •Задача 7.1
- •Задача 7.2
- •Глава 8. Расчеты рецептур в производстве алкидных смол
- •8.1. Химическая природа алкидов
- •8.2. Расчет рецептур алкидов по средней функциональности реакционной смеси
- •8.3. Примеры и задачи к главе 8
- •Пример 8.1
- •Решение
- •Пример 8.2
- •Решение
- •Пример 8.3
- •Решение
- •Пример 8.4
- •Решение
- •Пример 8.5
- •Решение
- •Пример 8.6
- •Решение
- •Пример 8.7
- •Решение
- •Задача 8.1
- •Задача 8.2
- •Задача 8.3
- •Задача 8.4
- •Задача 8.5.
- •Глава 9. Фенолоальдегидные смолы и другие полимеры
- •9.1. Особенности взаимодействия фенолов с альдегидами. Строение и отверждение фенолоальдегидных смол
- •9.2. Технология производства фенолоальдегидных смол
- •Периодический процесс получения твердой новолачной смолы
- •Производство резольных смол
- •9.3. Примеры и задачи к главе 9
- •Пример 9.1
- •Решение
- •Пример 9.2
- •Решение
- •Пример 9.3
- •Решение
- •Пример 9.4
- •Решение
- •Пример 9.5
- •Решение
- •Задача 9.1
- •Задача 9.2
- •Задача 9.3
- •Задача 9.4
- •Задача 9.5
- •Задача 9.6
- •Задача 9.7
- •Задача 9.8
- •Задача 9.9
- •Задача 9.10
- •Задача 9.11
- •Задача 9.12
- •Задача 9.13
- •Задача 9.14
- •Задача 9.15
- •Список литературы

Критический объем – объем занимаемый веществом при критическом состоянии (наибольший объем в жидком состоянии).
1.3. Основные критерии стадий химического превращения
Любую технологическую схему можно рассматривать как комплекс последовательных химических превращений, каждая из которых осуществляется в три стадии:
•подготовительная обработка исходного вещества;
•химическое превращение исходного вещества;
•выделение и очистка целевого продукта.
Основой для описания количественной взаимосвязи этих стадий служит материальный поток, величина и состав которого определяется главными показателями стадий химического превращения – конверсией сырья и выходом конечного продукта.
Конверсия исходного сырья – количество превращенного сырья (компонента сырья), отнесенное к загрузке реактора, выраженное в процентах или долях единицы.
Рассмотрим простейшую реакцию
A →B +C ,
где В – целевой продукт.
Пусть количество компонента А в загрузке реактора равно
в продуктах реакции GAк (кг/ч) или nAн и nAк (кмоль/ч). Тогда конверсию компонента А (в %) можно выразить следующим образом:
α = GAн −GAк |
100 = nAн −nAк 100 |
= GAпр 100 = nAпр 100 . |
||
GAн |
|
nAн |
GAн |
nAн |
Конверсия характеризует степень превращения сырья в целевые |
||||
и побочные |
продукты и, в |
конечном |
счете, количество сырья, |
|
подлежащего рециркуляции.
Выход целевого продукта в расчете на пропущенное сырье – количество целевого продукта, отнесенное к загрузке реактора, выраженное в % (масс.) или массовых долях.
Если количество целевого продукта обозначить GB (кг/ч), выход продукта В в расчете на пропущенное сырье GAн составит:
x= GB 100.
GAн
Для количественной оценки стадии химического превращения используют также показатель селективности (избирательности).
9
Селективность — доля (или процент) превращенного сырья, израсходованная на образование целевого продукта:
ψ |
B |
= |
|
nB |
100 . |
|
(0.1) |
||
|
|
|
|||||||
|
|
|
nAпр |
|
|
|
|||
Селективность процесса характеризует степень полезного |
|||||||||
использования сырья. |
|
|
|||||||
Количество |
сырья А, превращенного в продукт В, равно: |
||||||||
GA→B = nB M A . Отсюда следует, что |
|||||||||
ψ |
B |
= |
GA→B |
= nB M A = |
nB |
100 . |
|||
|
|
||||||||
|
|
|
GAпр |
GAпр |
nAпр |
||||
Селективность также определяют как отношение выхода целевого продукта к его стехиометрическому выходу или как отношение количества целевого продукта к его стехиометрическому количеству, которое могло бы образоваться при отсутствии побочных реакций.
Если бы реакция шла без образования побочных продуктов, то количество полученного продукта было бы равно:
GBстех = |
GAпр MB |
, |
(0.2) |
|
|||
|
M A |
|
|
а селективность:
ψ |
B |
= |
GB |
. |
(0.3) |
|
|||||
|
|
Gстех |
|
||
|
|
|
B |
|
|
Легко показать, что селективности, рассчитанные по уравнениям (0.1) и (0.3), будут одинаковы. Подставим выражение для GBстех из
уравнения (0.2) в уравнение (0.3):
ψ |
B |
= |
GB M A |
= |
nB |
. |
|
||||||
|
|
GAпр MB |
|
nAпр |
||
В литературе часто используют понятие «выход от теоретического», подразумевая под этим селективность, выраженную как отношение выхода целевого продукта к его стехиометрическому выходу. Такое выражение селективности («выход от теоретического») неприменимо к обратимым реакциям, так как в этом случае теоретическое или равновесное количество вещества В равно:
GAтеор = GBстех xBр ,
где xBр – равновесный выход продукта при данных условиях, доли
единицы.
С использованием основных показателей стадии химического превращения рассчитывают материальный баланс производства, расход сырья на единицу продукта и на заданную мощность аппарата, объемы
10

оборудования. Затем составляют тепловой баланс, определяют техникоэкономические показатели производства.
1.4. Элементы расчетов химических реакторов
Расчет реакторов для проведения химического взаимодействия является основной частью технологического расчета производства. Этот расчет сводится к определению основных конструкционных размеров аппаратов и их числа. Размеры и число аппаратов как периодического, так и непрерывного действия определяются их производительностью.
Производительность реакционного аппарата или установки – количество целевого продукта (кг, т, м3), получаемого в единицу времени (с, ч, сутки, год). Зафиксированная производительность аппарата (установки) называется мощностью.
Объем реакционной зоны (объем рабочей части) аппаратов непрерывного действия определяют по уравнению
VP =Vc τ,
где Vc –объемный расход (м3/с), а τ – время, необходимое для проведения процесса, с.
Площадь поперечного сечения аппарата составляет (в м2):
S = Vwc ,
где w – линейная скорость движения среды в аппарате, м/с. Определив площадь сечения, легко найти диаметр аппарата (в м):
D = 
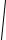 4πS .
4πS .
Высота (длина) реакционной зоны аппарата равна (в м):
H = VSP = w τ.
Для аппаратов, заполненных катализатором, объем рабочей части принимают равным объему катализатора VК (м3), который определяют исходя из объемной скорости газа (жидкости) или производительности катализатора.
Объемная скорость – объем газовой смеси (жидкости), проходящей через единицу объема катализатора в единицу времени (м3/(м3 ч) или ч-1):
VО = Vсырья ,
VК
откуда VК = Vсырья .
VО
11

Производительность катализатора – масса (объем) целевого продукта, снимаемого с единицы объема (массы) катализатора в единицу времени (кг/(м3 ч), м3/(м3 ч), кг/(кг ч), м3/( кг ч)):
NÊ = |
Nï ðî ä |
; |
NÊ = |
Nï ðî ä |
. |
|
|
||||
|
VÊ |
|
mÊ |
||
Для периодических процессов общий реакционный объем аппаратов равен (в м3):
VP = V24сут ϕτц ,
где Vсут – суточный объем перерабатываемых веществ; τц – время технологического цикла (на проведение собственного процесса и вспомогательных операций); ϕ – коэффициент заполнения аппарата (принимается от 0,4 до 0,9).
Выбор конструкции реактора зависит от следующих факторов:
•скорости протекания химических реакций (времени пребывания реакционной массы в реакционной зоне аппарата);
•оптимальных технологических параметров – температуры и давления; оптимальных условий тепло- и массообмена;
•экономических показателей.
Для расчета химического реактора чаще всего используют идеализированные модели, например:
•периодический реактор полного смешения (РПД);
•непрерывный реактор идеального вытеснения (РИВНД);
•непрерывный реактор полного смешения (РИСНД).
Химические процессы очень разнообразны и могут протекать в диффузионной, кинетической или переходной области. В общем виде скорость химико-технологического процесса можно выразить уравнением
r = k ∆C ,
где r – скорость процесса, k – константа скорости, ∆С – движущая сила процесса (изменение концентрации).
Достижение максимального выхода продукта определяется временем пребывания реагирующих веществ в реакционной зоне.
Необходимая вместимость реакционного аппарата, его производительность и интенсивность работы зависят от скорости протекания процесса.
Время пребывания реагирующих веществ в реакционной зоне (τ) определяют из кинетических уравнений первого, второго и третьего порядков. В реакциях первого порядка стехиометрический коэффициент прямой реакции равен единице, в реакциях второго порядка – двум,
12
