
- •По технике безопасности для студентов при работе в лабораториях
- •I. Теоретическая часть.
- •II. Конспекты лекций
- •Общие биохимические процессы в живых организмах
- •Раздел I. Строение и свойства белков
- •Занятие № 1
- •II.1. Работа: высаливание белков
- •Занятие № 2
- •II.1. Работа: диализ белка
- •Занятие № 3
- •Сводные вопросы к контрольной работе по разделу "строение и свойства белков"
- •Раздел II. Ферменты Занятие № 4
- •II.1.Работа № 1.Влияние температуры на
- •Занятие № 5
- •II.1. Работа № 1. Активность - амилазы слюны.
- •Занятие № 6
- •Занятие № 7 коллоквиум по разделу "ферменты" Вопросы к коллоквиуму
- •Раздел III. Витамины Занятие № 8
- •Сводные вопросы к контрольной работе по разделу "витамины"
- •II.1. Работа № 1. Качественная реакция
- •Раздел IV. Энергетический обмен Занятие № 9
- •Занятие № 10.
- •Занятие № 11.
- •II.1.Работа № 1. Качественная реакция на каталазу
- •Занятие № 12 коллоквиум по разделу: "энергетический обмен. Митохондриальная цепь переноса электронов. Общий путь катаболизма"
- •Раздел V. Биосинтез нуклеиновых кислот и белков. Молекулярные механизмы изменчивости. Занятие № 13
- •Занятие № 14
- •Сводные вопросы к контрольной работе по разделу «строение и функции нуклеиновых кислот»
- •II.1. Работа № 1. Выделение дезоксирибо-
- •Занятие № 15
- •Темы докладов к семинару
- •Занятие № 16 коллоквиум: "матричные биосинтезы.
- •Вопросы к коллоквиуму
- •Раздел VI. Б и о х и м и я к р о в и Занятие № 17
- •II.1.Работа № 1. Определение общего белка
- •Траншея с антителами
- •Занятие № 18.
Занятие № 12 коллоквиум по разделу: "энергетический обмен. Митохондриальная цепь переноса электронов. Общий путь катаболизма"
Вопросы к коллоквиуму
1. Источники и пути использования энергии для различных организмов. Соотношение между понятиями энергетический обмен, биологическое окисление, тканевое дыхание.
2. Обмен веществ и энергии как основа жизни. Общие понятия о метаболических путях и энергетическом обмене.
3. Эндергонические и экзергонические реакции в живой клетке.
4. Макроэргические соединения - универсальные аккумуляторы энергии при метаболизме. Цикл АДФ↔АТФ. Основные пути фосфорилирования АДФ и использования АТФ.
5. Современное представление о биологическом окислении. Значение работ А.Н.Баха и В.И.Палладина.
6. Строение митохондрий и структурная организация цепи переноса электронов и протонов.
7. Дегидрирование субстратов и окисление водорода как источник энергии для синтеза АТФ. Характеристика дегидрогеназ.
8. Место в цепи дыхательных ферментов и значение пиридинзависимых дегидрогеназ, структура коферментов (окисленных и восстановленных форм). Важнейшие субстраты НАД-зависимых дегидрогеназ.
9. Место в цепи дыхательных ферментов и значение флавинзависимых дегидрогеназ, структура коферментов (окисленных и восстановленных форм). Важнейшие субстраты ФАД-зависимых дегидрогеназ.
10. Место в цепи дыхательных ферментов и значение убихинона (KoQ), химическая природа и роль в окислительных процессах.
11. Цитохромы, цитохромоксидаза, химическая природа и роль в окислительных процессах.
12. Свободное окисление, окислительное и субстратное фосфорилирование.
13. Этапы продукции макроэргов в цепи дыхательных ферментов. Коэффициент Р/О.
14. Регуляция переноса электронов (дыхательный контроль). Роль некоторых биологически активных и лекарственных веществ.
15. Разобщение дыхания и фосфорилирования, терморегуляторная функция тканевого дыхания.
16. Строение митохондрий. Избирательная проницаемость митохондриальной мембраны для субстратов, АДФ и АТФ.
17. Нарушения энергетического обмена и гипоксические состояния.
18. Витамины РР и В2, убихинон. Роль в биологическом окислении.
19. Особенности микросомального и пероксисомального окисления. Роль токоферола и аскорбиновой кислоты в защите от токсического действия кислорода.
20. Цикл трикарбоновых кислот (последовательность реакций). Биологическое значение ЦТК.
21. Аллостерический механизм регуляции цикла лимонной кислоты (ЦТК).
22. Связь между общими путями катаболизма и цепью переноса электронов и протонов (на примере ЦТК).
Раздел V. Биосинтез нуклеиновых кислот и белков. Молекулярные механизмы изменчивости. Занятие № 13
ТЕМА. СТРОЕНИЕ НУКЛЕИНОВЫХ КИСЛОТ.
Цель занятия: 1.Повторить строение мононуклеотидов.
2.Усвоить структурные особенности ДНК и РНК, виды
химических связей в данных молекулах.
Исходный уровень знаний:
- нуклеиновые основания: виды, строение;
- структура мононуклеотидов;
- биологическая роль нуклеиновых кислот.
Содержание занятия.
I.2. Строение ДНК и механизм самовоспроизведения генов.
Виды РНК, их количественное соотношение и локализация.
Рибосомы и р-РНК.
Транспортные РНК: уникальность структуры, специфичность действия.
II.1.Работа № 1. ГИДРОЛИЗ НУКЛЕОПРОТЕИДОВ ДРОЖЖЕЙ
Для изучения химического состава нуклеопротеидов проводят кислотный гидролиз дрожжей, т.к. они богаты нуклеопротеидами. Специфическими реакциями для каждого вещества открывают продукты гидролиза - полипептиды, пуриновые основания, углевод и фосфорную кислоту.
а) Биуретовая реакция на полипептиды.
Химизм и порядок выполнения см. работу № 1 (стр.9-11)
РЕЗУЛЬТАТ:
б) Серебряная проба на пуриновые основания.
Химизм реакции:
NH2

 ⌡N
⌡N

 N
N
 +
AgNO3+NH4OH
+
AgNO3+NH4OH
N NH
NH2

 ⌡N
⌡N

 N
N
+ NH4NO3 + H2O
N N-Ag
Порядок выполнения работы.
К 10 каплям гидролизата добавить по каплям крепкий раствор аммиака (приблизительно 10 капель) до щелочной реакции, определяемой по лакмусу, опущенному в пробирку, затем добавить 10 капель 2% аммиачного раствора нитрата серебра. Не перемешивая, оставить пробирку на 3-5 минут.
РЕЗУЛЬТАТ:
в) Качественная реакция на пентозу (реакция Молиша).
Принцип метода и химизм реакции.
При взаимодействии концентрированной серной кислоты с пентозами происходит их дегидратация и образуется фурфурол, дающий с тимолом продукты конденсации красного цвета.



 3Н2О
CH3
3Н2О
CH3
H

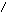
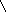 2COH-(CHOH)3-COH
+
2COH-(CHOH)3-COH
+
 Конц.
COH ―ОН
Конц.
COH ―ОН
H2SO4 O │
H3C-CH-CH3
рибоза фурфурол тимол
 продукты
конденсации красного цвета
продукты
конденсации красного цвета
Порядок выполнения работы:
К 10 каплям гидролизата дрожжей добавить 3 капли 1% спиртового р-ра тимола, перемешать и по стенке пробирки осторожно прибавить 20-30 капель концентрированной серной кислоты и встряхнуть.
РЕЗУЛЬТАТ:
г) Молибденовая проба на фосфорную кислоту.
Химизм реакции.
 H3PO4+12(NH4)MoO4+21HNO3
H3PO4+12(NH4)MoO4+21HNO3
(NH4)3P ∙ 12MoO3 + 21NH4NO3 + 12H2O
фосфомолибденовокислый
аммоний (желтый осадок)
Порядок выполнения работы.
К 10 каплям гидролизата прилить 20 капель молибденового реактива и кипятить несколько минут. При этом жидкость (не осадок) окрашивается в лимонно-желтый цвет. Пробирку охладить в струе холодной воды.
РЕЗУЛЬТАТ:
ВЫВОДЫ:
III.2. Контрольные вопросы.
Что такое нуклеопротеиды?
В каких тканях содержится много нуклеопротеидов?
Укажите продукты гидролиза нуклеопротеидов.
Какие белки входят в состав нуклеопротеидов? Укажите их особенности.
Какие качественные реакции на продукты гидролиза нуклеопротеидов Вы знаете?
Материал для самоподготовки: I а)1. с. 86-88, 96-113; II; III.
