
Общая микробиология
.pdf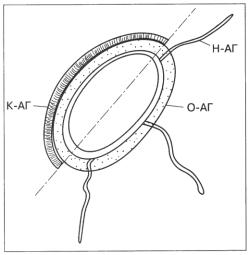
Definition). По структуре они представляют собой гликопротеиды, многие из которых относятся к суперсемейству иммуноглобулинов.
CD-антигены используют для выявления отличий в группах клеток, из которых наиболее широкое распространение получили маркеры иммунокомпетентных клеток. Например. CD3 экепрессируется на популяции Т-лимфоцитов, CD4 характерен для субпопулянии Т-хелперов, a CD8
— цитотоксических Т-лимфоцитов Т-киллеров. CD lla обнаруживается на цитоплазматических мембранах моно- и гранулоцитов, а CD 1lb — на естественных киллерах. CD19— 22 являются маркерами В-лимфоцитов.
Список CD-маркеров довольно обширный, он насчитывает около 200 вариантов. Основные CD-маркеры клеток, участвующих в иммунном ответе, представлены в табл. 10.1. Информация о структуре закодирована в различных участках генома, а экспрессия зависит от стадии дифференцировки клетки и ее функционального состояния.
CD-антигены имеют диагностическое значение в клинике иммунодефицитных состояний, а также в научно-исследовательской работе. Типирование CD-маркеров осуществляется в серологических реакциях с использованием моноклональных антител (реакция иммунофлюоресценции, цитотоксический тест и др.).
10.1.5. Антигены микробов В структуре микробов определяется несколько типов антигенов. При этом
антигенный состав микроба во многом зависит от его эволюционного и таксономического положения. Принципиальные различия имеют антигены бактерий, вирусов, грибов и простейших.
Вместе с тем микробные антигены могут быть общими для отдельных систематических категорий. Так, существуют антигены, характерные для целых семейств, родов и видов. Внутри видов могут быть выделены серологические группы (серогруппы), варианты (серовары) или типы (серотипы). Антигены микробов используют для получения вакцин и сывороток, необходимых для диагностики, профилактики и лечения инфекционных или аллергических заболеваний, а также в диагностических реакциях.
Рис. 10.2. Основные бактериальные антигены (пояснения в тексте).
10.1.5.1. Антигены бактерий
Вструктуре бактериальной клетки различают жгутиковые, соматические, капсульные и некоторые другие антигены (рис. 10.2). Жгутиковые, или Н-антигены, локализуются в локомоторном аппарате бактерий — их жгутиках. Они представляют собой эпитопы сократительного белка флагеллина. При нагревании флагеллин денатурирует, и Н-антиген теряет свою специфичность. Фенол не действует на этот антиген.
Соматический, или О-антиген, связан с клеточной стенкой бактерий. Его основу составляют ЛПС. О-антиген проявляет термостабильные свойства
—он не разрушается при длительном кипячении. Однако соматический антиген подвержен действию альдегидов (например, формалина) и спиртов, которые нарушают его структуру.
Если проиммунизировать животное живыми бактериями, имеющими жгутики, то будут вырабатываться антитела, направленные одновременно против О- и Н-антигенов. Введение животному прокипяченной культуры стимулирует биосинтез антител к соматическому антигену. Культура бактерий, обработанная фенолом, вызовет образование антител к жгутиковым антигенам.
Капсульные, или К-антигены, располагаются наповерхности клеточной стенки. Встречаются у бактерий, образующих капсулу. Как правило, К-антигены состоят из кислых полисахаридов (уроновые кислоты). В то же время у бациллы сибирской язвы этот антиген построен из полипептидных цепей. По чувствительности к нагреванию различают три типа К-антигена: А, В, и L. Наибольшая термостабильность характерна для типа А, он не денатурирует даже при длительном кипячении. Тип В выдерживает непродолжительное нагревание (около 1 часа) до 60 °С. Тип L быстро разрушается при этой температуре. Поэтому частичное удаление К-антигена возможно путем длительного кипячения бактериальной культуры.
На поверхности возбудителя брюшного тифа и других энтеробактерий, которые обладают высокой вирулентностью, можно обнаружить особый вариант капсульного антигена. Он получил название антигена вирулентности, или Vi-антигена. Обнаружение этого антигена или специфичных к нему антител имеет большое диагностическое значение.
Антигенными свойствами обладают также бактериальные белковые токсины, ферменты и некоторые другие белки, которые секретируются бактериями в окружающую среду (например, туберкулин). При взаимодействии со специфическими антителами токсины, ферменты и другие биологически активные молекулы бактериального происхождения теряют свою активность. Столбнячный, дифтерийный и ботулинический токсины относятся к числу сильных полноценных антигенов, поэтому их используют для получения анатоксинов для вакцинации людей.
Вантигенном составе некоторых бактерий выделяется группа антигенов с сильно выраженной иммуногенностью, чья биологическая активность играет ключевую роль в формировании патогенности возбудителя. Связывание таких антигенов специфическими антителами практически полностью инактивирует
вирулентные свойства микроорганизма и обеспечивает иммунитет к нему. Описываемые антигены получили название протективных. Впервые протективный антиген был обнаружен в гнойном отделяемом карбункула, вызванного бациллой сибирской язвы. Это вещество является субъединицей белкового токсина, которая ответственна за активацию других, собственно вирулентных субъединиц — так называемого отечного и летального факторов.
10.1.5.2. Антигены вирусов В структуре вирусной частицы различают несколько групп антигенов: ядерные
(или коровые), капсидные (или оболочечные) и суперкапсидные. На поверхности некоторых вирусных частиц встречаются особые V-антигены— гемагглютинин и фермент нейраминидаза. Антигены вирусов различаются по происхождению. Часть из них — вирусоспецифические. Информация об их строении картирована в нуклеиновой кислоте вируса. Другие антигены вирусов являются компонентами клетки хозяина (углеводы, липиды), они захватываются во внешнюю оболочку вируса при его рождении путем почкования.
Антигенный состав вириона зависит от строения самой вирусной частицы. Антигенная специфичность простоорганизованных вирусов связана с рибо- и дезоксирибонуклеопротеинами. Эти вещества хорошо растворяются в воде и поэтому обозначаются как S-антигены (от лат. solutio — раствор). У сложноорганизованных вирусов часть антигена связана с нуклеокапсидом, а другая — локализуется во внешней оболочке — суперкапсиде.
Антигены многих вирусов отличаются высокой степенью изменчивости. Это связано с постоянным мутационным процессом, который претерпевает генетический аппарат вирусной частицы. Примером могут служить вирус гриппа, вирусы иммунодефицитов человека.
10.1.6. Процессы, происходящие с антигеном в макроорганизме Процесс проникновения антигена и его контакт с иммунной системой протекают
поэтапно и имеют свою динамику во времени. При этом на каждом этапе появления и распространения в макроорганизме антиген сталкивается с мощным противодействием развитой сети разнообразных факторов иммунитета (см. табл.
9.3.).
Существуют разнообразные пути проникновения и распространения антигена в макроорганизме. Они могут появляться внутри самого макроорганизма (эндогенное происхождение) или поступать извне (экзогенное происхождение). Экзогенное происхождение предполагает, что антиген может проникнуть в макроорганизм:
через дефекты кожных покровов и слизистых (как результат ранений, микротравм, укусов насекомых, расчесов и др.);
путем всасывания в желудочно-кишечном тракте (эндоцитоз эпителиальными клетками);
межклеточно (при незавершенном фагоцитозе, облигатном или факультативном внутриклеточном паразитировании микроб может разноситься по всему организму);
чресклеточно (так распространяются облигатные внутриклеточные паразиты, например, вирусы).
Ворганизме антиген разносится лимфой (лимфогенный путь) и кровью (гематогенный путь) по различным органам и тканям. При этом он распределяется не хаотично — антиген чаще всего фильтруется в лимфатических узлах, а также в лимфоидной ткани печени, селезенки, легких и других органов, где вступает в контакт с разнообразными факторами иммунной защиты.
Ответная реакция этих факторов заключается в инактивации и удалении (элиминации) антигена из макроорганизма. Первыми вступают в действие факторы врожденного иммунитета, так как эта система, несмотря на ее многообразие и сложность отдельных ее компонентов, не требует длительного времени для активации. Если антиген не был инактивирован или элиминирован в течение 4 ч, в активную работу включается система факторов приобретенного иммунитета. Эффективность их действия обеспечивается путем специфического распознавания «свой-чужой» и выработки соответствующих факторов регуляции и иммунной защиты (специфические антитела, клоны антигенореактивных лимфоцитов).
Совокупный эффект всех звеньев и уровней иммунной защиты макроорганизма, независимо от степени их вовлечения в процесс, направлен на:
связывание и блокирование биологически активных участков молекулы антигена;
разрушение или отторжение антигена; 3) полную утилизацию, изоляцию (инкапсуляции) или выведение остатков
антигена из макроорганизма.
Витоге достигается полное или частичное восстановление гомеостаза. Параллельно формируется иммунная память, толерантность или аллергия.
10.2. Иммунная система человека
Для осуществления специфической функции надзора за генетическим постоянством внутренней среды, сохранения биологической и видовой индивидуальности в организме человека существует иммунная система. Эта система достаточно древняя, ее зачатки обнаружены еще у круглоротых.
Принцип действия иммунной системы основан на распознавании «свой-чужой», а также постоянной рециркуляции, воспроизводстве и взаимодействии ее клеточных элементов.
10.2.1. Структурно-функциональные элементы иммунной системы Иммунная система — это специализированная, анатомически
обособленная лимфоидная ткань. Она разбросана по всему организму в виде различных лимфоидных образований и отдельных клеток. Суммарная масса этой ткани составляет 1—2 % от массы тела. В анатомическом плане иммунная система подразделена на центральные и периферические органы.
К центральным органам иммунитета относятся костный мозг и тимус (вилочковая железа), к периферическим — лимфатические узлы, скопления лимфоидной ткани (групповые фолликулы, миндалины), а также селезенку, печень, кровь и лимфу.
С функциональной точки зрения можно выделить следующие органы
иммунной системы:
воспроизводства и селекции клеток иммунной системы (костный мозг, тимус);
контроля внешней среды или экзогенной интервенции (лимфоидные системы кожи и слизистых);
контроля генетического постоянства внутренней среды (селезенка, лимфатические узлы, печень, кровь, лимфа).
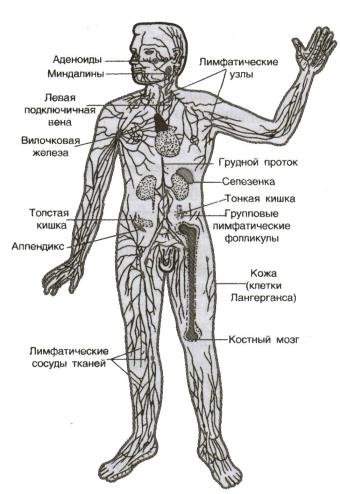
Основными функциональными клетками являются лимфоциты. Их число в организме достигает 1012. Кроме лимфоцитов, к числу функциональных клеток в составе лимфоидной ткани относят мононуклеарные и гранулярные лейкоциты, тучные и дендритные клетки. Часть клеток сосредоточена в отдельных органах иммунной системы, другие — свободно перемещаются по всему организму. Схематическое строение иммунной системы приведено на рис. 10.3.
Рис. 10.3. Органы иммунной системы человека.
10.2.1.1. Центральные органы иммунной системы Центральными органами иммунной системы являются костный мозг и
вилочковая железа (тимус). Это органы воспроизведения и селекции клеток иммунной системы. Здесь происходит лимфопоэз — рождение, размножение (пролиферация) и дифференцировка лимфоцитов до стадии предшественников или зрелых неиммунных (наивных) клеток, а также их
«обучение». Внутри тела человека эти органы имеют как бы центральное расположение.
У птиц к центральным органам иммунной системы относят сумку Фабрициуса (bursa Fabricii), локализованную в области клоаки. В этом органе происходит созревание и размножение популяции лимфоцитов — продуцентов антител, вследствие чего они получили название В-лимфоциты (см. разд. 10.2.1.3.1.1). У млекопитающих этого анатомического образования нет, и его функции в полной мере выполняет костный мозг. Однако традиционное название «В-лимфоциты» сохранилось.
Костный мозг локализуется в губчатом веществе костей (эпифизы трубчатых костей, грудина, ребра и др.). В костном мозге находятся полипотентные стволовые клетки, которые являются родоначальницами всех форменных элементов крови и, соответственно, иммунокомпетентных клеток. В строме костного мозга происходит дифференцировка и размножение популяции В-лимфоцитов, которые затем разносятся по всему организму кровотоком. Здесь же образуются предшественники лимфоцитов, которые впоследствии мигрируют в тимус, — это популяция Т-лимфоцитов. Фагоциты и некоторые дендритные клетки также образуются в костном мозге. В нем можно обнаружить и плазматические клетки. Они образуются на периферии в результате терминальной дифференцировки В-лимфоцитов, а затем мигрируют назад, в костный мозг.
Вилочковая железа, или тимус, или зобная железа, располагается в верхней части загрудинного пространства. Этот орган отличает особая динамика морфогенеза. Тимус появляется в период внутриутробного развития. К моменту рождения человека его масса составляет 10— 15 г. окончательно он созревает к пятилетнему возрасту, а максимального размера достигает к 10-12 годам жизни (масса 30-40 г). После периода полового созревания начинается инволюция органа — происходит замещение лимфоидной ткани жировой и соединительной.
Тимус имеет дольчатое строение. В его структуре различают мозговой и корковый слои. В строме коркового слоя находится большое количество эпителиальных клеток коры, названных «клетки-няньки», которые своими отростками образуют мелкоячеистую сеть, где располагаются «созревающие» лимфоциты. В пограничном, корково-мозговом слое располагаются дендритные клетки тимуса, а в мозговом — эпителиальные клетки мозгового слоя.
Предшественники Т-лимфоцитов, которые образовались из стволовой клетки в костном мозге, поступают в корковый слой тимуса. Здесь под влиянием тимических факторов они активно размножаются и дифференцируются (превращаются) в зрелые Т-лимфоциты, а также «учатся» распознавать чужеродные антигенные детерминанты.
Процесс "обучения" состоит из двух этапов, разделенных по месту и времени, и включает «положительную» и «отрицательную» селекцию.
Критерием «обученности» является качество Т-клеточной антигенной рецепции (специфичность и аффинность) и жичнеспособность клетки.
«Положительная» селекция происходит в корковом слое при помощи эпителиальных клеток. Суть ее заключается в «поддержке» клонов Т-лимфоцитов, рецепторы которых эффективно связались с экспрессированными на эпителиальных клетках собственными молекулами МНС, независимо от структуры инкорпорированных собственных олигопептидов. Активировавшиеся в результате контакта клетки получают от эпителиоцитов коры сигнал на выживание и размножение (ростовые факторы тимуса), а нежизнеспособные или ареактивные клетки погибают.
«Отрицательную» селекцию осуществляют дендритные клетки в пограничной, корково-мозговой зоне тимуса. Ее основная цель — «выбраковка» аутореактивных клонов Т-лимфоцитов. Клетки, позитивно реагирующие на комплекс МНС-аутологичный пептид, подвергаются уничтожению путем индукции у них апоптоза.
Итоги селекционной работы в тимусе весьма драматичны: более 99 % Т-лимфоцитов не выдерживают испытаний и погибают. Лишь менее 1 % клеток превращается в зрелые неиммунные формы, способные распознать в комплексе с аутологичными МНС только чужеродные биополимеры. Ежесуточно около 106 зрелых «обученных» Т-лимфоцитов покидают тимус с крово- и лимфотоком и мигрируют в различные органы и ткани.
Созревание и «обучение» Т-лимфоцитов в тимусе имеют важное значение для формирования иммунитета. Отмечено, что эссенциальное отсутствие или недоразвитие тимуса ведет к резкому снижению эффективности иммунной защиты макроорганизма. Такое явление наблюдается при врожденном дефекте развития вилочковой железы — аплазии или гипоплазии органа (см. разд. 12.4), ее хирургическом удалении или радиационном поражении в детском или юношеском возрасте. Между тем тимэктомия у взрослых практически не приводит к серьезным дефектам в иммунитете.
10.2.1.2. Периферические органы иммунной системы К периферическим органам иммунной системы относят селезенку, аппендикс,
печень, миндалины глоточного кольца, групповые лимфоидные фолликулы, лимфатические узлы, кровь, лимфу и др. В этих органах локализуются иммунокомпетентные клетки, которые непосредственно осуществляют иммунный надзор. Здесь также проходит иммуногенез — размножение и окончательная дифференцировка их предшественников. В функциональном плане периферические органы иммунной системы могут быть подразделены на органы контроля жидких сред организма (лимфатические узлы, селезенка), контроля его кожных и слизистых покровов (лимфатические фолликулы) и контроля внутренней среды (тканевые мигрирующие клетки).
Лимфатические узлы — мелкие округлые анатомические образования бобовидной формы, которые располагаются по ходу лимфатических сосудов. Каждый участок тела имеет регионарные лимфоузлы. В общей сложности в организме человека насчитывается до 1000 лимфоузлов. Лимфатические узлы выполняют функцию биологического сита — через них фильтруется лимфа, происходящая из всех покровных тканей, задерживаются и концентрируются антигены. Через лимфоузел проходит в
среднем около 109 лимфоцитов в час.
Встроении лимфоузла различают корковое и мозговое вещество. Соединительно-тканными трабекулами кора разделена на сектора. В ней выделяют поверхностный корковый слой и паракортикальную зону. В секторах поверхностного коркового слоя расположены лимфатические фолликулы с центрами размножения В-лимфоцитов (герминативные центры). Здесь же обнаруживаются фолликулярные дендритные клетки, способствующие созреванию В-лимфоцитов. Паракортикальный слой — это зона Т-лимфоцитов и интердигитальных дендритных клеток, потомков клеток Лангерганса. Мозговое вещество образовано тяжами соединительной ткани, между которыми располагаются макрофаги и плазматические клетки.
Впределах лимфоузла происходит антигенная стимуляция иммунокомпетентных клеток и включается система специфического иммунного реагирования, направленная на обезвреживание антигена.
Селезенка — это орган, через который фильтруется вся кровь. Располагается в левой подвздошной области и имеет дольчатое строение. Лимфоидная ткань образует белую пульпу. В ее строении различают первичные лимфоидные фолликулы, которые окружают артерии по их ходу, и вторичные, располагающиеся на границах первичных фолликулов. Периартериальные лимфоидные скопления преимущественно заселены Т-лимфоцитами, а вторичные — В-лимфоцитами и плазматическими клетками. Кроме того, в строме селезенки обнаруживают фагоциты и ретикулярные дендритные клетки.
Вселезенке, как в сите, задерживаются антигены, оказавшиеся в кровотоке, сорбированные не эритроцитах и «состарившиеся» эритроциты. Поэтому этот орган еще называют «кладбищем эритроцитов». Здесь происходит антигенная стимуляция иммунокомпетентных клеток, развитие специфической иммунной реакции на антиген и его обезвреживание.
Печень играет особую роль в иммунной системе. В ней находится более половины всех тканевых макрофагов и большая часть естественных киллеров. Лимфоидные популяции печени обеспечивают толерантность к пищевым антигенам, а макрофаги утилизируют иммунные комплексы, в том числе сорбированные на «стареющих» эритроцитах.
Групповые лимфатические фолликулы (пейеровы бляшки) являются скоплением лимфоидной ткани в слизистой оболочке тонкой кишки. Такие образования также находятся в червеобразном отростке слепой кишки — аппендиксе. Кроме того, на всем протяжении желудочно-кишечного тракта, начиная с пищевода и кончая анальным отверстием, располагаются единичные лимфатические фолликулы. Они обеспечивают местный иммунитет слизистой кишки и ее просвета и регулируют видовой и количественный состав ее микрофлоры.
Скопление лимфоидных элементов в виде миндалин глоточного кольца обеспечивает местный иммунитет в носоглотке, ротовой полости и верхних дыхательных путях, защищает их слизистые от внедрения микробов и других генетически чужеродных агентов воздушно-капельным или
воздушно-пылевым путем и регулирует локальную нормофлору.
Лимфа — жидкая ткань организма, которая содержится в лимфатических сосудах и узлах. Она включает в себя все соединения, поступающие из межтканевой жидкости. Основными и практически единственными клетками лимфы являются лимфоциты. В ее составе эти клетки осуществляют кругооборот в организме.
Кровь. В ней циркулируют предшественники и зрелые Т- и В-лимфоциты, полиморфно-ядерные лейкоциты, моноциты. Лимфоциты составляют 30 % от общего числа лейкоцитов. Одномоментно в крови присутствует менее 2 % от общего числа лимфоцитов.
10.2.1.3. Клеточные популяции иммунной системы Специфическую функцию иммунной защиты непосредственно
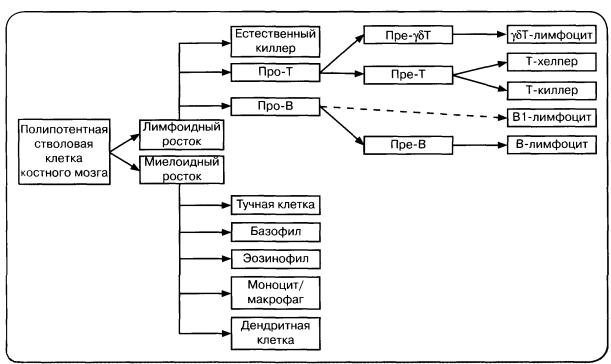
осуществляет многочисленный пул клеток миелоидного и лимфоидного ростков крови: лимфоциты, фагоциты и дендритные клетки. Это основные клетки иммунной системы. Кроме них в иммунный ответ может вовлекаться множество других клеточных популяций (эпителий, эндотелий, фибробласты и др.). Перечисленные клетки различаются не только морфологически, но и по своей функциональной направленности, по маркерам (специфические молекулярные метки), по рецепторному аппарату и продуктам биосинтеза. Тем не менее большую часть клеток иммунной системы объединяет близкое генетическое родство — они имеют общего предшественника, полипотентную стволовую клетку костного мозга
(рис. 10.4).
На поверхности цитоплазматической мембраны клеток иммунной системы существуют особые молекулы, которые служат их маркерами. С помощью специфических антител против этих молекул удалось разделить клетки на отдельные субпопуляции. В 1980-х годах была принята международная номенклатура мембранных маркеров лейкоцитов человека. Они получили название CD-антигены (аббр. от англ. Cluster of Differentiation, или Definition).
В настоящее время важнейшие субпопуляции клеток иммунной системы идентифицируют серологически при помощи моноклональных антител или в генетическом анализе.
По функциональной активности клетки-участники иммунного ответа подразделяют на регуляторные (индукторные), эффектор-ные и АПК. Регуляторные клетки управляют функционированием компонентов иммунной системы путем выработки медиаторов — иммуноцитокинов и лигандов. Эти клетки определяют направление развития иммунного реагирования, его интенсивность и продолжительность. Эффекторы являются непосредственными исполнителями иммунной защиты. Они воздействуют на объект либо непосредственно, либо путем биосинтеза биологически активных веществ со специфическим эффектом (антитела, токсические субстанции, медиаторы и пр.).
АПК выполняют несложную, но очень ответственную задачу. Они захватывают, про-цессируют (перерабатывают путем ограниченного протеолиза) и представляют антиген иммунокомпетентным клеткам
(Т-хелперам) в составе комплекса с МНС II класса. АПК лишены специфичности в отношении самого антигена. За счет спонтанной сорбции молекула МНС II класса может включать в себя любые эндоцитированные олигопептиды, как свои собственные, так и чужие. Установлено, что большая часть комплексов МНС II класса содержит аутогенные молекулы и лишь малая доля — чужеродный материал.
Рис. 10.4. Схема иммуногенеза (пояснения в тексте).
Наличие на мембране МНС II класса является обязательным, но не единственным признаком АПК. Для осуществления профессиональной деятельности необходима экспрессия ко-стимулирующих факторов (CD40, 80, 86), а также множества молекул адгезии.
Последние обеспечивают тесный, пространственно стабильный и продолжительный контакт АПК с Т-хелпером. Помимо МНС II класса АПК экспрессируют молекулы CD1. С их помощью клетки могут презентировать липосодержащие или полисахаридные антигены.
Наиболее типичными АПК, относящимися к разряду «профессиональных», являются (по активности) дендритные клетки костномозгового происхождения, В-лимфоциты и макрофаги. Дендритные клетки почти в 100 раз эффективнее макрофагов. Функцию «непрофессиональных» АПК могут также выполнять некоторые другие клетки в состоянии активации — это, в первую очередь, эпителиальные и эндотелиоциты.
Осуществление целенаправленной функции по иммунной защите макроорганизма возможно благодаря наличию на клетках иммунной системы специфических антигенных рецепторов (иммунорецепторов). По механизму рецепции они подразделяются на прямые и непрямые. Прямые
