
Органическая химия - Лекции - МГУ - Ненайденко - 2004 / Лекция 17 - Методы получения индола
.pdf
Лекция 17
Методы получения индола.
Свойства бензотиофена и бензофурана.
Химия пиридина

Синтезы Рейсерта, Маделунга, Хеметсбергера.
Понятия о рекционной способности бензотиофена и бензофурана.
Ароматичность пиридина. Пиридин как основание. Реакции пиридина с алкилгалогенидами. Окисление и восстановление пиридина. Окисление боковой цепи алкилпиридинов. Реакции электрофильного замещения в пиридине: нитрование, сульфирование, галогенирование. Пиридин N-оксид, использование в синтезе. Алкилпиридины как CH-кислоты. Нуклеофильное замещение. Реакционная способность 2-, 3-, 4- галогенпиридинов. Пиридоны, строение и реакционная способность, получение с помощью реакции диазотирования. Замещение атомов водорода в пиридинев реакциях с амидом натрия (Чичибабин). Металлорганические производные, синтез функциональных производных.
Синтез индолов по Рейссерту
H H |
|
H |
EtO CO2Et |
|
OEt |
|
O |
||
H |
H |
|||
|
||||
O |
|
O |
CO2Et |
|
|
H2/Pt |
|||
N |
|
N |
NHO2 |
|
O |
|
O |
Me |
|
Me |
CO Et |
EtO |
HNO3 |
|
|
||
H2SO4 |
|
+ |
2 |
|
|
CO2Et |
|
||
Me |
NO2 |
|
||
Me |
|
|
|
CO2Et |
H2/Pt |
|
|
|
|
|
CO2Et |
|
|
NOO2 |
AcOH |
|
|
Me |
|
Me |
N |
|
|
|
|
|
H |
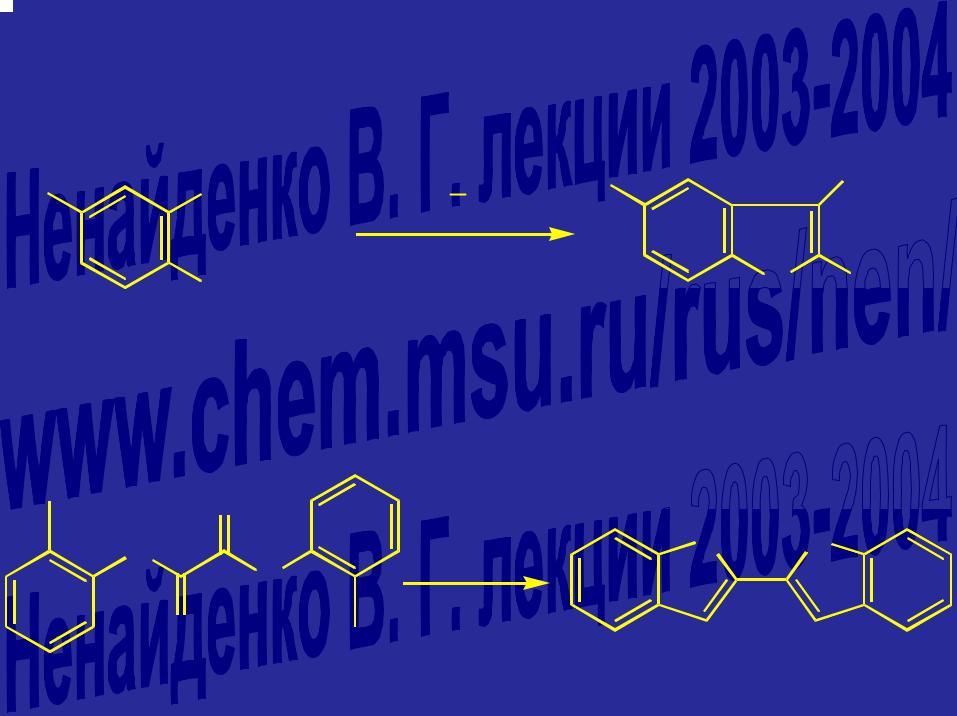
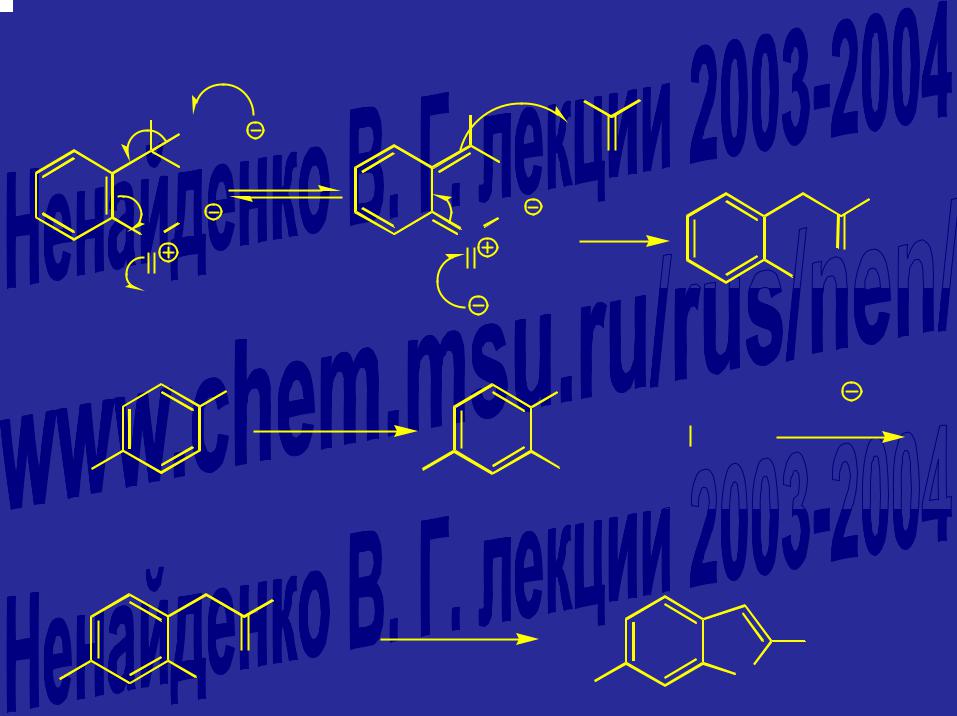
Синтез индолов по Маделунгу
R1 |
CH2R2 |
R1 |
|
R2 |
B |
|
|
||
|
NHCOR3 |
200-400OC |
N |
R3 |
|
|
|||
|
|
|
H |
|
R2,R3=H,Alk,Ar
H |
O |
|
H |
H |
|
|
|
N |
N |
||
N |
N |
t-BuOK |
|||
|
|
||||
|
|
|
|
||
O |
H |
300 oC |
|
45% |
|
|
|
|
|

Современная модификация синтеза Маделунга
CH3 |
CH2Li |
|
BuLi |
|
NHCOR |
или (i-Pr)2NLi |
|
N |
C |
R |
|
|
|
|
|
||||
|
|
|
|
Li |
O |
|
|
|
H |
H |
|
~H |
|
|
|
|
H |
|
H |
|
|
|
|
|
|
|
|
|
|
||
N |
R |
N |
|
|
|
N |
R |
|
|
|
|
||||
OLi |
R |
|
|
H |
|
||
Li |
|
|
|
|
|||
|
|
|
|
|
|
|

Синтез индолов по Хеметсбергеру
O
N3 |
CO2Me R |
N3 |
O 145 oC |
MeONa 
 O
O
R
H
R

 N O R
N O R

 N O
N O
O 
 O
O

Реакционная способность бензотиофена
NO2
BuLi |
|
HNO3 |
|
Li |
S |
Ac2O |
S |
S |
|||
|
|
RCOCl |
|
E |
HaI2 |
AlCl |
COR |
|
|
3 |
|
|
HaI |
|
|
E |
|
|
S |
S |
|
|
|
S |
|
|

Реакционная способность бензофурана
|
H |
|
HaI |
HaI2 |
HaI |
|
HaI + |
|
H |
O |
|
O |
O HaI |
O |
|
Me2NCHO |
CHO |
|
|
POCl3 |
||
O |
O |
||
|
|
BuLi |
E |
|
Li |
E |
O |
O |
O |

Пиридины – слабые основания
∆pK |
a |
монозамещённых пиридинов (в H O)a |
|
||||
|
|
|
|
|
2 |
|
|
|
|
Me |
Ph |
NH2 |
OMe |
Cl |
NO2 |
2-замещённые |
|
0.8 |
0.1 |
1.7 |
-1.9 |
-4.5 |
-7.8 |
3-замещённые |
|
0.5 |
-0.4 |
0.9 |
-0.3 |
-2.4 |
-4.4 |
4-замещённые |
|
0.8 |
0.3 |
4.0 |
1.4 |
-1.4 |
-3.6 |
|
N |
N |
N |
|
|
H |
обычный имин |
|
|
пиперидин |
пиридин |
|||
pK |
a |
11.2 |
pK ~9 |
pKa 5.5 |
|
|
a |
|
|

Электрофилы атакуют атом азота в пиридине
|
RX |
|
N |
N |
X |
|
R |
|
|
|
X = I, SO3C6H4CH3
N |
N |
N |
BF4 |
N |
CF3SO3 |
|
SO3 |
BH3 |
NO2 |
F |
|||
|
|
