
- •3 Описание технологического процесса и схемы производства цеха
- •3.1 Стадия оксимирования
- •3.1.1 Описание технологического процесса оксимирования
- •3 4 5 7
- •3.1.2 Описание технологической схемы оксимирования
- •3.2 Стадия перегруппировки и нейтрализации
- •3.2.1 Описание технологического процесса перегруппировки и нейтрализации
- •3.2.2 Описание технологической схемы перегруппировки
- •3.2.2.1 Описание технологической схемы при работе по одноступенчатой схеме
- •3.2.2.2 Описание технологической схемы при работе по двухступенчатой схеме
- •3.2.3 Описание технологической схемы нейтрализации
- •3.3 Стадия экстрагирования
- •3.3.1 Описание технологического процесса экстрагирования
- •3.3.2 Описание технологической схемы экстрагирования
- •3.4 Стадия ионообменной очистки
- •3.4.1 Описание технологического процесса ионообменной очистки
- •3.4.2 Описание технологической схемы ионообменной очистки
- •3.4.2.1 Описание процесса регенерации ионообменных смол
- •3.5 Стадия выпаривания воды из водного раствора лактама
- •3.5.1 Описание технологического процесса выпаривания воды из водного раствора лактама
- •3.5.2 Описание технологической схемы выпаривания воды из водного раствора лактама
- •3.6 Стадия дистилляции лактама
- •3.6.1 Описание технологического процесса дистилляции лактама
- •3.6.2 Описание технологической схемы дистилляции лактама
- •3.6.2.1 Описание технологической схемы дистилляции лактама потоков а и с.
- •3.6.2.2 Описание технологической схемы дистилляции лактама поток в
- •3.7 Кристаллизация лактама
- •3.7.1 Описание технологического процесса кристаллизации лактама
- •3.7.2 Описание технологической схемы кристаллизации лактама
- •3.7.2.1 Описание технологической схемы барабанной установки кристаллизации лактама потоков а/в
- •3.7.2.2 Описание технологической схемы барабанной установки кристаллизации лактама потока с
- •3.7.2.3 Описание технологической схемы ленточной установки кристаллизации лактама
- •3.7.2.4 Описание технологической схемы работы установки упаковки кристаллического лактама в мешки (фирма " Libra ")
- •3.7.2.5 Описание технологической схемы работы установки паллетирования (фирма Мöllers )
- •3.7.2.6 Описание схемы оборудования компрессорных установков поз. К – 1, к – 4.
- •3.8 Хранение и отгрузка лактама
- •3.8.1 Описание технологической схемы приема, выдачи и хранения лактама
- •3.8.2 Описание технологической схемы отгpузки лактама
- •3.8.2.1 Заполнение железнодорожной цистерны
- •3.8.2.2 Заполнение автоцистерны
- •3.8.3 Хpанение кpисталлического лактама
- •3.8.4 Отгpузка кpисталлического лактама
- •3.8.5 Описание системы сбора и откачки проливов из железнодорожных цистерн
- •3.9 Описание системы подачи уплотняющей жидкости к насосам и их охлаждение
- •3.10 Описание системы дренажей
- •3.10.1 Стадия оксимирования
- •3.10.2 Стадия перегруппировки и нейтрализации
- •3.10.3 Стадия экстрагирования
- •3.10.4 Стадия ионообменной очистки
- •3.10.5 Стадия выпаривания воды из водного раствора лактама
- •3.10.6 Стадия дистилляции и лактама
- •3.10.7 Кристаллизация лактама
- •4 Нормы технологического режима, контроль производства и управление технологическим процессом
- •4.1 Нормы технологического режима
- •4.2 Контроль производства и управление технологическим процессом
-
Технологический регламент № 23/5 книга 1, стр.
71 из 326
3 Описание технологического процесса и схемы производства цеха
Процесс получения капролактама (лактама) состоит из следующих стадий:
1 Оксимирование (потоки А и В).
2 Перегруппировка и нейтрализация (потоки А и В).
3 Экстрагирование (потоки А и В).
4 Ионообменная очистка (потоки А, В, С)
5 Выпаривание воды из водного раствора капролактама (потоки А и В)
6 Дистилляция капролактама (потоки А, В, С).
7 Кристаллизация капролактама (барабанная установка потоки А, В, С, ленточная установка потоки А и В).
В связи с тем, что технологический процесс и схема получения лактама на потоках А и В стадий синтеза, экстрагирования, ионообмена, выпаривания, кристаллизации аналогичны друг другу, описание технологического процесса и схемы получения лактама приводится для потока А.
В связи с тем, что технологический процесс и схема производства стадии дистилляции лактама на потоках А и С аналогична друг другу описание приводится для потока А.
Описание схемы производства потока С стадии ионнообменой очистки, потока В стадии дистилляции лактама, потока С стадии кристаллизации приводится отдельно.
3.1 Стадия оксимирования
3.1.1 Описание технологического процесса оксимирования
Циклогексаноноксим (оксим) получают по открытой Мейером в 1882 г. реакции между гидроксиламинсульфатом (ГАС) и циклогексаноном (анон).
Реакция оксимирования протекает по следующему уравнению:
= О
= NОH
• 0,5 H2SO4

+ NH2OH • 0,5 H2SO4 == + H2O + 118 кДж/моль
Для сдвига равновесия реакции вправо в реакционную смесь вводят водный раствор аммиака, что приводит к образованию оксима и побочного продукта сульфата аммония:
=
NOH • 0,5 H2SO4 =
NОH

 +
+
+ NH4OH + 0,5(NH4)2SO4
+ H2O
NH4OH + 0,5(NH4)2SO4
+ H2O
Химизм процесса можно представить в следующем виде:


1 .
С = О + Н+
С+
- ОН
.
С = О + Н+
С+
- ОН
Взаимодействие анона с ГАС протекает по механизму электрофильного замещения. Электрофильный характер атома углерода карбонильной группы в молекуле анона усиливается протонированием кислородного атома карбонильной группы кислотой. При этом атом углерода приобретает положительный заряд.
2. Присоединение атома азота ГАС за счет неподеленной электронной пары к положительно заряженному атому углерода:

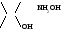 +
+
 С+
- ОН + NH2OH C
С+
- ОН + NH2OH C
3. Миграция атома водорода к кислородному атому карбонильной группы:
NHOH NH2OH
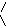

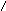
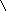
 + +
+ +
 С С
С С
OH H2O
4. Отщепление молекулы воды:
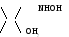
 + +
+ +
 С
С= NHOH + H2O
С
С= NHOH + H2O
5. Образование свободного оксима с выделением иона водорода (под воздействием аммиачной воды):

 +
+
 C
= NHOH С = NOH + H+
C
= NHOH С = NOH + H+
Лимитирующей стадией процесса оксимирования является стадия два, присоединение атома азота ГАС за счет неподеленной электронной пары к положительно заряженному атому углерода. Наивысшая скорость достигается при максимальном произведении концентраций:





C+ – OH * NH2OH
Имеется следующая зависимость концентрации от рН:
Концентрация

 NH2OH
NH2OH

C+ – OH
рН
