
Методы галогенирования в тонком органическом синтезе
.pdfФедеральное агентство по образованию
Московская государственная академия тонкой химической технологии им. М.В. Ломоносова
Кафедра химии и технологии биологически активных соединений им. Н.А. Преображенского
И.П. Ушакова, Н.А. Брагина, А.Ф. Миронов
МЕТОДЫ ГАЛОГЕНИРОВАНИЯ В ТОНКОМ ОРГАНИЧЕСКОМ СИНТЕЗЕ
Учебное пособие
Москва - 2005
www.mitht.ru/e-library
УДК 547.9(075.8)
Ушакова И.П., Брагина Н.А., Миронов А.Ф.
Методы галогенирования в тонком органическом синтезе Учебное пособие М., МИТХТ им. М.В.Ломоносова, 2005 – 46 с.
Утверждено Библиотечно-издательской комиссией МИТХТ им. М.В.Ломоносова в качестве учебного пособия.
Поз. 238/2005.
В учебном пособии представлен материал по методам введения атомов галогенов, применяемым в синтезе биологически активных соединений. Рассмотрены также методы дегалогенирования и замены галогенов на другие функциональные группы. Данное пособие является частью спецкурса, посвященного методам получения биологически активных соединений. Учебное пособие предназначено для бакалавров 4 курса, обучающихся по направлению 550800 “Химическая технология и биотехнология”.
Рецензент:
д.х.н., проф. Флид В.Р. (МИТХТ, кафедра физической химии)
© МИТХТ им. М.В.Ломоносова, 2005 г.
2
www.mitht.ru/e-library
Издание учебное |
|
СОДЕРЖАНИЕ |
|
|
ВВЕДЕНИЕ .................................................................................. |
4 |
|
|
1. |
ФТОРИРОВАНИЕ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ. .... |
5 |
|
2. |
ГАЛОГЕНИРОВАНИЕ С ИСПОЛЬЗОВАНИЕМ |
|
Ушакова Ирина Павловна |
|
МОЛЕКУЛЯРНЫХ ГАЛОГЕНОВ...................................... |
10 |
Брагина Наталья Александровна |
|
2.1. Хлорирование.................................................................. |
10 |
Миронов Андрей Федорович |
|
2.2. Бромирование.................................................................. |
19 |
|
|
2.3. Иодирование.................................................................... |
21 |
|
3. |
ГАЛОГЕНИРОВАНИЕ СМЕШАННЫМИ ГАЛОГЕНАМИ |
|
|
|
(ICl, IBr).................................................................................. |
24 |
МЕТОДЫ ГАЛОГЕНИРОВАНИЯ В ТОНКОМ |
4. |
ГАЛОГЕНИРОВАНИЕ С ИСПОЛЬЗОВАНИЕМ |
|
ОРГАНИЧЕСКОМ СИНТЕЗЕ |
|
ГАЛОГЕНОВОДОРОДОВ. .................................................. |
25 |
|
|
4.1. Присоединение галогеноводородов по кратной связи.25 |
|
Учебное пособие |
|
4.2. Взаимодействие галогеноводородов со спиртами....... |
27 |
|
|
4.3. Взаимодействие галогеноводородов с простыми |
|
|
|
эфирами................................................................................... |
28 |
|
5. |
ИСПОЛЬЗОВАНИЕ СЕРОСОДЕРЖАЩИХ |
|
|
|
ГАЛОГЕНИДОВ. .................................................................. |
29 |
|
|
5.1. Тионилхлорид (SOCl2).................................................... |
29 |
|
6. |
5.2. Сульфурилхлорид (SO2Cl2). ........................................... |
30 |
|
ИСПОЛЬЗОВАНИЕ ФОСФОРСОДЕРЖАЩИХ |
|
|
Подписано в печать_______ Формат 60х84/16. Бумага писчая. |
|
ГАЛОГЕНИДОВ. .................................................................. |
31 |
Отпечатано на ризографе. Уч. изд. листов 1. Тираж 150 экз. |
|
6.1. Фосфоргалогениды (PX3, PX5)....................................... |
31 |
Заказ № ____________ |
|
6.2. Галогеноксиды фосфора (POX3).................................... |
33 |
Лицензия на издательскую деятельность ИД № 03507 от |
7. |
6.3. Фосген (COCl2)................................................................ |
35 |
ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ, ИСПОЛЬЗУЕМЫЕ |
|
||
15.12.2000 |
|
КАК МЯГКИЕ ГАЛОГЕНИРУЮЩИЕ РЕАГЕНТЫ. ....... |
36 |
|
8. |
АНАЛИЗ ГАЛОГЕНСОДЕРЖАЩИХ СОЕДИНЕНИЙ. ... |
38 |
Московская государственная академия тонкой химической |
9. |
МЕТОДЫ ДЕГАЛОГЕНИРОВАНИЯ. ................................ |
38 |
технологии имени М.В. Ломоносова. |
|
9.1. Замещение галогена на гидроксильную группу. ......... |
38 |
|
|
9.2. Замещение галогена на аминогруппу. .......................... |
40 |
Издательско-полиграфический центр. |
|
9.3. Реакция Фишера.............................................................. |
40 |
|
|
9.4. Метод Габриэля............................................................... |
41 |
119571 Москва, пр. Вернадского 86. |
10. ТЕХНИКА БЕЗОПАСНОСТИ............................................ |
43 |
|
46 |
|
3 |
|
www.mitht.ru/e-library

ВВЕДЕНИЕ
Галогенированием органических соединений называют введение атома галогена (Hal) в молекулу с образованием связи С-Hal. Существует много методов галогенирования и целесообразность того или иного метода зависит как от природы галогена, так и от природы субстрата.
Химические превращения органических галогенидов исключительно многообразны (нуклеофильная замена атома галогена, реакции образования металлоорганических соединений, алкилирование и ацилирование алкил- и ацилгалогенидами и т.д.). Высокая химическая активность органических галогенидов позволяет широко использовать их в качестве промежуточных продуктов при синтезе органических и биологически активных соединений.
Основные типы реакций галогенирования:
-замещение атома водорода на галоген;
-присоединение молекулярных галогенов или галогеноводородов по кратным связям;
-замещение гидроксильной группы на галоген.
Галогенирование алканов и боковых цепей замещенных ароматических соединений протекает только по гомолитическому (радикальному) механизму. Процесс может инициироваться как термически, так и облучением светом с длиной волны 360 нм.
CH4  Hal2
Hal2 
 CH3Hal
CH3Hal  HHal
HHal  ∆H
∆H
hν
Hal2  2 Hal
2 Hal
Hal
 CH4
CH4  HHal
HHal  CH3
CH3
CH3  Hal2
Hal2  CH3Hal
CH3Hal  Hal
Hal
Расчет теплового эффекта реакции показывает, что спонтанный рост цепи возможен для фторирования и хлорирования (Табл.1). Но прямое фторирование технически трудно осуще-
4 |
45 |
www.mitht.ru/e-library
ЛИТЕРАТУРА
1.Б.В.Пассет. Основные процессы химического синтеза биологически активных веществ. - М., ГЭОТАР-МЕД, 2002.
2.Дж. Марч. Органическая химия. – М., Мир, 1987.
3.Ю.А. Овчинников. Биоорганическая химия. – М., Просвещение, 1988.
4.П. Сайкс. Механизмы реакций в органической химии. –
М., Мир, 1987.
5.П.Ласло. Логика органического синтеза.- М., Мир, 1998.
6.К.В. Вацуро, Г.А. Мищенко. Именные реакции в органической химии
44
ствить, хлорирование требует отвода тепла, бромирование – подогрева реакционной массы, а йодирование – специального инициирования реакции.
Табл.1. Тепловые эффекты реакций радикального галогенирования алканов.
Hal |
Тепловой эффект реакции, кДж/моль |
F |
460 |
Cl |
105 |
Br |
32 |
I |
-50 |
Значительное число органических галогенидов обладает биологической активностью. Так, ряд алифатических галогенидов проявляет наркотические свойства, ароматические – антимикробные. Практически во всех классах органических лекарственных соединений имеются высокоэффективные средства, в состав которых входит один или несколько атомов галогена.
Увеличение числа атомов галогена в молекуле соединения, как правило, приводит к увеличению его токсичности. Биологическую активность галогензамещенных органических соединений связывают как с их высокой растворимостью в жировых тканях, так и с высокой химической активностью (в частности, алкилирующей).
1.ФТОРИРОВАНИЕ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ.
Впромышленности F2 получают гидролизом KF.HF или KF.3HF. Хранят F2 в стальных баллонах, так как F2 пассивирует металлы, образуя на их поверхности защитную пленку.
5
www.mitht.ru/e-library

Прямое фторирование практически не применяется вследствие очень высокой экзотермичности процесса. В атмосфере фтора горит практически все. Это используют в технике для резки тугоплавких материалов. Для дезактивированных соединений прямое фторирование возможно при разведении фтора инертными газами:
R |
R |
|
F2 / N2 |
F |
HF |
|
|
Для фторирования органических соединений чаще всего используют некоторые соединения фтора:
1.1. Перфторидыкобальта и серебра.
Углеводород пропускают через нагретую до 200–250˚С трубку, заполненную СoF3. Последний при этом восстанавливается до CoF2, который можно регенерировать, пропуская газообразный фтор:
|
|
|
|
|
|
|
|
250 o |
||||||||
RH |
|
|
|
|
|
|
CoF3 |
|
RF |
|
|
HF |
|
|
|
CoF2 |
|
|
|
||||||||||||||
|
|
|
|
|
|
|||||||||||
2 CoF2 |
|
|
|
|
F2 |
|
2 CoF3 |
|||||||||
|
|
|
|
|
||||||||||||
В ходе реакции, как правило, образуются продукты исчерпывающего фторирования:
CH3 |
F |
CF3 |
|
CoF3 |
F |
F |
|
F |
F |
||
350o |
F |
||
F |
|||
|
F |
F F |
|
|
F |
6
10. ТЕХНИКА БЕЗОПАСНОСТИ
Как уже упоминалось, галогензамещенные органические соединения являются токсичными веществами. Они обладают наркотическими свойствами и в то же время местным раздражающим действием. Некоторые из них могут вызвать экзему и другие кожные заболевания. Алкиларилгалогениды, содержащие галоген в боковой цепи, часто являются веществами, сильно раздражающими дыхательные пути и глаза.
Токсичность галогенпроизводных повышается с увеличением числа атомов галогена в молекуле. В связи с этим необходимо уделять большое внимание герметизации оборудования, а выделяющиеся пары и газы должны направляться в систему улавливания.
Исходные соединения в синтезах и растворители часто являются взрыво- и пожароопасными веществами. Токсичными являются также галогенирующие агенты. Поэтому рабочее место должно быть оборудовано приточно-вытяжной вентиляцией.
Скорость подачи галогенирующего агента в реакцию должна строго контролироваться. По окончании галогенирования реакционная масса должна быть продута воздухом (в случае огневзрывоопасной среды – азотом) через систему улавливания соответствующих паров и газов. При розливе хлорированной смеси она должна быть нейтрализована содой или известью, а затем смыта водой. При розливе брома проводят постепенную дегазацию 20% водным раствором сульфитом натрия, пары брома дегазируют распылением 2-5% раствора кальцинированной соды с последующим проветриванием помещения.
43
www.mitht.ru/e-library
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
H |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
O |
H |
C OC2H5 |
|
|
|
|
|
O |
|
|||||
C2H5 CH CH2 C |
|
C |
H CH CH C |
|
||||||||||||||||||||||
OC2H5 |
|
|
|
|
OC H |
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
5 |
|
|
|
|
5 |
||||
|
|
|
C |
O |
|
|
|
|
|
|
|
|
|
C |
O |
|
|
2 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
OC2H5 |
|
|
|
|
|
|
|
|
|
OC H |
5 |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
H5C2 |
|
|
|
COOH |
|
||
H2/Ni |
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
C H |
CH |
CH C |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
t |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
2 5 |
C |
O |
OC2H5 |
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
O |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
OC2H5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H5C2 |
C |
O |
|
|
|
H5C2 |
|
C |
|
O |
|
|
||||
SOCl2 |
|
|
|
|
|
Cl |
CH2N2 |
|
|
CHN2 |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
O |
|
O |
|
|
|
|
|
O |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H C |
CH COOH |
1) SOCl2 |
|
H5C2 |
|
|
C H2C |
O |
|
|||||||
|
|
|
|
|
5 |
2 |
|
2 |
|
|
|
|
|
|
|
|
|
CH2Cl |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
Ag2O |
|
|
|
|
2) CH2N2 |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
O |
|
O |
|
|
3) HCl |
|
O |
O |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
NH |
H5C2 |
|
CH2 C CH2 N |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
O |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H5C2 |
CH2 C CH2 NH2 |
|
|
|
H5C2 |
|
|
|
CH2 |
N |
CH3 |
|||||
|
|
|
H3O |
|
|
|
|
CH3NCS |
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
O |
|
O |
|
|
|
|
|
|
|
O |
|
O |
|
N |
SH |
|
|
|
|
|
|
|
|
|
|
|
|
H5C2 |
CH2 |
|
CH3 |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
[O] |
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
O |
O |
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
42
При использовании AgF2 на поверхности серебра образуется защитная пленка фторида серебра, и серебро практически не расходуется:
2 Ag  F2
F2  2 AgF
2 AgF
2 AgF  F2
F2  2 AgF2
2 AgF2
RH  AgF2
AgF2  RF
RF  HF
HF  2AgF
2AgF
1.2. Тетрафторид серы (SF4).
Тетрафторид серы – это бесцветный токсичный газ (т.кип. - 38˚С), хорошо растворимый в бензоле, в воде разлагается с выделением диоксида серы. Реагент используют для фторирования кетонов и кислот:
R |
C O |
|
|
SF4 |
|
|
|
R |
CF2 |
|
|
|
SOF2 |
|||||||
R |
|
|
|
R |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
R |
|
COOH |
|
|
|
2 SF4 |
|
|
|
R |
|
CF3 |
|
|
|
2 SOF2 |
|
|
|
HF |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
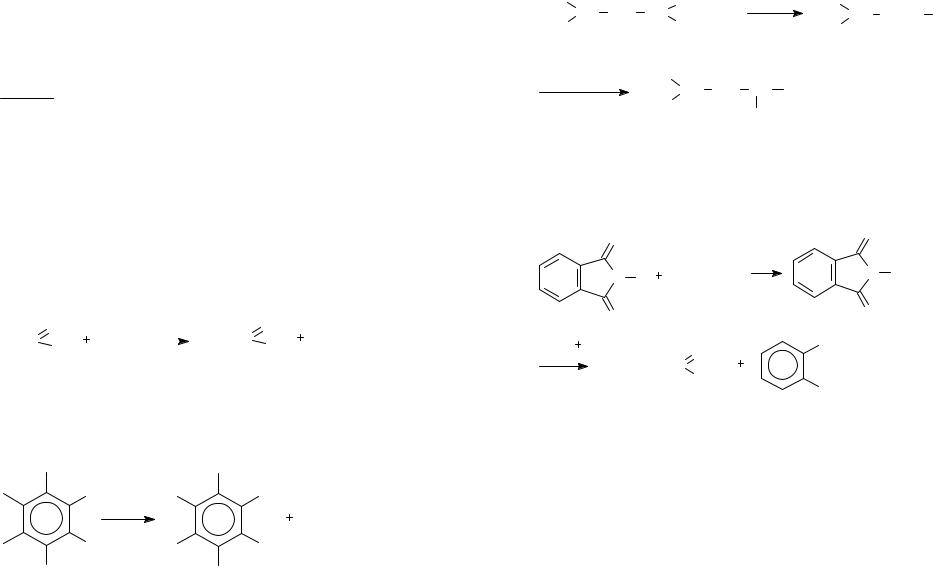
1.3. Перфторалкилгипофториты (СF3OF, CF2(OF)2) – это газообразные, очень токсичные соединения. Их получают при взаимодействии фтора с моноили диоксидом углерода. Используют для фторирования фенолов, N-ациланилинов, алкилбензолов:
R R R
F
CF3OF
F
7
www.mitht.ru/e-library
1.4. Фториды ксенона.
Фтор является настолько реакционноспособным, что взаимодействует с инертным газом ксеноном, образуя фториды состава XeF2 и XeF6. Эти фториды можно использовать для фторирования ароматических соединений:
ArH XeF2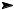 ArF
ArF  HF
HF
1.5. Фториды щелочных металлов.
Для получения приведенных выше реагентов используется F2, что значительно осложняет процессы и требует специального коррозионно-устойчивого оборудования. Поэтому более удобно работать с фторидами щелочных металлов (KF) и фтороводородом (HF).
В качестве примеров можно привести следующие реакции:
А) Замещение хлора на фтор в хлорангидридах кислот:
C |
H C |
O |
HF (KF, H+) C6H5C |
O |
HCl |
6 |
5 |
Cl |
|
F |
|
Замещение хлора на фтор в ароматических соединениях - реакция Бородина:
|
Cl |
|
F |
Cl |
Cl |
F |
F |
|
|
6 KF |
6 KCl |
Cl |
Cl |
F |
F |
|
Cl |
|
F |
8
H3C |
|
CH2 |
|
COOC2H5 OH |
|
|
H3C |
(CH ) |
|
||||
CH |
CH |
|
|
|
|
|
|
CH |
COOH |
||||
H3C |
|
|
|
COOC2H5 |
|
CO2 |
H |
2 2 |
|||||
|
|
|
|
C |
|
|
|||||||
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
1) Br2, P, I2 |
H3C |
CH2 |
CH |
COOH |
|
|
|
||||||
2) NH |
|
|
H |
CH |
|
|
|
||||||
3 |
|
C |
|
|
|
|
|
|
|
|
|
||
|
|
3 |
|
|
NH2 |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|||
9.4. Метод Габриэля.
Используется, в частности, в синтезе γ-аминомасляной кислоты (ГАМК):
O |
|
|
O |
|
|
|
|
N K |
Cl(CH ) CN |
N CH2CH2CH2CN |
|
|
2 3 |
|
|
O |
|
|
O |
H3O |
|
O |
COOH |
|
|
||
NH (CH ) C |
|
|
|
2 |
2 3 |
OH |
|
|
|
COOH |
|
|
|
|
|
Этот метод позволяет селективно заместить хлор при наличии других функциональных групп.
Реакции галогенирования и дегалогенирования широко используются в синтезе биологически активных веществ, например, в синтезе алкалоида пилокарпина.
Пилокарпин является основным препаратом для лечения глаукомы (снижает внутриглазное давление). Этот алкалоид содержится в листьях южноамериканских растений, впервые его строение было установлено в 1900 г., а первый химический синтез был выполнен А.Е.Чичибабиным и Н.А. Преображенским в 1933 г.:
41
www.mitht.ru/e-library

|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
|
|
|
|
|
|
50 o |
|
|
|
|
|
|
|
|
|
|
ONa |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NaOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
O2N |
|
|
|
|
|
|
NO2 |
|
|
|
|
|
O2N |
|
|
|
|
|
|
|
NO2 |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
9.2. Замещение галогена на аминогруппу. |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
R |
|
|
|
Hal |
|
|
|
|
|
|
NH |
|
|
|
R |
|
NH |
HHal |
|
NH3 |
R |
|
NH2 |
|
|
NH Hal |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
3 |
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
4 |
|||||||||||||||||
R |
|
|
NH2 |
|
|
|
|
|
R |
|
Hal |
|
|
|
|
|
|
R |
N |
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
RHal |
|
|
|
|
|
|
|
|
|
|
||||
R |
N H |
|
|
|
|
|
|
R |
|
|
Hal |
|
|
|
|
|
|
R |
N |
|
R4N Hal |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Из первичного галогенида под действием аммиака можно получить только четвертичную аммониевую соль, как как промежуточные соединения являются более реакционноспособными по сравнению с исходными.
Нуклеофильное замещение галогенов на аминогруппу в ароматических соединениях происходит в жестких условиях. Введение электронодонорных заместителей затрудняет, а электроноакцепторных облегчает протекание реакции:
Cl |
|
NH2 |
|
NH3 |
200 o, 100 атм |
||
CaCl2 |
(кат.) |
||
|
|||
9.3. Реакция Фишера.
Используется для получения α-аминокислот с одновременным удлинением цепи на одно углеродное звено:
40
Б) Замещение гидроксильной группы в спиртах и кислотах:
C2H5OH  HF
HF  C2H5F
C2H5F  H2O
H2O
CF3C |
O |
HF электролиз CF3C |
O |
OH |
F |
В) Присоединение по кратным связям, так называемое сопряженное фторирование, основанное на действии HF и сильной минеральной кислоты (HNO3, HCl и др.).
Например:
CF2 |
|
CH2 |
|
|
|
|
HF |
|
|
|
|
HNO3 |
|
|
|
|
|
|
|
|
|
F3C |
|
CH2 |
|
CH2 |
|
NO2 |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
HNO |
3 |
|
|
|
|
HF |
|
|
|
|
|
|
|
|
NO + |
|
|
|
H2O |
|
|
|
|
F- |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
C |
|
C |
|
|
|
|
NO2+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
C |
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NO2 |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
C |
|
C |
|
|
|
|
|
F |
|
|
|
|
|
|
|
|
|
|
C |
|
C |
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
NO2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NO2 F |
|
|
|
|
|
|
|
||||||||||||||||
9
www.mitht.ru/e-library
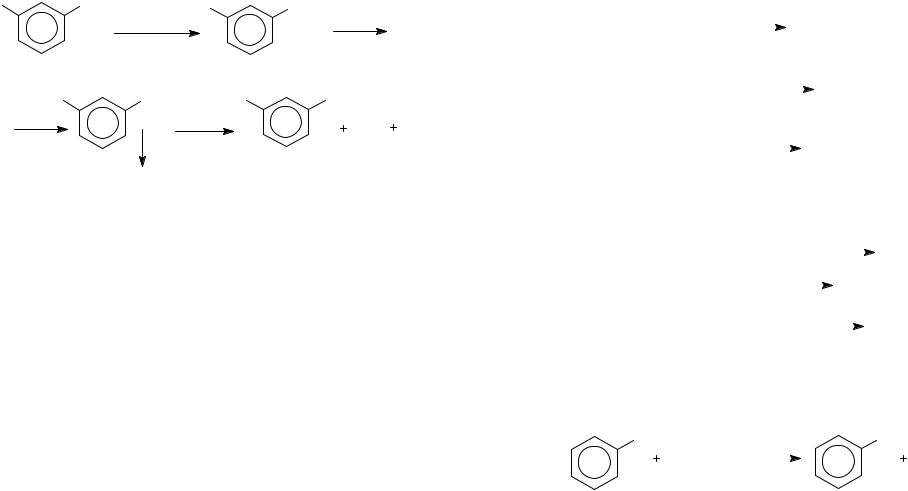
Г) Введение фтора в ароматические соединения через диазосоединения – реакция Шимана:
R |
NH2 |
R |
N2+Cl- |
|
NaNO2/HCl |
|
NaBF4 |
R |
N2+BF4- |
R |
F |
|
|
∆ |
BF3 N2 |
|
|
|
Выход продукта и температура разложения тетрафторбората арилдиазония зависят от строения исходного ароматического амина: чем ниже температура разложения, тем более гладко протекает реакция.
Следует помнить, что алифатические фториды – сильные яды. Фторорганические соединения используются в технике (тефлон, фреоны), медицине.
2. ГАЛОГЕНИРОВАНИЕ С ИСПОЛЬЗОВАНИЕМ МОЛЕКУЛЯРНЫХ ГАЛОГЕНОВ
2.1.Хлорирование.
Впромышленных масштабах хлор обычно хранят баллонах, где он находится под давлением в жидком состоянии. В небольших количествах в лаборатории газообразный хлор (Cl2) получают окислением хлороводорода:
10
Замещение галогена при третичном атоме углерода происходит под действием воды, при вторичном – под действием водного раствора соды или поташа, при первичном – под действием щелочи.
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
HCl |
|||||||||||||||
|
|
C |
|
|
Cl |
|
|
|
|
|
|
|
H2O |
|
|
|
|
|
R |
|
|
C |
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
2R |
|
|
|
|
CH |
|
|
|
Cl |
|
|
|
K2CO3 |
|
|
|
H2O |
|
|
|
|
2R |
|
|
|
CH |
|
|
|
|
OH |
|
|
|
|
|
2 KCl |
|
|
|
CO2 |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
R |
|
|
CH |
|
|
|
Cl |
|
|
|
|
|
KOH |
|
|
|
∆ |
|
|
|
R |
|
|
|
CH2 |
|
|
OH |
|
|
|
|
|
|
KCl |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
Замещение галогена происходит легче, если галоген находится в аллильном или бензильном положении, а также рядом с электроноакцепторной группой:
R |
|
CH |
|
|
|
CH |
|
|
|
|
CH Cl |
|
K |
CO |
3 |
|
|
|
|
|
H2O |
|
|
R |
|
CH |
|
|
|
CH |
|
CH2OH |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
2 C H CH |
Cl |
|
|
|
Ca(OH) |
2 |
|
|
|
|
H |
O |
|
|
|
|
|
|
|
2 C6H5CH2OH |
|
|
|
CaCl2 |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
6 |
5 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
CH3CH2 |
|
CHCOOH |
|
|
|
K2CO3 |
|
|
|
|
H2O |
|
|
|
CH3CH2 |
|
CHCOOH |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|||||
|
|
|
|
Br |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
В ароматическом ядре замена галогена на гидроксильную |
||||||||||||||||||||||||||||||||||||||||||||||||||
группу протекает в жестких условиях: |
|
|
ONa |
|
|
|
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
Cl |
|
|
|
|
|
|
|
|
|
300 o |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
2 NaOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NaCl |
|
|
|
|
H2O |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
200 атм |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Введение в ароматическое кольцо электроноакцепторных заместителей облегчает протекание реакции:
39
www.mitht.ru/e-library
