
304- Органическая химия_Черных В.П. и др_Х., 2007 -776с
.pdf
БелКИ
701
на. им установлено, что молекула состоит из двух полипептидных цепей, связанных между собой дисульфидными мостиками: а-цепь содержит 21 аминокислотный остаток и дополнительную дисульфидную связь, благодаря которой инсулин
впространстве образует петлю, а б-цепь — 30 остатков (рис. 35.6).
в1963—1964 году были синтезированы обе полипептидные цепи инсулина. инсулин различных ви-
дов животных и человека отличается по строению. Эти структурные различия приходятся на участок 8—10 цепи A. инсулин регулирует содержание глюкозы в крови, недостаток его в организме вызывает сахарный диабет.
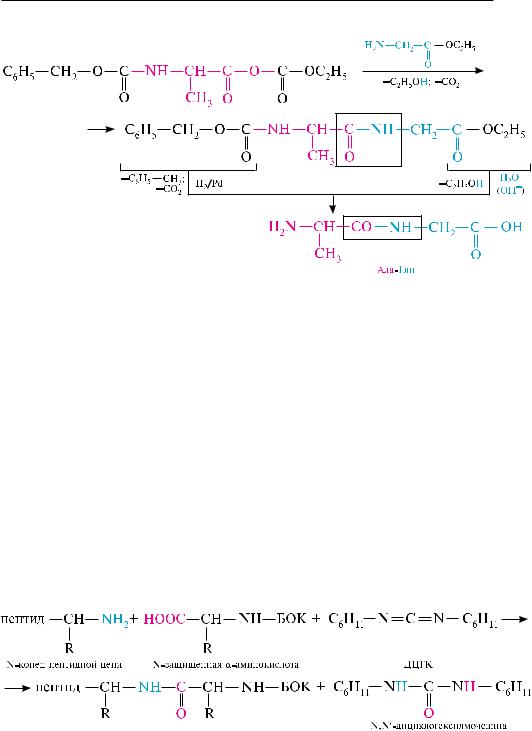
к полипептидам относятся некоторые широко применяемые антибиотики. Грамицидин с — циклический декапептид, используемый для лечения заболеваний, вызванных стрептококками, пневмококками и им подобным, содержит, кроме аминокислотных остатков L-ряда, два остатка D-фенилаланина.
35.3. синТеЗ ПеПТидОв
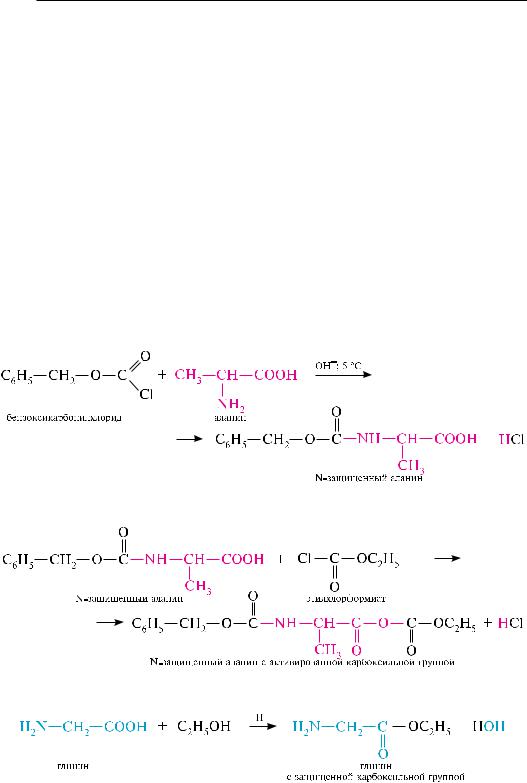
в основе синтеза пептидов лежит процесс образования пептидной (амидной) связи между карбоксильной группой одной -аминокислоты и аминогруппой — другой.
однако из-за диполярной природы -аминокислот (цвиттер-ионная структура) проведение реакции требует высокого температурного режима, что способствует различным нежелательным побочным процессам (например, циклизации с образованием дикетопиперазинов, см. с. 511). в процессе синтеза возникают сложности, связанные с необходимостью соединять остатки -аминокислот в определенной последовательности. например, при взаимодействии глицина и аланина возможно образование четырех дипептидов:

Глава 35
704
35.4. слОжные БелКи (ПрОТеиды)
в зависимости от структуры белки делят на простые (протеины) и сложные (протеиды). Последние, кроме белка, содержат в своей структуре химически свя-
занную с ним простетическую группу — небелковую часть молекулы. По природе простетической группы протеиды делят на липопротеиды, нуклеопротеиды, гли-
копротеиды, хромопротеиды, фосфопротеиды и металлопротеиды.
липопротеиды в качестве простетической группы содержат липиды, нуклеопротеиды — нуклеиновые кислоты, гликопротеиды — углеводы, хромопротеиды — пигменты, фосфопротеиды — фосфорную кислоту, металлопротеиды — металлы.
существуют также сложные белковые комплексы, в состав которых одновременно входят белки, липиды и углеводы, называемые гликолипопротеидами. они содержатся в соединительной ткани, клеточных стенках бактерий и др.
в зависимости от пространственной формы молекул белки делят на глобулярные и фибриллярные. Глобулярные белки имеют сферическую или эллипсоидную форму, фибриллярные — состоят из вытянутых нитевидных макромолекул, назы-
ваемых протеноидами.
Глобулярные белки (альбумин, глобулин) малоустойчивы к действию температуры, кислот и щелочей, а фибриллярные (белки волос, ногтей, эпидермиса; белки соединительной, костной, хрящевой ткани и др.) весьма устойчивы.
Под влиянием многих факторов (повышенная температура, изменение рн среды, уф- и -излучение и др.) происходит разрушение пространственной формы белков при сохранении первичной структуры. Этот процесс называется денатурацией бел-
ка (рис. 35.7).
денатурация является, как правило, необратимым процессом и приводит к потере биологических функций белков. Примером тепловой денатурации является «свертывание» яичных белков при варке яиц. При денатура-
ции происходит разрыв водородных связей, стабилизирующих пространственную форму белка. денатурированный белок теряет растворимость, в результате чего первоначальная пространственная форма его не может быть восстановлена. денатурация может быть также вызвана образованием нерастворимых солей белков. Это происходит при отравлении солями тяжелых металлов (ртути, свинца и др.). в качестве противоядия в таких случаях применяют белки с повышенным содержанием кислотных групп, например, яичный альбумин. выступая в качестве конкурента, эти белки связывают металлы с образованием нерастворимых солей, которые выводятся из организма.
глава 36
нуКлеинОвые КислОТы
Нуклеиновыми кислотами (полинуклеотидами) называют биополимеры, осу-
ществляющие хранение и передачу генетической информации во всех живых организмах, непосредственно участвующие в биосинтезе белка.
нуклеиновые кислоты (от лат. nucleus — ядро) впервые обнаружены в 1868 году швейцарским химиком иоганном фридрихом Мишером в ядрах клеток. Позже аналогичные вещества найдены в протоплазме клеток.
они входят в состав сложных белков — нуклеопротеидов, содержащихся во всех клетках организма человека, животных, растений, бактерий и вирусов. количество нуклеиновых кислот в различных нуклеопротеидах, кроме вирусных, колеблется в пределах от 40 до 65 %.
36.1. сТрОение нуКлеинОвыХ КислОТ
нуклеиновые кислоты, подобно белкам, представляют собой высокомолекулярные органические соединения, но в отличие от белков, образующих при гидролизе -аминокислоты, мономерными единицами нуклеиновых кислот являются нуклеотиды. Поэтому нуклеиновые кислоты называют еще полинуклеотидами.
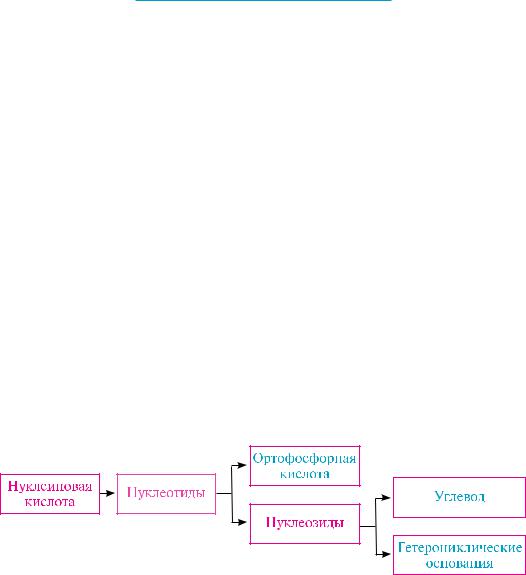
Мономеры нуклеиновых кислот — нуклеотиды — имеют также достаточно сложное строение. При гидролизе нуклеотидов образуется углевод, ортофосфорная кислота и гетероциклические основания.
Химическая структура, состоящая из углевода и гетероциклического основания,
называется нуклеозидом.
в целом гидролиз нуклеиновых кислот можно представить схематически:
в зависимости от природы углевода, входящего в состав нуклеотидов, нуклеиновые кислоты подразделяют на два вида — дезоксирибонуклеиновые кислоты (Днк), содержащие углевод 2-дезокси-D-рибозу и рибонуклеиновые кислоты (Рнк), включающие углевод D-рибозу.
2-дезокси-D-рибоза и D-рибоза входят в состав нуклеиновых кислот в -фу- ранозной форме:

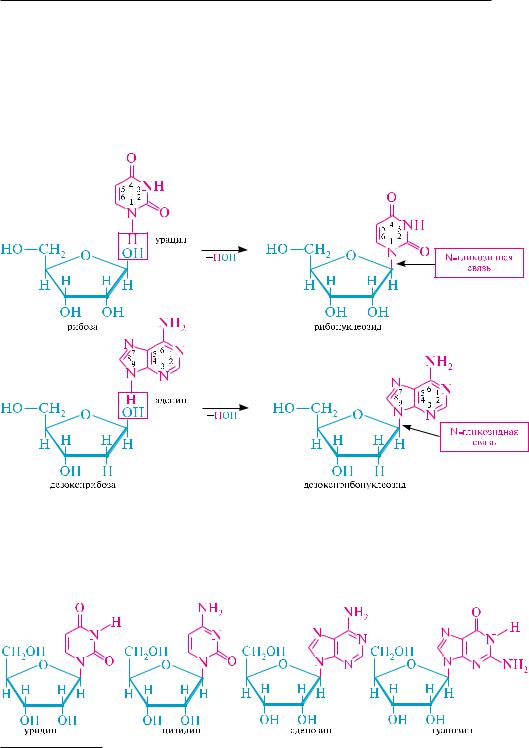
Глава 36
708
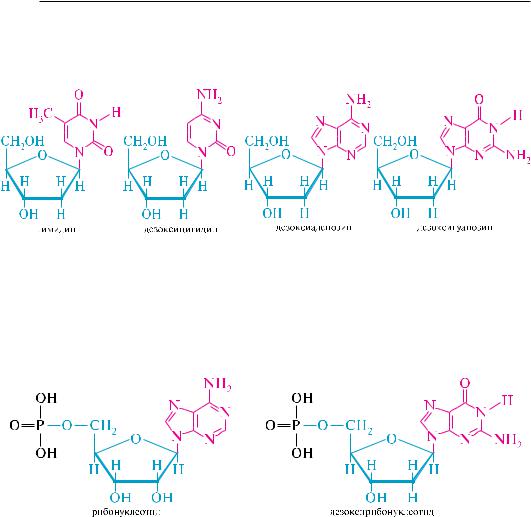
в названиях дезоксирибонуклеозидов дополнительно вводится префикс дезок- си-: дезоксиаденозин, дезоксигуанозин, дезоксицитидин. исключение составляет название нуклеозида, состоящего из дезоксирибозы и тимина — тимидин (вместо дезокситимидина).
являясь N-гликозидами, нуклеозиды в кислой среде подвергаются гидролизу. Пуриновые нуклеозиды гидролизуются очень легко, пиримидиновые — труднее.
внуклеиновых кислотах гидроксильная группа у с-5 или с-3 пентозного остатка нуклеозида этерифицирована ортофосфорной кислотой.
Структурная единица нуклеиновых кислот, состоящая из остатков нуклеозида
ифосфорной кислоты, называется нуклеотидом.
взависимости от природы пентозы различают рибонуклеотиды и дезоксирибо-
нуклеотиды.
в номенклатуре нуклеотидов используют два подхода. с одной стороны, их рассматривают как сложные эфиры — монофосфаты, а с другой — как кислоты
(табл. 36.1).
|
|
Таблица 36.1 |
номенклатура нуклеотидов |
|
|
|
|
|
названия нуклеотидов как монофосфатов |
|
названия нуклеотидов как кислот |
|
|
|
аденозин-5 -монофосфат (аМф) |
|
5 -адениловая кислота |
|
|
|
Гуанозин-5 -монофосфат (ГМф) |
|
5 -гуаниловая кислота |
|
|
|
цитидин-5 -монофосфат (цМф) |
|
5 -цитидиловая кислота |
|
|
|
уридин-5 -монофосфат (уМф) |
|
5 -уридиловая кислота |
|
|
|
дезоксиаденозин-5 -монофосфат (даМф) |
|
дезоксиадениловая кислота |
|
|
|
дезоксигуанозин-5 -монофосфат (дГМф) |
|
дезоксигуаниловая кислота |
|
|
|
дезоксицитидин-5 -монофосфат (дцМф) |
|
дезоксицитидиловая кислота |
|
|
|
тимидин-5 -монофосфат (тМф) |
|
тимидиловая кислота |
|
|
|
нУКлеИнОВЫе КИСлОТЫ |
|
|
|
70 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
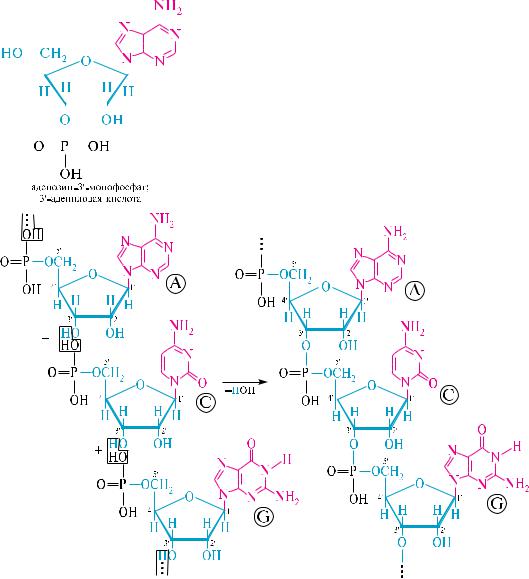
При гидролизе |
нуклеиновых кислот, |
наряду |
||
|
|
|
|
|
|
|
|
|
с нуклеозид-5 -фосфатами, образуются также нук- |
||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
леозид-3 -фосфаты. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Положение остатка фосфорной кислоты оп- |
||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
ределяется местом разрыва фосфодиэфирной связи |
||||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
между соседними нуклеотидами. |
|
|
||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
нуклеиновые кислоты |
представляют |
|
собой |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
продукты полимеризации мононуклеотидов. нук- |
||||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
леотиды связываются в длинные цепи с помощью |
||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
фосфодиэфирных |
связей, |
которые образуются |
||
|
|
|
|
|
|
|
|
|
|||||
с участием гидроксила при с-3 предыдущего нуклеотидного звена и гидроксила при с-5 последующего нуклеотидного звена:
Мононуклеотиды, динуклеотиды и их производные присутствуют в клетках также в свободном виде и играют важную роль в обмене веществ. во всех тканях организма, наряду с нуклеозидмонофосфатами, содержатся ди- и трифосфаты нуклеозидов.
особенно широко известны аденозин-5 -фосфат (аМф), аденозин-5 -дифос- фат (адф) и аденозин-5 -трифосфат (атф). Эти нуклеотиды способны взаимопревращаться путем фосфорилирования (присоединение одного или двух остатков фосфорной кислоты к аМф), либо дефосфорилирования (отщепление одного или двух остатков фосфорной кислоты от атф). При дефосфорилировании выделяется значительное количество энергии, использующееся в организме для протекания тех или иных биологических процессов, например, в биосинтезе белка.
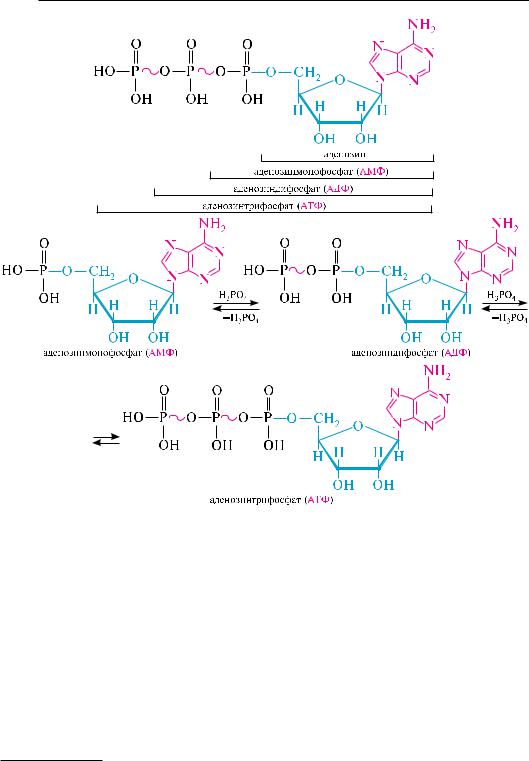

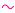 р между остатками фосфорной кислоты в молекулах нуклеозидполифосфатов является
р между остатками фосфорной кислоты в молекулах нуклеозидполифосфатов является