
304- Органическая химия_Черных В.П. и др_Х., 2007 -776с
.pdf
гаЛогеноПроизВодные угЛеВодородоВ
271
+ |
|
Cl |
N N |
CuCl |
|
Cl– |
+ N2 |
|
бензолдиазония хлорид |
|
хлорбензол |
Для введения атома галогена в боковую углеродную цепь аренов используют такие методы, как галогенирование алкиларенов и реакция хлорметилирования.
галогенирование алкиларенов. В отличие от галогенирования в ароматическое ядро, галогенирование в боковую цепь происходит без катализатора при высоких температурах или при облучении УФ-светом. Реакция протекает по механизму SR
(см. с. 139):
CH3 |
Cl2; hν |
CH2Cl |
CHCl2 |
CCl3 |
|
Cl2; hν |
|
Cl2; hν |
|
|
–HCl |
–HCl |
|
–HCl |
толуол |
|
бензилхлорид |
бензилиденхлорид |
бензилидинхлорид |
Галогенирование в боковую цепь идет, как правило, в α-положение относительно бензольного ядра, поскольку в этом случае образуется устойчивый свободный радикал бензильного типа (см. с. 129):
α |
hν |
|
|
|
ÑH2 CH3 + Cl2 |
ÑH |
CH3 + HCl |
||
|
Ñl
1-фенил-1-хлорэтан
В избытке галогена все атомы водорода при α-углеродном атоме в молекуле могут быть замещены на атомы галогена.
реакция хлорметилирования используется для получения арилметилхлоридов. Она основана на взаимодействии аренов с формальдегидом и хлороводородом в присутствии катализатора (AlCl3, ZnCl2). В процессе реакции атом водорода бензольного кольца замещается на хлорметильную группу:
O |
|
ZnCl2 |
CH2Cl |
|
+ H C |
+ HCl |
+ H2O |
||
|
||||
H |
|
|
бензилхлорид |
|
формальдегид |
|
|
Хлорметилирование относится к реакциям электрофильного замещения в аро-
матическом ряду. Атакующей электрофильной частицей является гидроксиметил-
+
катион CH2OH:
|
δ– |
|
|
|
|
|
|
|
|
|
δ+ O |
δ+ |
|
δ– |
+ |
|
|||||
H C |
+ H |
|
Cl |
|
|
|
|
CH2OH + Cl– |
||
|
|
|
|
|
||||||
|
|
|
|
|||||||
|
H |
|
|
|
|
|
|
|
|
|
+ |
|
|
CH2OH |
|
|
|
CH2Cl |
|||
CH2OH |
|
|
|
|
|
HCl; ZnCl2 |
||||
–H+ |
|
|
|
|
|
|
|
–H2O |
|
|
гаЛогеноПроизВодные угЛеВодородоВ
273
Cl |
Cu; 200 °C |
NÍ2 |
|
+ 2NÍ3 |
+ NH4Cl |
||
|
|||
хлорбензол |
|
анилин |
Вместе с тем подвижность атома галогена в галогенаренах резко возрастает при наличии в орто- или пара-положениях по отношению к атому галогена сильных электроноакцепторных заместителей (—NO2, —NO, —CN, —COOH, —SO3H и др.). Такие соединения называют активированными галогенаренами. Повышение реакционной способности связи углерод-галоген в активированных галогенаренах связано с увеличением дробного положительного заряда на атакуемом атоме углерода под влиянием электроноакцепторного заместителя:
|
O |
Cl δ+ |
N |
|
O |
Так, в молекуле 2,4-динитро-1-хлорбензола атом хлора довольно легко замещается на группы —ОН, —NH2, —OCH3 и др.:
|
|
|
OH |
|
|
|
NaOH (H2O); 100 °C |
|
NO2 |
|
|
|
||
|
|
|
|
|
|
|
–NaCl |
|
|
|
|
|
NO2 |
|
Cl |
2,4-динитрофенол |
|||
|
NH2 |
|||
|
NO2 |
|
||
|
||||
|
|
2NH3; 200 °C |
|
NO2 |
|
|
|
|
|
|
|
–NH4Cl |
|
|
NO2 |
NO2 |
|||
2,4-динитро-1-хлорбензол |
|
|||
|
|
|
2,4-динитроанилин |
|
|
|
|
|
OCH3 |
|
|
CH3OK |
|
NO2 |
|
|
|
||
–KCl
NO2
1-метокси-2,4-динитробензол
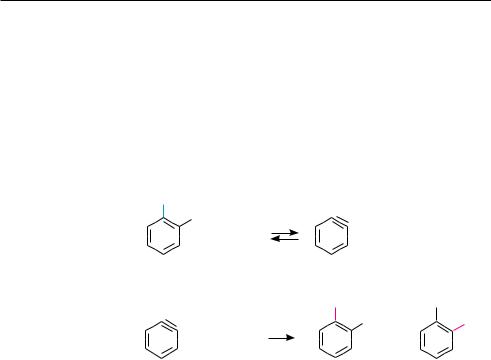
Реакции нуклеофильного замещения активированного атома галогена протекают по механизму SN2. Однако в отличие от реакций SN2 в алифатическом ряду, которые протекают в одну стадию и сопровождаются синхронными процессами разрыва связи C—Hal и образования связи C—Nu, бимолекулярное нуклеофильное замещение в ароматическом ряду происходит в две стадии. На стадии I атакующая нуклеофильная частица присоединяется к электрофильному атому
гаЛогеноПроизВодные угЛеВодородоВ
275
Все эти факты можно объяснить с позиций так называемого аринового механизма взаимодействия. Согласно данному механизму замещение атома галогена на нуклеофил идет не прямо, а через предварительное отщепление галогеноводорода и последующее присоединение нуклеофила. Сначала нуклеофильный реагент, будучи сильным основанием, отщепляет от молекулы галогенарена галогеноводород, образуя нестойкий, очень реакционноспособный промежуточный продукт — дегидробензол (арин), содержащий в своем составе тройную связь. Затем дегидробензол мгновенно присоединяет по месту тройной связи нуклеофильный реагент, причем ковалентную связь с нуклеофилом может образовать в равной степени каждый из двух, связанных тройной связью атомов углерода:
Cl |
|
* |
|
* |
H |
|
|
Стадия I |
+ NÍ2– |
+ NÍ3 + Cl– |
|
хлорбензол |
|
дегидробензол; |
|
|
|
àðèí |
|
* |
|
NÍ2 |
Í |
.. |
* Í |
* NÍ2 |
|
Стадия II |
+ NÍ3 |
|
+ |
анилин
Этот механизм называют еще механизмом элиминирования-присоединения.
Ароматические галогеноуглеводороды с атомом галогена в боковой цепи легко вступают в различные реакции нуклеофильного замещения. Соединения, в которых атом галогена изолирован от бензольного кольца двумя и более уг- лерод-углеродными связями, по активности в реакциях SN напоминают галогеналканы. Галогеноуглеводороды, содержащие атом галогена у α-атома углерода боковой цепи (бензилгалогениды), обладают повышенной реакционной способностью связи С—Hal. По активности в реакциях SN бензилгалогениды сходны с аллилгалогенидами. Нуклеофильное замещение атома галогена происходит в них по механизму SN1. Высокая подвижность атома галогена в бензилгалогенидах обусловлена большой устойчивостью бензильного катиона, образующегося после отщепления галогенид-иона (см. с. 123).
реакЦии ЭЛекТроФиЛьного замещениЯ В аромаТическом Ядре (SE )
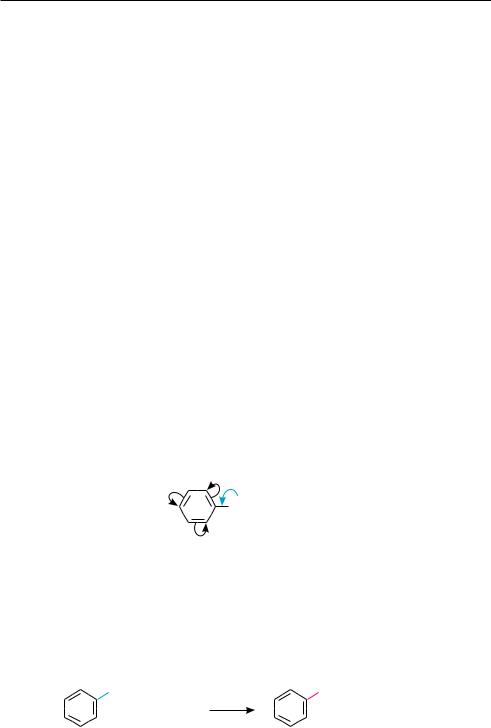
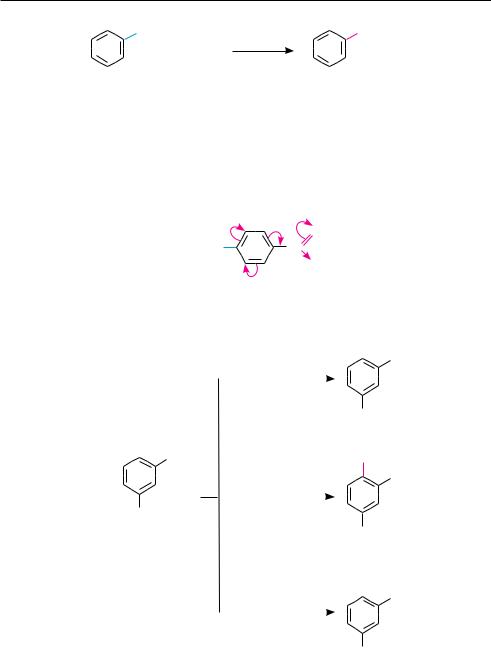
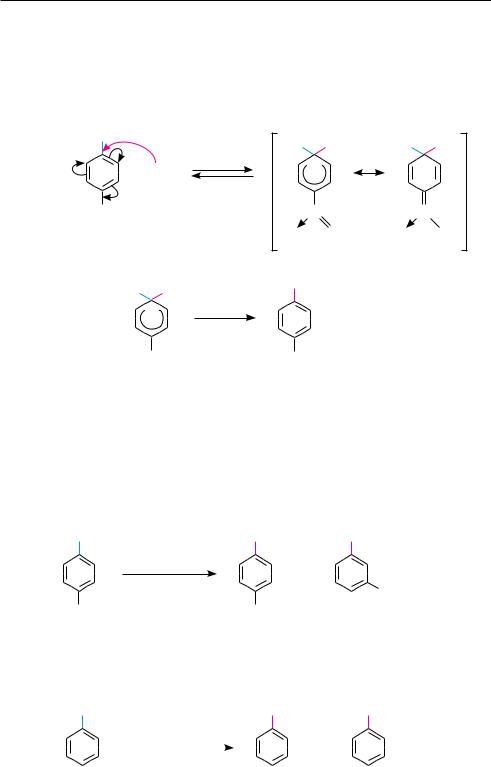
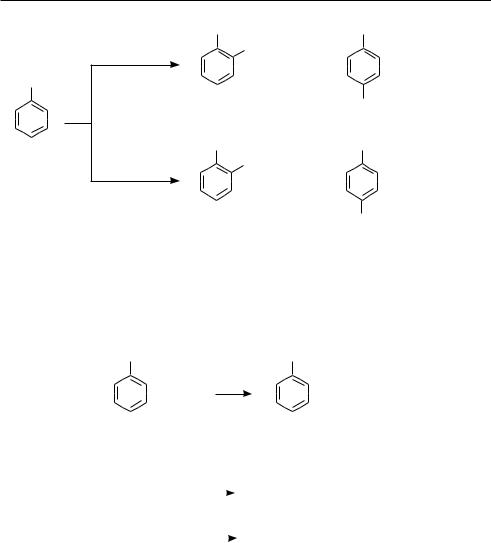
По ароматическому ядру галогенарены вступают в обычные реакции электрофильного замещения: галогенирование, нитрование, сульфирование и др. Как уже отмечалось, атом галогена, непосредственно связанный с ароматическим кольцом, проявляет отрицательный индуктивный и положительный мезомерный эффекты, причем в статическом состоянии –I-эффект > +М-эффекта. Поэтому атомы галогена в целом проявляют электроноакцепторные свойства по отношению к бензольному кольцу и тем самым снижают его реакционную способность в реакциях SЕ. Принимая участие в стабилизации σ-комплексов, образующихся при замещении в орто- и пара-положениях, атомы галогенов выступают как заместители I рода и направляют электрофильное замещение в орто- и пара-поло-
жения (см. с. 219.):
Глава 18
276
|
|
Cl |
Cl |
|
|
NO2 |
|
|
HNO3; H2SO4 |
+ |
|
Cl |
–H2O |
|
|
|
|
||
|
|
|
|
|
|
î-нитрохлорбензол |
NO2 |
|
|
ï-нитрохлорбензол |
|
|
|
Cl |
Cl |
|
H2SO4•SO3 |
SO3H |
+ |
|
–H2O |
|
|
|
|
|
|
|
|
î-хлорбензолсульфокислота |
SO3H |
|
|
ï-хлорбензолсульфокислота |
|
реакЦии с меТаЛЛами (меТаЛЛироВание)
Галогенарены легко вступают в реакцию с металлами — литием, натрием, магнием. При взаимодействии с магнием в среде диэтилового эфира образуются магнийорганические соединения (реактивы Гриньяра):
Br |
MgBr |
+ Mg ýôèð
фенилмагнийбромид
В условиях реакции Вюрца—Фиттига металлорганическое соединение образуется в качестве промежуточного продукта:
C6H5 |
|
Br + 2Na |
|
|
|
C6H5Na + NaBr |
||||
|
|
|
|
|||||||
бромбензол |
|
|
|
фенилнатрий |
||||||
C6H5Na + C6H5 |
|
Br |
|
|
C6H5 |
|
C6H5 + NaBr |
|||
|
|
|
|
|||||||
|
|
|
|
|
|
бифенил |
||||
18.7. ИДЕНТИФИКАЦИЯ ГАЛОГЕНОПРОИЗВОДНЫХ УГЛЕВОДОРОДОВ
18.7.1. химические меТоды
Наиболее простым методом обнаружения галогена в органическом соединении является проба Бейльштейна. Она основана на способности галогеноуглеводородов при нагревании с медью образовывать летучие меди (II) галогениды, окрашивающие пламя горелки в зеленый цвет. Проба Бейльштейна очень чувствительна, однако она не позволяет определить природу галогена. Нельзя также с ее помощью открыть фтор, поскольку меди (II) фториды нелетучи.
Для определения природы галогена в органическом веществе применяют метод сплавления с металлическим натрием. При сплавлении галогеноуглеводо-


278 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Глава 18 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
ческие вещества и находит широкое при- |
||||||||||||||||||||||||
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
менение как растворитель в химических |
|||||||||||||||||||||||
|
|
|
|
|
производствах, а также для извлечения |
|||||||||||||||||||||||
|
|
|
|
|
многих |
веществ |
из |
растительного |
сырья, |
|||||||||||||||||||
|
|
|
|
|
в частности жиров, алкалоидов, смол и др. |
|||||||||||||||||||||||
|
|
|
|
|
На свету хлороформ медленно окисля- |
|||||||||||||||||||||||
|
|
|
|
|
ется |
|
|
кислородом |
|
|
воздуха |
с образовани- |
||||||||||||||||
|
|
|
|
|
ем |
высокотоксичного вещества — фосгена |
||||||||||||||||||||||
|
|
|
|
|
и хлороводорода. Фосген может окисляться |
|||||||||||||||||||||||
|
|
|
|
|
далее, образуя молекулярный хлор и углеро- |
|||||||||||||||||||||||
|
|
|
|
|
да (IV) оксид: |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
Ñl |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|||
Федор Федорович (Фридрих конрад) |
|
|
|
|
|
|
|
|
|
|
|
[O] |
|
|
|
|
|
|
|
|
|
|
|
|||||
Ñl |
|
|
|
|
C |
|
|
Ñl |
|
|
|
Ñl |
|
|
C |
|
Ñl |
+ HCl |
||||||||||
|
|
БеЙЛьШТеЙн |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
(1838—1906) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
фосген |
|
|
||||||
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
Химик-органик, академик Петер- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
бургской академии наук с 1886 года. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Изучал |
химию под |
руководством |
|
|
|
|
|
|
|
|
|
|
|
[O] |
|
|
|
Ñl2 |
+ |
ÑO2 |
|
|||||||
Ñl |
|
|
|
C |
|
|
Ñl |
|
|
|
|
|
||||||||||||||||
Р. Бунзена, Ф. Вёлера, Ш. А. Вюрца. |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
Основная область научных иссле- |
|
|
Хлороформ обладает сильным нарко- |
|||||||||||||||||||||||||
дований — химия ароматических со- |
|
|
||||||||||||||||||||||||||
тическим действием. |
Ранее он применялся |
|||||||||||||||||||||||||||
единений. Предложил (1872) реакцию |
в медицине для усиления действия азота (I) |
|||||||||||||||||||||||||||
открытия |
галогенов |
в |
органических |
|||||||||||||||||||||||||
оксида при комбинированном ингаляцион- |
||||||||||||||||||||||||||||
соединениях (проба Бейльштейна). |
||||||||||||||||||||||||||||
ном наркозе, но в настоящее время из-за |
||||||||||||||||||||||||||||
Исследовал кавказскую нефть. Ини- |
||||||||||||||||||||||||||||
циатор создания и первый составитель |
высокой токсичности не используется. |
|||||||||||||||||||||||||||
многотомного справочника, включа- |
|
|
Йодоформ (трийодметан) CHI3. Твердое |
|||||||||||||||||||||||||
ющего информацию о всех известных |
кристаллическое вещество лимонно-желтого |
|||||||||||||||||||||||||||
на время выпуска |
очередного тома |
цвета с резким характерным устойчивым за- |
||||||||||||||||||||||||||
органических соединениях. |
пахом (т. пл. 116 °С). Практически не раство- |
|||||||||||||||||||||||||||
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
рим в воде, хорошо растворим в хлороформе |
|||||||||||||||||||||||
|
|
|
|
|
и диэтиловом эфире. |
Йодоформ с |
давних |
|||||||||||||||||||||
времен применяется в качестве антисептического средства в стоматологии, а также в форме присыпок и мазей для лечения инфицированных ран и язв.
Фторотан (2-бром-1,1,1-трифтор-2-хлорэтан). Бесцветная подвижная жидкость
|
|
F |
|
Br |
с запахом, напоминающим запах хлороформа (т. кип. 49—51 °С). |
||
|
|
|
Мало растворим в воде, хорошо растворяется в этаноле, диэтило- |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
вом эфире, хлороформе. Фторэтан обладает сильным наркотиче- |
F |
|
C |
|
ÑH |
|||
|
|
ским действием и низкой токсичностью. Он широко применяется |
|||||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
в медицинской практике в качестве средства для комбинирован- |
|
|
F |
|
Cl |
|||
|
|
|
|
|
|
|
ного ингаляционного наркоза. |
дифтордихлорметан (фреон-12) СF2Cl2. В обычных условиях дифтордихлорметан является газообразным веществом без запаха. Он не горюч, не взрывоопасен, не токсичен и не вызывает коррозии металлов. Указанные свойства позволяют использовать фреон-12 в качестве хладоагента в холодильных установках, а также в качестве пропеллента в производстве аэрозольных лекарственных препаратов.
хлорбензол C 6H5Cl. Бесцветная жидкость со своеобразным запахом (т. кип. 132 °С). С водой образует азеотропную смесь, содержащую 71,6 % хлорбензола. Рас-
гаЛогеноПроизВодные угЛеВодородоВ
279
творяется в бензоле, этаноле, хлороформе и других органических растворителях. Хлорбензол применяется в производстве фенола, анилина, лекарственных средств.
В медицинской практике широко применяют ряд йодсодержащих рентгено-
контрастных средств (йопаноевая, амидотризоевая, йоталамовая кислоты). Извест-
ны лекарственные препараты муколитического (бромгексина гидрохлорид), седа-
тивного (бромкамфора, бромизовал), противогрибкового (клотримазол) и других видов фармакологического действия.
|
|
NÍ2 |
|
|
|
NÍCOCÍ3 |
|
I |
I |
|
|
I |
I |
|
|
CÍ2 CÍ |
COOH |
ÍOOC |
CONÍCÍ3 |
|
|
|
I |
CÍ2 |
CÍ3 |
|
I |
|
|
|
йоталамовая кислота |
|||
|
|
йопаноевая кислота; |
|
|||
|
|
йопагност |
|
|
|
|
|
|
COÎÍ |
|
|
|
NÍ2 |
|
I |
I |
|
•2Í2O |
Br |
ÑÍ2 N |
|
|
|
|
|
•ÍCl |
|
Í |
COCÍN |
NÍCOCÍ |
|
|
ÑÍ3 |
|
3 |
|
|
3 |
|
|
|
|
|
I |
|
|
|
Br |
|
амидотризоевой кислоты дигидрат; |
|
|
бромгексина гидрохлорид; |
||
|
урографин; ангиографин |
|
|
|
бромобене |
|
разрушение озонового слоя
Озоновый слой находится над поверхностью Земли на расстоянии 15—30 км. Он предохраняет планету и все живое от опасного воздействия УФ-лучей Солнца. Впервые
всемидесятые годы прошлого столетия были обнаружены «озоновые дыры». Предполагают, что основной причиной, вызывающей истощение озонового слоя, является группа химических соединений — фторхлоруглероды (ФХУ). Они широко используются в производстве холодильников, кондиционеров, аэрозолей, а также в качестве растворителей и пенообразователей. Для них характерна термическая и окислительная устойчивость. ФХУ не способны разлагаться в нижних слоях атмосферы и, попадая в стратосферу, участвуют
вфотохимических реакциях.
FF
F |
|
|
|
hν |
F |
|
C. + Cl. |
|
C . .Ñl |
|
|||||||
|
|
|
||||||
|
|
|
|
|
|
|
|
|
Cl |
|
|
Cl |
|||||
Образовавшийся свободный радикал инициирует протекание цепной радикальной реакции, в которой могут принимать участие молекулы озона:
O3 + Cl. O2 + ClO.
O2 + ClO.
В 1987 году подписан Монреальский протокол по защите озонового слоя, призывающий к прекращению производства ФХУ. В качестве заменителей были предложены фторхлоруглеводороды; они менее устойчивы и разрушаются в тропосфере. Однако фторхлоруглеводороды относят к парниковым газам, способствующим усилению парникового эффекта. Проблема разрушения озонового слоя и глобального потепления климата Земли в настоящее время остается чрезвычайно актуальной.
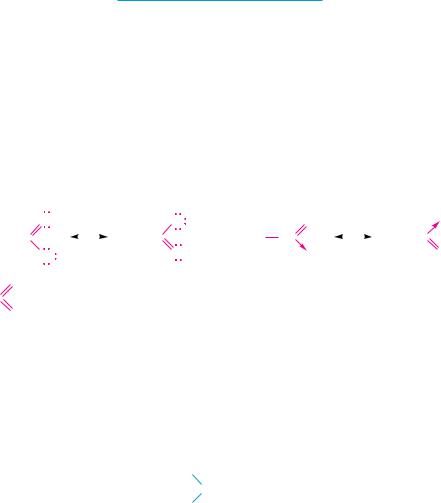
Глава 19
НИТРОСОЕДИНЕНИЯ
Нитросоединениями называют производные углеводородов, содержащие в своем составе одну или несколько нитрогрупп —NO2.
Нитрогруппа имеет планарное (плоское) строение. Атомы азота и кислорода находятся в состоянии sp2-гибридизации. Электронное строение нитрогруппы можно представить с помощью двух граничных структур, в которых один из атомов кислорода образует с атомом азота двойную, а другой — семиполярную связь:
|
|
|
+ |
O |
+ |
O– |
O |
|
|
|
O |
||||||
|
|
R |
|
N |
|
|
R |
|
N |
|
R N |
|
|
R |
|
N |
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
O– |
|
|
|
|
O |
O |
|
|
|
O |
||
+ |
O–1/2 |
Однако в реальной молекуле химические связи обоих атомов |
|||||||||||||||
R |
|
N |
|
|
кислорода с атомом азота равноценны, что изображается форму- |
||||||||||||
|
|
|
|||||||||||||||
|
|
|
O–1/2 лой с дробными зарядами. |
|
|
|
|
|
|
||||||||
|
В зависимости |
от природы |
углеводородного радикала, |
с которым связа- |
|||||||||||||
на нитрогруппа, различают алифатические и ароматические нитросоединения. Алифатические — могут быть насыщенными (нитроалканы) и ненасыщенными
(нитроалкены, нитроалкины). Ароматические нитросоединения могут содержать нитрогруппу, непосредственно связанную с бензольным ядром (нитроарены), и нитрогруппу в боковой цепи (нитроалкиларены). По расположению нитрогруппы в углеродной цепи нитроалканы и нитроарены с нитрогруппой в боковой цепи подразделяют на первичные, вторичные и третичные:
|
|
|
|
|
R |
|
|
R |
|||||
|
|
|
|
|
R |
|
|
|
|
|
|||
R |
|
CH2 |
|
NO2 |
CH |
|
NO2 |
|
C |
|
NO2 |
||
|
|
|
|
|
|||||||||
|
|
|
|
|
R |
|
|
|
|
|
|
||
первичное |
вторичное |
|
|
R |
|||||||||
третичное |
|||||||||||||
нитросоединение |
нитросоединение |
нитросоединение |
|||||||||||
В данной главе рассмотрены нитроалканы, нитроарены с нитрогруппой в бензольном кольце и нитроарены с нитрогруппой в боковой цепи.
19.1. НОМЕНКЛАТУРА. ИЗОМЕРИЯ
По заместительной номенклатуре названия нитроалканов и нитросоединений с нитрогруппой в бензольном кольце образуют добавлением префикса нитро- к названию родоначального углеводорода с указанием положения нитрогруппы в углеродной цепи:
