
s5_atomfiz_exam_nah_book
.pdf
Глава 10. Тонка структура атомного спектра водню
2. В ЯКИХ ІНТЕРВАЛАХ МОЖУТЬ ЗМІНЮВАТИСЬ НИЖЧЕ ВКАЗАНІ КВАНТОВІ ЧИСЛА: 1) n , 2) , 3) ml , 4) s , 5) ms , 6) j ,
7) m j .
Квантове число може змінюватися у межах:
1) 0 ; 2) |
0 n 1; 3) |
1 2 ; 4) |
1 2 ; 5) |
j 1/ 2 ; 7) |
1 ; 8) |
від до ; |
9) від |
s s ; 6)j до j .
3. УКАЖІТЬ, ЯКИМИ КВАНТОВИМИ ЧИСЛАМИ ОПИСУЄТЬСЯ СТАН АТОМА ІЗОЕЛЕКТРОННОГО РЯДУ ВОДНЮ В НАБЛИЖЕННІ:
А) НЕ ОПИСУЄ ТОНКУ СТРУКТУРУ СПЕКТРАЛЬНИХ ТЕРМІВ; Б) ОПИСУЄ ТОНКУ СТРУКТУРУ СПЕКТРАЛЬНИХ ТЕРМІВ.
У наближенні, що розглядається, стан вільного атома ізоелектронного ряду водню повністю описується наступним набором квантових чисел:
1)головне квантове число n ;
2)орбітальне квантове число ;
3)магнітне орбітальне квантове число m ;
4)спінове квантове число s ;
5)магнітне спінове квантове число ms ;
6)внутрішнє квантове число j ;
7)магнітне внутрішнє квантове число m j ;
8)спінове число ядра атома;
9)магнітне квантове число атома
4.ВІД ЯКИХ КВАНТОВИХ ЧИСЕЛ ЯВНО ЗАЛЕЖИТЬ ЕНЕРГІЯ ЕЛЕКТРОНА В АТОМІ ВОДНЮ ПРИ ВРАХУВАННІ А) ТОНКОЇ СТРУКТУРИ СПЕКТРІВ, Б) НАДТОНКОЇ СТРУКТУРИ СПЕКТРІВ?
1)n ; 2) s ; 3) j ; 4) ; 5) mj ; 6) mF ; 7) F .
Находкін М.Г., Харченко Н.П., Атомна фізика |
263 |
Глава 10. Тонка структура атомного спектра водню
5. ЯКА ВЕЛИЧИНА ЗМІЩЕННЯ ОСНОВНОГО РІВНЯ АТОМА ВОДНЮ ПО БОРУ, ЯКЩО ВРАХУВАТИ СПІН ЕЛЕКТРОНА?
1) R·α2/2; |
2) R·α2/4; |
3) R·α, де R- стала Рідберга, α – стала |
тонкої структури. |
4) Еіон ·R·α2/4. |
|
6. ЧОМУ В ДОСЛІДІ ЛЕМБА-РІЗЕРФОРДА ДЛЯ ЗБУДЖЕННЯ АТОМІВ ВОДНЮ ВИКОРИСТОВУЄТЬСЯ ПУЧОК ЕЛЕКТРОНІВ?
1)для збудження енергетичного рівня 22S1/2;
2)для збудження енергетичного рівня 22P1/2;
3)для збудження енергетичного рівня 22P3/2;
ТА ЯКА ЇХ ЕНЕРГІЯ?
4)менше 10 ЕВ;
5)більше 10 ЕВ.
7. У СКІЛЬКИ РАЗІВ ВЕЛИЧИНА НАДТОНКОЇ СТРУКТУРИ ОСНОВНОГО ТЕРМУ ВОДНЮ ВІДРІЗНЯТЬСЯ ВІД ВЕЛИЧИНИ ЛЕМБІВСЬКОГО ЗСУВУ ЦЬОГО ТЕРМУ?
1) 1,2·103; 2) 1,2·10-3; 3) 1/137.
8. НА СКІЛЬКИ РІВНІВ РОЗЩЕПИТЬСЯ РІВЕНЬ А) 2S , Б) 2 P ЗА РАХУНОК СПІН-ОРБІТАЛЬНОЇ ВЗАЄМОДІЇ?
1)0 ; 2) 1; 3) 2 ; 4) 3 .
ТА ЗА РАХУНОК |
ВЗАЄМОДІЇ ПОВНОГО МАГНІТНОГО |
МОМЕНТУ ЕЛЕКТРОНІВ |
ІЗ МАГНІТНИМ МОМЕНТОМ ЯДРА (СПІН |
ЯДРА ДОРІВНЮЄ 1 2 )? |
|
2)2 ; 3) 3 ; 4) 4 .
9.УКАЖІТЬ, ЯКІ МОЖЛИВІ ПЕРЕХОДИ З РІВНЯ 42S1 2 АТОМА
2 АТОМА
УТАКІ СТАНИ:
Находкін М.Г., Харченко Н.П., Атомна фізика |
264 |

Глава 10. Тонка структура атомного спектра водню
1) 52S |
; 2) 32 P |
; 3) 32 P |
; 4) |
42P |
; 5) |
42P |
; 6) |
42D |
; |
||||
1 2 |
|
|
1 2 |
|
3 2 |
|
|
1 2 |
|
3 2 |
|
3 2 |
|
7) 62P |
; 8) |
22S |
; 9) 22P |
. |
|
|
|
|
|
|
|||
|
3 2 |
|
|
1 2 |
|
3 2 |
|
|
|
|
|
|
|
Література
1.Матвеев А.Н. Атомная физика. Учеб. пособие для студентов вузов.-
М.: Высш. шк. –1989. – 489 с. ( §44, 72, 73).
2.Сивухин Д.В. Атомная и ядерная физика.: Учеб. пособие, часть 1, Атомная физика. М.: “ Наука”, Гл.ред. физ. мат. лит. - 1986. –416
с. (§40, 44 і 45).
3.Белый М.У., Охрименко Б.А. Атомная физика. - К.: “Вища шк.”.,
Голов. из-во., -1984. –271 с. (§6.4).
4.Гайда Р.П. Атомна фізика.- Львів. –1965. – 356 с. (§42).
5.Соколов А.А., Тернов И.М., Жуковский В.Ч. Квантовая механіка. -
М.: “Наука”. – 1979. - 528 с. , ил. (§18-21).
6.Вакарчук І.О. Квантова механіка: Підручник. 2-ге вид. доп. – Львів. ЛНУ імені Івана Франка, 2004, - 784 с. іл.
Додаткова література
1.Хоофт Г.T., Калибровочные теории сил между элементарными ча-
стицами, УФН, т135, в.3, 479-512, 1981.
2.Овечко В.С., Шека Д.І., Фізика атомів та атомних систем (від классики до квантів): Навчальний посібник, К.: Виданичополіграфічний центр «Київський університет», 2008, - 184с. (розділ 1.6. Фізичний вакуум).
Задачі
1.Харченко Н. П., Прокопенко О. В., Карлаш Г. Ю. Атомна фізика в задачах. Академдрук, - 2007. – 336с. (розділи 3, 4 і 5).
2.Мультимедійна демонстрація. Дослід Лемба-Різерфорда по дослі-
дженню лембівського зсуву енергетичних рівнів |
|
|
|
|
, |
|
для ато- |
|
|
|
|
||||||
ма водню. Тонка та надтонка структура головної лінії серії Лаймана для атома водню.
Находкін М.Г., Харченко Н.П., Атомна фізика |
265 |
Глава 11. Векторна модель атома
Глава 11. ВЕКТОРНА МОДЕЛЬ АТОМА
«Знання деяких принципів легко надолужує не знання деяких фактів»
Клод Гельвецій – французький філософ
11.1. Векторна модель атома. Типи зв’язку. 11.2. Нормальний (L-S) або Рас- сел-Саундеровський зв’язок. 11.3. Квантові числа складних атомів. 11.4. Правила відбору. 11.5. Правила Хунда (Гунда). 11.6. Систематика спектрів складних атомів з нормальним зв’язком. 11.7. Приклади застосування векторної моделі. 11.6. J-J зв’язок. 11.7. Висновки. 11.8. Контрольні запитання та вправи, тестові завдання. Література.
11.1. Векторна модель атома. Типи зв’язку
Визначення електронних станів багатоелектронних атомів - дуже складна задача. Тому на практиці їх аналіз здійснюють за допомогою наближених методів, наприклад, векторної моделі атома, яка дозволяє систематизувати квантові стани. Вихідним її положенням є те, що енергія електрона в складному атомі визначається електронною конфігурацією - розподілом електронів між наявними орбіталя-
ми (наприклад, електронна конфігурація атома водню є 1s1, гелію - 1s2, літію - 1s22s1, тощо) і комбінацією можливих спінових і орбітальних внесків, що призводять до повного кутового моменту атома.
Електронна конфігурація знаходиться за допомогою принципу Пау-
лі, згідно якого в електронному стані з чотирма квантовими числами (наприклад, n, , m ,, ms або n, , j, mj) може знаходитись тільки один електрон (глава 12, §12.3). Терми позначають через сумарні кутові моменти, які дає векторна модель. Оскільки в основне рівняння кутових моментів не входить потенціал U(r), то це значно спрощує аналіз багатоелектронних атомів. Визначення сумарного (повного) вектора кутового моменту (моменту кількості руху) зводиться у векторній моделі до алгебраїчного складання квантових чисел, що характеризують вектори кутових моментів електронів. Таким чином, у векторній моделі замість розв’язку складної задачі знаходження енергетичних рівнів атомів здійснюються класифікація або систематизація квантових станів. Вона полягає у знаходженні відповідних квантових чисел складної системи за допомогою комбінаторики квантових чисел більш простих (одноелектронних) систем і визначенні набору енергетичних рівнів, які належать одному терму, тобто мультиплетності термів.
Находкін М.Г., Харченко Н.П., Атомна фізика |
266 |
Глава 11. Векторна модель атома
Ця задача спрощується ще й тому, що електрони всіх заповнених оболонок, крім валентної, мають нульовий кутовий момент
LL 0, LS 0, LJ 0, і, замість розгляду внесків усіх Z електронів,
можна обмежитись розглядом лише валентних електронів. Однак залишається складність, зв’язана з вибором послідовності складання кутових моментів, яка залежить від інтенсивності взаємодії моментів між собою. Для спрощення складання кутових моментів валентних електронів прийнято розрізняти два граничних випадки моделей зв’язку: нормального (L-S або Рассел-Саундеровського) та j - j зв’язку.
Нормальним називається зв’язок, коли енергії взаємодії орбітальних (E - ) і спінових моментів (Es-s) кількості руху, в основі яких лежить електростатична квантова взаємодія, більші за енергію спінорбітальної взаємодії (E -s), магнітна взаємодія якої згідно (9.31) пропорційна квадрату сталої тонкої структури,
| E - | та | Es-s | > | E -s | . (11.1)
J-J зв’язком називається випадок, коли енергії орбітальної (E -) та спін-спінової (Es-s) взаємодій менші за енергію спін-орбітальної взаємодії (Е -s)
| E - | та | Es-s | < | Е -s | . |
(11.2) |
Жодна із розглянутих моделей не дає точного уявлення про справжній стан, тому що завжди існує внутрішня конкуренція між різними типами взаємодій. Навіть в одному атомі різні електрони взаємодіють за різними схемами. Але для легких атомів, у яких незначна спінорбітальна взаємодія, нормальна (Рассел-Саундерса) модель дозволяє описувати поведінку валентних електронів. У важких атомів, здебільшого, переважає j-j зв язок, бо у них суттєво збільшується спінорбітальна взаємодія. Взагалі векторна модель відіграє допоміжну роль мнемонічного правила.
11.2. Нормальний (L-S) або Рассел-Саундеровський зв’язок
Модель нормального зв’язку застосовується до атомів першої половини періодичної таблиці елементів Д.І. Менделєєва. В ній спочатку знаходять сумарний орбітальний момент кількості руху LL і сумарний спіновий момент LS , а потім знаходять повний момент кількості руху LJ
|
|
|
i Z |
|
i Z |
|
|
LJ |
LL LS |
L i |
Lsi |
(11.3) |
|||
|
|
|
i 1 |
|
i 1 |
|
|
Находкін М.Г., Харченко Н.П., Атомна фізика |
267 |

Глава 11. Векторна модель атома
Оскільки орбітальні та спінові моменти електронів на заповнених оболонках дорівнюють нулю, то в (11.3) залишиться сума моментів електронів на не заповненій валентній оболонці. Абсолютні значення
кутових моментів LJ , LL, LS визначаються новими квантовими чис-
лами: орбітальним L, спіновим S і квантовим числом сумарного моменту кількості руху J за допомогою співвідношень:
|
|
|
|
|
|
|
|
|
L |
|
|
|
J (J 1) |
|
|
|
J |
|
|
|
|
|
|
|
|
|
|
||||
|
L |
|
|
|
|
. |
|
|
|
|
L(L 1) |
(11.4) |
|||
|
L |
|
|
|
|
|
|
|
L |
|
|
|
|
|
|
|
|
|
S(S 1) |
|
|||
|
S |
|
|
|
|
|
|
|
|
|
|
|
|
||
А їх проекції на довільну вісь z |
|
|
|
|
|||
|
|
|
LJ ,z mJ |
|
|||
|
|
|
LL,z |
mL . |
(11.5) |
||
|
|
|
L |
m |
|
||
|
|
|
S ,z |
|
S |
|
|
магнітними квантовими числами mL, mS, mJ -, значення яких за-
лежать від квантових чисел L, S і J.
mL = L; (L - 1); (L - 2);..|L - N| |
|
mS = S; (S - 1); (S - 2);...|S - N| |
|
mJ = J; (J - 1); (J - 2);.....|J - N| |
(11.6) |
Нагадаємо, що для атомів із декількома валентними електро-
нами, L - квантове число сумарного орбітального моменту кіль-
кості руху електронів атома може мати лише цілі невід ємні значення, які відрізняються один від одного на одиницю і знаходяться в межах
між максимальним і мінімальним значеннями їх суми i . Для двох
|
|
|
|
|
i |
|
електронів з квантовими числами 1 і 2 |
|
|
|
|
|
|
L 1 2 , 1 2 -1, 1 2 2, |
, |
|
1 2 |
|
. |
(11.7*) |
|
|
Для трьох електронів спочатку визначають L |
попереднім способом |
||||
(11.7*), а потім аналогічно знаходять сумарний момент L , що склада- |
|||||
ється із моментів L і 3 |
|
||||
L L 3; L 3-1; , |
|
L 3 |
|
. |
(11.7) |
|
|
||||
Находкін М.Г., Харченко Н.П., Атомна фізика |
268 |
Глава 11. Векторна модель атома
|
|
LJ |
LL |
|
L |
L ,2 |
LS |
LS |
|
|
|
L ,1 |
Ls,2 |
Ls,1 |
|
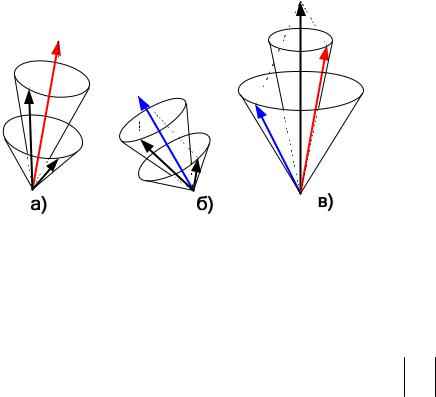
Рис. 11.1. Нормальний (Рассел-Саундерса) зв’язок:
а) - LL L ,i , б) - LS Ls,i , в) - LJ LL LS . i i i i
Цей розгляд продовжують до тих пір, поки не врахують усі Z* електронів на зовнішній не заповненій оболонці атома.
Квантове число сумарного спіну S також має тільки невід ємні значення, що відрізняються одне від одного на одиницю і знаходять-
ся між макальним і мінімальним значеннями алгебраїчної суми si
|
|
|
|
i |
Z |
Z |
Z |
Z |
|
S si ; si 1; |
si |
2;...; si N 0; |
(11.8) |
|
i 1 |
i 1 |
i 1 |
i 1 |
|
Квантове число J, яке характеризує сумарний кутовий момент LJ, набуває невід ємні значення, які відрізняються одне від одного на одиницю в межах
|
|
|
L S |
|
J L S |
|
|
(11.9) |
|||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|||
Коли L>S, то J набуває (2S+1) значень, а коли L<S, то J має (2L+1) |
|||||||||||
значень. При L = 0 |
J = S, а при S = 0 J = L. Кількість можливих станів |
||||||||||
- значень квантового числа J при даному значенні числа L визначає |
|||||||||||
мультиплетність термів (2S+1) (див. таблицю 11.1). |
|
|
|||||||||
Таблиця 11.1 Мультиплетність залежно від квантового числа S |
|
||||||||||
S |
0 |
|
|
|
½ |
1 |
|
3/2 |
2 |
|
|
2S+1 |
1 |
|
|
|
2 |
3 |
|
4 |
5 |
|
|
Мультиплетність |
Синглет |
|
дублет |
Триплет |
квартет |
Квінтет |
|
||||
Находкін М.Г., Харченко Н.П., Атомна фізика |
269 |

Глава 11. Векторна модель атома
Оскільки si = 1/2, то із формули (11.8) видно, що при Z непарних S
напівціле число, тобто мультиплетність парна (дублети, квартети тощо), а при Z парних S ціле число, тобто мультиплетність непарна (синглети, триплети, квінтети, тощо).
11.3. Квантові числа складних атомів
Атоми характеризуються такими квантовими числами: n -
головним, L - орбітальним, що визначає абсолютну величину повного орбітального моменту кількості руху, S - повного спіну і J -
повного моменту кількості руху (спінового і орбітального), mL, mS, mJ - магнітними квантовими числами сумарних орбітально-
го, спінового і спін-обітального моментів кількості руху електрона в складному атомі відповідно. У відсутності силових полів енергетичний рівень визначається трьома квантовими числами n, L, J. Кван-
тове число повного спіну S визначає мультиплетність термів за формулою (2S+1), а магнітні квантові числа визначають зміни енергії рівнів (енергетичне положенні термів) у присутності силових полів.
Для спектральних термів прийнято стандартне позначення:
ns np 2S+1 LJ ,
де для однозначності перед символами L, які позначаються великими латинськими літерами S, P, D, F, G, H, I і визначають стан атома за допомогою квантового числа L (таблиця 11.2), виписують символи малими латинськими буквами, які характеризують електронну конфігурацію даного атома, а мульти-
плетність 2S+1 ставлять праворуч зверху біля символу L, на-
приклад 2s2 2p1 2P1/2; 3s23p1
2P3/2; nd1 2D5/2 тощо.
L |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
|
S |
P |
D |
F |
G |
H |
I |
11.4. Правила відбору
Правила відбору вказують, які із можливих переходів між енергетичними рівнями в атомі дозволені, а які заборонені, у вигляді відповідних змін квантових чисел при переходах. Вони зв’язані з симетрією квантових систем, тобто з незмінністю (інваріантністю) їх властивостей при певних перетвореннях координат і часу, і відповідними законами збереження. Переходи з порушенням законів збереження
Находкін М.Г., Харченко Н.П., Атомна фізика |
270 |
Глава 11. Векторна модель атома
енергії, імпульсу, моментів кількості руху тощо у замкнених системах виключаються. Правила відбору в атомі визначають через ненульові матричні елементи оператора взаємодії дипольного моменту системи або більш складного квадрупольного моменту системи „атом плюс поле” в процесах випромінювання та поглинання світла. Тому розрізня-
ють правила відбору для дипольних і квадрупольних спонтанних переходів.
Раніше для спонтанних дипольних переходів у одноелектронних атомів ми отримали такі правила відбору:
1; |
m 0, 1; |
|
|
|
|
|
(11.10) |
j=0, 1; |
mj 0, |
. |
|
1 |
|
||
|
|
|
|
У багатоелектронних атомів, до яких можна застосувати модель нормального (L-S) зв’язку, спонтанні дипольні переходи відбуваються, коли виконуються такі правила відбору:
J 0; |
1; |
але J=0 J =0; |
mJ |
0; |
1; |
|
|
S 0; |
|
|
|
|
|
|
|
. (11.10*) |
|
|
|
L 1; mL 0, 1 |
|
|
|
|
|
|
|
||
У легких атомів найбільш імовірні переходи, для яких сумарне спінове число не змінюється S = 0. В атомах важких елементів можливі
інтеркомбінаційні переходи, для яких S =±1. Крім того, коли між електронами в атомі має місце сильна взаємодія й можуть збуджуватися більше одного електрона, то з’являється ще одне правило відбору для дипольних переходів:
L 0. |
(10.10**) |
Однак, ці переходи відбуваються досить рідко. Для квадрупольних переходів з’являються додаткові правила відбору: L 2; J 2.
11.5. Правила Хунда (Гунда)
Векторна модель не дає енергетичної послідовності термів. Для її визначення користуються трьома емпіричними правилами Хунда
(Гунда).
Перше правило Хунда. Для даної електронної конфігурації терми з більшою мультиплетністю мають більші абсолютні значення енергій:
Находкін М.Г., Харченко Н.П., Атомна фізика |
271 |

Глава 11. Векторна модель атома
2S1 1E(L) 2S2 1E(L) для S1 < S2 . (11.11)
Наприклад, триплетні терми на енергетичних діаграмах, де енергія зв’язаного електрона Е<0, знаходяться нижче, ніж дублетні чи синглетні терми.
Друге правило Хунда. Для даної електронної конфігурації та мультиплетності, тобто при заданих S, J і n, терми з більшими значеннями сумарного орбітального числа L мають більші за абсолютною величиною енергії, ніж терми з меншими значеннями L:
2S 1E(L ) |
|
2S 1E(L ) |
для L1 < L2 |
(11.12) |
||
1 |
|
2 |
|
|
|
|
Отже для даної конфігурації та мультиплетності має місце така ієра-
рхія термів з різними значеннями орбітального квантового числа L
|ES | > | EP | < | ED | ......
Третє правило Хунда. Для даної електронної конфігурації при заданих значеннях квантових чисел n, L і S чим менше квантове чис-
ло J, тим більша за абсолютною величиною енергія терма: |
|
|
| E J1 | > | EJ2 | для |
J1 < J2 |
(11.13) |
Така ієрархія має місце у випадку, коли валентна електрона оболонка заповнена наполовину, тобто не ній знаходиться електронів менше ніж 2 + 1. У випадку, коли електронна оболонка заповнена більше,
як на половину, тобто, коли на ній знаходиться електронів більше, ніж
2 + 1, то в (11.13) змінюється знак нерівності на протилежний і терми заглиблюються із збільшенням квантового числа J на енергетичних діаграмах, Е<0, |EJ1| < |EJ2| для J1 < J2.
Перші два правила засновані на врахуванні електростатичної взаємодії електронів, а третє - на врахуванні магнітної взаємодії.
Перше правило пояснюється детальними розрахунками обмінної взаємодії, які показують, що в атомі більшої мультиплетності, наприклад, триплетному, електронний розподіл виявляється більш стиснутим, ніж в атомі меншої мультиплетності, наприклад, синглетному, що підсилює притяжіння електронів до ядра. Воно компенсує відштовхування між електронами з однаково направленими спінами і дає виграш в енергії атомів з паралельними спінами по відношенню до атомів з антипаралельними спінами.
Друге правило відображає здатність електронів уникати один одного, якщо орбітальні моменти примушують їх рухатись в одному напрямку. Електронам, що рухаються в одному напрямку, простіше залишатись віддаленими один від одного, що зменшує кулонівське відштовхування. Якщо електрони рухаються в різних напрямках, то
Находкін М.Г., Харченко Н.П., Атомна фізика |
272 |
