
senchuk_v_v_biohimiya_kurs_lekcii
.pdf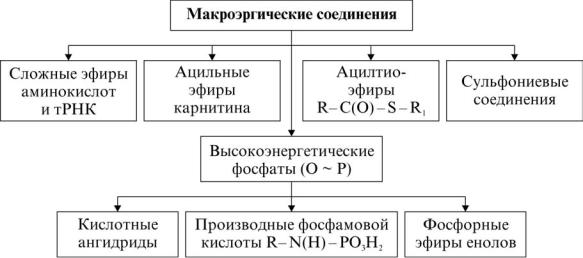
основана вся биохимия. Среди биохимических реакций к числу экзергонических относятся реакции окисления. Например, G полного аэробного окисления глюкозы по схеме С6Í12Î6 + 6Î26ÑÎ2 + 6Í2О составляет около –2 870 000 Дж/моль. У всех живых организмов эта энергия преобразуется путем сопряжения процесса окисления с синтезом 38 молекул универсального макроэргического соединения АТФ по реакции АДФ + Фн АТФ ( G ~ 35 000 Дж/моль). Запасенная энергия АТФ в свою очередь может трансформироваться в другие макроэргические соединения клетки и может утилизироваться в эндергонических биосинтетических реакциях (большинство природных соединений самопроизвольно не реагируют друг с другом и требуют активации), в транспорте ионов и молекул, в мышечном сокращении и др. Следовательно, с точки зрения термодинамики генерируемая в процессах биологического окисления энергия служит для поддержания живого организма в неравновесном состоянии.
Макроэргические соединения содержат особые высокоэнергетические связи (макроэргические связи) с – G гидролиза > > 20 000 Дж/моль, которые обозначают знаком ~ (табл. 6). Макроэргические соединения живых организмов весьма разнообразны по химической структуре и классифицируются следующим образом:
Важнейшие макроэргические соединения перечислены в таблице. Среди них особая роль принадлежит высокоэнергети- ческим фосфатам (О ~ Р). В молекуле АТФ только две последние фосфоангидридные связи являются макроэргическими. Величи- на гидролиза макроэргических связей АТФ занимает промежуточное положение среди макроэргических соединений. Именно в
172
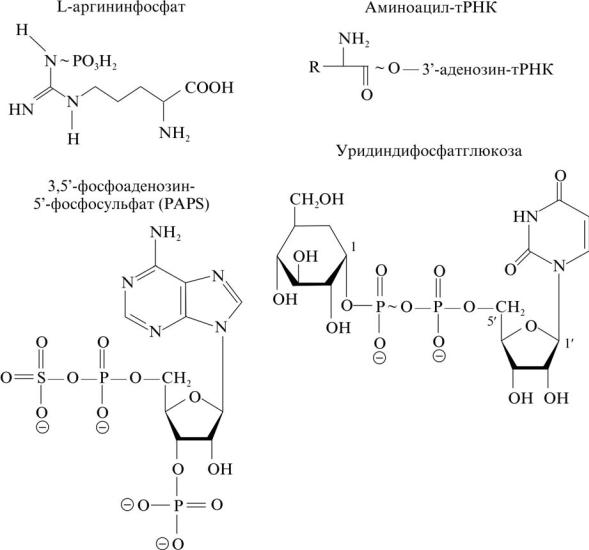
этом заключается уникальность и универсальность АТФ как макроэрга. Другие макроэргические нуклеотиды выполняют специализированные функции — ГТФ в биосинтезе белков, ЦТФ в синтезе липидов (в виде цитидиндифосфатхолина), УТФ в биосинтезе олиго- и полисахаридов (в виде, например, уридиндифосфатглюкозы). Четыре дНТФ (дАТФ, дГТФ, дЦТФ, ТТФ) используются в биосинтезе ДНК, а АТФ, ГТФ, ЦТФ и УТФ — в биосинтезе РНК. Фосфоенолпируват и 1,3-дифосфоглицерат являются метаболитами гликолиза и участвуют в субстратном фосфорилировании АДФ до АТФ. Креатинфосфат используется как источник для мышечного сокращения при недостатке кислорода. У насекомых эту функцию выполняет L-аргининфосфат (рис. 53). Ацилкарнитин служит для переноса жирных кислот
Ðèñ. 53. Макроэргические соединения
173

Таблица 6
Свободная энергия гидролиза природных макроэргических соединений
|
Соединение |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
– G, Äæ/ìîëü |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(pH = 7) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ацетиладенилат |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
62 500 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Фосфоенолпируват |
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
O ~ PO3H2 |
|
|
|
61 000 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
||||||||||
1,3-Дифосфоглицерат |
|
|
HO |
|
|
|
|
|
|
|
|
|
|
O — PO3H2 |
54 500 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
O ~ PO3H2 |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Карбамоилфосфат |
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
51 500 |
|||
|
|
|
H2N |
|
|
|
|
|
|
|
|
|
O ~ PO3H2 |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
3’,5’-öÀÌÔ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
49 000 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ацетилфосфат |
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
47 500 |
|||
|
|
|
H3C |
|
|
|
|
|
|
|
|
|
|
O ~ PO3H2 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
Àöèë-ÊîÀ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
35 000—48 000 |
|||
|
|
|
KoA |
|
|
|
|
S ~ |
|
— CH3 |
|||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S-Аденозилметионин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
44 000 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Креатинфосфат |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
N ~ PO3H2 |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
42 500 |
||
|
|
|
|
HN |
|
|
|
|
|
|
N |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|||||
АТР (внутренняя |
O |
|
O |
|
|
|
|
O |
|
|
|
14 000 |
|||||||||||
связь 3) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
32 500 |
АТР (внутренняя |
O — P ~ O — P ~ O — P — O — Рибоза |
35 000 |
|||||||||||||||||||||
связь 2) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
АТР (внутренняя |
O |
|
|
O |
|
|
|
|
|
O |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
Аденин |
|
||||||||||
связь 1) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
1 |
|
|
|
|
2 |
|
|
|
|
|
|
3 |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
Пирофосфат (Н4Ð2Î7) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
32 500 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ацилкарнитин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
30 000—35 000 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Уридиндифосфатглюкоза |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
28 000 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Цитидиндифосфатхолин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
27 500 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
174
через мембрану митохондрий. S-Аденозилметионин выполняет роль донора метильных групп в биосинтетических реакциях. Донором остатков серной кислоты является 3’-фосфоаденозин- 5’-фосфосульфат (рис. 53). В биосинтезе нуклеотидов используется активированная форма рибозы — 5-фосфорибозил-1-пиро- фосфат. Ацетил-КоА — это активированный двууглеродный продукт окисления моносахаридов и жирных кислот, подвергающийся полному окислению в цикле Кребса. Ацетилфосфат используется у микроорганизмов для фосфорилирования моносахаридов. Аминоацил-тРНК — это активированные формы аминокислот, вступающих в биосинтез белков (рис. 53). Карбамоилфосфат — это активированная форма аммиака для синтеза аргинина и мочевины, а также участник биосинтеза пиримидинов. Все эти макроэргические соединения образуются при прямом или опосредованном участии АТФ.

ЛИТЕРАТУРА
Основная
1.Березов, Т. Т. Биологическая химия / Т. Т. Березов, Б. Ф. Коровкин. М.: Медицина, 1990.
2.Ленинджер, А. Основы биохимии / А. Ленинджер. М.: Мир, 1985.
Ò.1—3.
3.Марри, Р. Биохимия человека / Р. Марри, Д. Греннер, П. Мейс, В. Родуэлл. М.: Мир, 1993. Т. 1—2.
4.Основы биохимии / под ред. А. А. Анисимова. М.: Высш. шк., 1986.
5.Учебник биохимии и молекулярной биологии / под ред. А. И. Арча- кова, А. Е. Медведева, В. П. Скулачева. М.: РАМН, 1999.
6.Филиппович, Ю. Б. Основы биохимии / Ю. Б. Филиппович. М., 1999.
Дополнительная
1.Албертс, Б. Молекулярная биология клетки / Б. Албертс, Д. Брей, Дж. Льюис и др. М.: Мир, 1986. Т. 1—5.
2.Албертс, Б. Молекулярная биология клетки / Б. Албертс, Д. Брей, Дж. Льюис и др. М.: Мир, 1994. Т. 1—3.
3.Ашмарин, И. П. Молекулярная биология / И. П. Ашмарин. Л.: ЛГУ,
1977.
4.Белки и пептиды. М.: Наука, 1995. Т. 1.
5.Бохински, Р. Современные воззрения в биохимии / Р. Бохински. М.: Мир, 1987.
6.Брухман, Э. Э. Прикладная биохимия / Э. Э. Брухман. М.: Мир, 1981.
7.Василенко, Ю. К. Биологическая химия / Ю. К. Василенко. М.: Высш. шк., 1978.
8.Кретович, В. Л. Основы биохимии растений / В. Л. Кретович. М.: Высш. шк., 1986.
9.Мецлер, Д. Биохимия / Д. Мецлер. М., 1980. Т. 1—3.
10.Николаев А. Я. Биологическая химия / А. Я. Николаев. М.: Высш. шк., 1989.
11.Овчинников, Ю. А. Биоорганическая химия / Ю. А. Овчинников. М.: Просвещение, 1987.
12.Спирин, Л. С. Молекулярная биология. Структура рибосом и биосинтез белка / Л. С. Спирин. М.: Высш. шк., 1986.
13.Страйер, Л. Биохимия / Л. Страйер. М.: Мир, 1985.
14.Строев, Е. А. Биологическая химия / Е. А. Строев. М.: Высш. шк.,
1986.
15.Óàéò, À. Основы биохимии / А. Уайт и др. М.: Мир, 1981. Т. 1—3.
16.Шамин, А. Н. История биологической химии. Формирование биохимика / А. Н. Шамин. М.: Наука, 1991.
17.Энкерт, Р. Физиология человека / Р. Энкерт, Д. Рэнделл, Дж. Огастин. М.: Мир, 1991. Т. 1—2.
Литература по методам в биохимии
1.Биохимическое исследование мембран / под ред. Э. Мэдди. М.: Мир,
1979.
2.Дарбре, А. Химия белка / А. Дарбре. М.: Мир, 1990.
3.Досон, Р. Справочник биохимика / Р. Досон, Д. Эллиот, У. Эллиот,
Ê.Джонс. М.: Мир, 1991.
176
4.Äîéñ, Ý. Количественные проблемы биохимии / Э. Дойс; под ред.
Ë.М. Гинодмана. М.: Мир, 1983.
5.Карасек, Ф. Введение в хромато-масс-спектрометрию / Ф. Карасек, Р. Клемент. М.: Мир, 1993.
6.Лабораторное руководство по хроматографическим и смежным методам / под ред. В. Г. Березкина. М.: Мир, 1982.
7.Остерман, Л. А. Методы исследования белков и нуклеиновых кислот: Электрофорез и ультрацентрифугирование / Л. А. Остерман. М.: Наука, 1981.
8.Остерман, Л. А. Исследование биологических макромолекул изоэлектрофокусированием, иммуноэлектрофорезом и радиоизотопными методами / Л. А. Остерман. М.: Наука, 1983.
9.Остерман, Л. А. Хроматографические методы исследования /
Ë.А. Остерман. М.: Наука, 1985.
10.Практикум по биохимии / под ред. С. Е. Северина, Г. А. Соловьевой. М.: МГУ, 1989.
11.Препаративная биохимия липидов / под ред. Л. Д. Бергельсона. М.: Мир, 1981.
12.Степаненко, Б. Н. Химия и биохимия углеводов / Б. Н. Степаненко. М.: Наука, 1967.
13.Шабарова, З. А. Химия нуклеиновых кислот и их компонентов / З. А. Шабарова, А. А. Богданов. М.: Наука, 1978.
Источники информации в Интернете
1.Биохимическая классификация и номенклатура. Свободный доступ на сайте Международного союза биохимии и молекулярной биологии www.chem.qmul.ac.uk/iubmb.
2.Лауреаты Нобелевских премий по химии, физиологии и медицине www.nobel.se.
3.Свободный доступ в крупнейшую базу научных данных в области биомедицинских наук MedLine, включая биохимию www.ncbi.nlm.nih.gov/ PubMed.
4.База данных по всем первичным структурам белков в свободном доступе www.ncbi.nlm.nih.gov/Genbank è www.swissprot.com.
5.Официальный сайт Федерации европейских биохимических обществ www.febs.org.
6.Научные издания в области биохимии, химии и смежных наук www.chemport.org.
7.Соросовский образовательный журнал www.issep.rssi.ru, где в свободном доступе находятся полные тексты обзорных статей по важнейшим разделам биохимии и молекулярной биологии.
8.Учебники, научные монографии, обзоры, лабораторные практикумы в свободном доступе на сайте практической молекулярной биологии www.molbiol.ru, на сайте www.nature.ru.
9.Лучшие обзорные статьи по биохимии в журнале «Annual Review of Biochemistry» можно найти на сайте www.ncbi.nlm.nih.gov/ PubMed.
10.Обзорные и экспериментальные статьи в журнале «Биохимия» (Москва) можно найти по ссылке на сайте практической молекулярной биологии.
11.Разнообразную полезную информацию по биохимии можно найти по адресам Московского государственного университета (включая доступ в библиотеку) www.msu.su, а также на сайте биологического факультета Белорусского государственного университета www.bio.bsu.by.

СОДЕРЖАНИЕ
ВВЕДЕНИЕ ............................................................................. |
3 |
АМИНОКИСЛОТЫ |
|
Строение, классификация и номенклатура аминокислот .............. |
8 |
Моноаминомонокарбоновые аминокислоты ................................ |
11 |
Моноаминодикарбоновые (кислые) аминокислоты и их амиды ....12
Диаминомонокарбоновые (оснoвные) аминокислоты ................... |
12 |
Гидроксиаминокислоты ........................................................... |
13 |
Тиоаминокислоты ................................................................... |
13 |
Гетероциклические аминокислоты ............................................ |
14 |
Физико-химические свойства аминокислот ................................ |
15 |
Биохимические свойства аминокислот ...................................... |
18 |
ПЕПТИДЫ |
|
Классификация и номенклатура пептидов ................................. |
23 |
Биохимические свойства пептидов ........................................... |
24 |
Структурно-функциональная организация пептидов ................... |
25 |
БЕЛКИ |
|
Биохимические свойства белков ............................................... |
32 |
Методы изучения структуры белков ......................................... |
33 |
Структурная организация белков ............................................. |
37 |
Денатурация и ренатурация белков .......................................... |
50 |
Биохимия гетеромерных белков ............................................... |
51 |
Хромопротеины ...................................................................... |
52 |
Флавопротеины ...................................................................... |
52 |
Гемопротеины ........................................................................ |
53 |
Фосфопротеины ...................................................................... |
56 |
Гликопротеины ...................................................................... |
58 |
Нуклеопротеины ..................................................................... |
61 |
Липопротеины ........................................................................ |
62 |
Металлопротеины ................................................................... |
63 |
НУКЛЕОЗИДЫ, НУКЛЕОТИДЫ, |
|
НУКЛЕИНОВЫЕ КИСЛОТЫ |
|
Азотистые основания .............................................................. |
70 |
Строение, классификация и номенклатура азотистых |
|
оснований .......................................................................... |
70 |
Нуклеозиды ........................................................................... |
72 |
Строение, классификация и номенклатура нуклеозидов ......... |
72 |
178
Нуклеотиды ........................................................................... |
75 |
Строение, классификация и номенклатура нуклеотидов ......... |
75 |
Нуклеиновые кислоты ............................................................ |
79 |
Химическое строение и свойства ДНК .................................. |
81 |
Третичная структура и надмолекулярные комплексы ДНК ......... |
88 |
Химическое строение и свойства РНК ....................................... |
91 |
УГЛЕВОДЫ |
|
Моносахариды (монозы) .......................................................... |
96 |
Строение, классификация и номенклатура моносахаридов ...... |
96 |
Физико-химические свойства моносахаридов ....................... |
102 |
Биохимические свойства моносахаридов ............................. |
102 |
Производные моносахаридов .............................................. |
103 |
Олигосахариды ..................................................................... |
105 |
Полисахариды ...................................................................... |
107 |
Гомополисахариды ................................................................ |
108 |
Строение, классификация и биохимические свойства ........... |
108 |
Гетерополисахариды ............................................................. |
111 |
Строение, классификация и биохимические свойства ................ |
|
ЛИПИДЫ |
|
Ацилглицерины .................................................................... |
116 |
Фосфолипиды ....................................................................... |
118 |
Глицерофосфолипиды ........................................................ |
121 |
Сфингофосфолипиды ......................................................... |
124 |
Гликолипиды ....................................................................... |
126 |
Жирные кислоты .................................................................. |
127 |
Эйкозаноиды ........................................................................ |
131 |
Терпены ............................................................................... |
136 |
Стероиды ............................................................................. |
140 |
Принципы структурной организации стероидов ................... |
140 |
Стероидные гормоны ............................................................. |
145 |
Половые гормоны ............................................................. |
145 |
Кортикостероиды .............................................................. |
148 |
Желчные кислоты ............................................................ |
150 |
Витамины группы D ......................................................... |
151 |
Сердечные гликозиды ........................................................ |
152 |
ВИТАМИНЫ И КОФЕРМЕНТЫ |
|
Водорастворимые витамины и коферменты .............................. |
157 |
Жирорастворимые витамины и коферменты ............................ |
164 |
Витаминоподобные соединения ............................................... |
168 |
МАКРОЭРГИЧЕСКИЕ СОЕДИНЕНИЯ ................................... |
171 |
ЛИТЕРАТУРА ...................................................................... |
176 |
Учебное издание
Сенчук Вадим Валентинович
БИОХИМИЯ
Курс лекций
В двух частях
Часть 1
БИОМОЛЕКУЛЫ
В авторской редакции
Технический редактор Г. М. Романчук
Корректор Н. И. Мирончик
Компьютерная верстка Т. В. Шестаковой
Ответственный за выпуск А. Г. Купцова
________________________________________________________________
Подписано в печать 18.08.2005. Формат 60 84/16. Бумага офсетная. Гарнитура Школьная. Печать офсетная. Усл. печ. л. 10,46. Уч.-изд. л. 8,95. Тираж 250 экз. Зак.
Белорусский государственный университет. Лицензия на осуществление издательской деятельности
¹ 02330/0056804 от 02.03.2004. 220050, Минск, проспект Независимости, 4.
Отпечатано с оригинала-макета заказчика. Республиканское унитарное предприятие
«Издательский центр Белорусского государственного университета». Лицензия на осуществление полиграфической деятельности
¹ 02330/0056850 от 30.04.2004. 220030, Минск, ул. Красноармейская, 6.
